乙二醇化学氧化制备乙醇酸催化剂研究进展
2022-12-27刘华伟
江 甜,刘华伟
(1.华烁科技股份有限公司,湖北 武汉 430074;2.华烁科技股份有限公司 工业气体净化精制与利用湖北省重点实验室,湖北 鄂州 436000)
乙醇酸是一种重要的精细化工原料,在医疗、食品工业、化妆品和生物聚合物单体中有广泛应用[1-4]。天然乙醇酸由于含量低且与其他物质共存形成了复杂组分而难以分离,目前市场上销售的乙醇酸几乎均来自化学合成[5-6]。乙醇酸的合成方法主要有甲醛羰基化[7-8]、氯乙酸或乙二腈水解[9-10]、乙二醛转化[11]和草酸电解还原[12]等,但都存在生产条件苛刻、催化剂成本高和副产物量大等缺点,因此需要开发反应条件温和、反应过程绿色并具有应用可行性的乙醇酸合成新路线[13]。
乙二醇是化学工业的重要起始原料,其成本较低、易大量获得。随着国内煤制乙二醇产业的爆发式增长,国内乙二醇产品未来也将面临着产能过剩等问题,因此以乙二醇为原料,通过氧化反应制备精细化工产品或将成为乙二醇产业链延伸和发展的方向[14]。近年来,乙二醇部分氧化制备乙醇酸受到广泛关注,研究[15-17]显示,该路线是一条可持续制备乙醇酸的途径,其中以乙二醇化学氧化法制备乙醇酸表现最为突出。乙二醇化学氧化制备乙醇酸的反应效果取决于反应条件和催化剂。目前学者已经研究了碱介质和多种金属催化剂,包括贵金属(Au、Ru、Rh、Pd、Ⅰr和Pt)和过渡金属(Mn、Ni和Cu)[18-19]的催化作用。碱介质对乙二醇氧化制乙醇酸反应具有催化作用,但强碱性介质会导致金属催化剂失活,因此学者着手研究在无碱介质中具有乙二醇氧化催化活性的催化剂,并于近两年取得了一定成效。
本文主要综述碱催化剂和碱性介质中贵金属催化剂、过渡金属催化剂及双金属组合催化剂对乙二醇化学氧化制备乙醇酸反应的催化效果,并介绍无碱介质中贵金属催化剂的最新研究进展,以期为同类技术研究提供参考。
1 乙二醇部分氧化制备乙醇酸方法
乙二醇部分氧化制备乙醇酸的方法主要包括生物催化氧化法、电化学氧化法和化学氧化法。乙二醇分子中含有两个一级羟基,通过羟基官能团的部分氧化可以获得乙醇酸(CH2OHCOOH)、乙二醛(CHOCHO)和乙醛酸(CHOCOOH)等高附加值产物,乙二醇部分氧化反应方程式见图1[20]。由图1可知,乙二醇氧化制备乙醇酸是乙二醇中部分—CH2OH基团氧化为—COOH基团的过程。
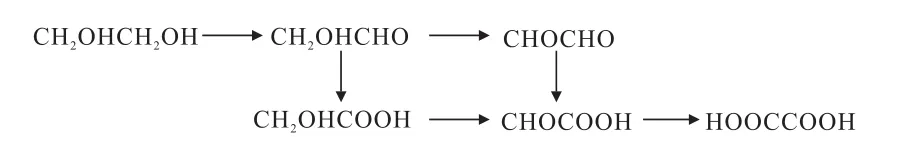
图1 乙二醇部分氧化反应方程式Fig.1 Reaction equation of ethylene glycol partial oxidation
生物催化氧化法、电化学氧化法和化学氧化法部分氧化乙二醇制备乙醇酸的优缺点见表1[18]。

表1 3种乙二醇部分氧化法制备乙醇酸的比较Table 1 Comparison of three methods for partial oxidation of ethylene glycol to prepare glycolic acid
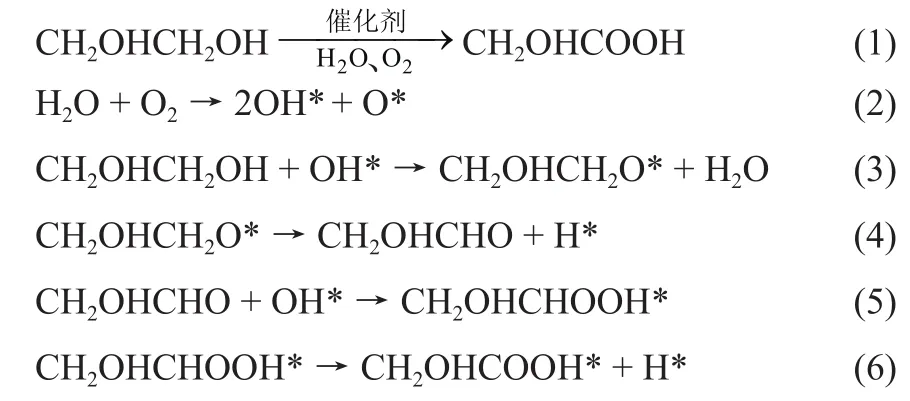
从上述反应机理可以看出,乙醇酸的形成经历了4个步骤,依次为羟基脱氢(式(3))、β-氢化物消除(式(4))、乙醇醛氧化(式(5))和C—H键脱氢(式(6))。通常在发生醇氧化反应之前,H2O将辅助O2分解成羟基(式(2));形成的羟基可以进一步参与后续氧化反应,游离的O*通过与H质子(式(4)和式(6))结合以促进O2和H2O的循环反应,继续形成OH*[30]。
由表1可知,生物催化氧化法多以乙酸杆菌属微生物的全细胞催化为主,但直接合成乙醇酸难度较大[21-22]。电化学氧化法反应迅速,但产物乙醇酸的抑制作用或催化剂失活都可能导致该反应偏离常规氧化途径,因此需要严格控制影响电化学氧化的参数,如乙二醇流速(接触时间)、动力学和反应途径等[23-25]。化学氧化法反应条件温和,但使用碱反应介质得到的乙醇酸盐需要纯化处理后才能获得乙醇酸,增加了分离提纯成本,而且强碱介质通常会导致负载型金属催化剂结构演变和金属烧结,使催化剂失活[26]。相比而言,化学氧化法工业化几率更高,开发前景更广阔。而为了获得高乙二醇转化率和乙醇酸选择性,选择合适的催化剂是关键[27-29]。乙二醇在催化剂活性中心上氧化为乙醇酸的反应机理见式(1)~式(6)[30]。
2 乙二醇化学氧化法制备乙醇酸催化剂研究进展
乙二醇化学氧化制备乙醇酸属于部分氧化反应,适宜的氧化剂和催化剂可以提高乙醇酸收率。清洁氧化剂主要有空气、O2及双氧水,其中O2作氧化剂最受关注。催化剂主要分为碱催化剂(水溶液中电离出的阴离子全是氢氧根离子的化合物,常用的碱是NaOH、KOH)和金属催化剂,金属催化剂主要包括贵金属催化剂、过渡金属催化剂和双金属组合催化剂。
2.1 碱催化剂
碱是激活水中醇类分子进行氧化反应的必要物质。单独NaOH(不存在任何金属催化剂)可作为醇在水中好氧氧化的催化剂[31]。对于乙二醇化学氧化制备乙醇酸反应,例如在温度为60~100 °C、O2压力为1.0 MPa的条件下,乙二醇水溶液在无NaOH时无法反应,当溶液中存在NaOH时,乙二醇可氧化为乙醇酸钠,但单独碱催化剂的活性偏低。VAN等[32]研究了KOH、NaOH和Ca(OH)2对碳纳米纤维(CNF)负载的Cu纳米颗粒催化剂(Cu/CNF)和Ni纳米颗粒催化剂(Ni/CNF)对乙二醇氧化制备乙醇酸反应的影响。在不添加碱的中性条件下,乙二醇几乎没有发生转化(乙二醇转化率< 1%);当碱与金属催化剂同时存在时,催化效果明显;而使用碱进行空白实验(无金属催化剂),当碱与乙二醇物质的量比为2时,乙二醇也几乎没有发生转化(乙二醇转化率< 1%),原因是无金属催化剂的水热过程仅在300 °C及以上的较高温度下发生。结合金属负载催化剂的反应机理分析,O2是合适的电子受体,可取代金属表面上的OH-电子以提供额外的OH*,OH*随后与脱质子乙二醇物种(HOCH2CO*)反应形成乙醇酸;而H2O的脱质子化不能轻易提供OH*,因此在中性条件下反应进行缓慢[33]。
相关研究表明,不同种类的碱,如KOH、NaOH或Ca(OH)2也会影响乙二醇氧化活性,其中KOH与NaOH作用效果相当,均优于Ca(OH)2,这与碱添加剂在非催化高温水热过程中的有效性一致,可能主要是由于碱的溶解性导致pH的差异[34]。SHⅠ等[18]还发现碱浓度对乙二醇在Pt和Pt-Fe催化剂上液相氧化制备乙醇酸反应有影响,其中低浓度(物质的量浓度,下同)碱不仅对Pt和Pt-Fe催化剂都有促进作用,还可增强Pt-Fe催化剂的协同效应;高浓度碱对两种催化剂都有抑制作用,原因是当使用过高浓度的碱时,碱中的OH-与乙二醇中的—OH基团竞争吸附,占据过多活性位置,从而抑制氧化反应。
综上,研究人员从碱催化剂类型和浓度对乙二醇化学氧化制备乙醇酸反应的影响入手,发现碱是水中乙二醇化学氧化活化的激活剂或促进剂。单独使用碱或金属作催化剂,催化活性都明显不及金属-碱协同催化剂,金属催化剂在实现乙二醇氧化反应的活性和选择性效果时,关键取决于共存的碱(一般为NaOH,本质上为OH-)[31]。
2.2 贵金属与碱协同催化剂
贵金属中的Au和大部分铂族金属(Ru、Rh、Pd、Ⅰr和Pt)均可作为乙二醇化学氧化制备乙醇酸催化剂的活性组分,但Ru[35]、Rh[36]和Ⅰr[37]主要用于非负载型催化剂,少量早期研究[38]显示Ⅰr也可用于负载型催化剂,如碳负载Ⅰr催化剂的最高乙醇酸产率为87%,而Pd、Pt和Au主要用于碱性溶液中乙二醇制乙醇酸负载型催化剂,研究最多的金属是Pd和Pt[39]。
在乙二醇催化氧化中,碳负载Pd或Pt催化剂的稳定性和选择性均较碳载Au催化剂差,一方面是反应中因为过氧化产生草酸盐时,通常还伴随C—C键断裂形成CO2、甲酸盐和碳酸盐等副产物[40-41];另一方面Pt和Pd用于乙二醇催化氧化反应时经常失活,Bi等助催化剂的引入具有提高催化活性和延长催化剂寿命的双重效果[34,42]。催化剂的贵金属负载量以及反应条件均对乙二醇转化率和乙醇酸选择性有直接影响。由表2可知,乙二醇氧化反应中,与Pd或Pt基催化剂相比,负载Au催化剂对乙醇酸的选择性更高,添加Bi助剂可进一步提高催化性能。同时,反应条件也非常关键,在反应温度为70 ℃,反应压力为300 kPa的条件下,乙二醇转化率为94%~100%,乙醇酸的选择性最高达96.3%。
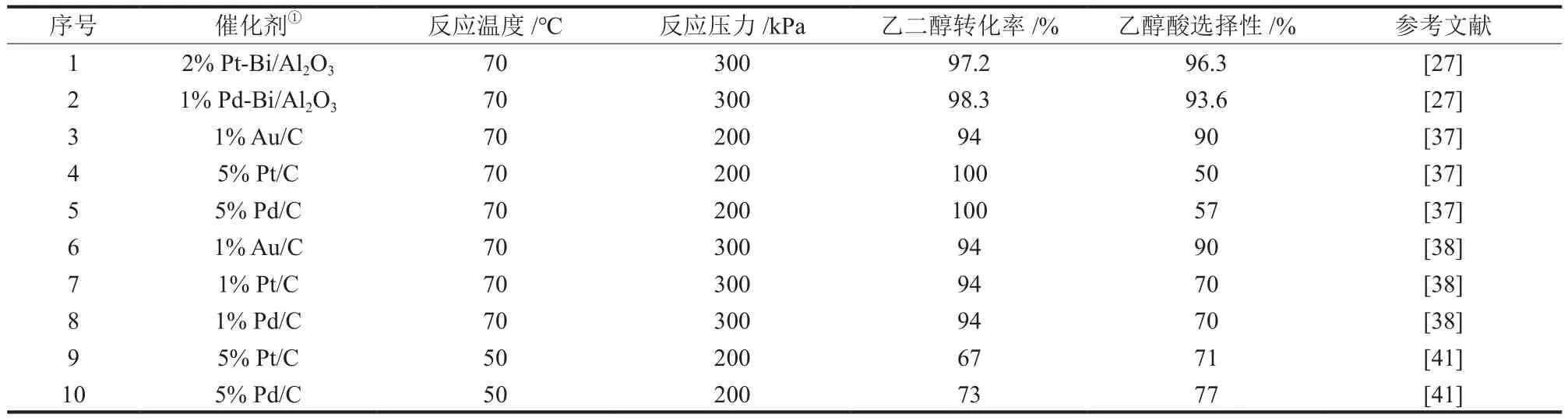
表2 不同金属负载催化剂催化乙二醇制备乙醇酸(盐)的催化性能Table 2 Catalytic performance of different metal supported catalysts in catalytic preparation of glycolic acid (glycolate) from ethylene glycol
由于负载Pd或Pt催化剂的稳定性和选择性要比负载Au催化剂差,学者对负载Au催化剂展开了集中研究,发现Au纳米颗粒催化乙二醇液相氧化为乙醇酸性能是可变的,取决于Au纳米颗粒的粒径、形状、载体和反应条件[44]。共沉淀[45]、沉积-沉淀[46]以及金溶胶固定[47]等方法均可用于制备具有乙二醇化学氧化活性的Au纳米颗粒。金溶胶固定法与沉积-沉淀法制备的碳负载Au催化剂相比,金溶胶固定法所制催化剂乙二醇的液相氧化活性显著增强[44]。由上述两种方法制备的碳负载Au的平均粒径(7~8 nm)虽然几乎相同,但高分辨率透射电镜照片显示两种催化剂形态截然不同,前者是均匀单分散的粒子,后者则是呈现聚集态的粒子,原因是前者使用预还原金属作为Au前驱体,从而避免了碳表面金属粒子聚集物的生长[48]。此外,学者还针对性开展了负载Au催化剂在乙二醇液相氧化中的载体效应研究,主要有氧化物(γ-Al2O3、TiO2、CeO2和Fe2O3)和活性炭,见表3。
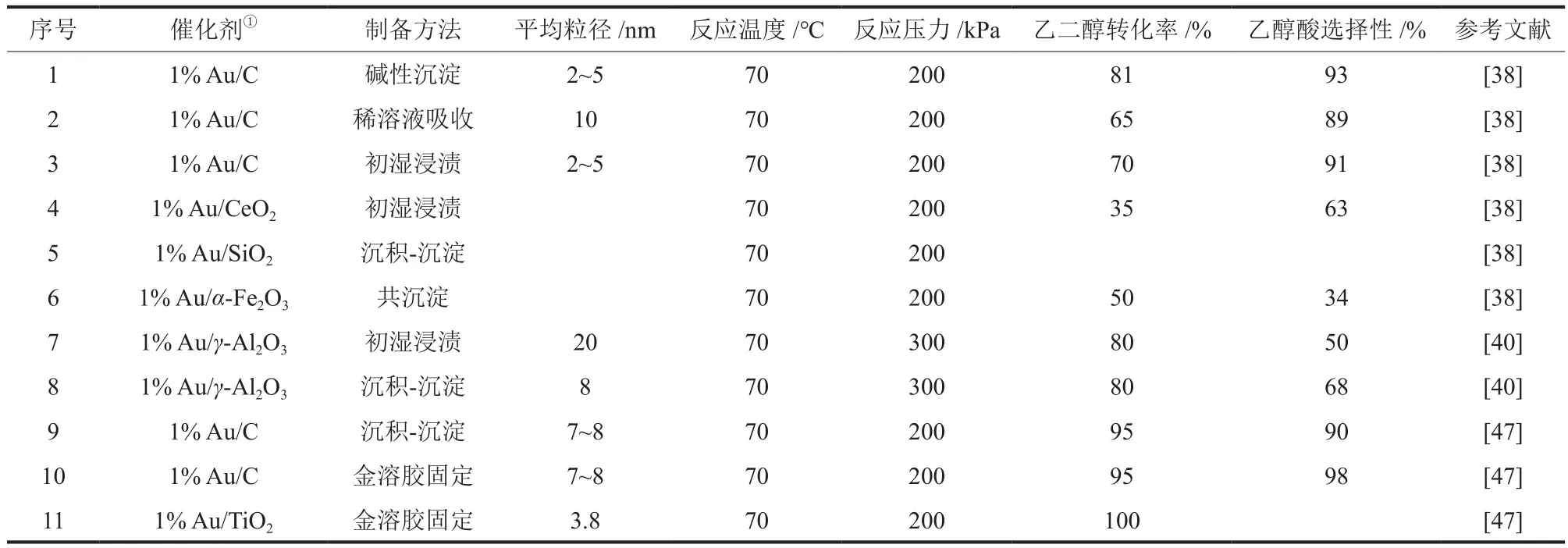
表3 Au纳米颗粒催化乙二醇化学氧化制备乙醇酸(盐)的催化性能Table 3 Catalytic performance of Au nanoparticles in catalytic preparation of glycolic acid (glycolate) by chemical oxidation of ethylene glycol
由表3可知,在相同的载体上、以不同胶体制备的Au催化剂只要具有相似大小的微晶,其在乙二醇氧化中表现出的活性相近,进一步证明了Au分散的重要性[48]。不同载体负载Au的催化效果显示,在研究的Au粒径范围内,氧化物载体通过减小负载颗粒粒径来增加活性,当使用活性碳作为载体时观察到相反的趋势,但平均粒径为7~8 nm的颗粒活性最优。两类载体显示出不同的活性,表明载体在负载Au催化剂中起到了支撑作用[41-49]。
综上,研究人员采用多种方法制备了一系列性能良好的乙二醇化学氧化制备乙醇酸贵金属催化剂。在碱性介质中,负载Au催化剂的稳定性和活性均优于负载Pd或Pt催化剂,原因可能是高度分散的Au纳米颗粒与载体间存在稳定作用力,活性物种既不易流失,也难以发生团聚。负载Pd或Pt催化剂添加Bi助剂后催化性能提高,催化剂寿命延长,原因是Bi与Pd或Pt间存在协同效应,优化了单一金属在催化剂上的分布,抑制了活性组分的团聚、烧结。
2.3 过渡金属与碱协同催化剂
Cu、Ni和Mn等过渡金属盐均具有催化乙二醇化学氧化制备乙醇酸的性能。除化石来源外,乙二醇的另一个稳定来源是可再生生物质资源,可通过充分利用生物质中的氧实现乙二醇在水中向乙醇酸的无氧化转化,而无需额外补充氧化剂[37]。VAN等[32]发现,Cu/CNF和Ni/CNF在无氧条件下将乙二醇转化为乙醇酸,乙醇酸的高选择性与金属催化剂和碱有关。CNF载体的主要优点是在碱性条件下不降解,稳定性较好。150~180 ℃时,在碱性条件下反应15 h,Cu/CNF作为催化剂,乙醇酸的选择性为96%,乙二醇转化率为82%;Ni/CNF作为催化剂,由于产生大量甲酸,乙醇酸选择性仅为31%[32]。SAKHAROV等[43]研究了30~90 ℃时,在二价铜盐(CuCl2·2H2O、CuSO4·5H2O 或 Cu(Ac)2·2H2O)和碱(NaOH或KOH)存在下,选用O2氧化乙二醇水溶液直接生成乙醇酸盐的选择性,当温度为90 ℃时,乙醇酸盐选择性为55.0%,而当温度为30~50 ℃时,乙醇酸盐选择性约为3.5%。
WAⅠBA等[50]以稳定的Mn富土金属络合物([HN(C2H4PPh2)2]Mn(CO)2Br)为催化剂,在低温及惰性Ar气氛下制备了高产率、高选择性的乙醇酸,其中 5 × 10-3mol乙二醇在有机溶剂中,140 ℃下反应9 h,乙二醇转化率为100%,乙醇酸收率> 99%,而以H2O为溶剂时未检测到乙醇酸。
综上,研究人员以Cu、Ni和Mn 3 种过渡金属为活性组分,在碱性介质中用于乙二醇氧化制备乙醇酸反应。以H2O为溶剂时,催化性能排序为Cu盐>Ni盐> Mn络合物,以醇为溶剂时,Mn络合物的催化性能优于Cu盐,具体原因未见报道。当载体可在碱性介质中稳定存在时,Cu负载催化剂催化效果优于非负载催化剂,说明负载型金属催化剂和均相碱的结合对于乙二醇氧化制备乙醇酸反应至关重要。
2.4 双金属组合与碱协同催化剂
双金属组合催化剂在乙二醇化学氧化制备乙醇酸反应中表现优异,双金属组合主要是双贵金属或贵金属与过渡金属组合。乙二醇在单金属Au、Pd、Pt、Mn和Cu催化剂上的化学氧化可生成乙醇酸,与单金属催化剂相比, Au-Pt、Au-Pd和Pt-Pd催化剂在加快氧化速率方面表现出双金属协同效应[18,51]。为了降低贵金属催化剂成本,学者对贵金属与过渡金属组合催化剂展开了研究,SHⅠ 等[18]制备了高活性、高选择性Pt-Fe/CeO2双金属催化剂,用于乙二醇化学氧化制备乙醇酸。目前,双金属组合催化剂,特别是由贵金属和过渡金属构成的双组分核壳催化剂在乙二醇氧化反应中得到了广泛应用,过渡金属组分的引入,提高了催化剂的抗中毒能力。
2.5 无碱介质单贵金属催化剂
强碱性氧化介质通常会导致负载型金属催化剂的结构演变和金属烧结。近3年来学者对无碱介质中提高乙二醇化学氧化制备乙醇酸的贵金属催化剂性能的研究工作已取得了一定的进展。DU等[52]制备了Pt/NaY催化剂,可在无碱介质中催化乙二醇化学氧化制备乙醇酸。ZHOU等[5]使用PtMn/MCM-41纳米催化剂在无碱介质中催化乙二醇化学氧化,乙醇酸产率最高可达86.4%。以上催化剂可在无碱介质中催化乙二醇氧化,是因为界面活性中心强烈的电子耦合效应导致催化剂自激活。
3 结语
本文综述了乙二醇化学氧化制备乙醇酸的催化剂研究进展,包括碱催化剂、碱性介质中贵金属催化剂、过渡金属催化剂以及双金属组合催化剂。分析发现:(1)单独碱或金属催化剂对乙二醇化学氧化制备乙醇酸反应均有一定催化活性,但活性偏低。(2)碱既是乙二醇氧化的激活剂,也是抑制剂。基于此,为提高金属催化剂催化乙二醇氧化的性能,采用恰当浓度的碱与金属形成协同催化剂,催化效果较为理想。(3)由于双金属协同效应,在贵金属中添加合适的第二金属进一步提升了催化效果。
值得关注的是,针对乙二醇化学氧化制备乙醇酸催化剂的研究大部分需要使用碱,而碱性介质导致金属催化剂容易失活、产物后处理成本增加等问题。目前在无碱介质中提高乙二醇氧化效果的催化剂的开发工作处于起步阶段,未来需要深入研究以加深对新催化体系以及反应机理的理解,进而辅助开发可在温和、无碱条件下高效催化乙二醇化学氧化制备乙醇酸的催化剂。
