浅谈环氧乙烷灭菌作为特殊过程在半月板缝合器产品中的过程确认
2022-12-23杨韩丽
杨韩丽
(上海傲派医疗科技有限公司,上海 200000)
半月板缝合器产品属于无菌植入性医疗器械。按照GMP要求,企业应选择适宜的方法对该类产品进行灭菌,明确灭菌工艺和产品无菌保证水平(SAL),并提供灭菌确认的相关研究资料。本次研究在符合生产质量管理规范要求下[1],结合本公司的半月板缝合器产品,描述了半月板缝合器产品灭菌工艺的选择及灭菌确认过程。
1 灭菌工艺的选择
1.1 灭菌方法的研究
无菌医疗器械是一种无活微生物的产品。该类医疗器械灭菌方法的选择是产品设计工艺研究的重要环节,目前可充分参考YY/T 1265—2015、YY/T 1267—2015和YY/T 0884—2013等标准考虑材料与灭菌方法的相容性,并考虑灭菌方法对产品成品(包括包装材料)的适宜性及影响[2]。除此之外,设计开发过程还可以借鉴市场上已有同类产品的灭菌方式,通过对比分析并输出文件资料确定产品最终灭菌方法。
1.2 灭菌方法的选择
半月板缝合器产品主要在经皮或内窥镜下软组织修复手术中作为缝合闭合器使用,主要用于半月板修复重建手术[3]。产品主要由固定棒(聚醚醚酮或其他高分子材料)、缝线(超高分子量聚乙烯或其他材料)、插入器组件(不锈钢)和手柄(ABS)等组成,产品结构如图1所示,且采用单层吸塑盒与Tyvek片材包装。半月板缝合器产品的原材料与常用灭菌方式的相容性总结如表1[4-5]所示。根据YY/T 1431—2016《外科植入物 医用级超高分子量聚乙烯纱线》的附录A.5,超高分子量聚乙烯材质缝线推荐使用环氧乙烷灭菌,同时分析该灭菌方式对半月板缝合器各组成原材料、包装材料、产品结构、产品性能和使用方式等的影响,以及通过国家药品监督管理局数据查询,取得注册证的同类产品大多是环氧乙烷灭菌,最终可得到环氧乙烷灭菌方法适宜半月板缝合器灭菌的结论。

图1 产品结构图
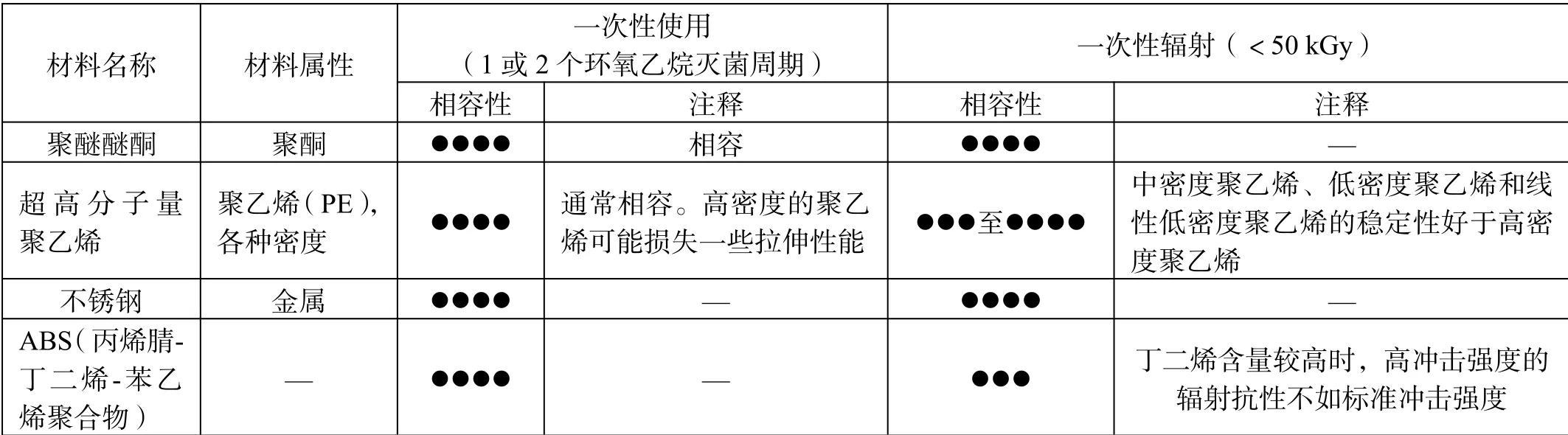
表1 原材料与常用灭菌方式的相容性
2 灭菌过程确认
2.1 灭菌确认的目的
灭菌确认的目的是证明预期灭菌工艺所设定的灭菌工艺过程及参数,能够保证半月板缝合器产品达到公认的无菌保证水平(SAL,等于10-6)[6]及产品性能安全有效。
2.2 灭菌机构的选择
医疗器械制造商往往将灭菌过程作为特殊过程并委托给有能力的环氧乙烷灭菌机构。在正式委托前,需根据质量管理体系要求对灭菌机构进行供方审核,并查验灭菌机构的营业执照及质量体系证书(ISO 11135)等资料,确认资质。同时核查灭菌机构是否按照GB 18279或ISO 11135系列标准的要求对灭菌设备进行定期确认并查看文件资料。签订灭菌委托质量协议后,在委托期间,每年至少进行一次审核。
2.3 产品定义和技术评审
根据GB/T 18279.2—2015/ISO/TS 11135-2:2008第7章要求,产品在灭菌确认前需对产品进行产品定义和技术评审。产品定义是为了了解待灭菌产品的基本信息条件,并通过基本信息条件判定产品是否可划分为一个环氧乙烷产品族。技术评审是对新产品或改进的产品及已确认的产品和/或用于确认现存的环氧乙烷过程的过程挑战装置(PCD)进行比较[7]。本次研究仅针对半月板缝合器的首次灭菌确认,故技术评审仅针对同一注册单元内各规格型号,比较出内部过程挑战装置。
2.3.1 产品定义
半月板缝合器产品定义包括产品的本身、初包装、其他任何附件、说明书及初包装内的其他物品,还包括产品预期功能说明及现有制造和灭菌过程[7]。产品定义过程还应考虑GB/T 18279.2—2015/ISO/TS 11135-2:2008中7.1.1要求。通过产品定义的方式评估半月板缝合器,从产品结构类似、包装方式一致、预期用途一致、制造过程一致、为一次性使用、装载方式一致等方面,可得到结论:一个注册单元内半月板缝合器产品各规格可划分为一个环氧乙烷产品族进行灭菌确认。
2.3.2 技术评审
对半月板缝合器产品进行技术审核,宜从产品结构、产品生物负载、加工方式、产品包装、产品装载评估各规格型号,从比较中选择最难的内部过程挑战装置的规格。新产品首次灭菌确认可参考GB/T 18279.2—2015/ISO/TS 11135-2:2008要求。上海傲派医疗科技有限公司半月板缝合器产品通过技术评审,无法判断出最难的内部过程挑战装置,故依据结构方面的差别,最终选出2种不同规格的产品作为内部过程挑战装置1号(IPCD-1)和内部过程挑战装置2号(IPCD-2),在短周期进行抗性对比得出最难灭菌的内部过程挑战装置。
2.4 灭菌确认
灭菌确认可以证明某一特定过程能够持续和有效地生产出符合无菌保证水平要求的产品[7]。灭菌确认由多个阶段组成:安装鉴定(IQ)和运行鉴定(OQ)、性能鉴定(PQ)[7]。
2.4.1 安装鉴定(IQ)和运行鉴定(OQ)
上海傲派医疗科技有限公司产品灭菌确认是委托有资质的机构共同完成,其中安装和运行鉴定由灭菌机构实施,但医疗器械制造商需监控审核。
灭菌机构提供的安装鉴定报告,上海傲派医疗科技有限公司需按照GB/T 18279.2—2015/ISO/TS 11135-2:2008中9.1要求审核灭菌机构设备的安装是否符合适用的规范和要求[7]。灭菌机构提供的运行鉴定报告,上海傲派医疗科技有限公司需按照GB/T 18279.2—2015/ISO/TS 11135-2:2008中9.2要求审核,重点包含温湿度分布测试、柜室泄漏测试、抽真空速率以及柜室壁温研究[7]。
审核过程中需理解各项要求的审核目的,便于更好地理解灭菌确认过程。
2.4.2 性能鉴定(PQ)
性能鉴定包括进行超出常规监视范围外的严格的微生物和物理测试,以证明灭菌过程的有效性和再现性。性能鉴定通常是在安装和运行鉴定完成后开始的。接受准则宜包括灭菌过程参数和微生物挑战符合规范[7]。
2.4.2.1 性能鉴定——微生物鉴定
微生物性能鉴定(MPQ)通常采用至少有一个参数设置低于正常生产参数值的灭菌过程来实施。最经常调整的参数是气体作用时间、气体浓度和过程温度。选择用于微生物性能鉴定的过程比建立的常规过程参数更具有挑战性(就能达到无菌可能性方面)[7]。微生物挑战通俗可以理解为产品在规定的灭菌参数下均能保证无菌,为了满足灭菌过程杀灭率的保守性确定,上海傲派医疗科技有限公司半月板缝合器选择常用的过度杀灭法:选择较短的EO暴露时间(远远少于半周期循环时间),按照已确认的产品灭菌装载(根据灭菌柜和灭菌托盘规划)放置IPCD和正常生产的产品(产品规格从技术评审可知)、按照GB 18279.1—2015/ISO 11135-1:2007标准中附录C放置EPCD,运行一个短周期。半月板缝合器如上文2.3.2所述,IPCD选择有2种,如图2、图3所示。

图2 IPCD-1示意图

图3 IPCD-2示意图
EPCD的选择有3种,生物指示剂(BI)包装在一层、两层、三层复合薄膜包装内,形式如图4、图5、图6所示。

图4 EPCD-1示意图

图5 EPCD-2示意图

图6 EPCD-3示意图
运行短周期预期达到的结果,EPCD阳性率高于或等于IPCD阳性率[8],从而选择出合适的EPCD和最难灭菌的IPCD,且产品测试结果必须显示无菌。才能证明产品负载的抗性低于PCD的抗性。上海傲派医疗科技有限公司灭菌确认短周期运行结果:产品测试均无菌,IPCD-1为最难灭菌产品,EPCD-1为最合适的日常监测用挑战装置。
2.4.2.2 性能鉴定——物理性能鉴定
物理性能鉴定应证明:①过程再现性,应包括至少3次连续的、有计划的鉴定运行,且满足所有规定的接受准则;②负载满足拟定的常规过程规范规定的接受准则[9]。上海傲派医疗科技有限公司半月板缝合器物理性能鉴定选用的半周期法,是保守性灭菌过程方法——过度杀灭法常采用的方法之一。总共运行3次连续的试验,结果为生物指示剂全部灭活,以确认最小暴露时间。规定的暴露时间至少为此最小时间的2倍[6]。半月板缝合器根据微生物鉴定中最后的选择,半周期3次循环中,按照已确认的灭菌装载放置EPCD与IPCD以及温湿度监控仪(或灭菌柜自带),预期结果为IPCD和EPCD内生物指示剂全部灭活,才能证明产品在日常灭菌过程中能够达到10-6无菌保证水平。上海傲派医疗科技有限公司3次半周期结束,完全达到了预期结果,且核查过程参数均维持在规定范围内。
2.4.3 整周期
在性能鉴定后,需运行至少2次整周期,预期效果为:①过程参数符合规定的灭菌参数过程规范;②PCD无微生物生长;③产品的性能、稳定性和包装完整性在2次灭菌后能符合产品既定的质量要求。此处提及一点,上海傲派医疗科技有限公司产品由于装载一致,故主要从产品性能和包装考虑,选择了具有不同产品性能要求的代表规格运行整周期。整周期结论,上海傲派医疗科技有限公司半月板缝合器产品的PCD无微生物生长,且产品性能和包装在两次灭菌后不影响产品质量,过程参数满足既定规范。
3 总结
产品灭菌除上述环氧乙烷灭菌确认外还包含环残解析验证、日常放行规范、保持灭菌过程有效性等需符合GMP要求,此研究不一一赘述。环氧乙烷灭菌确认是个特殊且复杂的确认过程,依据GB 18279.1—2015/ISO 11135-1:2007标准规定的流程和《医疗器械生产质量管理规范》规定的要求,完成产品环氧乙烷灭菌过程中各流程的确认。以本文的半月板缝合器产品为例,需知悉在实际灭菌确认过程中不同产品要具体分析其灭菌细节,且和灭菌委托机构保持有效沟通。随着医疗器械行业的快速发展,质量管理体系核查愈来愈严格,企业需在产品设计开发过程中充分考虑灭菌方法和确定灭菌供应商,并对产品灭菌过程进行严格的确认和核查,提高企业灭菌确认的技能。
