生物活性炭工艺的除锰效能及作用机制
2022-12-15冯昌龙李聪聪许展鹏
冯昌龙,刘 成,李聪聪,兰 童,许展鹏,陈 卫
(河海大学环境学院,江苏南京 210098)
自来水中的锰含量过高不仅会致使管道结垢、用户端“红水”现象,还会引起一系列的神经及呼吸系统疾病[1]。我国《生活饮用水卫生标准》(GB 5749—2022)明确规定锰质量浓度限值为0.1 mg/L。地下水除锰研究和工程应用较多,涉及到的除锰方法主要包括化学氧化、吸附、离子交换、膜过滤、催化氧化和生物氧化等[2-5],其中生物氧化和催化氧化在目前工程应用中最普遍,且以除锰滤池为主要的应用方式。滤料的种类是影响除锰效果的关键因素,主要有石英砂、锰砂等传统滤料,及聚乙烯球、煤粉球等新型滤料[6-7]。而前者处理效能有限,后者制备复杂、成本高。近年来以水库为典型代表的地表水源水出现了Mn(Ⅱ)周期性超标的现象[8],一般采用“投加氧化剂+过滤”的方式来处理,存在处理成本高、运行效果稳定性差等问题。臭氧-生物活性炭(O3-BAC)工艺是水厂中广泛应用的深度处理工艺,能实现污染物的广谱性去除[9]。初步的研究结果表明,BAC对Mn(Ⅱ)具有一定的去除效果[10],但缺乏BAC除锰的系统性研究,其作用机制及途径也需进一步明确。
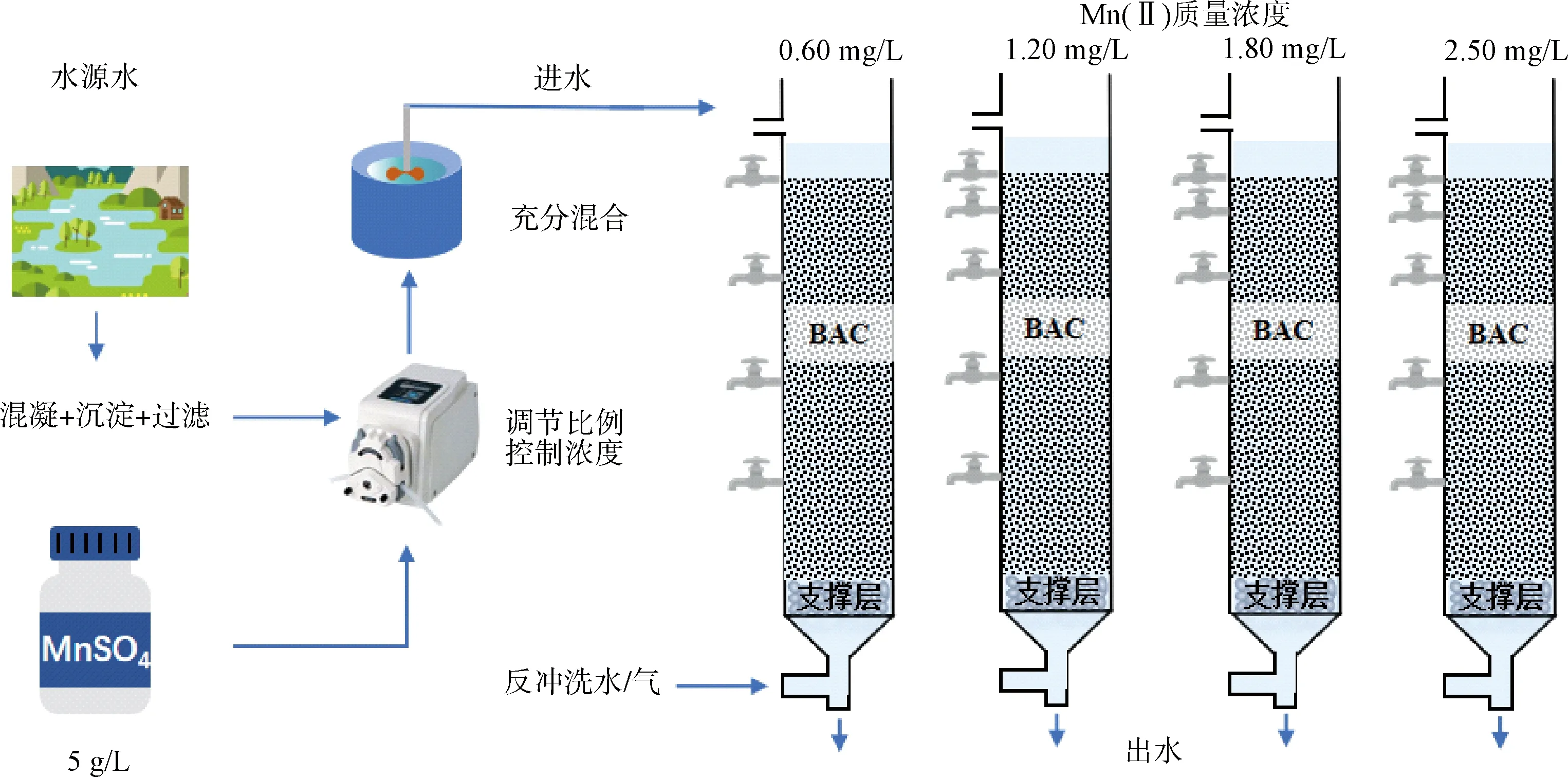
图1 试验流程及装置示意图Fig.1 Schematic Diagram of Test Process and Pilot Units
因此,本文利用水厂实际原水(滤池出水),考察BAC在不同水质条件、运行参数下的除锰效能,并探讨BAC上锰的转化途径及去除机制,进一步分析了其在应用过程中可能存在的问题及解决途径。论文可为锰超标地表水源水的处理提供一定的参考。
1 材料与方法
1.1 进水及材料
待处理原水取自太湖流域某水厂滤后水,投加MnSO4配制相应浓度的含锰原水,具体水质如表1所示。
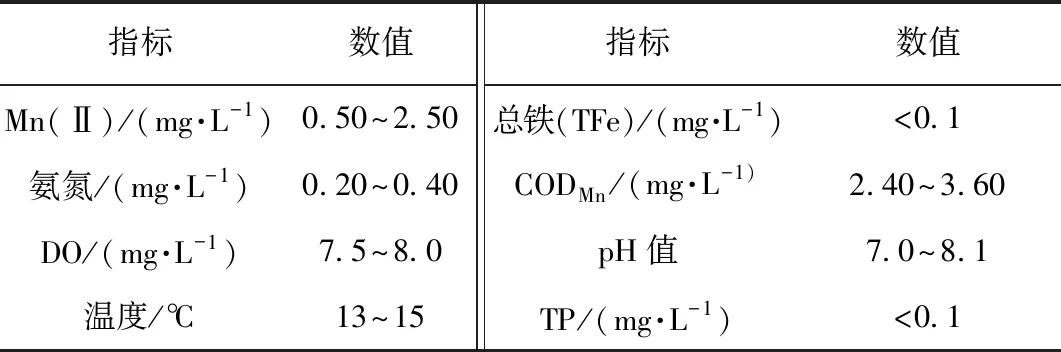
表1 进水水质Tab.1 Inflow Water Quality
试验过程中使用的HCl、H2SO4、(NH4)2S2O8、KMnO4等药品均为分析纯或化学纯。使用Mill-Q系统制备试验用超纯水。
1.2 试验装置及流程
如图1所示,装置由内径为40 mm、高度为1.5 m的PVC柱搭建。BAC填料采用新的颗粒活性炭(GAC),粒径为8~30目,填充深度为1.2 m。滤柱自下而上每间隔0.3 m设有取样口,底部填充0.1 m粒径为1~3 mm的石英砂作为支撑垫层。
1.3 试验方法
装置采用下向流方式运行,利用蠕动泵将滤后水和MnSO4母液(5 g/L)按比例泵入进水管道(锰质量浓度控制在0.60、1.20、1.80、2.50 mg/L),经充分混合后流进BAC柱。反洗周期设定为10 d,反冲程序为“气冲2 min-气水联合反冲4 min-水冲6 min”。其中气冲强度为10 L/(s·m2),水冲强度为5 L/(s·m2)。滤速设置在6~15 m/h,每个工况条件连续运行90 d,期间每2 d取水样测定Mn(Ⅱ)浓度,每隔5 d收集BAC样品,测定相应指标。
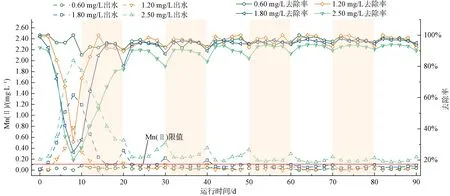
图2 不同进水Mn(Ⅱ)浓度下BAC工艺的出水水质及Mn(Ⅱ)去除率 (滤速为12 m/h)Fig.2 Treated Water Quality and Mn(Ⅱ) Removal Rate of BAC Process under Different Inflow Mn(Ⅱ) Concentrations (Filtration Rate Was 12 m/h)
1.4 测定及分析方法
Mn(Ⅱ)浓度测定:取样后3 h内使用过硫酸铵-分光光度法测定。
BAC颗粒的吸附及氧化能力测定:使用氮气吸附法测定总孔容积,2,2’-联氮-双(3-乙基苯并噻唑啉-6-磺酸)(ABTS)显色法测定漆酶(MCOs)活性[11]。
BAC颗粒上的锰形态测定:针对BAC样品,使用“四步连续提取”及“亮柏蓝染色法”对不同存在方式的锰提取测定,实现单位质量BAC上“自由态、吸附态、生物态和氧化态”的锰脱附及定量[12]。
BAC颗粒上的锰氧化物(MnOx):利用扫描电子显微镜-能谱分析(SEM-EDS,S4800,Hitachi)对其表面形貌和元素分布进行了表征。
微生物群落和Mn(Ⅱ)氧化基因的丰度:高通量测序技术(16S rRNA基因扩增和宏基因组测序)。样本的宏基因组数据与自定义Mn(Ⅱ)氧化基因数据库对齐,以获得每个目标基因的丰度。SOAPaligner软件用于量化每个样本中Mn(Ⅱ)氧化基因的丰度。基因丰度的计算方法如式(1)。
(1)
其中:RPKMi——每千碱基每百万次映射读取的读取数;
Ri、∑Rj和Li——映射到给定单基因的读取数、映射到所有单基因的读取数和给定单基因的总长度。
2 结果
2.1 BAC工艺的除锰效能
除锰滤池的效能一般会受到进水水质、滤速等因素的影响[5],因此,考察了BAC工艺在不同进水Mn(Ⅱ)浓度及滤速下的除锰效能,结果如下。
2.1.1 不同进水Mn(Ⅱ)浓度下的除锰效能
考察了不同进水Mn(Ⅱ)浓度下BAC的除锰效果,结果如图2所示。
BAC工艺的启动期与进水中Mn(Ⅱ)含量直接相关,较高的进水Mn(Ⅱ)含量会导致启动时间明显延长,进水Mn(Ⅱ)质量浓度为2.50 mg/L时的启动期达到22 d,但相较于锰砂滤池60~100 d的启动期[1]短很多,并可省略回流、降低滤速等针对性操作。稳定运行期间,BAC工艺对质量浓度为0.60~1.80 mg/L的Mn(Ⅱ)的去除率稳定在95.00%以上,出水中Mn(Ⅱ)含量降低至0.09 mg/L以下。在2.50 mg/L的高Mn(Ⅱ)质量浓度下,BAC工艺仍能保持90.00%以上的去除率。这与已有的针对锰砂滤池除锰的研究结果有一定差别(进水Mn(Ⅱ)质量浓度超过1.80 mg/L时,去除率小于80%[5])。这是由于BAC表面的微生物丰度高、种群丰富,对高Mn(Ⅱ)环境有更好的适应性,还能实现Mn(Ⅱ)的协同氧化[13]。
图1还可以看出,反冲洗后,Mn(Ⅱ)去除率均有一定程度的下降,并在1~2 d后恢复。原因可能在于反冲洗会冲刷掉BAC上附着的部分锰氧化细菌(MnOB)。随着运行时间延长,反冲洗对除锰效果产生的负面影响逐步减弱。
2.1.2 不同滤速下的除锰效能
考察了不同滤速下BAC的除锰效果,结果如图3所示。
随着滤速增加,BAC工艺的启动时间变长,除锰效能减弱。滤速由6 m/h增至12 m/h时,启动时间由9 d增至11 d,但稳定运行期间Mn(Ⅱ)的平均去除率仍高达96.33%。由于材料特性限制,大多数单级锰砂滤池的运行流速在6~8 m/h[5]。滤速提高时,滤料与水中Mn(Ⅱ)的接触、反应时间更加短暂。反应时间、温度等条件一定时,微生物将Mn(Ⅱ)氧化为Mn(Ⅳ)的速率理论上是非生物氧化的10~106倍,且更加彻底[14]。因此,BAC工艺能在滤速12 m/h下运行,很大程度上是由于其粗糙的表面有利于生物附着,丰富的孔隙、沟壑能在水流冲击时为微生物提供保护,保障了生物Mn(Ⅱ)氧化的活跃发生。这也意味着相同处理负荷下,BAC工艺比锰砂滤池占地面积更小,建设和运行成本更低。然而,滤速过大时,水流的剪切作用会破坏BAC滤层的稳定性,影响MnOB的定殖。试验表明,滤速增至15 m/h时,BAC工艺的出水水质明显变差。故此后的研究、应用宜将滤速控制在15 m/h以内。
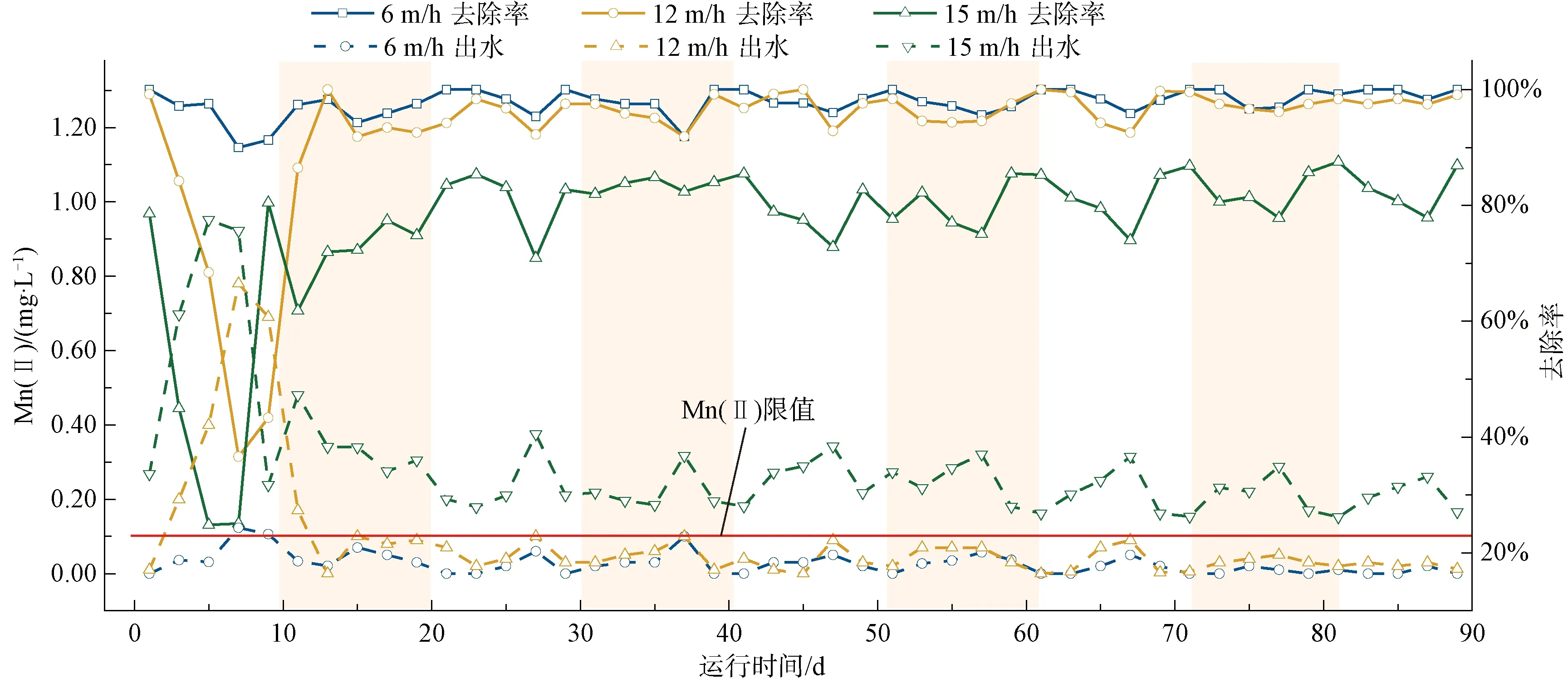
图3 不同滤速下BAC工艺的出水水质及Mn(Ⅱ)去除率 [进水Mn(Ⅱ)质量浓度为1.20 mg/L]Fig.3 Treated Water Quality and Mn(Ⅱ) Removal Rate of BAC Process under Different Filtering Rates [Inflow Mn(Ⅱ) Mass Concentration Was 1.20 mg/L]
2.2 BAC除锰机制探讨
传统锰砂滤池中,MnOx催化氧化和MnOB生物氧化在除锰过程中的主导地位仍存在争议。BAC的材料特性及生物赋存能力与砂质滤料存在差异,其除锰机制需要进一步探讨。
2.2.1 锰归趋及MnOx特征
为了明确锰在BAC工艺内的归趋,对BAC上的残余态、吸附态及生物态的锰含量及其转化情况进行了测定,结果如图4所示。
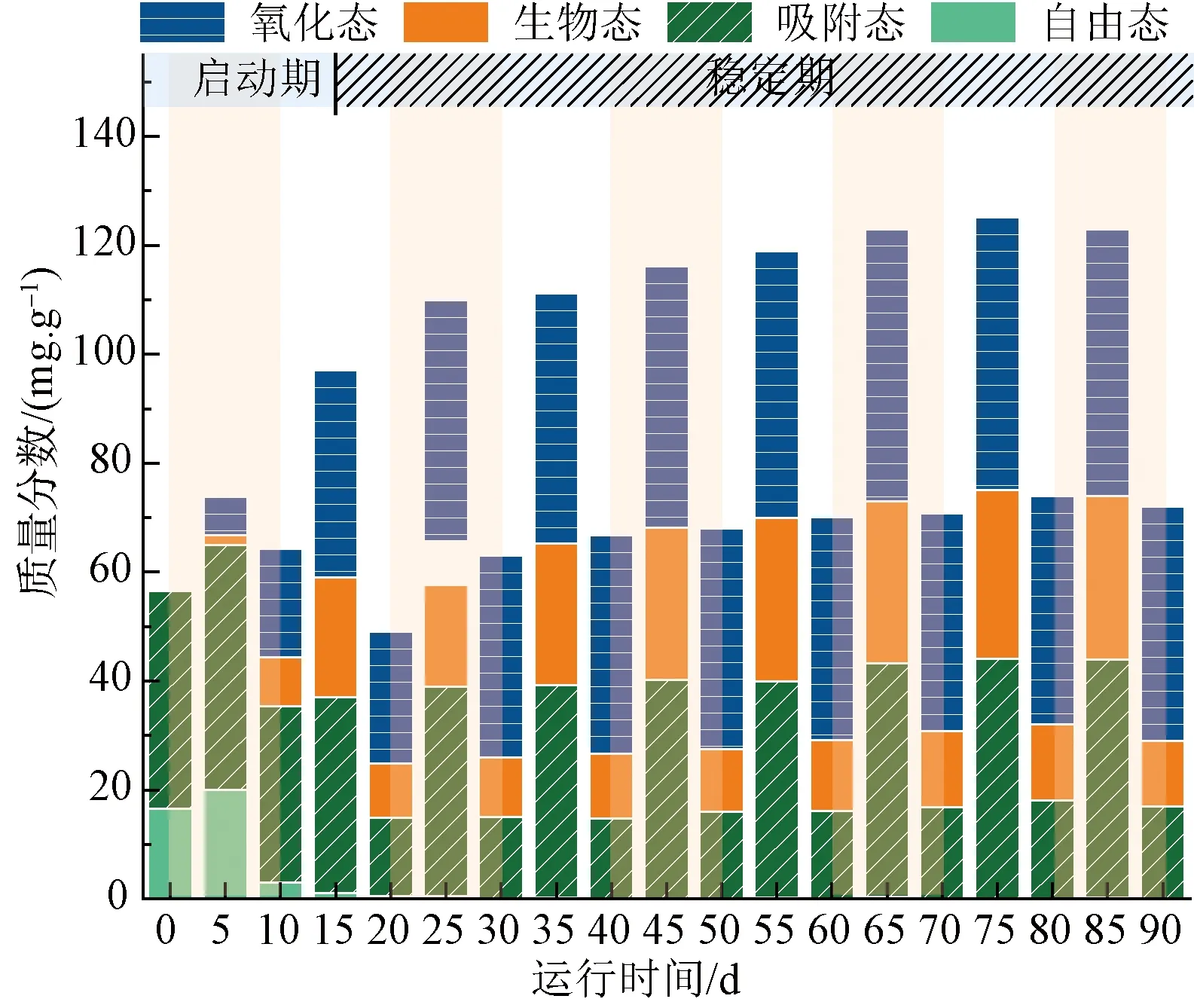
图4 BAC工艺中锰的归趋转化 [进水Mn(Ⅱ)质量浓度为1.2 mg/L,滤速为12 m/h]Fig.4 Preservation and Conversion of Manganese in BAC Process [Inflow Mn(Ⅱ) Mass Concentration Was 1.2 mg/L, Filtration Rate Was 12 m/h]
启动期的锰主要以吸附态和自由态存在,两者第5 d达到最高值,与2.1小节中出水Mn(Ⅱ)峰值的出现时间接近,表明BAC出现了吸附饱和现象。而此时氧化态与生物态的锰含量小于12%,MnOB的氧化作用很弱,无法及时释放吸附位点。运行第5~15 d,随着氧化锰和生物锰占比由12%增至62%,BAC上的锰赋存总量增加,出水Mn(Ⅱ)含量降低。这表明MnOx和MnOB在除锰过程中发挥了积极作用。稳定运行期间,BAC能够赋存110~120 mg/g的锰,较传统砂质滤料显著增加[15]。每隔10 d进行反冲洗,由图4可以看出,反冲洗通过去除吸附态和生物态锰释放41%~49%的锰容量,从而实现“高效吸附-氧化赋存-脱附更新”持续发生。
使用SEM-EDS表征BAC上的MnOx的形态特征、元素组成,以验证锰的归趋转化。原始BAC表面有很多孔隙和沟壑结构[图5 (a)],具备良好的Mn(Ⅱ)吸附和MnOB富集潜能。第10 d的BAC样品[图5 (b)]上出现的疏松絮状结构是物理化学来源的MnOx[11],证明非生物作用在启动阶段发挥了主要作用。第50 d,MnOx转化为带有球型颗粒的不规则立体结构[图5 (c)],是生物源锰氧化物(BMO)的典型特征[16],证明锰氧化过程中微生物的参与变多。BMO的立体结构利于BAC颗粒与Mn(Ⅱ)反应,还可为MnOB提供增殖场所,催化Mn(Ⅱ)的氧化[17]。EDS映射中,Mn元素占比由10 d的26%提升至43%,也证明了这点。

图5 BAC表面MnOx的形态特征Fig.5 Characteristics of MnOx on the Surface of BAC
2.2.2 BAC除锰的主要途径分析
如前所述,吸附态、氧化态和生物态的锰在BAC上共存,即非生物作用(吸附、催化氧化)和生物作用在BAC工艺中均存在。分别对两种作用的实现途径进行分析。
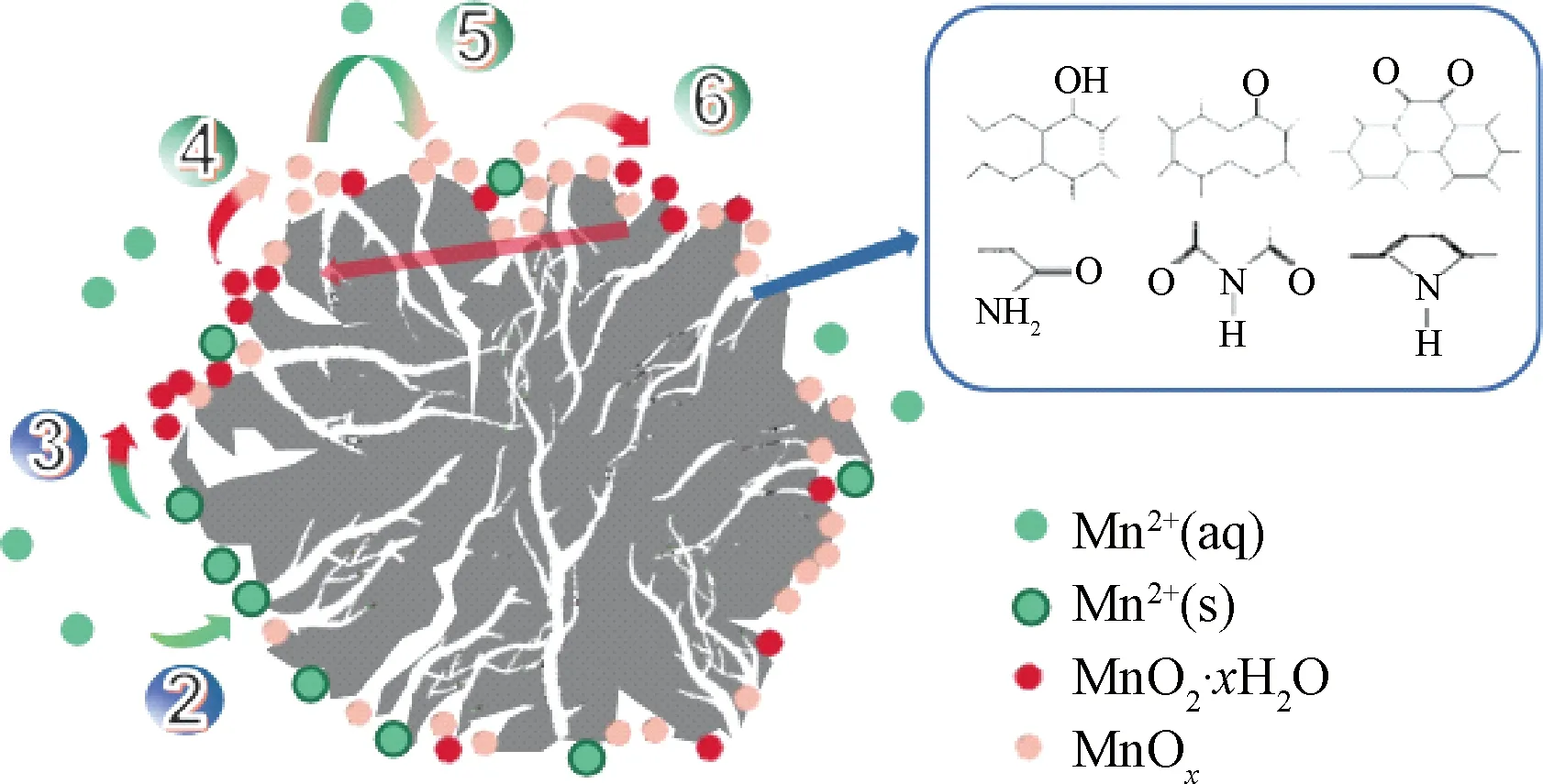
图6 BAC上的非生物除锰过程Fig.6 Abiotic Manganese Removal Processes on BAC
如图6所示,BAC上的非生物作用包括吸附和自然氧化[式(2)、式(3)]、催化氧化[式(4)~式(6)]。前者主要受水体pH和氧化还原电位影响,后者主要受Mn(Ⅱ)和MnOx含量影响[18]。BAC表面丰富的孔隙结构和碱性官能团(酚羟基、羰基、醌基等)有利于Mn(Ⅱ)的吸附和自然氧化,优异的MnOx持附能力加快了催化氧化反应,从而促进了滤池的启动。然而,非生物除锰过程易受吸附位点数量和pH环境的影响,稳定性较差。2.2.1小节中锰归趋及MnOx特征的变化也表明,随着运行时间的增加,微生物在除锰过程中发挥的作用更加明显。
(2)
Mn2++O2+(x+1)H2O→MnO2·xH2O+2H+
(3)
(4)
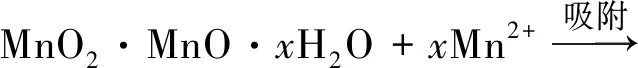
(5)
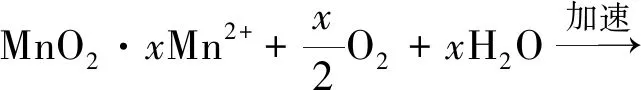
(6)
为验证生物氧化在BAC除锰过程中的作用,考察了MnOB的优势地位及氧化酶活性。16 S rRNA测序结果如表2所示,稳定运行期内,滤池深度为30、60、90 cm处(编号B1、B2、B3)的BAC上丰度前5的菌属均为分枝杆菌(Bacillus)、生丝微菌、硝化螺旋菌、土微菌(Pedomicrobium)和鞘脂单胞菌,它们都已被证明是MnOB[19]。相比之下,砂质填料上的MnOB种类和相对丰度都更低[1,20],这也造成了两者在除锰效能上的差距。多数MnOB通过多铜氧化酶(MCOs)氧化Mn(Ⅱ),故MCOs的丰度可以很好地衡量MnOB的氧化能力。如图7所示,BAC池中检测到6种MCOs(mnxG、mcoA、cumA、moxA、cueO和cotA),它们介导了Pedomicrobium、Bacillus等MnOB的Mn(Ⅱ)氧化过程[19]。综上,BAC上的MnOB优势地位明显,其多种属共存、多途径作用的特征保障了不同条件下BAC工艺的高效稳定除Mn(Ⅱ)。
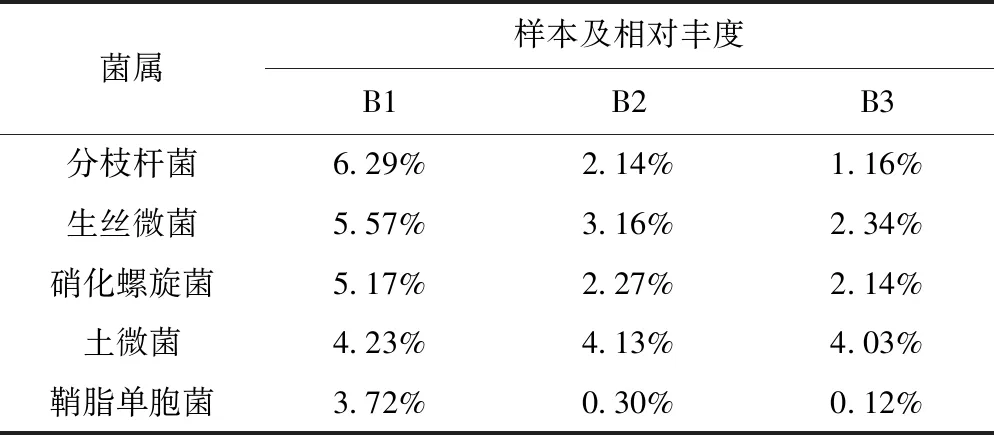
表2 滤池不同深度BAC上的MnOB占比及其与已有研究的比较Tab.2 Proportion of MnOB on BAC under Different Depths in Filter
已有研究[18]指出,生物Mn(Ⅱ)氧化过程传质效率高、对pH依赖性小,主导了滤池中的Mn(Ⅱ)氧化。本研究中,BAC上MnOB及MCOs的富集也证明了稳定运行期内的生物氧化发挥了重要作用,但其主导地位仍需进一步明确。
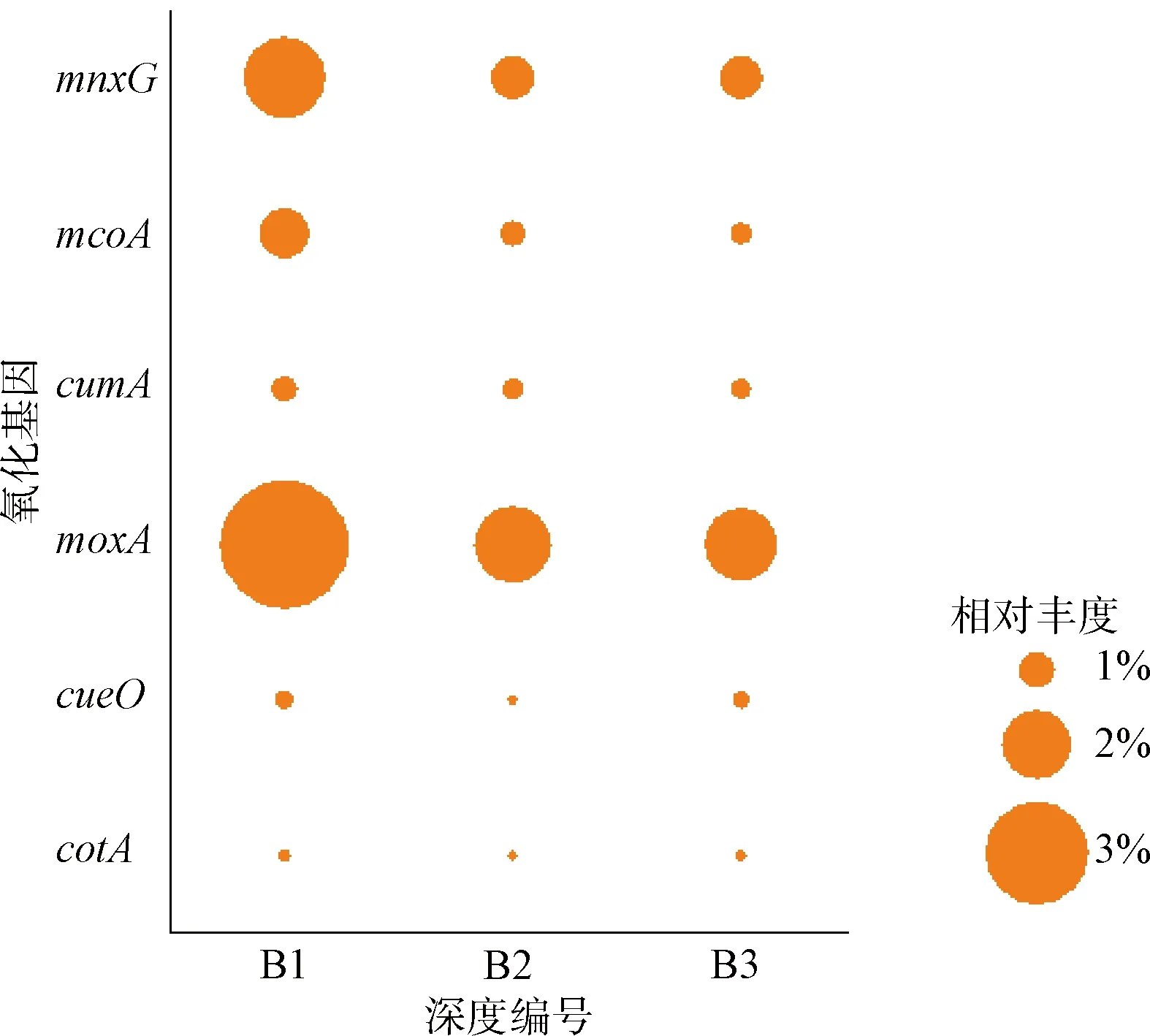
图7 BAC上的Mn(Ⅱ)氧化基因类型及丰度Fig.7 Types and Abundance of Mn(Ⅱ) Oxidation Genes on BAC
2.2.3 稳定运行期间生物氧化主导地位的确立
使用BAC的总孔容积、MnOx含量分别代表吸附、催化氧化作用,MnOB丰度和MCOs活性代表生物氧化作用。稳定运行期内多次取样并测定上述指标,分析它们与滤层的Mn(Ⅱ)氧化能力之间的相关性,结果如图8所示。
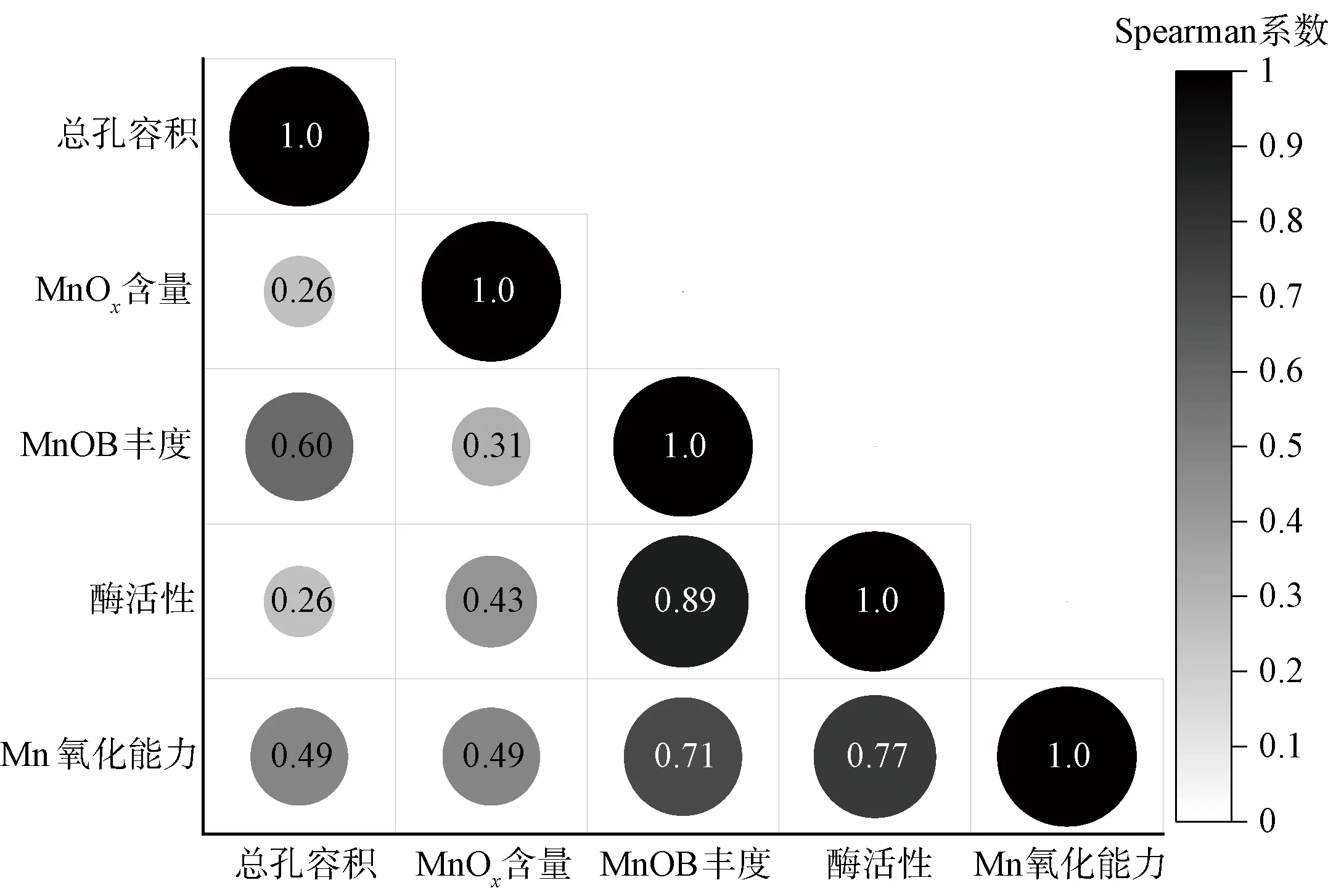
图8 BAC总孔容积、MnOx含量、MnOB丰度、MCOs活性与除Mn(Ⅱ)能力的相关性Fig.8 Correlation among Total Pore Volume,MnOx Content,MnOB Abundance,MCOs Activity and Mn(Ⅱ) Removal Capacity of BAC
可以看出,稳定运行期内BAC的Mn(Ⅱ)氧化能力与总孔容积、MnOx含量的相关性较差,即吸附和催化氧化在BAC除锰过程中发挥的作用有限。而BAC的Mn(Ⅱ)氧化能力与MnOB丰度、MCOs活性的Spearman系数分别为0.71、0.77,相关性显著,表明稳定运行期内生物氧化在BAC除锰过程中占主导地位。
3 BAC工艺除锰存在的问题及解决途径
地表水中的Mn(Ⅱ)含量波动大,常出现季节性超标现象。因此,进一步考察了进水Mn(Ⅱ)含量动态变化时BAC工艺的除锰效能,提出并验证了针对性的强化途径。
3.1 进水Mn(Ⅱ)含量变化时的除锰效能
针对季节性锰超标——“Mn(Ⅱ)浓度突然增加,持续1~2个月后消失”的水质特征,考察了BAC工艺在Mn(Ⅱ)突发时的净化效能和Mn(Ⅱ)负荷消失后的释锰风险,结果如图9所示。
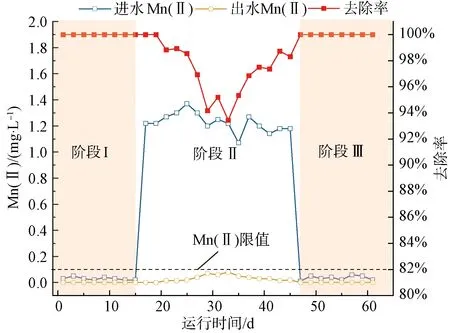
图9 进水Mn(Ⅱ)含量变化时BAC工艺的除锰效能[滤速为12 m/h,阶段I、Ⅲ不投加Mn(Ⅱ);阶段Ⅱ投加1.2 mg/L的Mn(Ⅱ)]Fig.9 Manganese Removal Efficiency of BAC Process as Inflow Mn(Ⅱ) Concentration Changes [Filter Rate Was 12 m/h,No Mn(Ⅱ) Dosage in Stage I and Ⅲ;Stage Ⅱ Added 1.2 mg/L Mn(Ⅱ)]
如图9所示,进水Mn(Ⅱ)质量浓度突增至1.20 mg/L时(阶段Ⅱ),Mn(Ⅱ)去除率出现了明显的波动,出水Mn(Ⅱ)浓度先升高后降低,最高值已接近0.10 mg/L的限值。这表明突增的Mn(Ⅱ)负荷对BAC上的敏感菌群造成了负面影响。第36 d后,出水中Mn(Ⅱ)逐渐降低,说明BAC工艺具备一定的自我调控能力。然而,如试验所示,调控的周期长达30 d,且周期内除锰效能稳定性很差。这是由于BAC工艺的自我调控基于群落的稳态恢复以及富Mn(Ⅱ)环境对MnOB的定向筛选[21]实现,是一种缓慢的被动调控。考虑到实际应用需求,为充分保障出水水质稳定,需要进行针对性的强化。
此外,BAC对MnOx的持附能力强,Mn(Ⅱ)负荷消失后(阶段Ⅲ),出水Mn(Ⅱ)质量浓度维持在0.02 mg/L以下,基本不存在释锰现象。
3.2 O3-BAC工艺强化除锰
深度处理中,常将O3作为BAC的前置氧化单元(即O3-BAC工艺),以实现污染物的预氧化,提高整体工艺的去除效能。因此,考察了O3-BAC工艺在进水Mn(Ⅱ)稳定及动态变化下的除锰效能及稳定性。
如图10(a)所示,进水Mn(Ⅱ)浓度稳定时,O3前处理能够有效提升BAC对Mn(Ⅱ)的去除效果,将出水中的Mn(Ⅱ)质量浓度稳定控制在0.05 mg/L以下。由沿程Mn(Ⅱ)浓度变化可知,O3发挥了氧化剂作用,将25%~30%的Mn(Ⅱ)氧化为MnOx,配合后续BAC工艺,实现了Mn(Ⅱ)去除效果的提升。
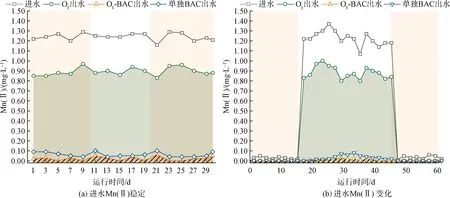
图10 BAC/O3-BAC工艺的除锰效能 (O3投加量为1.0 mg/L,接触时间为10 min,滤速为12 m/h)Fig.10 Manganese Removal Efficiency of BAC/O3-BAC (Dosage of O3 Was 1.0 mg/L,Contact Time Was 10 min,Filtration Rate Was 12 m/h)
如图10(b)所示,进水Mn(Ⅱ)浓度突增时,O3-BAC工艺的除锰稳定性较单独BAC工艺有了显著提升。一方面,O3氧化了进水中的部分Mn(Ⅱ),降低了后续BAC工艺的处理负荷,便于其进行自我调控;另一方面,O3氧化生成的MnOx呈特殊的片层富羟基结构,具备吸附和催化氧化的能力[2],其被BAC截留后,能够形成“活性滤膜”,有利于MnOB的富集和传质。此外,O3-BAC工艺除Mn(Ⅱ)时,可以根据进水Mn(Ⅱ)浓度变化调整O3工艺的启闭及投加量,实现高效、迅速的主动调控。
3.3 原水中有机物、氨氮对BAC除Mn(Ⅱ)效能的影响
地表水水质条件易受外界环境影响,在Mn(Ⅱ)超标的同时还存在氨氮、高锰酸盐指数(CODMn)为代表的相关有机污染,如哈尔滨、甘肃、宁夏等地区。鉴于此,考察了氨氮、CODMn对BAC除Mn(Ⅱ)效能的影响。
参考已有研究中的较不利条件,保持进水中的Mn(Ⅱ)质量浓度为1.80 mg/L,通过投加NH4Cl和腐殖酸(HA)将氨氮、CODMn的质量浓度分别调整为1.00、4.00 mg/L,考察BAC对各类污染物的去除效能,结果如图11所示。由图11(a)可知,进水中的氨氮、CODMn对Mn(Ⅱ)的去除有显著影响。第6 d投加NH4Cl、HA后,Mn(Ⅱ)的去除率显著下降,并在18 d后稳定在90.00%左右,出水质量浓度已超过0.10 mg/L的限值。如图11(b)、图11(c)所示,BAC对氨氮、CODMn的去除效能良好,出水满足相应限值要求。BAC可能优先选择性去除氨氮、CODMn。这也表明微污染原水条件下,滤池出水是否达标的决定性因素为Mn(Ⅱ)。为保障出水达标,于第20 d反冲后将滤速由12 m/h降低至6 m/h。可以看出,降低滤速后,3种污染物的去除率均有所上升,出水中Mn(Ⅱ)质量浓度逐渐稳定低于0.10 mg/L。因此,在微污染原水条件下,适当调整BAC工艺的运行流速,可以保障出水的水质稳定。
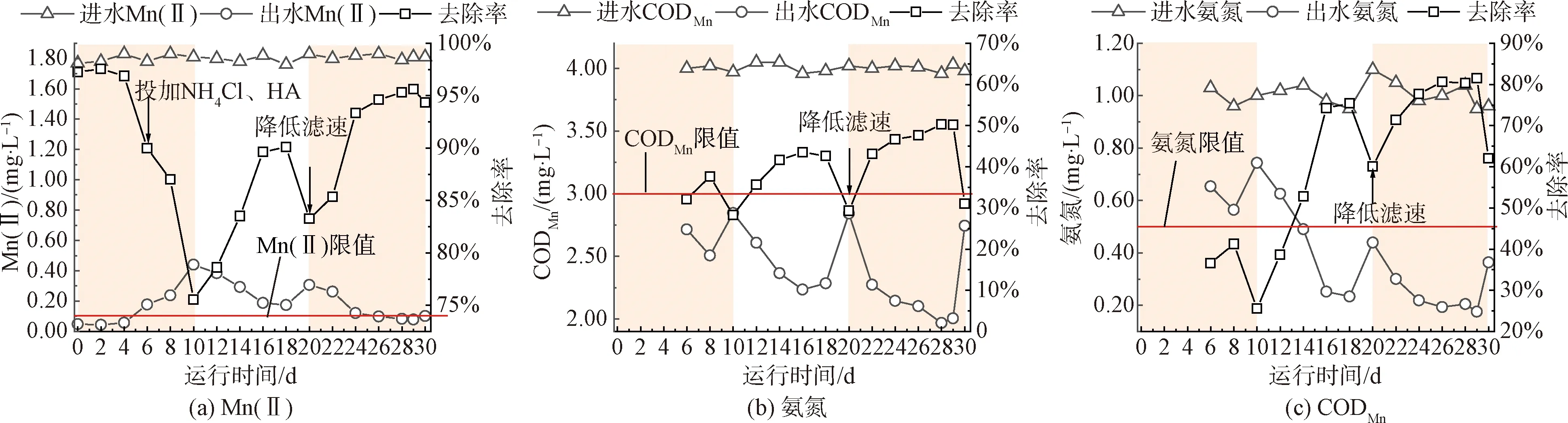
图11 进水中同时存在Mn(Ⅱ)、氨氮、CODMn时BAC对污染物的去除效能Fig.11 Removal Efficiency of BAC on Pollutants as Mn(Ⅱ),Ammonia Nitrogen and CODMn Existing in Inflow Simultaneously
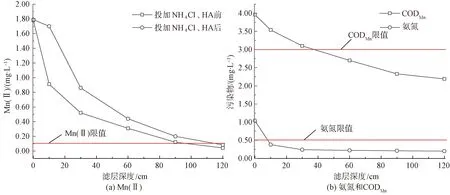
图12 污染物在BAC工艺中的沿层去除Fig.12 Removal of Pollutants along Filter Layer in BAC Process
为探究BAC工艺对3种污染物的去除选择性,进一步考察了它们在滤层沿程的去除情况,结果如图12所示。由图12(a)可知,投加NH4Cl、HA后,Mn(Ⅱ)从10 cm以下的滤层才开始去除,明显滞后于进水中只含Mn(Ⅱ)的情况,这直接导致了出水Mn(Ⅱ)浓度的增高。图12(b)中,氨氮的质量浓度在表层10 cm迅速降低至0.35 mg/L。这说明BAC滤层出现了功能分区,并优先降解氨氮。只有氨氮降低到一定浓度之下,Mn(Ⅱ)才能够被去除。相比之下,CODMn则在整个滤层内逐渐降低,说明有机物可以与氨氮、Mn(Ⅱ)同步去除。这与张建林等[22]得出的结论类似。这是由于Mn(Ⅱ)和发生氧化还原的电位值要求较高(>400 mV),而氨氮只需要200~400 mV,两者共存时氨氧化微生物更易形成优势地位。因此,BAC池的除Mn(Ⅱ)效能受氨氮影响很大,应用中需密切关注进水中氨氮的浓度。
4 结论
本文建立了小试规模的下向流BAC池,并连续运行了90 d。通过测定BAC工艺在不同条件下的处理效能,明确该过程中Mn(Ⅱ)赋存、转化特征及途径,得出以下结论。
(1)BAC工艺具有良好的除锰效能,其除锰效果与进水Mn(Ⅱ)浓度、运行流速密切相关,BAC工艺在进水Mn(Ⅱ)质量浓度为0.60~1.80 mg/L、流速不超过12 m/h时均能自然挂膜,高效除Mn(Ⅱ),对Mn(Ⅱ)超标水源水具有广泛适用性,且占地面积小,建设和运行成本低。
(2)启动期,锰主要存在于吸附和自由态,以疏松絮状的MnOx附着在BAC上;稳定运行期,锰主要存在于氧化和生物态,以不规则立体网状的BMO附着在BAC上。反冲洗通过去除吸附态和生物态锰,释放41%~49%的锰容量,保障除Mn(Ⅱ)过程的持续发生。
(3)BAC工艺的除锰途径包括吸附、催化氧化及生物氧化。BAC良好的吸附效能及丰富的表面官能团有利于Mn(Ⅱ)和MnOx附着,加快了催化氧化反应,缩短了滤池的启动时间。稳定运行期内,BAC上的除锰过程由生物氧化主导,其表面存在的5种MnOB和6种MCOs保障了不同条件下除锰过程的高效、稳定。
(4)Mn(Ⅱ)负荷消失后,BAC工艺基本不存在释锰风险,但其在进水Mn(Ⅱ)浓度突增时存在适应周期长(30 d)、除锰效能有一定波动的问题。试验表明,使用前置O3氧化强化BAC(即O3-BAC)除锰工艺,不仅能够在进水Mn(Ⅱ)浓度稳定时有效提升Mn(Ⅱ)的去除效果,将出水中的Mn(Ⅱ)质量浓度稳定控制在0.05 mg/L以下;还能在进水Mn(Ⅱ)浓度突增时实现高效、迅速的主动调控,增强整体工艺的除锰稳定性。
(5)原水的氨氮、有机物会对BAC工艺的除Mn(Ⅱ)效能产生一定的影响。微污染原水条件下,滤池出水是否达标的决定性因素仍为Mn(Ⅱ)。此条件下,适当降低滤速可以保障出水的水质稳定。氨氮的氧化顺序较Mn(Ⅱ)更加靠前,对Mn(Ⅱ)的氧化影响很大,应用过程中需密切关注进水中氨氮的浓度,防止Mn(Ⅱ)穿透滤层。
