读图识图 理解振荡反应的周期性
——深度剖析一道化学选考试题
2022-12-10廖旭杲
廖旭杲
(浙江省宁波市鄞州中学 315104)
科学在于简洁,行文也如此,大凡能用图表传达的,就毋需文字赘述,以达图文并茂而言简意赅之效果.高考命题专家深谙此理,近年不少选考化学试题信息多以图表形式呈现,要求学生读图识表,解图析表,理解并接受图表中蕴含的信息,据此进一步分析推理,解答相关问题.兹举一例加以说明之.
2021年6月浙江省选考化学试题第29题是一道关于化学反应原理的大题,满分10分,考生普遍反映题面新颖,不易拿全分,考后有不少师生在研究该题,也有各种解析在网上或报刊中刊载,有些语焉不详,尤其是如何理解热交换过程,如何理解振荡反应的周期性等难点问题不少学生还是困惑不已,笔者试图对此作一分析,供大家继续讨论.
试题(2021年6月·浙江选考·29)含硫化合物是实验室和工业上的常用化学品.请回答:


①该温度下反应的平衡常数为____.
②平衡时SO2的转化率为____.
(3)工业上主要采用接触法由含硫矿石制备硫酸.
①下列说法正确的是____.
A.须采用高温高压的反应条件使SO2氧化为SO3
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和SO2的转化率
D.在吸收塔中宜采用水或稀硫酸吸收SO3以提高吸收速率
②接触室结构如图1所示,其中1~4表示催化剂层.图2所示进程中表示热交换过程的是____.
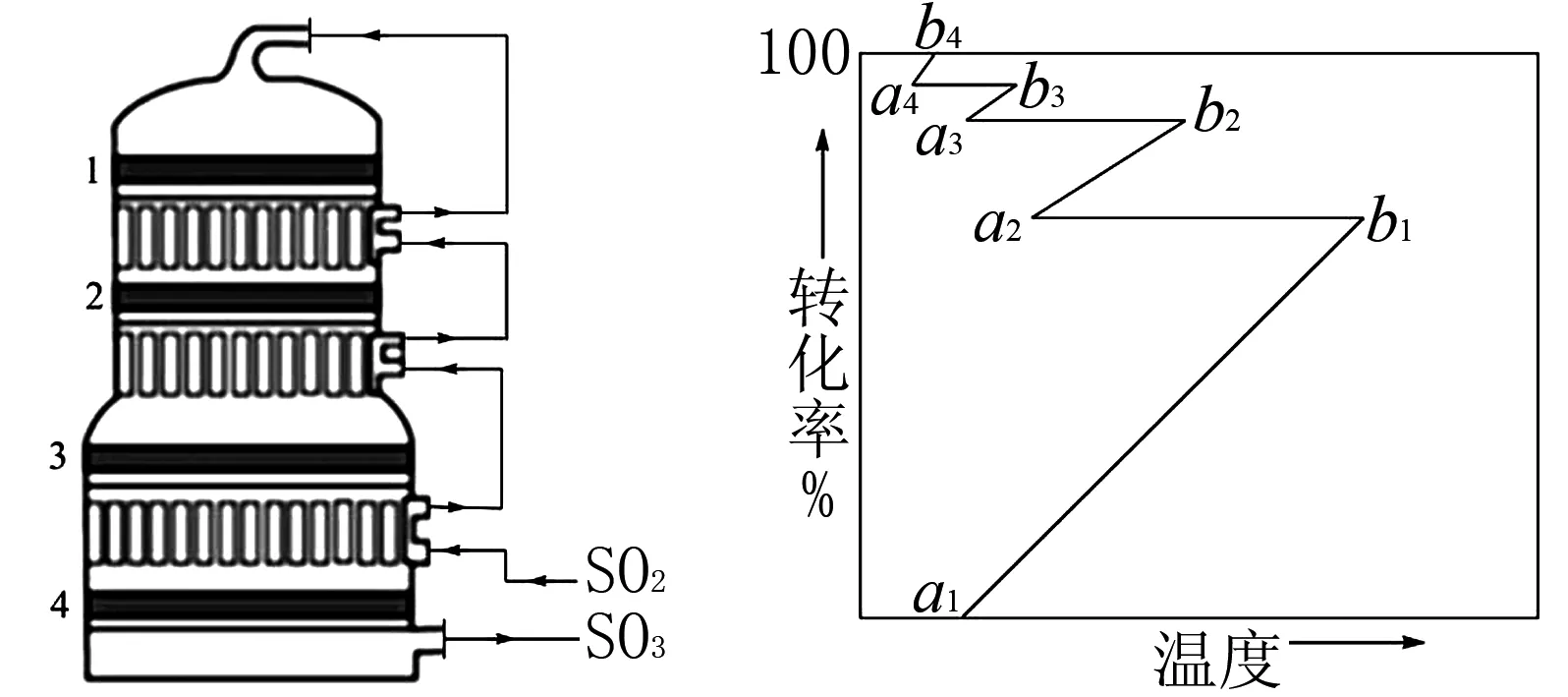
图1 图2
A.a1→b1B.b1→a2C.a2→b2D.b2→a3E.a3→b3F.b3→a4G.a4→b4


图3
(4)一定条件下,在Na2S-H2SO4-H2O2溶液体系中,检测得到pH-时间振荡曲线如图4,同时观察到体系由澄清→浑浊→澄清的周期性变化.可用一组离子方程式表示每一个周期内的反应进程,请补充其中的2个离子方程式.

图4

Ⅱ.①____

Ⅳ.②____
解析(1)第一小题就可能刚好戳中一些学生的软肋:对该反应常温下不反应,需要加热才有现象,高中教师再三强调,部分同学对此印象深刻,所以他们认为该反应常温下不自发,高温才自发,但是寻找理由时,又看出ΔS>0,且题中告知ΔH<0,按理应该在任何温度下均自发呀,一时不知如何作答,困惑不已.其实反应是否自发与反应是否真正发生,肉眼可见是两码事,前者属化学热力学范畴,后者则是化学动力学范畴.由于该反应ΔH<0,ΔS>0,因此该反应在任何温度下都能自发进行;但是在常温下该反应速率极慢,现象不明显,需要加热才能看到明显的实验现象.
(2)①根据题中所给的数据:



学生一般简易计算快速得出答案:α(SO2)=44/50=88%.
(3)①A项,在常压下SO2催化氧化反应中,SO2的转化率已经高达九成多,所以出于成本的考虑,工业采用常压生产,这在教材中是一典型案例,学生应该熟悉,当然工业上有采用高压的反应条件,但不是必须的,所以A项说法不正确;
B项,进入接触室之前的气流中含有会使催化剂中毒的物质,需经净化处理以防止催化剂中毒,B说法不正确;

D项,SO3与水反应放出大量的热,在吸收塔中若采用水或稀硫酸吸收SO3,反应放出的热量会使硫酸形成酸雾从而影响SO3被水吸收导致SO3的吸收效率减小,因此,在吸收塔中不宜采用水或稀硫酸吸收SO3,而是采用浓硫酸吸收,得到的是发烟硫酸,D说法不正确.
综上,本小题符合题意的只有C项.
②本小题考察学生的识图能力,顺着箭头理解流程:原料气(题中以SO2示意之)进入“竹林”(热交换气器),与“竹腔”内的反应混合物进行热交换,原料气得到预热,同时使反应混合物降温,不致使温度过高超过催化剂的活性温度(注意:这里一般不考虑平衡问题,因为气流较快,没有足够的时间去到达平衡,所以不需要考虑降温使平衡右移之类的.)按图所示,这种热交换过程重复三次后,原料气的温度达到催化剂的活性温度,从顶部进入反应釜内,在催化剂的表面发生SO2的催化氧化反应,该反应放热,使混合气体温度升高,随后便与“竹林”间的较冷的原料气进行热交换,又把温度降下来,再到下一层催化剂表面发生氧化反应,如此重复数次,原料利用率大大提高.理解了图1的意思,再结合图2曲线的走向,不难发现b1→a2、b2→a3、b3→a4三过程是热交换过程(温度降低,SO2的转化率未变),剩余的三个过程则是发生催化氧化反应的过程,总的SO2的转化率不断攀升,因此本小问选BDF;
③解答本小题,学生需辨别平衡转化率与转化率属两个概念,平衡转化率是相应条件下最大的转化率,所以可以先画出平衡转化率:由于该反应为放热反应,随着温度的升高,SO2的平衡转化率减小,是一单调递减函数,故可画曲线Ⅱ;
由于反应混合物与催化剂层的接触时间较少,在实际的反应时间内反应还没有达到化学平衡状态,故在相应温度下SO2的转化率低于其平衡转化率.

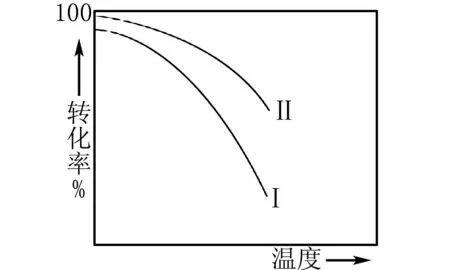
图5
再来验证为什么曲线Ⅰ是一单调递减函数:

(4)由pH-时间振荡曲线可知,在Na2S-H2SO4-H2O2溶液体系中,溶液的pH呈平缓、增大、减小的周期性变化,同时题意告知可观察到体系由澄清→浑浊→澄清的周期性变化.
在振荡曲线中截取一段,当作一周期,如图6所示:

图6
四步反应关系如图7所示:
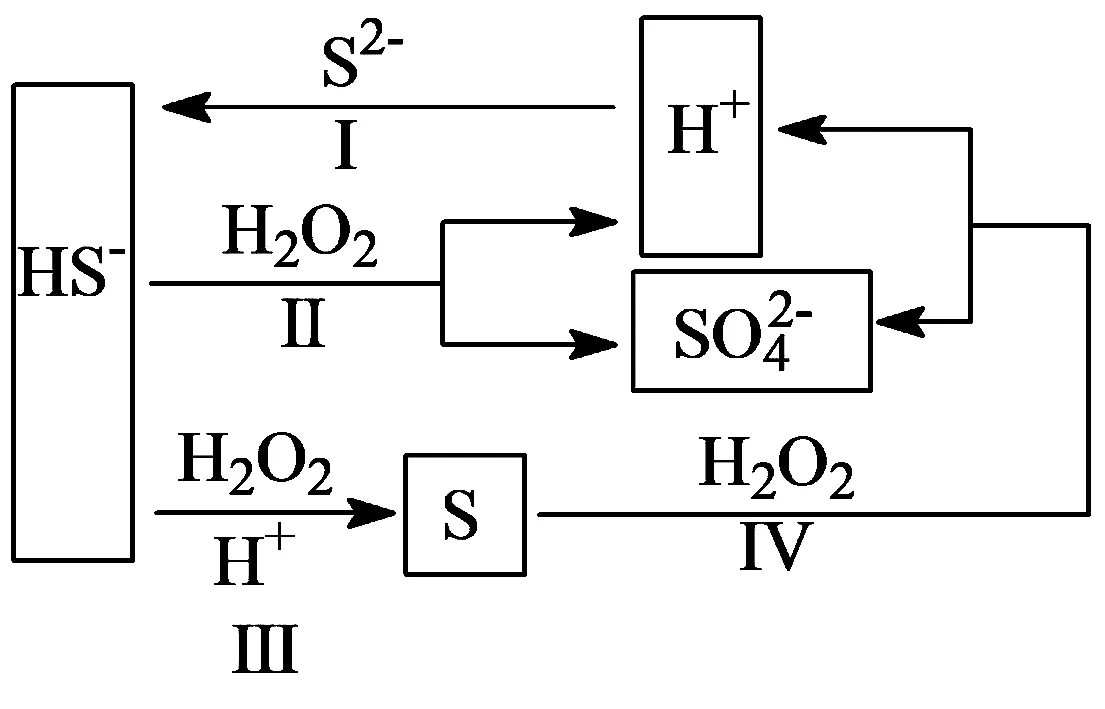
图7



故可推测每一个周期内的反应进程中依次发生了如下离子反应:




综上,pH:6→8→6,体系澄清→浑浊→澄清,因此周期性名副其实.
关于振荡反应,有学生认为振荡反应不消耗原料,这种看法是错误的.振荡反应是会消耗一定的物质的,就比如教材上曾经介绍的碘钟反应,其本质也就是氧化剂与还原剂的反应:氧化剂氧化碘离子变成碘单质与淀粉显色,还原剂还原碘单质使颜色褪去;而体系内的氧化剂与还原剂在碘离子-碘单质这个桥梁的存在下几乎不发生副反应(因此也就可以把碘离子-碘单质理解成催化这个氧化还原反应的催化体系,让本来难以发生的反应发生).它所谓的振荡,或是周期性变化,也就是碘充当了氧化还原反应的中间介质,正如本题中的氢离子与硫单质,他们共同搭建起了S2-被双氧水氧化这一反应的桥梁,而这个振荡的结果,就是以S2-被氧化为硫酸根作为终结(如图8所示).因此,要明晰振荡反应所谓周期性与反应物质守恒之间的区别.

过氧化氢型碘钟 碘酸盐型碘钟图8
参考答案:(1)不同温度下都能自发,是因为ΔH<0,ΔS>0
(2)①6.7×103mol·L-1②88%
(3)①C ②BDF ③



