羧基化磁性Fe3O4 复合材料对Pb2+的吸附性能研究
2022-11-17宋月红徐辉吴林林安文强罗腾礼代卫丽
宋月红, 徐辉, 吴林林, 安文强, 罗腾礼, 代卫丽
(1.商洛学院 化学工程与现代材料学院 陕西省尾矿资源综合利用重点实验室, 陕西 商洛 726000;2.陕西省矿产资源清洁高效转化与新材料工程研究中心, 陕西 商洛 726000;3.湖南省益阳市南县检验检测中心, 湖南 益阳 413000)
尾矿库的堆积造成库区周边土壤和水体的重金属污染日益严重, 重金属毒性高, 能够在植物和生物体中蓄积, 不易代谢, 因此, 如何有效控制尾矿库区水体中的重金属污染已经成为该领域研究热点之一[1-2]。
去除重金属的方法主要有物理法、 化学法和生物法[3-4], 其中物理法成本较低但是不能有效脱除重金属离子; 生物法对环境影响较小但是容易造成二次污染; 化学法常用的有沉淀法、 电解法和吸附法, 其中, 吸附法因其操作简单、 成本低、 应用范围广而备受科研工作者的青睐[5-6]。 Fe3O4因其原料易得、 制备简单、 具有磁性容易回收和分离等特点而备受关注。 单纯的Fe3O4吸附能力有限, 满足不了实际使用需求, 因此, 对其进行修饰来提高其吸附性能是研究发展的趋势[7-8]。 Wang 等[9]研究表明氨基功能化的Fe3O4@SiO2核壳结构的磁性纳米材料对于Cu2+、 Pb2+和Cd2+的吸附效果良好, 并且该吸附剂易于分离和再生。 Saravanan 等[10]合成了修饰后尺寸为8 ~15 nm 的磁性纳米粒子, 在不同条件下研究了对Cd2+、 Cu2+、 Pb2+、 Ni2+、 Zn2+、 Hg2+多种重金属离子的吸附性能, 试验结果表明, 该磁性纳米粒子对Cd2+的吸附效果最好, 吸附容量为106.8 mg/g, 对Hg2+的 吸 附 效 果 较 差, 为35.07 mg/g。 张立志等[11]采用共沉淀法制备出了超顺磁性纳米Fe3O4@SiO2功能化材料, 对Cd2+的最大吸附容量为69.49 mg/g, 材料重复使用3 次后对Cd2+的去除率仍达73% 以上, 研究表明其吸附机制为Cd2+与材料表面的—OH 发生配位反应。
本研究以液相沉淀法合成磁性Fe3O4-SiO2, 再通过酰胺化反应得到羧基化磁性Fe3O4复合材料(Fe3O4-SiO2-COOH), 采用FTIR、 XRD、 VSM 和SEM 对其结构进行表征, 考察复合材料对Pb2+的吸附性能, 以及吸附时间、 温度、 pH 值和Pb2+初始浓度等对其性能的影响, 并探究了其吸附机理,以期为该类材料的开发及吸附重金属的实际应用提供依据。
1 材料与方法
1.1 试剂和仪器
FeCl3·6H2O, FeSO4·7H2O, 浓氨水, 正硅酸乙酯, 3-氨丙基三乙氧基硅烷(APTS), 柠檬酸, 甲醇, 硝酸铅, 乙二胺四乙酸二钠, 均为分析纯; 蒸馏水为实验室自制。
X-射线衍射仪(XRD), 红外光谱仪(FTIR),扫描电子显微镜(SEM), X-MAX 能谱(Mapping),振动样品磁强计(VSM), X 射线光电子能谱仪(XPS), 双束紫外可见分光光度计(UV-Vis)。
1.2 羧基化磁性Fe3O4 复合材料的制备
称取13.0 g FeCl3·6H2O 和6.5 g FeSO4·7H2O 分别溶于100 mL H2O 中, 并置于三口瓶中, 搅拌下加入浓NH3·H2O 调节体系pH 值为10.0, 80 ℃反应40 min, 然后滴加30 mL 正硅酸乙酯和20 mL 甲醇的混合溶液, 反应2 h 后, 采用磁分离法经H2O和甲醇反复洗涤5 次备用, 记为Fe3O4-SiO2。 取5.0 g Fe3O4-SiO2磁性颗粒分散于150 mL 甲醇中,加入20 mL 的3-氨丙基三乙氧基硅烷(APTS), 60℃下反应12 h, 最后加入一定量的柠檬酸, 反应20 h 后磁分离洗涤, 得到Fe3O4-SiO2-COOH 复合材料。
1.3 试验用水
用分析天平称取3.312 1 g Pb(NO3)2, 用去离子水溶解定容至1 000 mL, 得到浓度为0.01 mol/L的Pb2+溶液, 作为吸附试验的基础液, 用0.1 mol/L HCl 调节体系的pH 值。
1.4 试验方法
称取(0.1±0.000 2)g Fe3O4-SiO2-COOH 复合材料放入锥形瓶中, 加入100 mL 0.01 mol/L Pb(NO3)2溶液。 于恒温振荡器上振荡一定时间后取上层清液离心, 测定上清液中Pb2+剩余浓度, Fe3O4-SiO2-COOH 对Pb2+的吸附量计算公式如下:
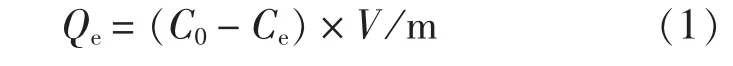
式中: C0为初始时Pb2+质量浓度, mg/L; Ce为吸附后Pb2+质量浓度, mg/L; V 为Pb2+溶液的体积, L; m 为Fe3O4-SiO2-COOH 的投加量, g。
1.5 分析方法
Pb2+浓度测定用EDTA 进行络合滴定。
2 结果与讨论
2.1 Fe3O4-SiO2-COOH 复合材料结构分析
2.1.1 FTIR 分析
Fe3O4和Fe3O4-SiO2-COOH 的FTIR 图谱如图1所示。 在Fe3O4图谱中, 578 和474 cm-1处的2 个特征峰分别对应Fe3O4中四面体和八面体空隙中的Fe—O 键[12], 这一特征峰在Fe3O4-SiO2-COOH 图谱中也可以观察到, 表明所制备的复合材料中包覆有Fe3O4。 与Fe3O4样品相比, Fe3O4-SiO2-COOH 图谱中可以看到在2 924 和2 852 cm-1处出现了2 个新的吸收峰, 归属于C—H 的非对称和对称伸缩振动峰; 1 103 cm-1处的吸收峰归属于Si—O—C 的伸缩振动峰[13]; 1 728 cm-1处的吸收峰归属于C==O 的对称伸缩振动峰[14], 1 632 cm-1处的吸收峰为N—H 的 弯 曲 振 动 峰[15], 以 上 结 果 表 明Fe3O4-SiO2-COOH 材料已被成功制备。
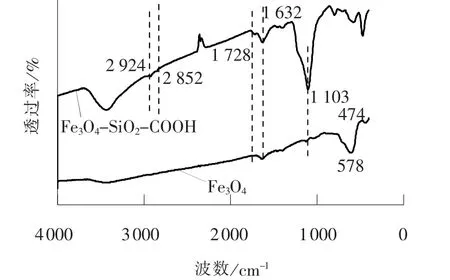
图1 Fe3O4 和Fe3O4-SiO2-COOH 的红外表征图谱Fig. 1 FT-IR spectra of Fe3O4 and Fe3O4-SiO2-COOH
2.1.2 XRD 分析
Fe3O4和Fe3O4-SiO2-COOH 的XRD 图谱如图2所示。 从图2 可以看出, 图谱中2 条曲线出现的衍射峰和Fe3O4标准卡片(JCPDS No.75-0449)的特征衍射 峰 位置基 本一致, 在2θ 为30.36°、 35.76°、43.47°、 57.51° 和63.16° 出 现 的 衍 射 峰 分 别 对 应Fe3O4(220)、 (311)、 (400)、 (422)和(440)的 晶面, 没有其他物质的衍射峰出现, 表明修饰后的Fe3O4-SiO2-COOH 中包覆着Fe3O4, 并且不含其他类型的铁氧化物。 Fe3O4-SiO2-COOH 的XRD 图谱中没有出现SiO2的特征衍射峰, 表明SiO2主要以无定型形态沉积在Fe3O4表面, 修饰后的样品化学成分没有发生改变, 但结晶度有所下降, 进一步说明Fe3O4被成功包覆。
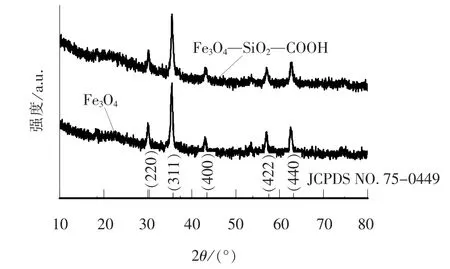
图2 Fe3O4 和Fe3O4-SiO2-COOH 的XRD 图谱Fig. 2 XRD patterns of Fe3O4 and Fe3O4-SiO2-COOH
2.1.3 磁化曲线分析
Fe3O4和Fe3O4-SiO2-COOH 的磁滞回线如图3所示。 从图3 可知, Fe3O4和Fe3O4-SiO2-COOH 的磁滞曲线呈S 型, 矫顽力和剩余磁场强度都很小,表明两者具有超顺磁性。 Fe3O4和Fe3O4-SiO2-COOH的饱和磁化强度分别为75.8、 31.7 emu/g, 说明非磁性的物质成功嫁接到Fe3O4的表面, 使得材料整体的磁化强度下降。 尽管Fe3O4-SiO2-COOH 的饱和磁化强度有所减小, 但仍可以在外加磁场下进行快速分离、 回收、 再生和重复利用。
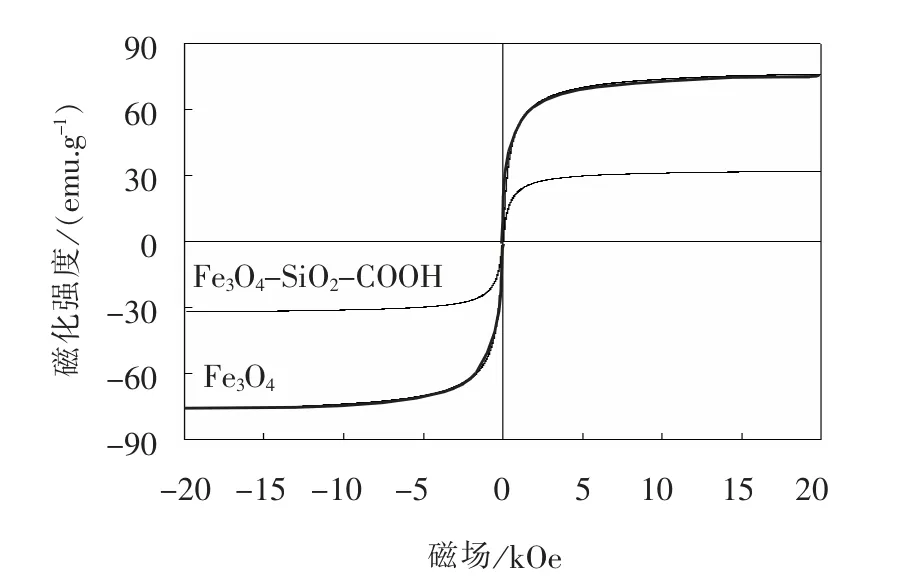
图3 Fe3O4 和Fe3O4-SiO2-COOH 的磁化曲线Fig. 3 Magnetization curves of Fe3O4 and Fe3O4-SiO2-COOH
2.1.4 表观形貌分析
Fe3O4-SiO2-COOH 的SEM 和Mapping 照 片 如图4 所示。 从SEM 图片可以看出Fe3O4-SiO2-COOH 为连接在一起的颗粒组成, 表面不光滑, 单个颗粒尺寸约为60 nm。 从元素分布图可以看出,Fe 元素集中在样品的核心区域, Si、 C、 O 和N 元素均在相同位置均匀分布, 这主要是因为在Fe3O4的外部包覆着SiO2, 同时, 柠檬酸也被成功接枝到Fe3O4上。

图4 Fe3O4-SiO2-COOH 的SEM 和元素分布Fig. 4 SEM and element distribution of Fe3O4-SiO2-COOH
2.2 Fe3O4-SiO2-COOH 复合材料的吸附性能研究
2.2.1 吸附时间对吸附量的影响及吸附动力学研究
向100 mL Pb2+溶 液 中 加 入(0.1 ± 0.000 2) g Fe3O4-SiO2-COOH 复合材料, 中性条件下, 于45℃恒温振荡器中振荡一段时间, 离心处理后测定上清液中Pb2+的浓度, 计算Fe3O4-SiO2-COOH 对Pb2+的吸附量, 考察吸附时间对吸附量的影响, 结果如图5 所示。
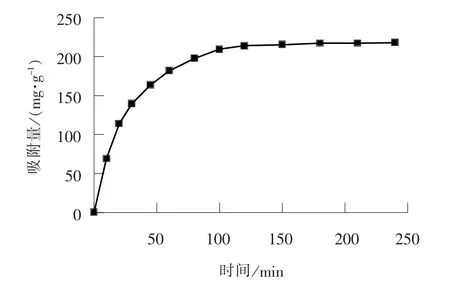
图5 吸附时间对Fe3O4-SiO2-COOH 吸附Pb2+的影响Fig. 5 Influence of adsorption time on Fe3O4-SiO2-COOH adsorbing Pb2+
从图5 可以看出, Fe3O4-SiO2-COOH 复合材料对Pb2+的吸附量随着时间的延长而逐渐增加, 在0 ~80 min 内吸附量增加较快, 80 ~120 min 吸附量增加较慢, 120 min 基本达到平衡, 其平衡吸附量为213.5 mg/g。 吸附初期Fe3O4-SiO2-COOH 复合材料表面活性位点较多, 溶液中的Pb2+可以通过络合作用快速地吸附到材料上[15], 随着吸附时间的延长, Fe3O4-SiO2-COOH 复合材料表面活性位点数目逐渐减少, 导致吸附速率降低直到吸附平衡。
采用准一级动力学和准二级动力学方程来模拟Fe3O4-SiO2-COOH 复合材料对Pb2+的吸附过程, 进一步探究其去除机理。
准一级动力学方程:
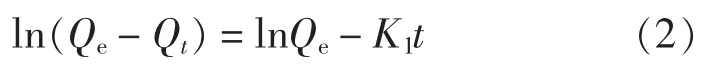
准二级动力学方程:
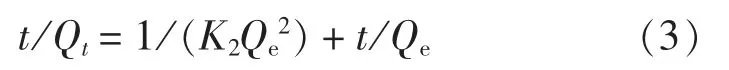
式中: Qe为平衡吸附量, mg/g; Qt为t 时刻的吸附量, mg/g; t 为吸附时间, min; K1和K2分别为准一级、 准二级速率常数, min-1、 g/(mg·min)。
Fe3O4-SiO2-COOH 复合材料吸附Pb2+的准一级和准二级动力学方程拟合曲线如图6 所示, 相关参数 如 表1 所 示。 K1和K2分 别 为0.019 43 min-1和0.003 466 g/(mg·min), 相对应的Qe分别为102.45和212.31 mg/g, 可以看出准二级动力学拟合的结果和试验数据较为接近。 同时, 准二级动力学方程拟合的相关系数为0.999 4, 远远高于准一级动力学 方 程 的 相 关 系 数0.889 4, 表 明Fe3O4-SiO2-COOH 复合材料对Pb2+的吸附符合准二级动力学方程, 主要以化学吸附为主。
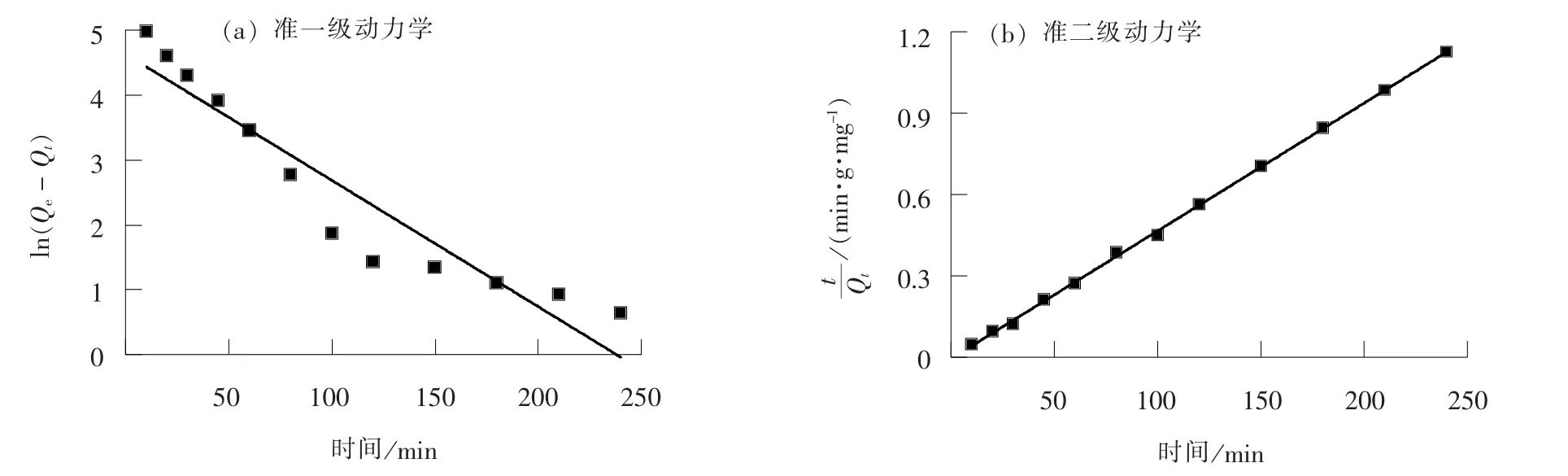
图6 Fe3O4-SiO2-COOH 吸附Pb2+的动力学拟合曲线Fig. 6 Kinetic fitting curves of Fe3O4-SiO2-COOH adsorbing Pb2+

表1 Fe3O4-SiO2-COOH 复合材料吸附Pb2+的动力学拟合参数Tab. 1 Kinetic fitting parameters of Fe3O4-SiO2-COOH composite material adsorbing Pb2+
2.2.2 温度对吸附量的影响向100 mL Pb2+溶 液 中 加 入(0.1 ± 0.000 2) g Fe3O4-SiO2-COOH 复合材料, 中性条件下, 于不同温度下振荡120 min, 离心处理后测定上清液中Pb2+的剩余浓度, 考察温度对吸附量的影响, 结果如图7 所示。 从图7 可以看出, 随着温度的升高,Fe3O4-SiO2-COOH 复合材料对Pb2+的吸附量呈增加趋势。 当温度从25 ℃上升到55 ℃时, 吸附量从173.8 mg/g 升高至221.6 mg/g, 说明该吸附反应为吸热反应, 升高温度可以促进反应的进行, 这是因为温度升高使分子运动速率加快, 会促进Fe3O4-SiO2-COOH 复合材料表面的活性位点与Pb2+发生作用, 导致吸附量增加。
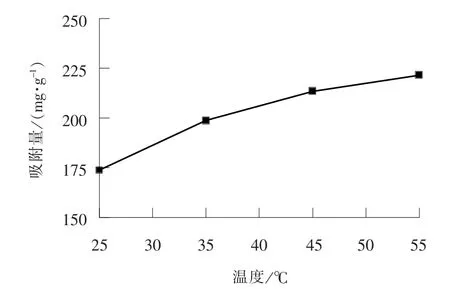
图7 温度对Fe3O4-SiO2-COOH 吸附Pb2+的影响Fig. 7 Effect of temperature on Fe3O4-SiO2-COOH adsorbing Pb2+
2.2.3 pH 值对吸附量的影响
向100 mL Pb2+溶 液 的 锥 形 瓶 中 加 入(0.1 ±0.000 2) g Fe3O4-SiO2-COOH 复合材料, 改变体系的pH 值, 于55 ℃恒温振荡器中振荡120 min, 离心处理后测定上清液中Pb2+的剩余浓度, 考察pH值对吸附量的影响, 结果如图8 所示。 从图8 可以看出, pH 值对Pb2+吸附量的影响较大, 随着pH值的增加, 吸附量呈现出先增大后减小的趋势; 在pH 值为5 时, 吸附量最大, 为233.8 mg/g, 这是因为当pH 值较低时, Fe3O4-SiO2-COOH 表面的—COOH 容易与H+发生质子化, 导致络合能力下降,随着pH 值的增大, 材料表面的—COOH 解离程度增大, 从而增加了与Pb2+结合的活性位点, 使活性位点络合能力增强, 导致吸附量增加; 进一步升高pH 值, Pb2+逐渐以羟基络合物或者Pb(OH)2的形式存在[15], 减弱了材料对Pb2+的络合能力, 导致吸附量降低。
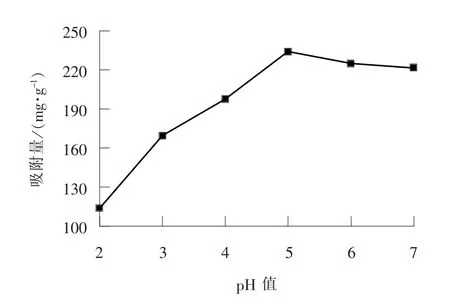
图8 pH 值对Fe3O4-SiO2-COOH 吸附Pb2+的影响Fig. 8 Effect of pH value on Fe3O4-SiO2-COOH adsorbing Pb2+
2.2.4 Fe3O4-SiO2-COOH 对Pb2+的等温吸附研究
将(0.1±0.000 2)g Fe3O4-SiO2-COOH 复合材料分别加入不同浓度的Pb2+溶液中, 调节体系pH 值为5, 于55 ℃的恒温振荡器中振荡120 min, 离心处理后测定上清液中Pb2+的浓度。 采用均匀单层吸附的Langmuir 和非均匀吸附的Freundlich 等温方程对试验数据进行拟合分析, 相关参数如表2所示。
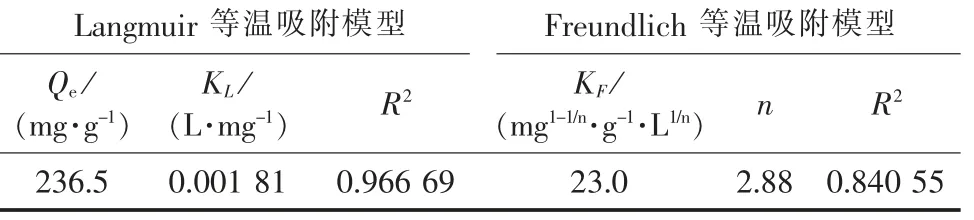
表2 Fe3O4-SiO2-COOH 复合材料吸附Pb2+的等温吸附参数Tab. 2 Isotherm adsorption parameters of Fe3O4-SiO2-COOH composite material adsorbing Pb2+
Langmuir 方程为:
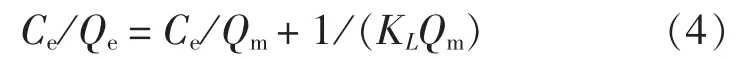
Freundlich 方程为:
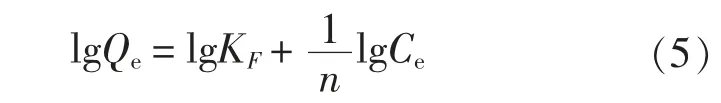
式中: Qe为平衡吸附量, mg/g; Qm为理论饱和吸附量, mg/g; Ce为溶液的平衡质量浓度, mg/L; KL为平衡吸附常数, L/mg; KF为Freundlich 常数, n 为吸附容量经验常数。
从拟合的结果来看, Langmuir 等温吸附模型的相关系数R2为0.966 69, 表明Fe3O4-SiO2-COOH 对Pb2+的吸附主要倾向于单分子层吸附。
2.2.5 Fe3O4-SiO2-COOH复合材料吸附Pb2+前后的XPS 分析
Fe3O4-SiO2-COOH 复合材料吸附Pb2+前后的XPS 图谱如图9 所示。 由图9(a)可知, 样品在吸附Pb2+前主要存在O1s、 C1s、 N1s 和Si2p 元素特征峰, 吸附之后出现了Pb4f 的元素特征峰, 说明Pb2+被成功吸附。 图9(b)中, 137.1 eV 和141.9 eV所对应的峰分别为Pb4f7/2和Pb4f5/2的特征峰。 在全谱图中几乎没有看到Fe2p 的峰, 这是因为外层包裹的壳的厚度超过了XPS 所能探测的最大深度。图9(c)、 (d)为O1s 图谱, 529.5 eV 和530.3 eV 分别归属于C==O 和C—O[16], 当Fe3O4-SiO2-COOH吸附Pb2+之后, C==O 和C—O 对应的峰分别移至530.4 eV 和531.6 eV, 这是因为Fe3O4-SiO2-COOH在吸附Pb2+的过程中羟基和羧基络合了Pb2+。 图9(e)、 (f)为C1s 图谱, 282.2、 283.2、 284.4、 286.2 eV 分别归属于C—N、 C—C、 C—O 和C==O[17],材料吸附Pb2+之后, C—O 和C==O 对应的峰位分别移至285.4、 286.8 eV, 进一步说明了羟基和羧基在Fe3O4-SiO2-COOH 对Pb2+的吸附过程中起到了作用。
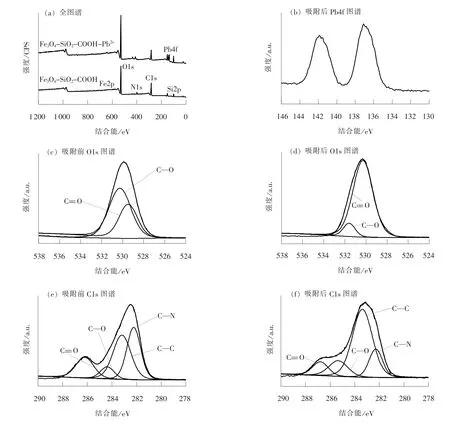
图9 Fe3O4-SiO2-COOH 复合材料吸附Pb2+前后的XPS 图谱Fig. 9 XPS spectra of Fe3O4-SiO2-COOH composite material before and after adsorption of Pb2+
3 结论
(1) 通过液相沉淀法制备出羧基化磁性Fe3O4-SiO2-COOH 复合材料, 该复合材料可以吸附Pb2+,并且在磁场的作用下可以实现快速分离和再生。 对其结构进行表征, 考察了吸附时间、 温度、 pH 值和Pb2+的初始浓度对其吸附性能的影响, 探究复合材料对Pb2+吸附性能。 吸附试验结果表明, 在pH 值为5, 温度为55 ℃, 吸附时间为120 min,Pb2+溶 液 的 初 始 浓 度 为0.01 mol/L, Fe3O4-SiO2-COOH 投加量为1 g/L 的条件下, Fe3O4-SiO2-COOH复合材料对Pb2+的吸附容量最大, 为233.8 mg/g。
(2) Fe3O4-SiO2-COOH 复合材料对Pb2+的吸附动力学过程符合准二级动力学方程, 以化学吸附为主; 吸附热力学符合Langmuir 等温吸附模型, 以单分子层吸附为主。
