巴彦乌拉铀矿床酸法浸铀的水岩反应堵塞机理
2022-10-14刘亚洲刘春雨
刘亚洲,罗 跃,李 寻,王 兵,刘春雨
(1.东华理工大学 核资源与环境重点实验室,南昌 330013;2.东华理工大学 水资源与环境工程学院,南昌 330013)
巴彦乌拉铀矿床主要采用酸法地浸采铀工艺,该铀矿床的铀资源含量丰富,且铀矿体具有埋藏浅、含矿含水层渗透性好等特点。铀矿资源的开采方式主要有以下3种:地下开采、露天开采以及地浸开采[1]。目前,原地浸出采铀(简称为地浸采铀)方法是国内外铀矿采冶主流方法之一[2]。随酸法地浸采铀工艺投入使用,溶浸液的迁移和铀矿石在酸中的溶解,酸逐渐被消耗,导致溶浸液的p H值逐渐增大,随p H值增大到一定程度时,浸出液中的金属阳离子出现沉淀现象,金属沉淀物会对铀发生吸附作用,促使铀发生沉淀[3-4],由此导致浸出液中铀的含量的变化[5-7],以及铀矿资源的开采量逐年下降。因此此次浸泡试验与模拟对铀矿山酸法地浸采铀效率的影响,对开采铀矿资源等有着重要意义。
核能是新型清洁能源之一,铀(U)作为十分重要的核燃料,日益受到国内外高度重视。高柏等[8]研究发现铀矿石以四价铀形式存在铀矿物中,以沥青铀矿为主,与方解石、黄铁矿紧密共生,酸法浸铀中浸出铀主要以六价铀的形式存在,六价铀存在形式主要为UO2(CO3)4-3、UO2(CO3)2-2、UO2CO3。在酸法浸铀中以UO2+2、UO2SO4、UO2(SO4)2-2为主几乎不存在,而(UO2)2(OH)+5、UO2Cl+、(UO2)2(OH)2+2等形式依然存在。碳酸铀酰主要形式为UO2(CO3)2-2、UO2(CO3)4-3(96.8%),UO2CO3(3.12%),其他存在形式不足万分之一。焦学然等[9]通过研究得出,当地下水中矿化度、Mg2+、Ca2+、HCO-3、SO2-4浓度过高易产生石膏、方解石沉淀从而引起化学堵塞。许根福[10]根据CO2+O2中性地浸采铀矿山工业试验,认为在p H值为6.0~9.0时易产生FeOOH沉淀堵塞矿层。值得注意的是,地浸采铀研究区内矿石所在矿层的地下水经常发生堵塞的现象,即渗透系数发生显著减小。根据以往研究[11],主要是钙离子与硫酸根离子相结合产生大量硫酸钙沉淀以及三价铁离子与其他阴离子相结合生成铁矿物沉淀。酸法地浸采铀过程中主要以石膏、针铁矿、赤铁矿为沉淀物[12]。陈万利[13]通过研究巴彦乌拉铀矿酸法地浸过程含矿含水层化学堵塞机理发现,酸法地浸过程中注入强酸性溶浸液与黄铁矿发生化学反应后生成Fe3+,会得到铁矿物沉淀,造成含矿含水层的化学堵塞,影响铀的浸出。因此铀的迁移还需考虑其他沉淀物溶解的影响。
本文是基于巴彦乌拉铀矿地区铀矿样分析,确定了三种主要影响铀浸出的杂质矿物(石膏、针铁矿、赤铁矿),然后利用PHREEQC的反应路径模拟来分析浸泡试验,探索不同杂质矿物对铀浸出的影响,基于此,建立化学形态模拟和溶解度模拟,来分析三种杂质矿物在铀浸出过程中的作用,从而确定石膏、针铁矿、赤铁矿杂质矿物在酸法地浸采铀中的影响。
1 材料与方法
1.1 浸泡试验材料
试验样品:试验样品来自巴彦乌拉铀矿矿床(中国内蒙古)。据前人研究结果[13-14],铀矿石以低品位铀矿石(铀品位≤0.016%)为主,矿石中铀赋存形式以铀矿物为主。试验研究所取铀矿石为砂岩型,主要为疏松、次疏松、灰色、深灰色砂岩或砾岩矿石。
主要试剂:盐酸、硫酸、过硫酸铵、EDTA试剂、磺基水杨酸。
试验主要仪器和设备:铁架台、烧杯、500 m L锥形瓶、保鲜膜、10 m L移液枪、10 m L移液管、p H计、Eh计、滴定管、恒温震荡器(摇床)等。
1.2 试验方法
采用浸泡试验方法,在500 m L锥形瓶分别装入3.5、5.0、6.5 g/L浓度的硫酸溶液300 m L,再分别加入粒径为小于0.3 mm、0.3~1.0 mm、1.0~3.0 mm、大于3.0 mm 的四种铀矿样品各10 g,最终为40 g的混合粒径样品,用保鲜膜封住锥形瓶瓶口,然后放入恒温(25℃)摇床中震荡培养,每隔一段时间取样检测浸出液的各个离子的浓度、p H值、Eh值等。
1.3 水质分析方法
利用p H值测定器测定浸出液的p H值,利用Eh值测定器测定浸出液的氧化还原电位Eh值。
1)金属阳离子:取过滤好的10 m L溶浸液样品,使用ICP-MS检测Ca2+、Al3+、Na+、Mg2+、K+、U、Si。而浸出液中Fe3+、总Fe使用EDTA络合滴定法测定,酸度使用容量法滴定。
2)阴离子:取过滤好的10 m L溶浸液样品,使用离子色谱对样品中的SO2-4浓度进行分析测定。
2 地球化学模拟
2.1 模拟机理
1)物质存在形式
水文地球化学就是地下水在移动过程中,与介质发生多种多样的物理化学反应,其中包括溶解-沉淀、碳酸平衡、吸附-解吸以及氧化还原等。依据地质、水文地质条件不同,这些作用往往控制着一个地区地下水的化学成分。水文地球化学主要研究内容为地下水中的物质成分以及形成作用、地下水中的化学元素的迁移过程和形式、人类活动对地下水化学成分以及形成作用的影响。水文地球化学模式是研究物质迁移的重要组成部分,分别为质量平衡模式、质量转化模式以及质量迁移模式三种基本类型[15]。此次模拟是以研究物质的存在形式为主体,然后在能量、质量和电荷守恒三大定律的基础上,研究物质在酸法浸出铀的溶浸液中的存在形式。
地下水中矿物的物质存在形式(配合物Xi)以及浓度(Ci)计算原理是:配合物的浓度可以看成为J个组分的总和(j=1,2,…,Nc)。设组分的总和为Nx,i配合物的浓度Xi为:

式中,axij为配合物i中的化合数;Cj为j组分的浓度,配合物i由j个组分组成。
根据质量守恒定律,配合物化学平衡关系为:

j组分的水溶相的总浓度为:

2)饱和指数(SI)
地下水矿物的饱和指数(Saturation Index)简称SI,是判断水环境矿物沉淀与溶解状态的重要参数。其计算公式为:

式中:IAP—离子活度积;KSP—溶度积常数。
因此,判断地下水中某一矿物是过饱和状态还是欠饱和状态,应计算出其固相的饱和指数是正数、负数还是零。当SI>0时,该矿物溶解不能自发进行,在溶液中为过饱和状态;当SI=0时,该矿物溶解达到平衡,在溶液中为饱和状态;当SI<0时,该矿物溶解可自发进行,在溶液中为不饱和状态[16]。
2.2 PHREEQC软件简介
PHREEQC软件是美国地质调查局(USGS)用于水文地球化学模拟开发,可以用于解决多种低温水文地球化学反应计算的计算机软件,包括正向模拟以及反向模拟,几乎能解决水、气、岩土相互作用系统中所有平衡热力学和化学动力学问题,包括水溶物配合、吸附解吸、离子交换、表面配合、溶解沉淀、氧化还原。PHREEQC是一个加入了非确定项控制的水一岩作用模拟软件。PHREEQC可进行化学形态模拟和溶解度模拟[17]。本文使用PHREEQC软件的化学形态模拟模块以及溶解度模拟模块,这两部分模块可计算溶液中的各物质组分的化学形态以及各种相关矿物所处的饱和状态。
化学形态—溶解度计算提供了动态系统中的“瞬时”状态,即当已知水样的化学组成,并假设了各溶液物种处于化学平衡的状态时(均相平衡),可通过计算获得溶液中存在的各种离子和分子的浓度与活度。
3 结果与讨论
3.1 浸出液水化学特征
3.1.1 铀离子与Ca2+浓度值变化
根据图1数据可知,在相同浓度的溶浸液中,铀离子的浓度随时间的增长而变大;且溶浸液的浓度逐渐增大,铀离子浓度也在上升。浸泡试验表明:相同浓度的溶浸液,时间越长,溶浸液浓度越大,铀离子浸出效果越好。不同浓度的溶浸液(3.5、5.0、6.5 g/L)平均浸出铀浓度为10.826 7、12.348 6、13.654 9 mg/L,分别占平均金属离子浓度值的0.563 0%、0.535 3%、0.526 7%。由于铀离子浓度过低,后续模拟中不再考虑铀离子存在形式以及所占比例。而Ca2+初始浓度是随溶浸液浓度增大而增大,由于溶浸液浓度越大,Ca2+浸出效果越好,故溶浸液浓度越大,Ca2+浓度越大。但随时间的递增,高浓度溶浸液(6.5 g/L H2SO4)中 Ca2+浓度下降速度最快,低浓度溶浸液(3.5 g/L H2SO4)中Ca2+浓度下降速度最慢,中浓度溶浸液(5.0 g/L H2SO4)中Ca2+浓度下降速度在两者之间,由于高浓度溶浸液中的浓度含量高,容易与Ca2+结合生成CaSO4(石膏)沉淀,且浓度越大,生成的 CaSO4(石膏)沉淀越快,所以高浓度溶浸液(6.5 g/L H2SO4)中Ca2+浓度下降速度最快。

图1 浸出液中U和Ca2+浓度随时间变化结果Fig.1 The concentration of U and Ca2+in leaching solution changed with time
3.1.2 Fe2+、Fe3+、Mg2+、Al3+浓度值
在浸泡试验中∑Fe的浓度不高,且∑Fe中主要以Fe2+的形式存在。根据图2数据可知,Fe2+、Fe3+、Mg2+、Al3+浓度随溶浸液浓度增加而增大。由于铀矿石在酸性溶浸液中逐渐溶解,导致矿物里面的金属阳离子浓度增大;而浓度总体变化趋势是随时间的增加而下降。由于可以与其他金属阳离子相结合生成沉淀,故浓度逐渐减小。
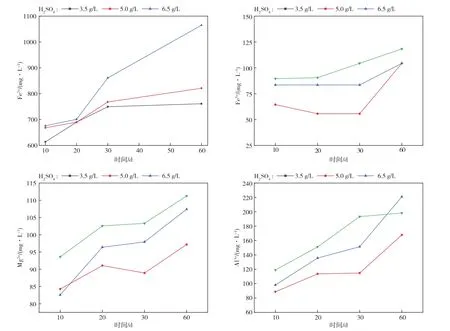
图2 浸出液中Fe2+、Fe3+、Mg2+、Al3+浓度随时间变化结果Fig.2 The concentration of Fe2+ ,Fe3+ ,Mg2+and Al3+in leaching solution changed with time
3.1.3 p H值 与 Eh值
由图3可以看出,随溶浸液浓度的增加,p H值明显依次减小,Eh值逐渐增大,由于不同浓度的溶浸液在溶解铀矿时,H+不断浸入,p H值不断减小,浸出液中的Fe3+浓度增大,导致Eh值增大。此外,相同浓度的硫酸溶液的p H值总体是随时间增加而增大,Eh值总体是随时间增加而减小,由于H+不断被消耗,p H值增大,随反应进行Fe3+会转换成Fe2+,氧化性降低,所以Eh值会逐渐减小。酸性越大,浸出离子效果越好。

图3 浸出液中p H值、Eh值随时间变化结果Fig.3 The concentration of p H value and Eh value in leaching solution changed with time
综上所述,并结合浸泡试验浸出液各个离子平均浓度值来说(图4),浸出液金属阳离子的浓度变化趋势基本一致,总体都是上升趋势;而是下降趋势,由于可以与其他金属阳离子形成络合物和沉淀,导致浓度逐渐减少。

图4 浸出液各离子平均浓度随时间结果Fig.4 Average concentration of each ion in the leaching solution changed with time
3.2 化学形态和溶解度模拟
根据浸出液化学成分分析,利用地球化学模拟软件(PHREEQC),对浸泡试验的浸出液中元素存在形式进行化学形态和溶解度模拟,得到各个元素的主要衍生化学形态组分(表1)。根据表1数据显示,除基本组分之外,各衍生物基本为SO2-4的络合物。

表1 浸泡试验浸出液化学组分的主要存在形式Table 1 The main forms of chemical components in liquefaction leached by immersion test /%
3.2.1 Fe3+与Fe2+主要化学形态以及饱和度
图5数据显示,Fe主要以离子形式存在,主要为Fe2+、FeSO+4。二价铁离子的络合物中FeSO4所占比重最大,二价铁其他络合物在∑Fe中所占比重很小,可忽略不计。与Fe2+相比,Fe3+模拟结果显示,Fe3+所占比重较小。三价铁离子的络合物中FeSO+4络合物占主导地位。在同一浓度溶浸液中Fe2+、Fe3+和相对应的络合物FeSO4、FeSO+4成反比例关系,当Fe2+、Fe3+比重增大,FeSO4、FeSO+4比例减小;当Fe2+、Fe3+比重减小,FeSO4、FeSO+4比例增大。

图5 浸出液Fe3+、Fe2+所占比重结果Fig.5 The proportion of Fe3+and Fe2+in the leaching solution
3.2.2 Al3+与 Mg2+主要化学形态
Al3+、Mg2+是浸出液中重要化学组成元素,Al3+浓度在浸泡试验浸出液中与 Mg2+浓度相似,图6中数据表明,Al主要以Al3+的形式存在,而铝离子络合物主要以AlSO+4的形式存在;Mg主要以Mg2+的形式存在,而镁离子络合物中 MgSO4所占比重最多,其他存在形式的离子络合物(例如:Al(SO4)2-、MgOH+)所占比例之和不足1%,可忽略不计。在同一浓度溶浸液中Al3+、Mg2+和相对应的络合物AlSO+4、MgSO4成反比例关系,当Al3+、Mg2+比重增大,AlSO+4、MgSO4比例减小;当Al3+、Mg2+比重减小,AlSO+4、MgSO4比例增大。3.2.3 SO2-4主要化学形态
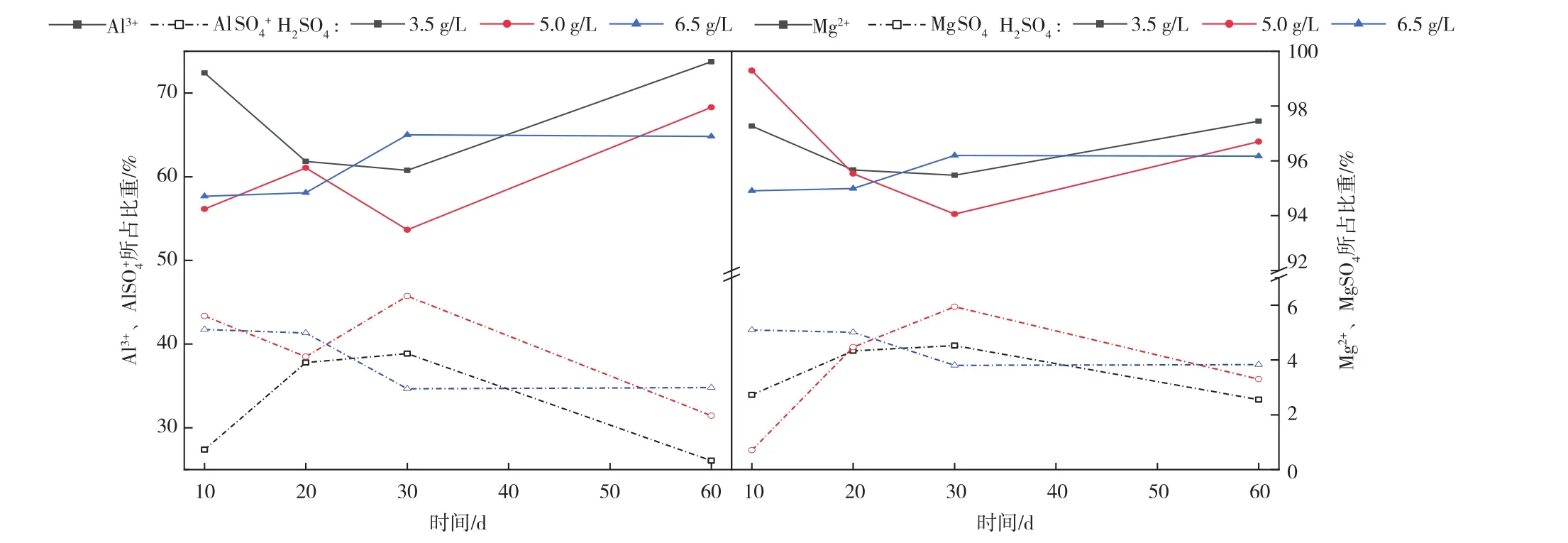
图6 浸出液Al3+、Mg2+所占比重结果Fig.6 The proportion of Al3+and Mg2+in the leaching solution
在浸出液中,阴离子主要存在形式为SO2-4。从图7可以明显看出,SO2-4存在形式广泛,其中SO2-4、HSO-4、AlSO+4所占比重较为明显。对于SO2-4而言,由于采用的是酸法浸出,故SO2-4浓度值均较高,且SO2-4易与其他阳离子相结合形成不同形式的衍生物,高浓度还易产生沉淀,对地浸开采不利。

图7 浸出液SO2-4所占比重结果Fig.7 The proportion of SO2-4 in the leaching solution
3.3 饱和度
根据图8数据显示,硬石膏(CaSO4)和石膏(CaSO4·2 H2O)、针铁矿 (FeOOH)和赤铁矿(Fe2O3)的饱和指数总体变化趋势大体相同。硬石膏与石膏、针铁矿与赤铁矿的饱和指数与溶浸液浓度和反应时间有关,其中反应时间越长,饱和指数越大;硬石膏与石膏的饱和指数总体上随溶浸液浓度增大而增大,而针铁矿与赤铁矿饱和指数总体上随溶浸液浓度增大而减小。这表明:硬石膏与石膏、针铁矿与赤铁矿随反应时间增大,沉淀量逐渐增大;且硬石膏与石膏是偏酸性条件下发生沉淀,针铁矿与赤铁矿偏碱性条件下发生沉淀。
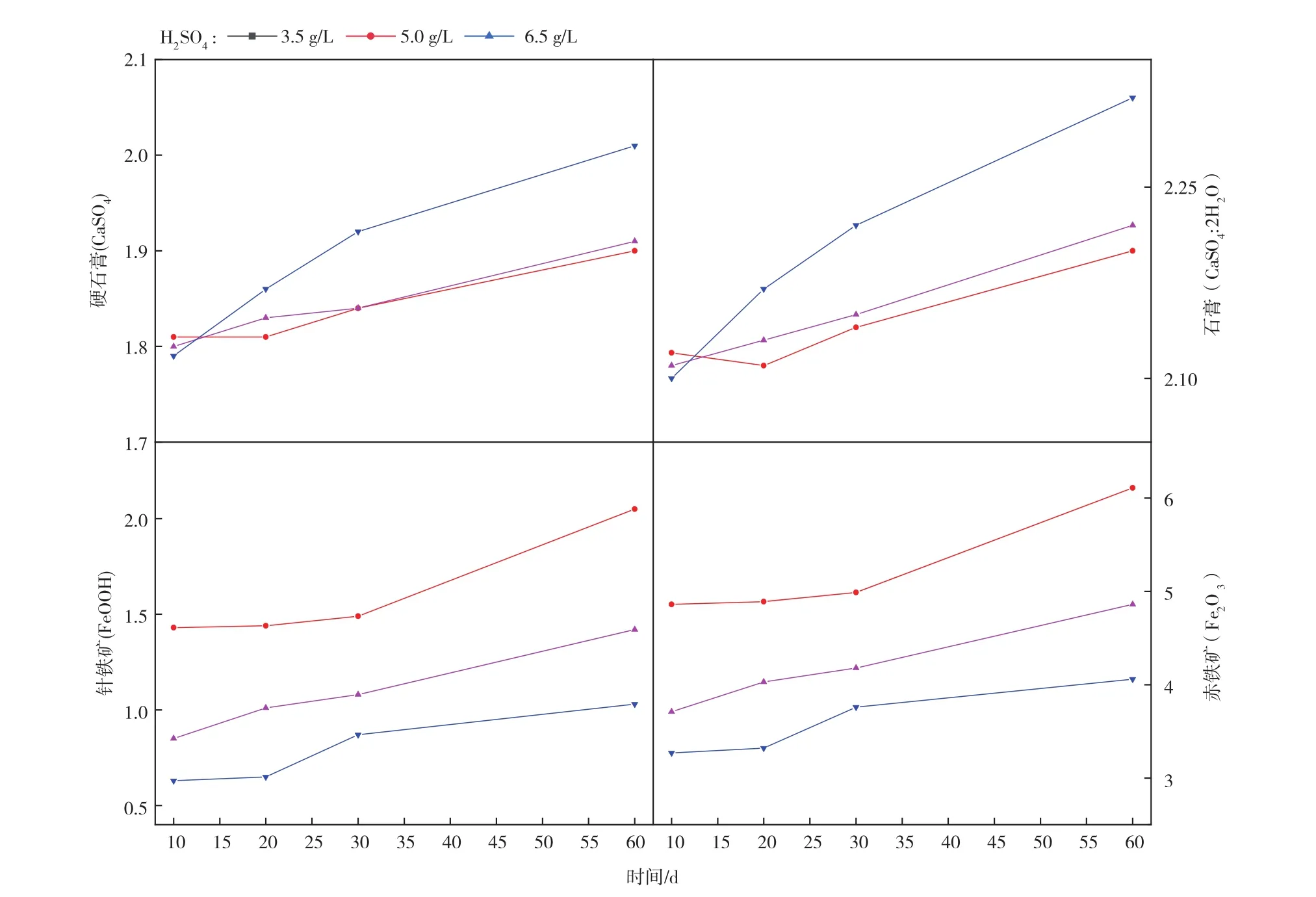
图8 不同浓度溶浸液的浸出液中硬石膏(CaSO4)、石膏(CaSO4·2H2 O)、针铁矿(FeOOH)、赤铁矿(Fe2 O3)饱和指数随时间变化结果Fig.8 The saturation index of anhydrite(CaSO4),gypsum(CaSO4·2H2 O),goethite(FeOOH),and hematite(Fe2 O3)in leach solution with different concentrations changed with time
4 结论
本文在分析了巴彦乌拉铀矿物质存在形式以及浸出液的化学组分成分的基础上,运用了地球化学模拟(PHREEQC)的方法,对浸出液进行了化学形态和溶解度模拟,研究铀矿物与溶浸液相互作用过程,讨论巴彦乌拉铀矿矿床的化学堵塞机理,并得到了以下几个结论:
1)在浸出液中,元素的存在形式表明,溶液中的金属阳离子铁、铝、镁主要与SO2-4相结合,所形成的衍生组分分别为FeSO4(3.32%)、FeOH2+(7.08%)、FeSO+4(49.97%)、AlSO+4(37.86%)、MgSO4(2.73%)、CaSO4(6.53%)、HSO-4(30.36%)。
2)巴彦乌拉铀矿矿床的主要沉淀物是石膏、铁矿物,石膏沉淀主要是CaSO4·2 H2O,铁矿物沉淀是由Fe3+、Eh值、p H值和浓度共同影响导致。
3)化学形态和溶解度模拟表明,石膏、铁矿物是堵塞空隙的主要沉淀物。当高浓度溶浸液注入到地下含矿含水层,浸铀的同时,也溶解了碳酸盐,导致Ca2+、Fe3+浓度上升,使反应条件指数大于0。当地下水溶液中Ca2+、Fe3+浓度反应指数大于0时,石膏与铁矿物就会发生沉淀,堵塞含矿含水层致使石膏和铁矿物沉淀物产生,从而堵塞了矿层孔隙。
