次氯酸钙-水杨酸钠分光光度法测定水质中氨氮
2022-10-14雍晓蕾黄朝颜王照丽
蒋 艳,雍晓蕾,*,黄朝颜,刘 煦,佟 玲,王照丽
(1.成都市排水有限责任公司,四川成都 610063;2.成都市环境保护科学研究院,四川成都 610072)

氨氮检测方法有分光光度法、电极法、滴定法等。分光光度法由于灵敏度高、稳定性好,是氨氮检测最常用的方法,主要以纳氏试剂分光光度法和水杨酸分光光度法为主[1-3]。近些年,由于配制纳氏试剂的多种方法均含有汞的化合物和强碱,对环境和人体危害严重,产生的废液不可直接排放,需另行处理,大大增加了检测成本[2]。目前越来越多的检测人员更愿选择所用试剂无毒、对环境污染小、产生废液可以直接排放的水杨酸法检测氨氮,更符合现代检测机构的环保理念[4-7]。
国标方法水杨酸法检测氨氮的检出上限仅为1.00 mg/L,同时需要显色60 min,耗时较长,在较高氨氮浓度的工业废水以及应急快速检测等方面均有较大限制[1]。此外,该法所用次氯酸钠溶液化学性质不稳定,需要经常对其有效氯及游离碱进行验证,较短的保质期也增加了新溶液配制频率,带来了检测的不便和浪费。水杨酸法检测氨氮是通过检测氨氮与次氯酸盐和水杨酸盐反应生成的水溶性蓝色化合物的吸光度变化来确定氨氮的含量,目前已有不少研究者选择稳定性更好的二氯异氰酸钠代替次氯酸钠用于水质氨氮检测[6-9]。次氯酸钙作为一种含氯稳定、价格更便宜的次氯酸盐,目前还尚未有用于水质氨氮检测的报道。本研究选择次氯酸钙代替次氯酸钠,通过优化其与水杨酸钠等试剂的加入比、显色时间、显色温度等条件,拟为水质氨氮快速、准确检测提供一种更优的方法。
1 试验部分
1.1 仪器与试剂
仪器:普析TU-1901紫外-可见光分光光度计;上海雷磁PHS-3C型pH计;梅特勒AL204电子天平;北京中兴伟业DZKW-4电子恒温水浴锅;10 mL具塞比色管;电子移液器、移液管等。所有玻璃器皿在使用前均先用每升含有100 g氢氧化钾和900 mL乙醇的清洗溶液清洗,再用去离子水多次冲洗。
试剂:水杨酸钠、酒石酸钾钠、亚硝基铁氰化钠、次氯酸钙(有效氯含量为60%)、NaOH均为分析纯,购自Sigma-Aldrich公司;氯化铵(NH4Cl)为优级纯。其中混合试剂A为亚硝基铁氰化钠、水杨酸钠、酒石酸钾钠、NaOH质量比为4∶60∶20∶5的混合溶液,即每100 mL混合试剂A含1.0 g亚硝基铁氰化钠、15.0 g水杨酸钠、5.0 g酒石酸钾钠、1.25 g NaOH。混合试剂B为NaOH和次氯酸钙质量比为6∶1的混合溶液,即每100 mL含3.0 g NaOH和0.5 g次氯酸钙。1 000 mg/L的氨氮标准贮备液的配制为称取在100~105 ℃干燥 2 h的NH4Cl 3.819 0 g,溶于无氨水,再转移到 1 000 mL棕色容量瓶中,稀释至标线备用,以此为基础稀释成试验所需的不同浓度的氨氮标准溶液。
1.2 试验原理
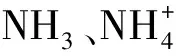
1.3 试验方法
取300 μL混合试剂A和300 μL混合试剂B的上清液加入10.0 mL具塞比色管,再分别加入0.00、0.50、1.00、3.00、5.00 mL质量浓度为1.00 mg/L的氨氮标准使用液和1.00、2.00、2.50 mL质量浓度为10.0 mg/L的氨氮标准使用液,配制成0、0.05、0.10、0.30、0.50、1.00、2.00、2.50 mg/L 8个不同质量浓度的标准系列,混匀定容。在室温反应20 min后,用10 mm比色皿在697 nm比色测定其吸光度并做3个平行,参比溶液为去离子水。实际样品则在最优试验条件下进行氨氮浓度测定。
2 结果与讨论
2.1 反应条件的选择
2.1.1 药剂的选择
水杨酸法检测氨氮是在亚硝基铁氰化钠存在下,氨氮与水杨酸盐和次氯酸盐生成水溶性蓝色化合物,其显色吸光度与氨氮含量成正比,满足朗伯尔定律。国标法HJ 536—2009测氨氮时水杨酸溶解需要调pH,且选用次氯酸钠作为次氯酸离子的来源,使用时需准确测定其有效氯和游离碱值,步骤繁琐且次氯酸钠不稳定,不宜长期存贮。目前已有不少研究者选择二氯异氰酸钠代替次氯酸钠用于水质氨氮检测[5-8],而次氯酸钙与二氯异氰酸钠一样具有有效氯含量高、缓释时间长和性质稳定等优点,且更易得,价格也更便宜,故本文选择次氯酸钙参与显色反应。
2.1.2 试剂用量选择
在空白样和含有0.50、2.50 mg/L氨氮的标准溶液中加入不同量的混合试剂A和混合试剂B,在(25±2)℃的室温下显色20 min后,用10 mm比色皿在697 nm测定吸光度,结果如表1所示。由表1可知,随着混合试剂A和混合试剂B加入量的增加,其吸光度值也随之增加。但在加入400 μL混合试剂A和混合试剂B时,溶液显色受试剂亚硝基铁氰化钠影响,稳定性不佳,且空白样吸光度大于0.030[1-2]。故混合试剂A和混合试剂B的用量均为300 μL最佳。
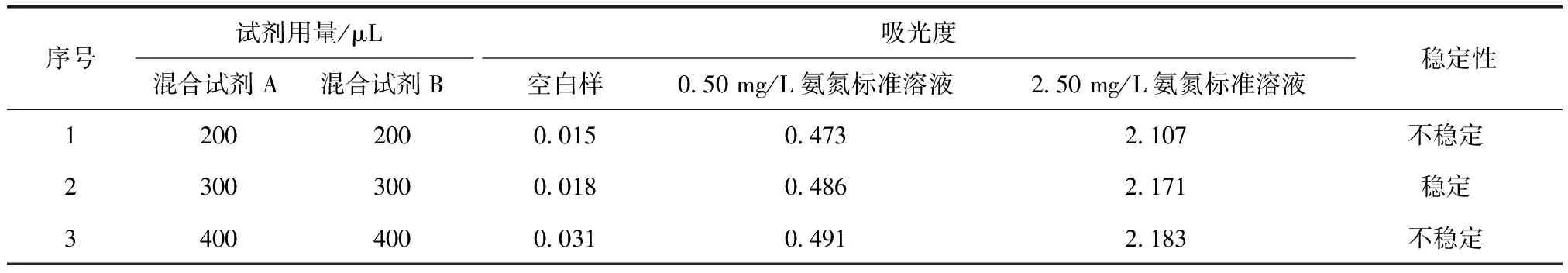
表1 混合试剂A与混合试剂B的用量对显色吸光度的影响
2.1.3 显色时间选择
分别取0.30、1.50、2.50 mg/L的氨氮标准溶液,在(25±2)℃室温下,按照1.3小节试验步骤进行试验。从加样定容就开始进行吸光度的扫描,记录90 min的结果如图1所示。不论低、中、高氨氮浓度均在加入5 min左右就开始出现快速的化学反应;10~15 min时,吸光度逐渐趋于平衡;待显色20 min后,化学反应完全完成,吸光度基本不变。由此可知,采用本法测定水中氨氮的显色时间为20 min,这是HJ 536—2009标准规定的60 min显色时间的1/3。
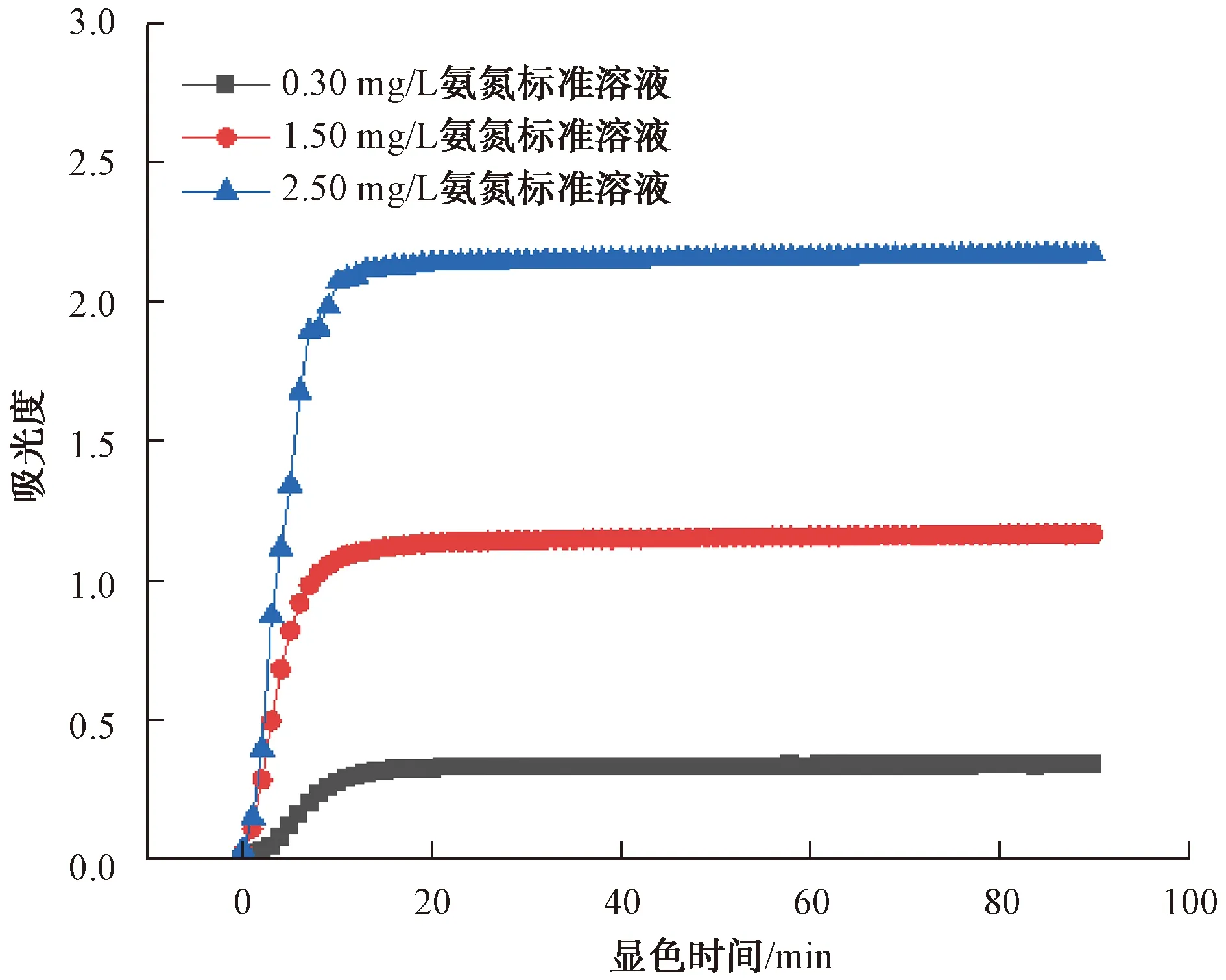
图1 时间与吸光度的变化曲线
2.1.4 显色温度选择
选取0.50 mg/L和2.50 mg/L 氨氮标准溶液,通过水浴条件考察了5、10、20、25、30、35、40、45 ℃温度条件下,显色20 min后的吸光度值(图2)。结果表明,低于10 ℃和高于35 ℃时,氨氮反应液的吸光度值均偏低,当温度在10~35 ℃时,其吸光度变化误差不大于2%。因此,反应温度以10~35 ℃为宜。
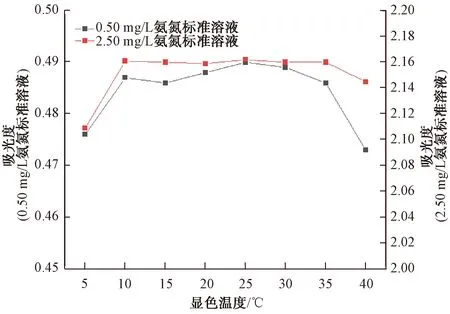
图2 不同温度下吸光度变化
2.2 试剂稳定性
随着混合试剂A和混合试剂B的失效,所测得的氨氮浓度会比实际值低。为确定混合试剂A和混合试剂B的有效使用时间,试验采用固定间隔时间在同一温度下,即25 ℃时,对最高量程氨氮浓度按照1.3小节试验方法进行结果测定,根据此测量值较实际浓度降低的误差来确定混合试剂A与混合试剂B的有效使用时间[9]。试验连续10周,每间隔一周检测2.50 mg/L氨氮标准溶液的检测结果。由图3可知,第1~8周的结果相对误差均小于2%,但到了第9周,检测结果显著降低,相对误差也超过了5%。因此,本方法所用混合试剂A与混合试剂B需要于4 ℃低温密封避光存放,有效期为2个月。
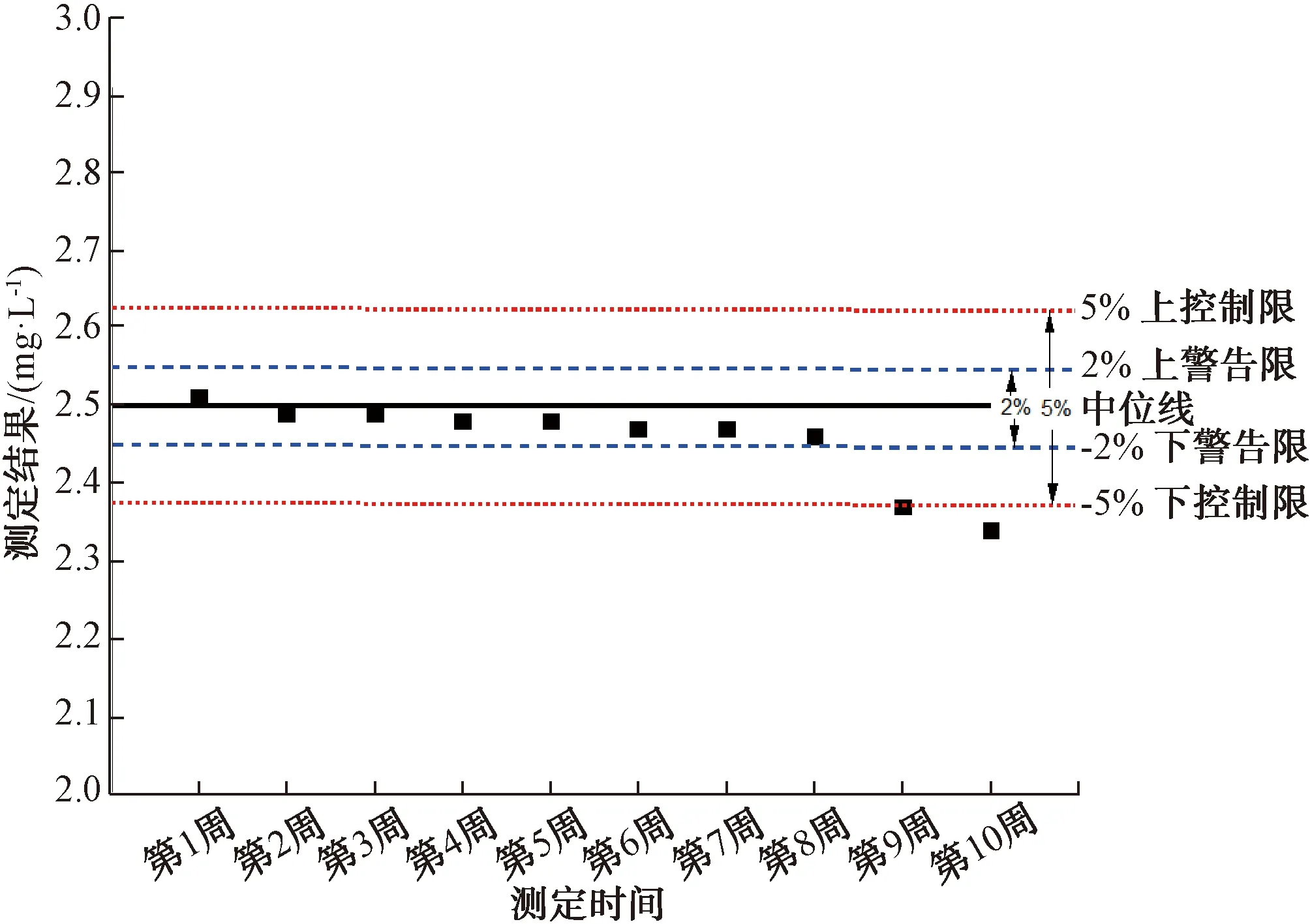
图3 混合试剂A和混合试剂B的有效使用时间试验
2.3 标准曲线与检出限
由图4可知,NH4Cl质量浓度在0~2.50 mg/L时,其含量与吸光度呈良好线性关系,线性方程为y=0.867x+0.007,线性相关系数R为0.999 8,说明该方法检测范围相比HJ 536—2009扩大了2.5倍。
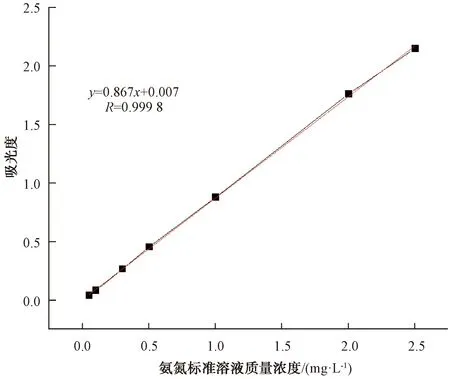
图4 氨氮的标准曲线
对质量浓度为0.03 mg/L的氨氮标准使用液分两组各测定8次,吸光度分别为0.033、0.035、0.038、0.037、0.032、0.035、0.038、0.034和0.032、0.036、0.038、0.037、0.035、0.036、0.034、0.036,带入曲线得到氨氮质量浓度分别为0.030、0.032、0.036、0.035、0.029、0.032、0.036、0.031 mg/L和0.029、0.033、0.036、0.035、0.032、0.033、0.031、0.033 mg/L。根据《环境监测分析方法标准制修订技术导则》(HJ 168—2020)[10]中附录 A1.1的一般确定方法,按式(1)得到方法检出限(MDL)分别为0.008 mg/L和0.006 mg/L,均满足选择的氨氮标准使用液在所得MDL的3~5倍的要求,故选择较大数据(0.008 mg/L)为本方法的MDL。
MDL=t(n-1,0.99)×S
(1)
其中:n——样品的平行测定次数;
t——自由度为n-1,置信度为99%时的t分布值(单侧);
S——n次平行测定的标准偏差。
当平行测定次数为8时,t值为2.998。
2.4 准确度和精密度试验
按照1.3小节试验方法的样品分析的全部步骤,用本法对生态环境监测标准样品研究所的标准样品[GSB 07-3164-2014号,保证值为(9.13±0.36)mg/L]进行7次平行测定。7次测定结果分别为9.17、9.05、9.28、9.19、9.31、9.22、9.01 mg/L,均满足保证值的不确定度要求,样品的平均值为9.18 mg/L,相对标准偏差为1.21%。选取某城镇污水处理厂再生水及地表水分别进行0.20 mg/L和0.50 mg/L两个质量浓度氨氮的加标,加标方法为在100.0 mL水样中加入0.2 mL或0.5 mL质量浓度为100.0 mg/L的氨氮标准溶液,每种样品做3个平行样,得到再生水和地表水的加标回收率分别为 94.0%、102.6%和102.0%、99.4%,说明该方法的精密度和准确度均良好(表2)。此外,HJ 536—2009 国标方法在消除干扰中提到水样中存在高浓度的钙会影响检测结果,而本研究所用次氯酸钙溶液为上清液,且用量较小,且从方法的精密度和准确度良好也验证了少量钙离子对检测结果不存在干扰,这与团体标准T/CPMA 021—2020[11]结论一致。
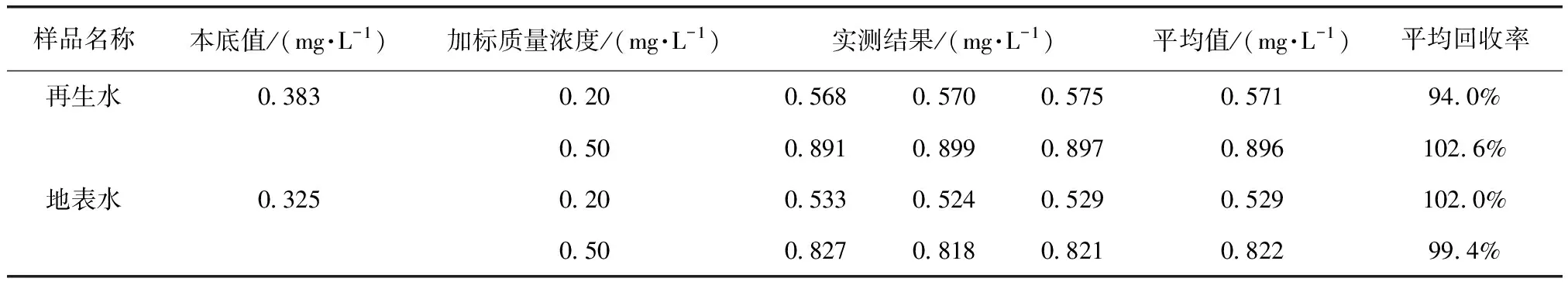
表2 加标回收试验 (n=3)
2.5 实际样本测定
选取某工业废水、某城镇生活污水、再生水和地表水4类实际水样,用该方法与 HJ 536—2009 国标方法进行对比。由表3可知,本试验方法与 HJ 536—2009 国标方法在精密度和准确度上基本一致,说明方法准确可靠。另外,由于该方法的检测范围比 HJ 536—2009 国标方法扩大了2.5倍,对于氨氮含量比较高的水样减少了取样过程中的稀释倍数,使得最终的测量结果相对误差略微低于HJ 536—2009 国标方法,表明检测量程范围的扩大有利于提高方法准确性。
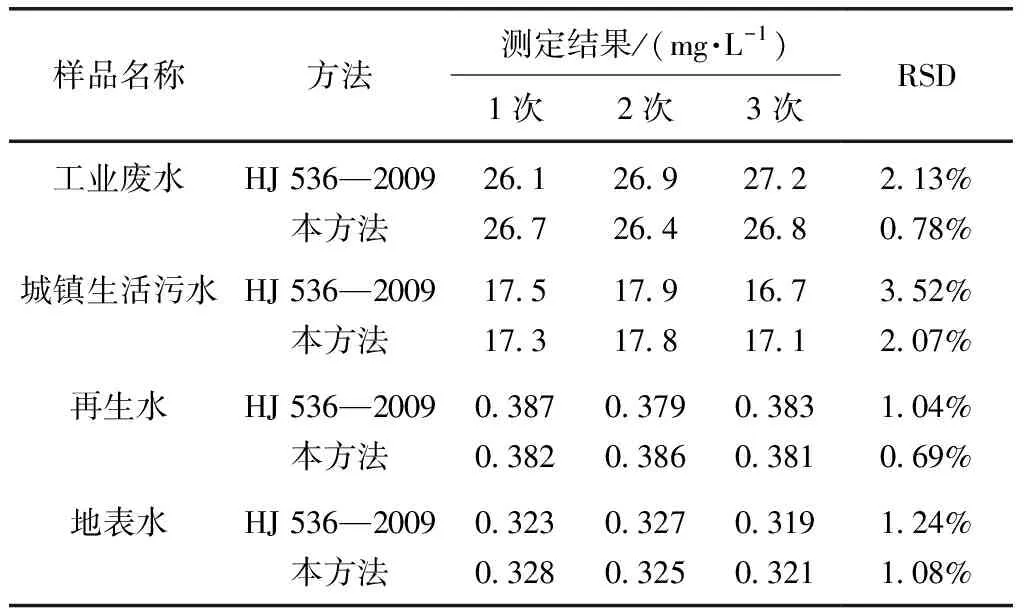
表3 该方法与HJ 536—2009的对比 (n=3)
3 结论
本研究建立了次氯酸钙-水杨酸钠分光光度法,可快速简便测定水质中的氨氮含量。通过配制水杨酸钠、亚硝基铁氰化钠混合显色剂,优化试剂配比,结果表明仅需反应20 min,氨氮便可显色完全,且氨氮质量浓度在0~2.50 mg/L时与吸光度线性良好,线性相关系数达到0.999 0以上。与HJ 536—2009国标法比较,检测范围扩大了2.5倍,显色时间为规定时间的1/3,准确度和精密度与HJ 536—2009国标法基本一致。另外,碱性次氯酸钙溶液与水杨酸钠、亚硝基铁氰化钠混合显色剂分别仅需加入300 μL参与反应,不仅节省了反应试剂用量,还降低了人工劳动强度,操作更简便。所建立新方法通过混合试剂的开发缩短了检测时间,并且不存在有毒有害试剂,不造成环境二次污染,可广泛推广于地表水、再生水、生活污水、工业废水等不同水体的氨氮测定。
