Na0.67Mn0.7Ni0.2Cu0.1O2的空气稳定性提升及其钠离子电池性能研究
2022-09-19黄志雄吴柄屿金子涵卢俊杰施少君
黄志雄,吴柄屿,金子涵,卢俊杰,杨 刚,施少君
(常熟理工学院 a.江苏省新型功能材料重点建设实验室;b.材料工程学院,江苏 常熟 215500)
0 引言
随着锂离子电池的不断发展以及其在电子产品、电动汽车等领域的运用,锂的需求量日益增加且锂资源在全球的分布不均使其价格日益昂贵[1].因此,开发其他二次电池来取代锂离子电池变得尤为迫切.钠作为全球储量丰富的元素(地球上含量排名第六),是不错的选择.同时,钠离子电池的反应机理与锂离子电池类似,且钠离子的标准氢电势是-2.71 V和锂离子的标准氢电势(-3.04 V)十分接近,因此钠离子电池有望在未来取代锂离子电池[2-3].
钠离子电池正极材料是决定钠离子电池性能的关键组成部分.正极材料主要包括层状氧化物、聚阴离子材料、普鲁士蓝材料和有机正极材料[4-5].其中层状正极氧化物由于其较高的理论容量、简易的制备流程和较高的充放电电压脱颖而出.而NaxMnO2由于Mn的资源广泛且价格低廉成了最主流的钠离子电池正极层状氧化物之一[6].但是由于高自旋的Mn3+的Jahn-Teller效应会引起相变和结构坍塌从而导致循环性能变差,且存放在空气中时,H2O和CO2容易与之反应生成NaOH和Na2CO3[7].为了克服这些问题,掺杂是最简单高效的办法.Hwang课题组[8]用Ni和Fe掺杂NaMnO2来缓解Jahn-Teller效应.他们制备的NaNi0.2Fe0.55Mn0.25O2能够在0.1 C下有125.4 mAh·g-1的容量且循环20圈容量保持率高达95.4%.Yang课题组证明了用高氧化态的过渡族金属能提高材料的空气稳定性[9].
本研究设计了一种Ni和Cu双掺杂取代Mn的Na0.67Mn0.7Ni0.2Cu0.1O2正极材料.该材料具有较好的电化学性能和空气稳定性.其中, Ni2+/Ni4+和Cu2+/Cu3+的高氧化还原电位为材料提供了高容量,而“双掺”又能很好地稳定该化合物,抑制其与空气中的H2O和CO2的反应.除此之外, Ni和Cu取代Mn还能缓解材料在循环过程中的Jahn-Teller效应,延长材料的循环寿命.
1 实验
1.1 材料合成
前驱体 Mn0.7Ni0.2Cu0.1CO3的合成:Mn、Ni和Cu 的硫酸盐按照7∶2∶1的比例加入40 mL的去离子水中,不断搅拌形成澄清透明的溶液A. 取沉淀剂NH4HCO3加入60 mL乙醇和去离子水的混合溶液中不断搅拌,命名为溶液B.缓缓将溶液A倒入溶液B中,不断搅拌后再倒入水热釜中,在200 ℃下反应16 h.冷却后在水和乙醇中离心3次得到前驱体(Mn0.7Ni0.2Cu0.1CO3).最后将前驱体放置于烘箱中干燥.
钠离子电池层状正极材料 P2-Na0.67Mn0.7Ni0.2Cu0.1O2的制备:按化学计量比取前驱体Mn0.7Ni0.2Cu0.1CO3(2 g)和 Na2CO3(0.67 g,过量10%) 均匀研磨混合后放入马弗炉中,在900 ℃下煅烧16 h.冷却后取出得到钠离子电池层状正极材料 P2-Na0.67Mn0.7Ni0.2Cu0.1O2.
1.2 材料表征
采用 Rigaku Smart-Lab X-ray diffractometer(扫描速度4°/min)对电极材料进行物相分析.采用扫描电子显微镜(SEM,Hitachi SU 8000)和透射电子显微镜(TEM, HRTEM,JEOL-2100F, 200 kV)对材料进行微观形貌结构分析.
1.3 电化学性能测试方法
工作电极的制备:将活性材料P2-Na0.67Mn0.7Ni0.2Cu0.1O2、导电碳和黏结剂PVDF 按照8∶1∶1的质量比混合后加入适量NMP.然后将黏稠液涂覆到铝箔上,放入烘箱在110 ℃下干燥24 h.对电极采用Na金属片,隔膜采用商用的玻璃纤维隔膜,电解液采用1 mol/L NaClO4溶于PC 和 5 vol%的FEC混合溶液.
电池测试:扣式电池的电化学性能在LAND CT2001A蓝电测试系统上进行.同时,在电化学工作站CHI660E上进行电池的循环伏安法(CV)测试.
2 结果与讨论
2.1 材料表征
首先,通过XRD分析了Na0.67Mn0.7Ni0.2Cu0.1O2和Na0.67MnO2的物相特征.如图1所示,XRD图谱中峰形十分尖锐,半高宽很小,说明本研究中合成的Na0.67Mn0.7Ni0.2Cu0.1O2和Na0.67MnO2结晶性都很好.同时,没有出现其他明显的杂峰,证明没有明显的杂质存在.经物相检索,XRD图谱与PDF#54-0894卡片的峰形、峰位、峰强相对应.其中,(002)峰是材料的主峰,它的出现证明了所得到的材料属于P2结构,对应的过渡族金属氧化物层和钠层的排序是AB BA排布.此外,Na0.67Mn0.7Ni0.2Cu0.1O2的(002)峰有一定的向左偏移,证明了在Ni和Cu加入后,材料的层间距扩大,有利于钠离子的传输.
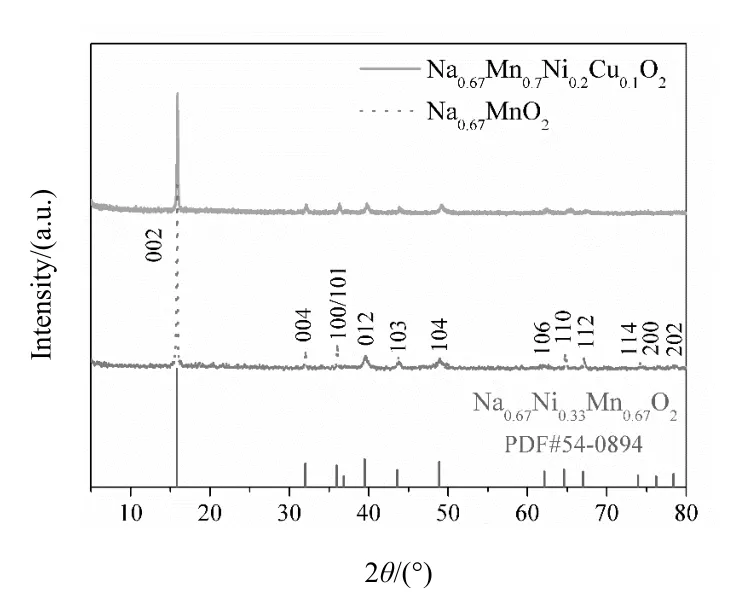
图1 Na0.67Mn0.7Ni0.2Cu0.1O2和Na0.67MnO2的XRD
本研究使用SEM来表征材料的形貌,如图2(a)~图2(b)所示.可以看出Na0.67MnO2是无定型的纳米颗粒,而Na0.67Mn0.7Ni0.2Cu0.1O2是均匀的球形.这样的球形形貌有利于缓解材料在充放电过程中的膨胀和收缩.然后通过TEM表征了材料的微观结构,如图2(c)和图 2(d)所示.可以看出,Na0.67MnO2的晶格条纹对应的是(100)面,这主要是由于Na0.67MnO2是沿着(100)面生长的.而Na0.67Mn0.7Ni0.2Cu0.1O2的晶格条纹对应的是(002)晶面,与XRD中得到的结果一致.这主要由于材料在合成过程中的球面生长.Na0.67MnO2的生长方式容易导致材料在充放电过程中溶解,且加剧材料的Jahn-Teller效应.而Na0.67Mn0.7Ni0.2Cu0.1O2的生长方式比较稳定,最外面的面比较稳定,能够有效抑制材料的溶解,并且一定程度上缓解材料的Jahn-Teller效应.为了证明材料中元素分布均匀,本研究做了TEM mapping的测试.如图3所示,可以看出Mn、Ni、Cu的分布十分均匀,没有其他杂质,同时也证明了材料中Cu的存在.这样的均匀分布证明了材料中没有Mn的团聚,而Ni和Cu的均匀分布能有效缓解电化学反应过程中锰的溶解和Jahn-Teller效应的发生.

图2 (a)Na0.67MnO2的SEM形貌图;(b)Na0.67Mn0.7Ni0.2Cu0.1O2的SEM形貌图;(c)Na0.67MnO2的高分辨TEM;(d)Na0.67Mn0.7Ni0.2Cu0.1O2的高分辨TEM

图3 Na0.67Mn0.7Ni0.2Cu0.1O2的Mapping图
2.2 电化学性能
循环伏安法(CV)被用来研究Na0.67Mn0.7Ni0.2Cu0.1O2在循环过程中的氧化还原反应情况,如图4所示.在3.5 V左右的氧化还原峰主要是由Ni2+/Ni3+/Ni4+和部分Mn3+/Mn4+的氧化还原引起的.而在高电压4.25 V左右的氧化还原峰主要是由Cu2+/Cu3+的氧化还原反应引起的.这也证明了Cu是有氧化还原活性的,能给电池提供容量.在2.3 V左右的氧化还原峰对主要归因于Mn3+/Mn4+的氧化还原反应.这些氧化还原反应的可逆性很高,所以Na0.67Mn0.7Ni0.2Cu0.1O2的循环稳定性能较好.

图4 Na0.67Mn0.7Ni0.2Cu0.1O2的循环伏安法(CV)
Na0.67Mn0.7Ni0.2Cu0.1O2和Na0.67MnO2在100 mA·g-1下循环50圈的恒流充放电性能如图5所示.可以看出,由于Jahn-Teller效应,Na0.67MnO2的放电容量快速衰减,其循环稳定性较差.而由于Ni和Cu的取代,Na0.67Mn0.7Ni0.2Cu0.1O2展现出较好的放电比容量和循环稳定性.初始放电容量高达129.6 mAh·g-1,在循环50圈后仍有100.6 mAh·g-1的放电比容量,其容量保持率约为77.6%.可以明显看出,Ni和Cu的氧化还原不仅能提供容量,还能一定程度上缓解Mn的Jahn-Teller效应,从而使材料的循环性能较为稳定.
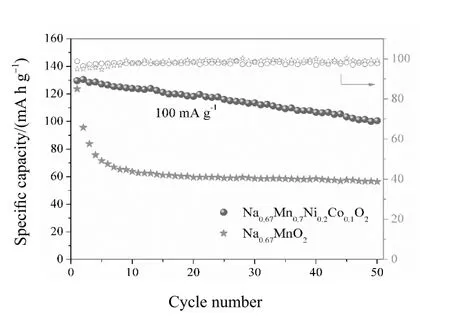
图5 Na0.67Mn0.7Ni0.2Cu0.1O2和Na0.67MnO2在100 mA·g-1下的恒流充放电性能
2.3 空气稳定性
最后,由于材料制备完成后需要存储和运输,因此其空气稳定性十分重要.本研究将Na0.67Mn0.7Ni0.2Cu0.1O2置于空气中10 d,然后测试其XRD来研究空气稳定性.从图6中可以看出,材料的XRD衍射峰几乎没有改变,证明了材料在空气中存储10 d后仍然十分稳定.这主要是由Ni2+/Ni4+和Cu2+/Cu3+的较高氧化还原电压导致的.这也证明了Ni和Cu的掺杂能十分有效地稳定材料的结构.
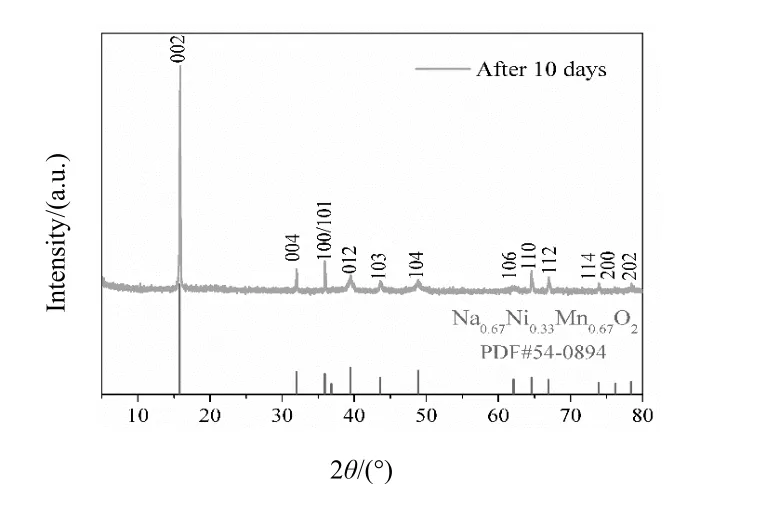
图6 Na0.67Mn0.7Ni0.2Cu0.1O2在空气中放置10 d后的XRD
3 结论
本研究采用水热法合成了Ni和Cu取代Mn的P2-Na0.67Mn0.7Ni0.2Cu0.1O2钠离子电池正极层状氧化物.由于Ni2+/Ni4+和Cu2+/Cu3+的氧化还原电位较高,所以其在空气中不容易与H2O和CO2反应,同时Ni和Cu的掺杂能提供容量,并且缓解了Mn的Jahn-Teller效应和抑制锰的溶解,从而有效提高了材料在循环过程中的稳定性.P2-Na0.67Mn0.7Ni0.2Cu0.1O2在100 mA·g-1下初始放电容量高达129.6 mAh·g-1,在循环50圈后仍然有100.6 mAh·g-1的放电比容量.这样的P2-Na0.67Mn0.7Ni0.2Cu0.1O2是钠离子电池正极材料中的有力竞争者.
