炮姜炮制过程中6-姜酚的转化规律及抗氧化活性变化研究
2022-09-13王学芹顾从文黄保生韩燕全吴德玲
王学芹,卜 超,顾从文,黄保生,韩燕全,洪 燕,吴德玲
1安徽中医药大学第一附属医院 国家中医药管理局中药制剂三级实验室,合肥 230031;2安徽中医药大学 中药复方安徽省重点实验室,合肥 230012
干姜为姜科植物姜ZingiberofficinaleRose.的干燥根茎,味辛,性温,具有温中散寒,回阳通脉,温肺化饮的功效[1]。炮姜是其临床常用的炮制品,经砂烫炮制后可以缓和干姜的辛辣之性,并增加其温经止血之功效。研究表明,姜酚类成分是姜中主要的辛辣和活性成分,包括6-姜酚、8-姜酚、10-姜酚和12-姜酚等数十种,其具有抗氧化、抗炎解热、神经保护和抗肿瘤等多种药理活性[2-5]。姜中姜酚类成分以6-姜酚含量最高,也是《中国药典》2020版中生姜、干姜和炮姜含量测定的指标成分。抗氧化活性是6-姜酚具有的主要药理活性之一,6-姜酚分子结构中具有β-羟基酮以及酚羟基的结构,因此在清除羟基自由基、超氧自由基以及脂质过氧化物等方面具有很好的效果,还能有效的保护过氧化氢所致的DNA损伤,是一种性质优良的天然抗氧化剂[6,7]。课题组前期对干姜炮制前后的化学成分的定性和定量分析结果表明,干姜在炮制成炮姜后,姜酚类成分含量明显降低,其中,6-姜酚的含量降低在15%~42%之间;而6-姜烯酚、8-姜烯酚和10-姜烯酚等成分含量则显著升高,且在炮制过程中会有新成分姜酮的产生[8]。但是,炮制对炮姜姜酚成分转化的规律及其活性影响等尚不完全明确,值得进一步研究。
干姜炮制成炮姜后,由于其所含姜酚类成分的“质”“量”变化,药效作用也发生了相应的转变。为了探讨炮姜炮制过程中姜酚类成分的转化规律以及其成分转化对活性的影响,本实验通过测定不同砂烫工艺的炮姜样品中6-姜酚、6-姜烯酚和姜酮的含量变化,结合6-姜酚单体模拟炮制方法,探讨6-姜酚及其转化产物6-姜烯酚、姜酮随炮制时间和炮制温度的变化规律;同时,采用体外抗氧化的方法,初步验证成分转化与抗氧化活性的相关性,以期能为揭示炮姜的炮制机理提供依据。
1 材料
1.1 仪器
Waters Acquity UPLC超高效液相色谱仪(美国Waters 公司);分析天平(1/10万,上海梅特勒-托利多有限公司,ME55);超声波清洗仪(江苏省昆山超声仪器有限公司,KQ-300DE);离心机(科大创新股份有限公司中传分公司,KDC-16H);酶标仪(Thermo Fisher Scientific,1510-02261C)。
1.2 试药
6-姜酚(纯度≥ 98.0%,批号13012303)、6-姜烯酚(纯度为≥ 98.0%,批号DST190623-030)、姜酮(纯度为≥ 98.0%,批号DST190513-032)对照品均购于成都德思特生物技术有限公司;色谱级甲醇(Sigma,批号67-56-1);色谱级乙腈(Sigma,批号75-05-8);屈臣氏蒸馏水(广州屈臣氏食品饮料有限公司,批号20210302);1,1-二苯基-2-三硝基苯肼(DPPH,上海源叶生物科技有限公司,批号TN1121CB14);2,2′-联氨双(3-乙基苯并噻唑啉-6-磺酸)(ABTS,批号HA23)、2,4,6-三吡啶基三嗪(TPTZ,批号D1417044)均购于上海笛柏生物科技有限公司。
干姜饮片购于铜陵禾田中药饮片股份有限公司(批号20191012),经本文通讯作者安徽中医药大学第一附属医院韩燕全主任中药师鉴定符合《中国药典》2020版项下性状鉴别规定。
2 方法与结果
2.1 不同砂烫工艺对干姜中6-姜酚、6-姜烯酚及姜酮含量的影响
2.1.1 样品的制备
称取净干姜饮片每份100 g,共计10份。留取一份备用,其余参考课题组前期的研究方法[9],于(170 ± 2)、(190 ± 2)、(210 ± 2)℃分别砂烫6、7、8 min,制备成不同工艺的炮姜(见表1)。实验中测定离锅底1.0 cm处温度设定为砂烫温度,不断翻炒至试验设定时间,急出锅,筛去砂子,放凉,粉碎,过40目筛,即得不同砂烫工艺的炮姜样品粉末,实验重复进行两次,结果取平均值。
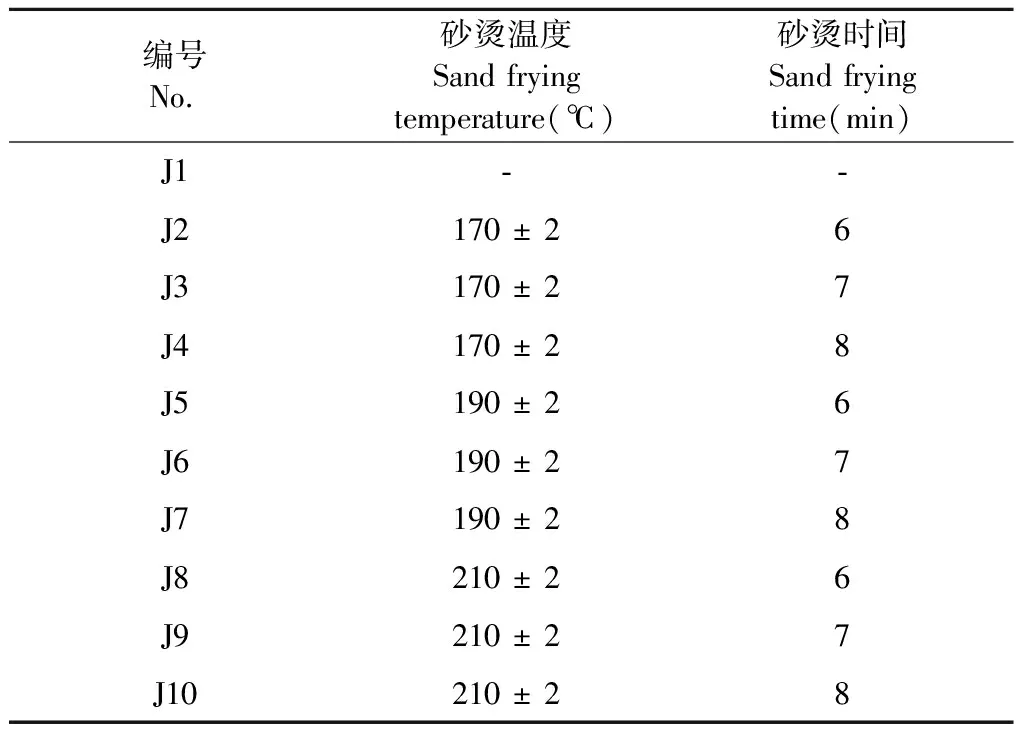
表1 干姜和不同砂烫工艺的炮姜样品
2.1.2 对照品溶液的制备
精密称取6-姜酚、6-姜烯酚、姜酮对照品适量,加甲醇制成每1 mL含6-姜酚0.831 mg、6-姜烯酚0.434 mg、姜酮0.170 mg的对照品储备液,精密移取上述对照品储备液1.0、2.0、3.0、4.0、5.0 mL 置于10 mL量瓶中,加甲醇定容至刻度,摇匀,得到系列浓度的混合对照品溶液。
2.1.3 供试品溶液制备
取干姜和不同砂烫工艺的炮姜样品粉末(过40目筛)约0.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇20 mL,称定重量,超声处理(功率150 W,频率40 kHz)30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.1.4 色谱条件
色谱条件:Agilent ZORBAX Eclipse Plus C18色谱柱(2.1 × 100 mm,1.8 μm);乙腈(A)-水溶液(B)为流动相,梯度洗脱:0~12 min,10%→75% A;12~17 min,75% A;17~18 min,75%→90% A;18~22 min,90% A;22~23 min,90%→10% A,23~25 min,10% A,检测波长为280 nm,流速为0.25 mL/min,柱温为30 ℃,进样量:2 μL,UPLC图见图1。
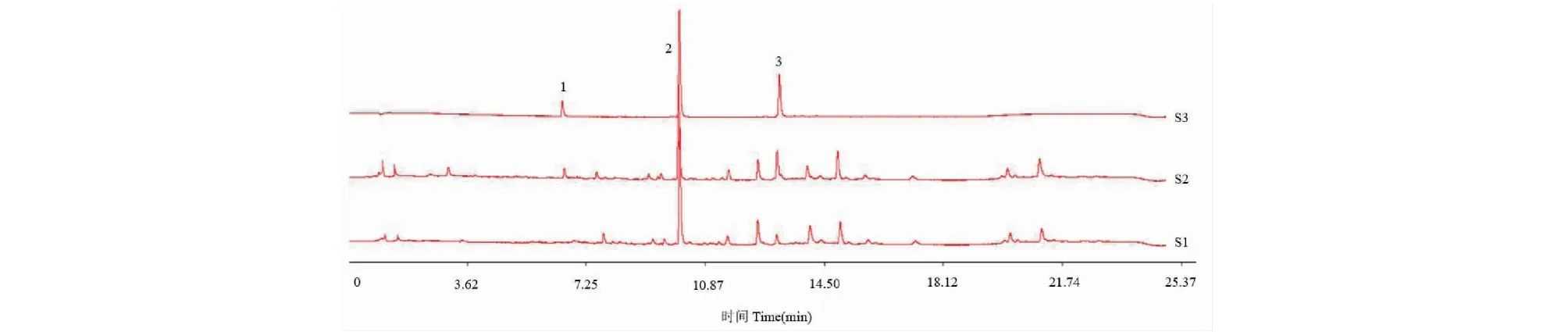
图1 干姜(S1)、炮姜(S2)和混合对照品(S3)的UPLC图
2.1.5 方法学考察
2.1.5.1 检测限与定量限
分别取6-姜酚、6-姜烯酚、姜酮对照品溶液适量,加入甲醇溶液逐步稀释,以信噪比 3∶1时对应对照品浓度为检测限(limit of detection,LOD),以信噪比10∶1时对应对照品浓度为定量限(limit of quantitation,LOQ)进行测定,结果见表2。
2.1.5.2 线性关系考察
分别精密吸取“2.1.2”项下不同质量浓度的混合对照品溶液,按“2.1.4”项下色谱条件检测,测定峰面积,以6-姜酚、6-姜烯酚、姜酮的质量浓度为横坐标(X),色谱峰面积(Y)为纵坐标,绘制标准曲线,计算回归方程,回归方程见表2。
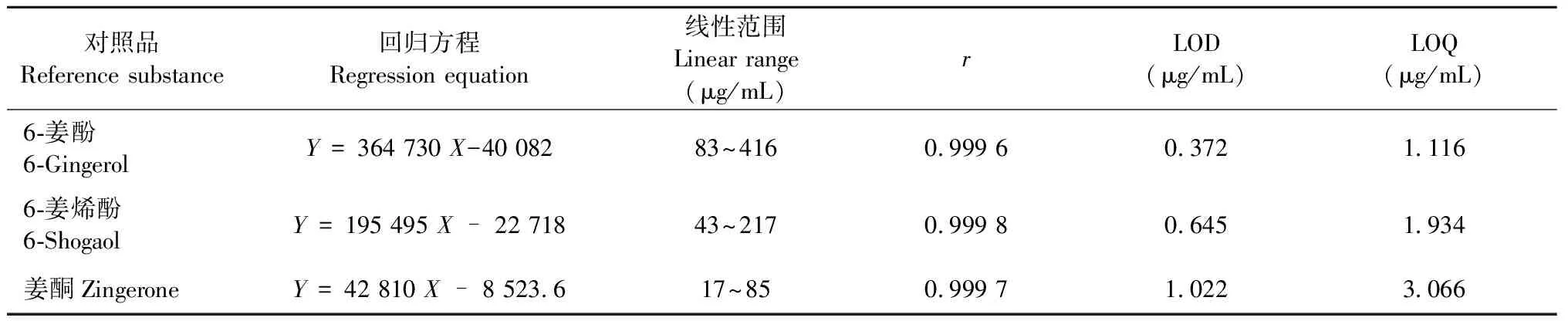
表2 6-姜酚、6-姜烯酚和姜酮的线性回归方程
2.1.5.3 精密度试验
精密吸取“2.1.2”项下混合对照品溶液2 μL,按“2.1.4”项下色谱条件连续进样6次,计算6-姜酚、6-姜烯酚、姜酮峰面积的RSD分别为0.96%、0.73%、0.18%,表明仪器精密度良好。
2.1.5.4 稳定性试验
取10号(J10)供试品溶液,按“2.1.4”项下色谱条件,分别在0、2、4、8、12、24 h进样测定,计算6-姜酚、6-姜烯酚、姜酮的峰面积的RSD分别为2.50%、2.26%、3.16%,表明样品中这三种姜酚类成分在24 h内稳定性良好。
2.1.5.5 重复性试验
取5号(J5)炮姜样品粉末,按“2.1.3”项下制备方法制备6份供试品,再按“2.1.4”项下条件测定,计算6-姜酚、6-姜烯酚、姜酮含量的平均值分别为5.02、1.03、0.09 mg/g,RSD分别为1.67%、1.56%、2.58%,表明该方法重复性良好。
2.1.5.6 加样回收试验
取6号(J6)炮姜样品粉末0.25 g左右,精密称定,共 6 份,加入各对照品母液适量,按“2.1.3”项下方法制备供试品溶液,按“2.1.4”项下色谱条件测定,计算加样回收率和RSD值,结果见表3。
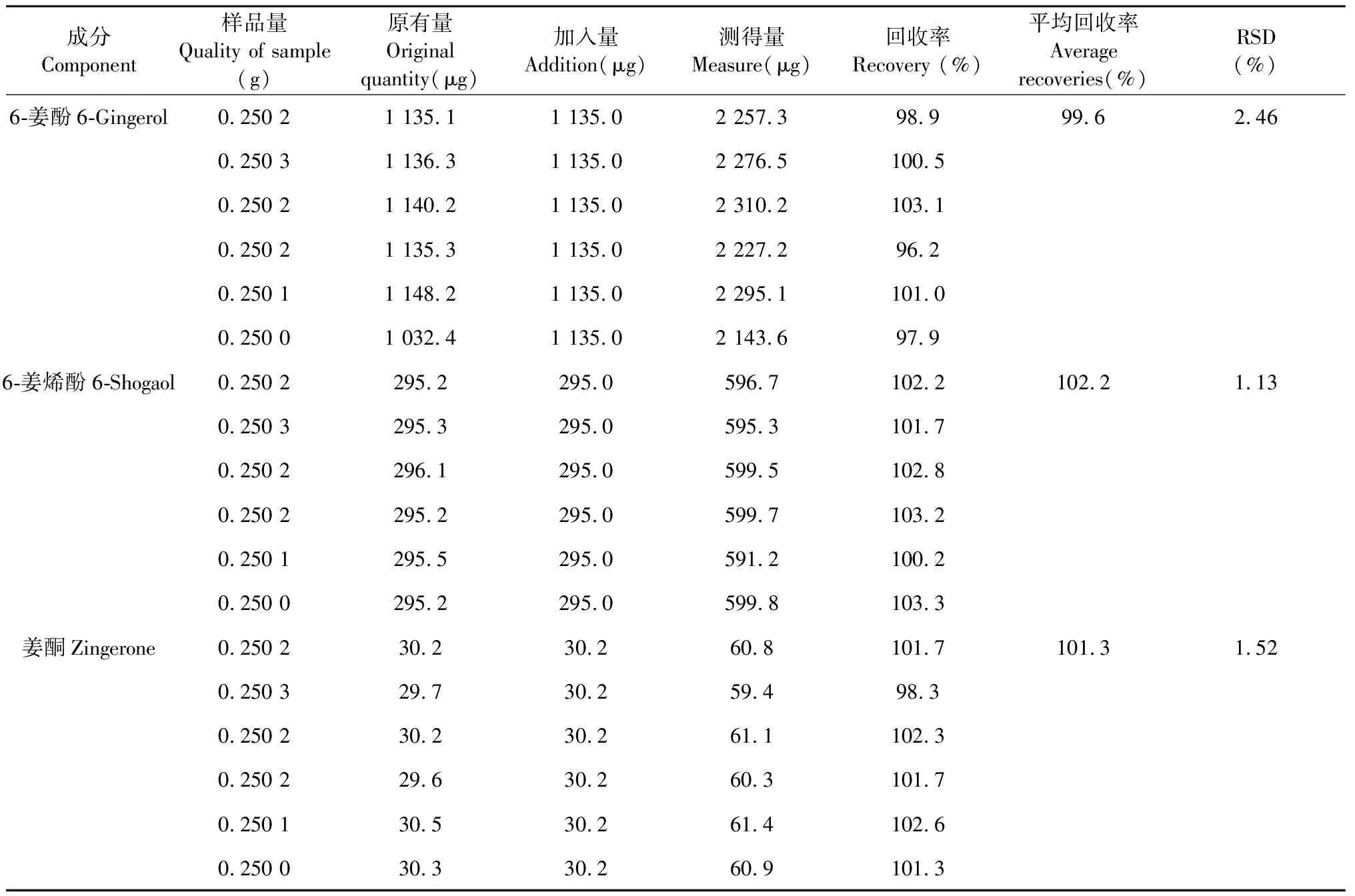
表3 6-姜酚、6-姜烯酚和姜酮的加样回收率实验结果
2.1.6 样品含量测定
取“2.1.3”项下的供试品溶液,按“2.1.4”项下色谱条件测定,进样量为2 μL,根据外标法计算6-姜酚、6-姜烯酚、姜酮的含量,结果见表4。
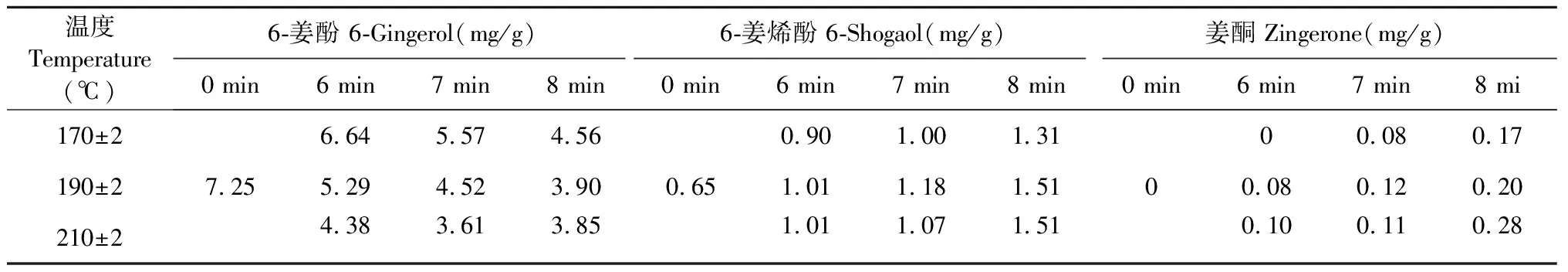
表4 不同砂烫温度和时间对干姜中6-姜酚、6-姜烯酚及姜酮含量的影响(n=2)
结果表明,随着砂烫时间的延长和温度的升高,6-姜酚含量逐渐降低,6-姜烯酚和姜酮的含量逐渐升高。其中,干姜样品和(170±2)℃砂烫6 min的炮姜样品中均未检测到姜酮,在温度和时间达到一定程度,即(170±2)℃砂烫7 min和(190±2)℃砂烫6 min时才检测到姜酮的产生,说明姜酮为干姜经炮制后新生成的成分。
2.2 模拟炮制对6-姜酚及其转化产物6-姜烯酚、姜酮含量的影响
2.2.1 6-姜酚模拟炮制供试品的制备
精密称定6-姜酚对照品 5 mg左右,共21份,置于10 mL容量瓶中,留取一份备用,其余于170、190、210、230 ℃下,分别油浴4、6、8、10、12 min,放冷,加甲醇溶解定容,即得6-姜酚模拟炮制的供试品溶液。
2.2.2 6-姜酚模拟炮制产物的含量测定
取“2.2.1”项下的供试品溶液,按“2.1.4”的色谱条件进样,6-姜酚和其模拟炮制品的代表性UPLC图见图2,S2~S5分别为6-姜酚170、190、210、230 ℃油浴8 min的模拟炮制品。
图2 6-姜酚(S1)和模拟炮制品(S2~S5)的代表性UPLC图
通过计算6-姜酚模拟炮制品中6-姜酚及其转化产物6-姜烯酚和姜酮的含量,以含量对炮制温度和时间作图,得三种成分含量随炮制时间、温度的变化趋势图,结果见图3。
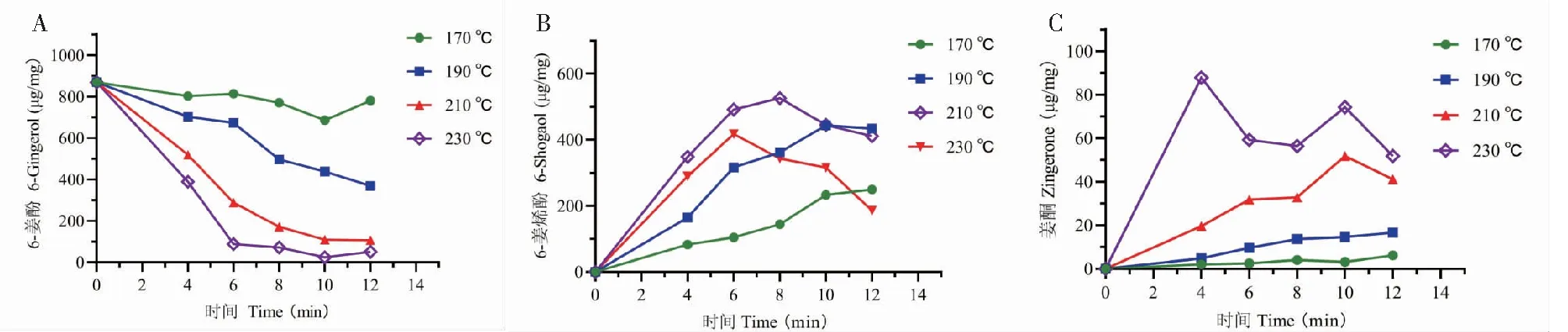
图3 6-姜酚、6-姜烯酚和姜酮含量变化趋势(n=2)
图3结果显示,6-姜酚、6-姜烯酚和姜酮的含量随油浴时间和油浴温度的变化呈现一定的量变规律。图3A可见,6-姜酚在油浴温度为170 ℃时,随着油浴时间的延长,含量呈现缓慢下降的趋势;油浴温度达到190 ℃、6 min时下降趋势开始加快,当温度达到230 ℃以上时,6-姜酚含量呈现加快下降趋势,但6 min之后降低幅度较平缓。
由图3B可见,6-姜烯酚含量在190 ℃以内时,随着油浴时间的延长逐渐上升,在10 min时达到平台期,当温度在210 ℃以上时,上升趋势进一步加快,但在6 min左右时开始呈现下降趋势;姜酮的量变规律如图3C所见,当油浴温度在190 ℃以内时,随着油浴时间的延长呈现缓慢上升的趋势,当温度在210 ℃以上时,姜酮的上升速率开始加快,且210 ℃和230 ℃均在10 min 时开始下降。
2.2.3 6-姜酚模拟炮制结果分析
根据文献报道,姜烯酚类成分尤其是6-姜烯酚主要存在于干姜中,生姜中含量较少[10,11]。这可能与生姜在干燥过程中姜酚类成分发生脱水反应生成姜烯酚类有关,而姜酮只有在加工成炮姜过程中才出现,表明姜酮的产生需要达到一定的温度和时间。本实验模拟炮制的结果证实了6-姜酚在油浴加热后生成了6-姜烯酚和姜酮,如图2和图3可见,其主要机理是6-姜酚在一定温度下会发生脱水反应而生成6-姜烯酚,而在温度达到210 ℃左右时,可引发逆羟醛缩合反应生成姜酮和己醛[12]。6-姜酚的转化机理见图4。
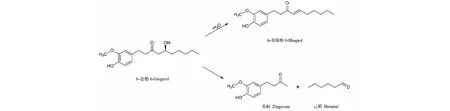
图4 6-姜酚转化机理图
2.3 抗氧化活性测定
2.3.1 供试品溶液的制备
按照“2.1.3”方法制备不同砂烫工艺的炮姜样品供试品溶液,按照“2.2.1”的方法制备6-姜酚模拟炮制产物供试品溶液,再用甲醇分别稀释至1 mg/mL和30 μg/mL。
2.3.2 DPPH自由基清除活性
参考文献的方法,稍加改进[13]。在96孔板中分别加入100 μL 0.1 mmol/L的DPPH-甲醇溶液和100 μL“2.3.1”项下供试品溶液,充分混匀,置酶标仪中避光孵育30 min,在517 nm 测定反应溶液的吸光度值(A),以100 μL甲醇和100 μL供试品溶液为对照组(A1)。以100 μL DPPH溶液和100 μL甲醇为空白组(A0)。每组平行设置三个复孔,按清除率公式计算各样品的清除率:DPPH清除率=[1-(A-A1)/A0]×100%,结果见图5。
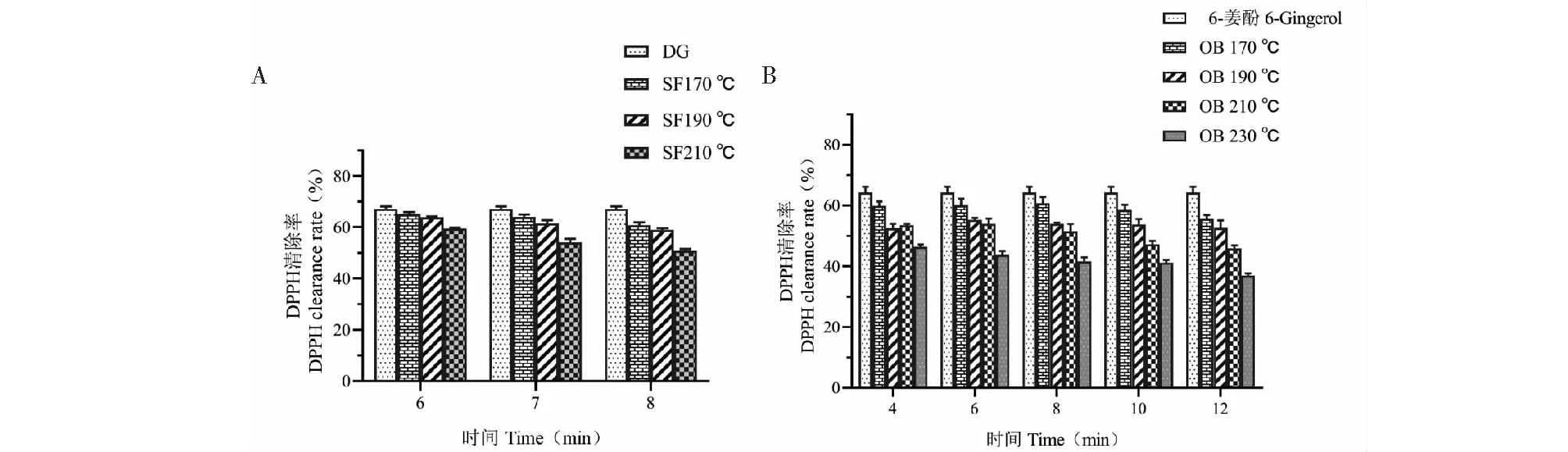
图5 不同砂烫工艺的炮姜样品和6-姜酚模拟炮制产物对DPPH的清除作用
炮姜样品和6-姜酚模拟炮制产物的DPPH清除率均随炮制时间的延长和温度的升高逐渐降低。由图5A所示,当砂温度在190 ℃、时间7 min以内时,炮姜样品的DPPH清除率会缓慢降低,当温度在210 ℃、时间8 min以上时,DPPH清除率则会显著降低;由图5B所示,6-姜酚模拟炮制产物比炮姜样品更易受温度和时间的影响,其DPPH清除率在油浴190 ℃、4 min时即出现显著下降变化。
2.3.3 ABTS 自由基清除活性
参考文献的方法,稍加改进[14]。将7.4 mmol/L ABTS溶液与2.6 mmol/L过硫酸钾溶液混合,置于暗处孵育12 h,得ABTS储备液。使用前将ABTS储备液用蒸馏水稀释至ABTS工作液。在96孔板中分别加入20 μL供试品溶液和180 μL的ABTS工作液,于室温孵育6 min后,在734 nm处测量反应溶液的吸光度值(A),以20 μL供试品溶液和180 μL蒸馏水为对照组(A1),以20 μL ABTS和180 μL蒸馏水为空白组(A0),按清除率公式计算各样品的清除率:ABTS清除率=[1-(A-A1)/A0]×100%,结果见图6。
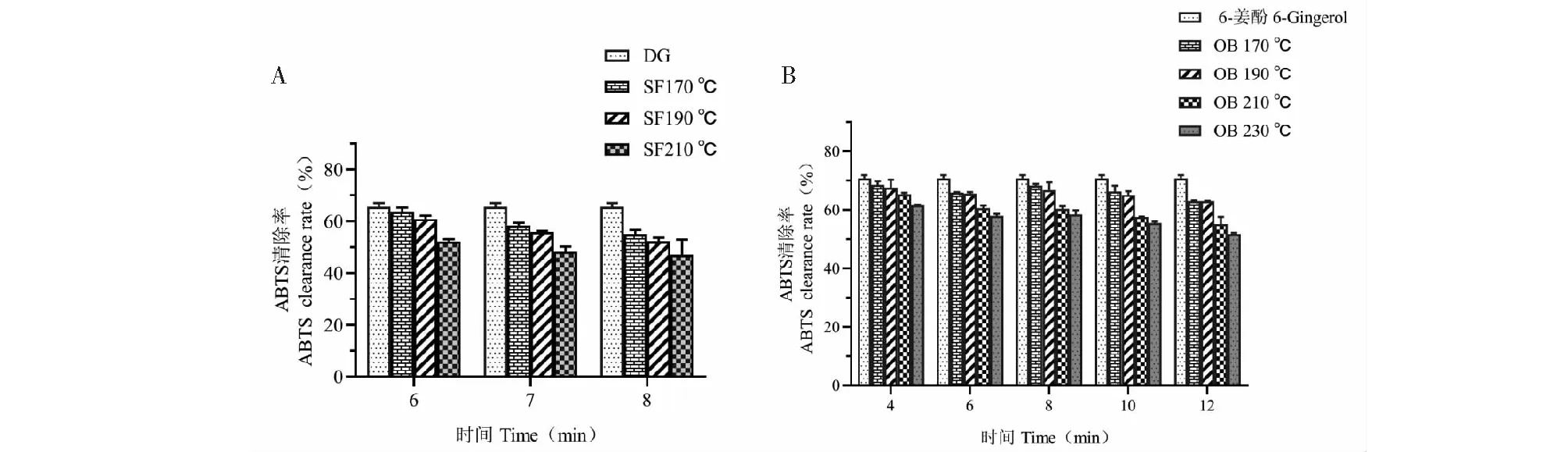
图6 不同砂烫工艺的炮姜样品和6-姜酚模拟炮制产物对ABTS的清除作用
由图6A所示,炮姜样品的ABTS清除率变化趋势与DPPH清除率结果相似,其中下降最显著的为210 ℃砂烫8 min的炮姜样品,下降了16.32%,相同时间下,温度越高,ABTS清除率下降越显著;由图6B可见,6-姜酚模拟炮制产物的ABTS清除率变化趋势总体呈逐渐下降的趋势,并随着油浴时间的延长和温度的升高逐渐显著。
2.3.4 总还原能力测定(FRAP法)
参考文献的方法,稍加改进[15]。将100 mL 300 mmol/L乙酸盐缓冲液,10 mL 10 mmol/L TPTZ工作液,10 mL 20 mmol/L FeCl3溶液混合,避光保存,得FRAP工作液,于96孔板中分别加入20 μL供试品溶液和180 μL的FRAP工作液,振摇混匀,在室温下反应30 min,于593 nm处测定吸光度值(A样);以甲醇为空白组记(A0)。
以不同浓度FeSO4溶液的吸光度值为纵坐标,质量浓度为横坐标,绘标准曲线,FeSO4的回归方程为A= 0.837 5X+ 0.057 3(r= 0.999 1),在质量浓度为0.239~1.217范围内线性关系良好。以公式A=A样-A0计算,代入上述标准曲线,计算FeSO4当量,结果见图7。
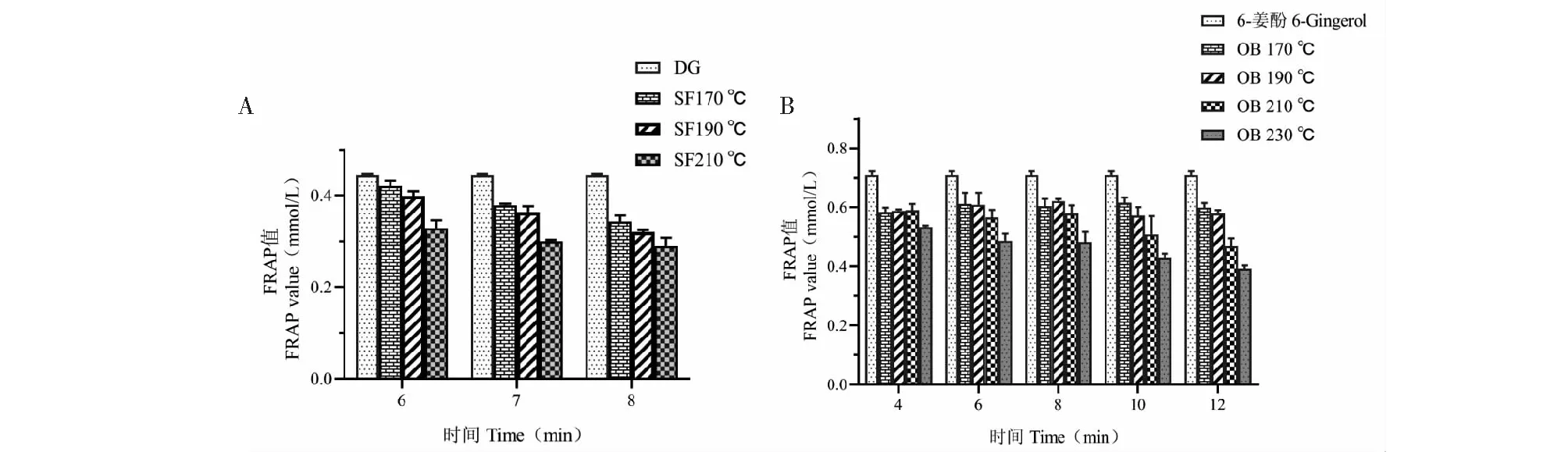
图7 不同砂烫工艺的炮姜样品和6-姜酚模拟炮制产物的总还原能力
由图7A所示,炮姜样品的总还原能力的变化趋势与DPPH和ABTS清除率变化趋势一致,210 ℃的炮姜样品的总还原能力随砂烫时间的延长逐渐降低后趋于稳定;在图7B中,模拟炮制产物的总还原能力在油浴时间较短时,没有明显的变化规律,当油浴时间延长至10、12 min时,总还原能力才呈现逐渐降低的趋势。
2.4 6-姜酚含量与抗氧化性相关性分析
为了排除干姜和炮姜样品中其他成分对抗氧化活性的影响,实验以6-姜酚及其模拟炮制产物作为研究对象,采用SPSS 23.0软件对模拟炮制产物中6-姜酚含量与DPPH清除率、ABTS清除率和总还原能力等抗氧化性指标进行相关性分析,Prism graphpad 8.0.1绘图,结果见表5和图8。
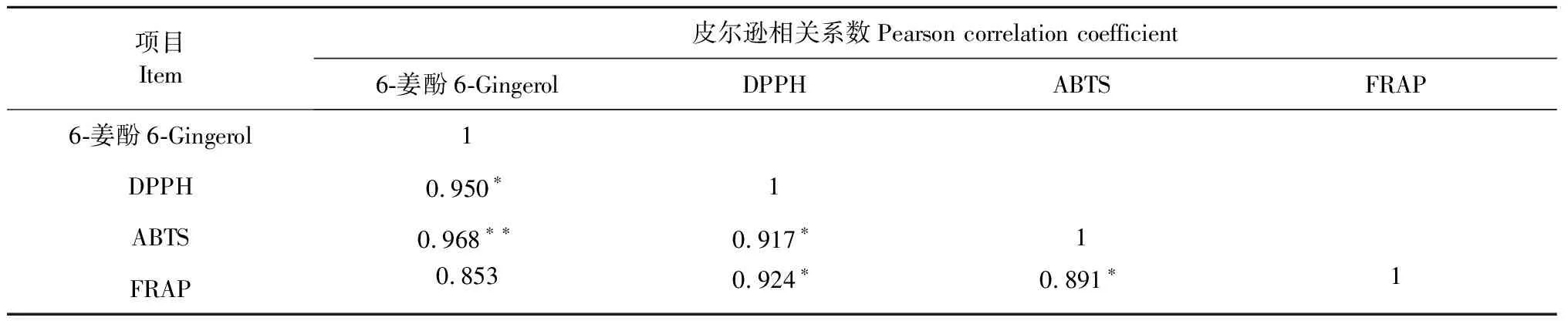
表5 6-姜酚含量与抗氧化性相关性分析

图8 6-姜酚含量与抗氧化性相关性分析热图
由表5和图8可知,6-姜酚含量与ABTS清除率在0.01水平极显著正相关,6-姜酚含量与DPPH清除率、FRAP 清除率在0.05水平显著正相关,因此6-姜酚含量与抗氧化性之间存在相关性。
3 讨论与结论
课题组前期在炮制温度180~200 ℃,炮制时间6、7、8 min中优选炮姜的炮制工艺,本实验在此基础上选取了170±2、190±2、210±2 ℃分别炮制6、7、8 min的工艺,制备不同砂烫工艺的炮姜样品。预实验对6-姜酚模拟炮制的温度和时间进行了考察,发现油浴温度在170 ℃以下时,6-姜酚模拟炮制产物中未能检测到姜酮,当油浴温度在250 ℃,油浴时间15 min时,6-姜酚模拟炮制产物已出现碳化现象,因此我们选取油浴温度170、190、210、230 ℃,时间4、6、8、10、12 min 来作为6-姜酚模拟炮制的条件考察。
通过不同砂烫工艺炮姜样品中6-姜酚含量及抗氧化活性结果分析,可以看出当砂烫温度在(190±2)℃、时间7 min以内时,炮姜样品的外观符合炮制品质量要求,其6-姜酚的含量也满足炮姜的质量控制要求,对抗氧化活性的影响也较小。因此,在确定炮姜的炮制工艺时,砂烫温度应选择在190 ℃左右,砂烫时间7 min为宜,这与课题组前期优选的炮姜炮制工艺195 ℃,7 min相近。6-姜酚模拟炮制结合体外抗氧化实验的结果表明,其含量与抗氧化活性之间存在显著正相关,即随着炮制时间的延长和炮制温度的升高,6-姜酚部分转化为6-姜烯酚和姜酮,使得炮姜的抗氧化活性也逐渐降低减弱,这表明炮制加工会在一定程度上减弱炮姜样品的抗氧化活性。
本文对6-姜酚模拟炮制产物中6-姜酚及其转化产物6-姜烯酚和姜酮的量变规律及对抗氧化活性的影响进行了初步研究,因6-姜酚含有酚羟基和β-羟基酮,有较明确的抗氧化活性,因此选择了体外抗氧化这一指标,能够初步体现其活性变化。由于干姜炮制成炮姜,主要增强了其温经止血功效,我们后续将更有针对性地选择与炮姜功效相关的指标如凝血、止血等,通过细胞实验和整体动物实验综合评价炮制过程中姜酚类成分转化对炮姜功效的影响。
