电感耦合等离子体串联质谱测定婴幼儿谷类辅助食品中的重金属镉
2022-09-05蔡松韬谢华林黄建华
蔡松韬, 谢华林, 黄建华
1. 湖南工学院材料科学与工程学院, 湖南 衡阳 421002 2. 长江师范学院化学化工学院, 重庆 408100 3. 湖南省中医药研究院中药研究所, 湖南 长沙 410013
引 言
婴幼儿谷类辅助食品是婴幼儿营养的重要能量来源[1]。 食品中的Cd残留会损害呼吸系统, 对肝或肾脏造成积蓄性危害, 并会引起骨质疏松和软化, 国际癌症研究机构(IARC)将Cd确定为一类致癌物[2]。 为此, 欧盟对婴幼儿谷类辅助食品中Cd残留制定了0.04 mg·kg-1的限量标准。 婴幼儿谷类辅助食品的主要原料为大米, 而水稻极易从其生长的土壤和水中吸收重金属Cd积累到谷粒中, 导致大米中Cd的残留浓度相对较高[3]。 最近, 香港消委会抽取17款婴幼儿谷类辅助食品进行检测发现, 包括多个国际名牌在内的近八成样本检出了重金属Cd。 基于我国GB 10769—2010《食品安全国家标准婴幼儿谷类辅助食品》中并没有对Cd的最高残留规定限量标准, 国家卫生健康委员会和国家市场监督管理总局首次对婴幼儿谷类辅助食品中Cd的残留制定了0.06 mg·kg-1的临时限量标准。 因此, 建立精准可靠测定婴幼儿谷类辅助食品中Cd含量的分析方法具有重要且紧迫的现实意义。
目前, 国内外对食品中Cd的残留进行了大量研究[4-6], 但即使采用电感耦合等离子体质谱(ICP-MS)所面临的干扰仍然是影响准确测定Cd的难题。 在Mo基质中, Cd的所有同位素均会受到Mo基离子干扰, 甚至采用高分辨率的扇形磁场(SF)ICP-MS也无法消除[7]。 通过沉淀和固相萃取分离基质是ICP-MS测定复杂基体中痕量Cd的重要手段[8], 但耗时的化学分离过程增加了样品污染和分析物损失的风险。 碰撞反应池(CRC)为ICP-MS提供了消除干扰的通用方法, 但碰撞模式无法消除同量异位素的干扰, 而反应历程不可预知导致反应副产物离子的形成会影响分析结果的准确性和稳定性, 为更好地控制反应过程, 传统的四极杆ICP-MS(ICP-QMS)通常采用反应活性较弱的H2为反应气通过原位质量法消除干扰[9]。
电感耦合等离子体串联质谱(ICP-MS/MS)利用增设在CRC的第一四极杆质量过滤器(Q1), 仅允许指定质荷比(m/z)的离子进入CRC, 极大地提高了CRC中的选择性反应, 通过第二四极杆质量过滤器(Q2)选择高丰度无干扰的目标m/z离子(分析元素产物离子)进入检测器, 为复杂基质样品中痕量以及超痕量元素的测定提供了强有力工具[10-12]。 本研究采用微波消解处理婴幼儿谷类辅助食品, 利用ICP-MS/MS测定其中的重金属元素Cd的含量, 基于MS/MS模式下选择性反应的化学分离功能, 分别以H2, NH3/He(V/V=1/9, He为缓冲气)、 O2为反应气, 对比分析质谱干扰的消除效果, 旨在为婴幼儿谷类辅助食品中重金属Cd的精准测定提供高通量分析方法。
1 实验部分
1.1 材料与试剂
1 000 mg·L-1的Mo, Sn和Cd单元素标准溶液, 10 mg·L-1的Rh内标溶液, 65%(w/w)的超纯硝酸, 30%(w/w)的超纯双氧水, 德国Merck; 标准参考物质米粉(SRM 1568b), 美国国家标准与技术研究院, 辽宁大米(GBW10043)、 四川大米(GBW10044)、 湖南大米(GBW10045), 中国地质科学院地球物理地球化学勘查研究所; 6种婴幼儿谷类辅助食品购自于大型生活超市。 硝酸采用亚沸蒸馏进一步提纯, 超纯水为Milli-Q超纯水机制得。
1.2 仪器和设备
Agilent 8800 ICP-MS/MS仪, 美国Agilent公司。 MARs 5微波消解系统, 美国CEM公司。 Milli-Q超纯水机, 美国Millipore公司。 ICP-MS/MS工作参数和操作条件为: RF功率, 1 550 W; 采样深度, 8 mm; 载气流量, 1.08 L·min-1; 辅助气流量, 1.80 L·min-1; 积分时间, 1 s; 重复测定次数, 3; 反应气, H2, NH3/He, O2; H2流量, 7.0 mL·min-1; NH3/He流量, 5.0 mL·min-1; O2流量, 0.4 mL·min-1。
1.3 样品预处理
将婴幼儿谷类辅助食品于105 ℃温度下烘干至恒重。 准确称取约0.25 g(精确到0.000 1 g)烘干样品于微波消解罐中, 加超纯水润湿后依次加入65%(w/w)的硝酸4 mL和30%(w/w)的双氧水2 mL, 敞口静置20 min后进行微波消解: (1)5 min斜坡升温120 ℃; (2)3 min斜坡升温150 ℃; (3)5 min斜坡升温190℃, 保持15 min; 所有步骤的消解功率均为1 600 W。 消解结束后自然冷却至室温, 转移至25 mL容量瓶中定容。 采用相同的过程制备空白溶液。
1.4 方法
配制0.0, 0.1, 0.5, 2.0和10 μg·L-1的Cd系列标准溶液和1 mg·L-1的Rh内标溶液, 使用“T”型内标混合接头将Rh内标溶液与分析溶液在线混合, 对标准溶液、 样品溶液和空白溶液进行测定。 利用ICP-MS/MS自带的MassHunter软件绘制校准曲线, 进行线性验证。 利用校准曲线计算样品中Cd的含量。
2 结果与讨论
2.1 反应气的选择
Cd有8种稳定的天然同位素, 其中106Cd和108Cd的丰度低(均小于2%)不宜采用, 本文选择Cd的其余6种同位素为分析同位素。 在婴幼儿谷类辅助食品样品中, Mo在高温等离子体中形成的MoO+, MoN+, MoC+会对110Cd+,111Cd+,112Cd+,113Cd+,114Cd+,116Cd+的测定形成干扰, 同时,110Pd+,112Sn+,113In+,114Sn+,116Sn+会对110Cd+,112Cd+,113Cd+,114Cd+,116Cd+的测定形成同量异位素干扰。 通常情况下, 在谷类食物中Sn的含量与Cd相当, Mo含量远高于Cd, 而Pd和In的含量远低于Cd, 因此, Sn和Mo所形成的干扰会影响Cd的精准测定, 而Pd和In所形成的干扰可以忽略。 NH3/He和O2作为消除干扰最通用和最有效的两种反应气体, 在ICP-MS/MS分析中得到了广泛应用, 而H2在ICP-QMS是使用频率较高的反应气, 由于NH3/He和O2拥有强大的去除干扰功能, 在ICP-MS/MS分析中使用H2作为反应气消除质谱干扰已逐渐减少。 本文采用100 μg·L-1的Mo和1 μg·L-1的Sn混合标准溶液中加入1 μg·L-1的Cd标准溶液, 在MS/MS模式下, 分别采用H2, NH3/He和O2为反应气, 利用原位质量法消除干扰, 考察110Cd,111Cd,112Cd,113Cd,114Cd,116Cd的背景等效浓度(BEC), 结果见表1。
从表1可以看出, 采用H2反应气时6个Cd同位素的BEC最大, 采用O2反应气的BEC最小。 通过对混合标准溶液进行质谱扫描发现, MoO+, MoN+和MoC+能与H2, NH3/He和O2发生质量转移反应, 而Sn+不与H2和NH3/He发生质量转移反应(见图1)。 虽然112Sn和114Sn的丰度均小于1%, 但仍然对112Cd和114Cd的测定造成了轻微干扰, 而高丰度116Sn严重干扰116Cd的测定。 因此, 采用H2和NH3/He为反应气, 均可选择110Cd,111Cd,113Cd为分析同位素消除干扰。 由于H2仅能与Ar基离子快速反应, 与其他干扰离子反应速度较慢, 对于高浓度Mo基质中Cd的测定难以彻底消除干扰。

表1 不同反应气下Cd的背景等效浓度(BEC)
在O2反应模式下, Sn+与O2的反应虽然是吸热过程(ΔHr>0), 但在八极杆偏置负电压的作用下, 所产生的质心碰撞能会促进Sn+与O2反应, 使Sn+发生质量转移生成SnO+, 从而消除112Sn对112Cd,114Sn对114Cd的干扰, 减轻116Sn对116Cd的干扰(见图2)。 虽然在O2反应模式下, 6个Cd同位素获得的分析灵敏度略低于NH3/He反应模式, 但BEC明显比NH3/He反应模式低。 因此, 本实验选择O2反应气消除质谱干扰。
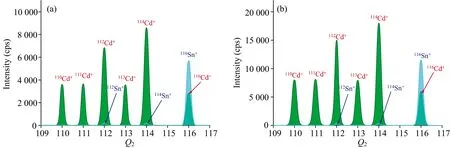
图1 (a)H2反应模式和(b)NH3/He反应模式下混合标准溶液(100 μg·L-1 Mo+1 μg·L-1 Sn+1 μg·L-1 Cd)的峰形图

图2 O2反应模式下混合标准溶液(100 μg·L-1 Mo+1 μg·L-1 Sn+1 μg·L-1 Cd)的峰形图
2.2 反应气流量的优化
在MS/MS模式下, 采用国际标准参考物质米粉(SRM 1568b)对反应气O2流量进行了优化。 考察了不同O2流量下, 选择110Cd,111Cd,112Cd,113Cd,114Cd为分析同位素对SRM 1568b 中Cd测定结果的影响, 结果见图3。

图3 O2流量对测定标准参考物质SRM 1568b 中Cd的影响
可以看出, 随着O2流量的增加, 5个Cd同位素的测定结果变小并逐渐接近SRM 1568b的认定值, 表明干扰逐渐被消除。 当O2流量达到0.25 mL·min-1时,112Cd和114Cd的测定值与SRM 1568b的认定值基本一致, 但110Cd,111Cd,113Cd的测定结果仍然偏大; 当O2流量达到0.4 mL·min-1时, 5个Cd同位素的测定值均与SRM 1568b的认定值一致, 继续增大O2流量,110Cd,111Cd,112Cd,113Cd,114Cd的测定值基本不再发生变化。 因此, 本实验选择O2流量为0.4 mL·min-1。
2.3 内标元素的选择
内标法不仅能校正基体效应, 而且能校正仪器的信号漂移[13]。 In有2个稳定的同位素113In和115In, 高丰度115In由于与Cd同位素的质量和电离电位接近, 通常被选择为Cd的内标元素, 但113In会对本实验中分析同位素113Cd产生干扰。 Rh存在稳定的唯一同位素103Rh, 其质量和电离电位与Cd接近, 在O2反应模式下,103Rh+与O2的反应为吸热过程, 虽然有少量103Rh16O+生成, 但通过对1 μg·L-1的Rh标准溶液质谱扫描图谱可以看出, 近80%的103Rh+没发生质量转移反应。 因此, 本实验选择103Rh+为内标监测离子来校正质谱响应信号的变化。
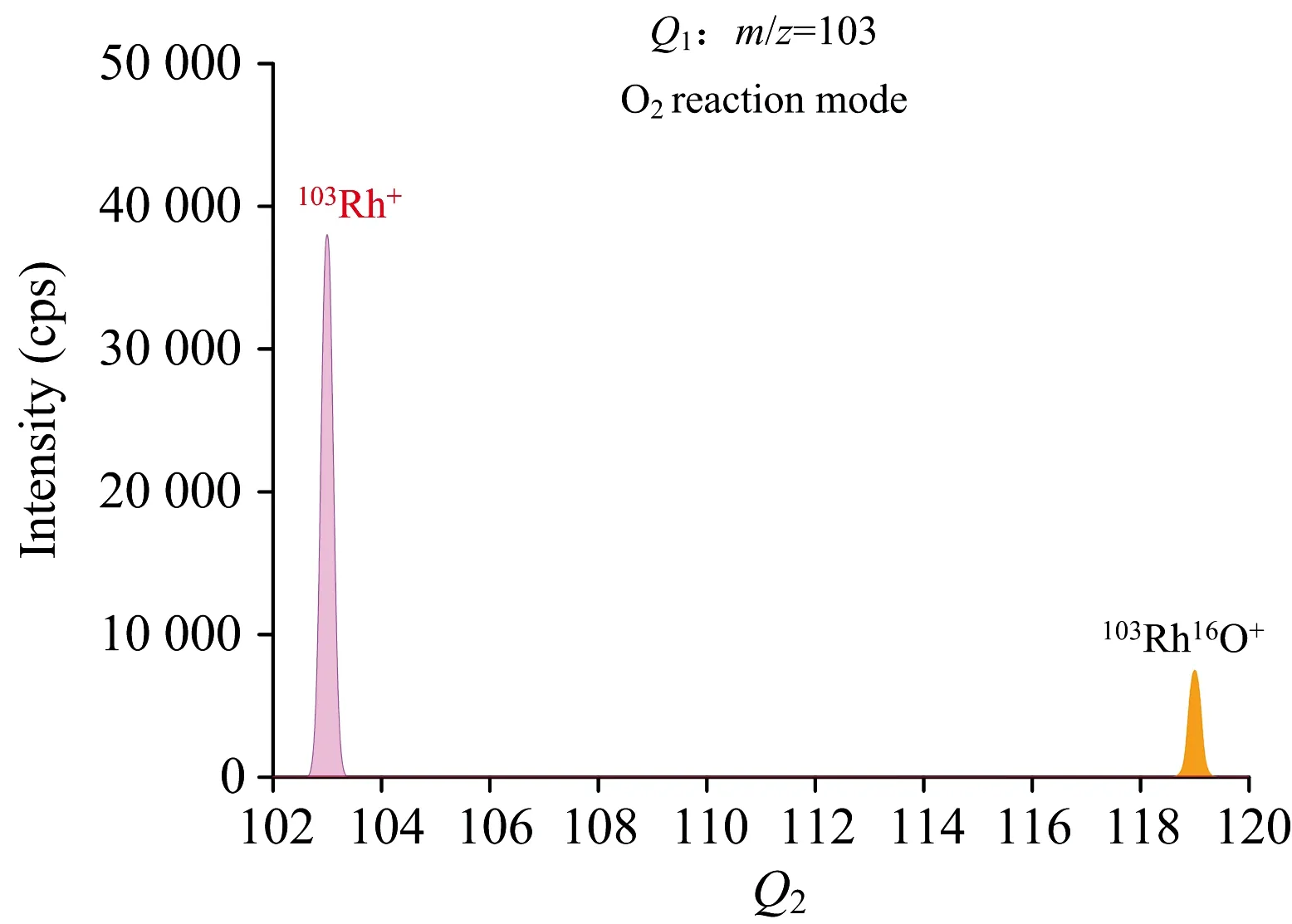
图4 在O2反应模式下1 μg·L-1的Rh标准溶液质谱图
2.4 线性关系与检出限
在优化的ICP-MS/MS条件下, 按实验方法对Cd系列标准溶液进行测定, 以Cd相对信号强度(分析元素Cd与内标元素Rh的信号强度比值)所对应的浓度自动进行线性回归, 建立Cd同位素的校准曲线。 采用所建立的方法对空白溶液连续测定10次, 计算Cd同位素的标准偏差, 以3倍标准偏差所对应的浓度为仪器的检出限(LOD)。 从表2可以看出, Cd同位素在各自的线性范围内具有良好的线性关系, 线性相关系数≥0.999 8。 Cd的LOD为2.03~13.4 ng·L-1, 其中111Cd的LOD最低。 因此, 本实验选择111Cd为分析同位素用于方法的准确性评价和样品分析。
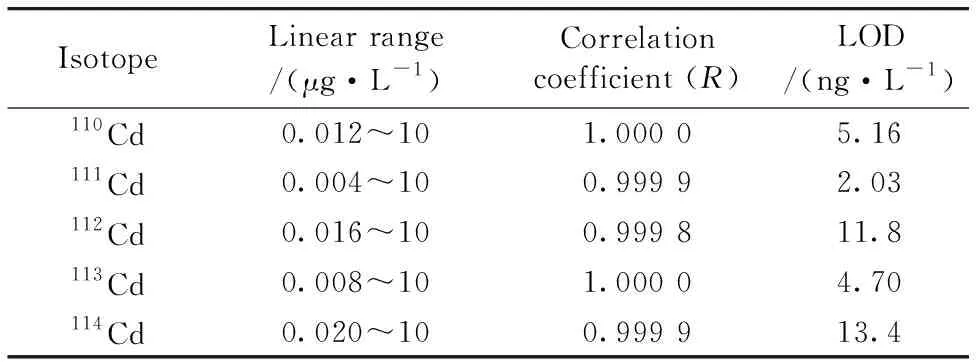
表2 Cd同位素的线性关系和检出限(LOD)
2.5 方法的准确性评价
采用本方法和国标法(GB5009.268—2016)对4个标准参考物质进行对比分析, 每个样品重复测定6次, 选择t检验法对两种分析方法的测定结果进行统计学分析。 通过表3可以看出, 本方法的测定值与标准参考物质的认定值基本一致。 统计分析表明, 在95%的置信水平, 本方法与国标法的测定结果无显著性差异(p>0.05), 验证了本方法准确可靠。

表3 标准参考物质的分析结果(n=6)
2.6 实际样品分析
应用本方法对6种婴幼儿谷类辅助食品中的重金属Cd含量进行测定, 并采用国标法(GB5009.268—2016)进行验证, 每个样品重复测定6次。 从表4可以看出, 本方法与国标法的测定结果一致, 所选6种国内外婴幼儿谷类辅助食品中均检出了重金属Cd, 但含量不仅低于我国制定的0.06 mg·kg-1临时限量标准, 也低于欧盟制定的0.04 mg·kg-1限量标准, 通过食用这6种婴幼儿谷类辅助食品所摄入的重金属Cd不具有潜在的健康风险。
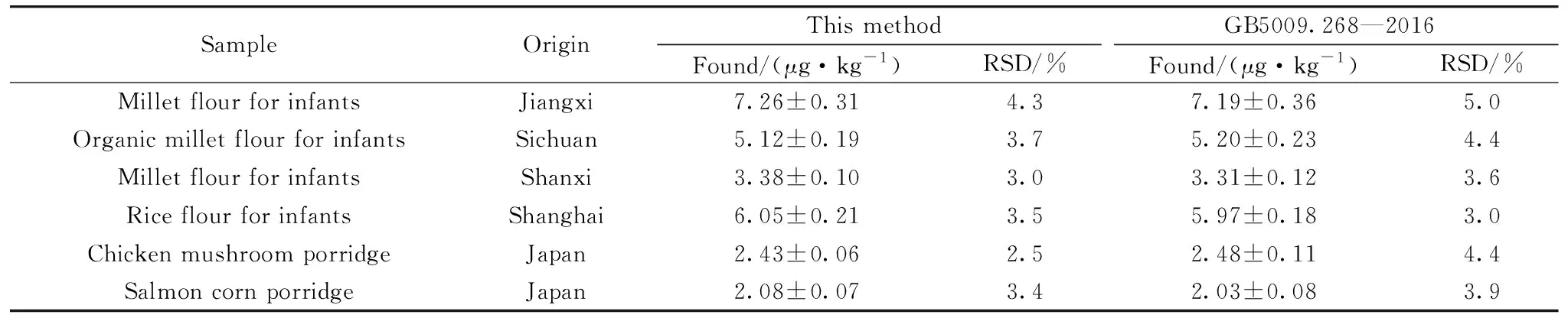
表4 婴幼儿谷类辅助食品中Cd含量的分析结果(n=6)
3 结 论
建立了利用ICP-MS/MS的O2反应模式消除干扰测定婴幼儿谷类辅助食品中重金属Cd的新方法。 在MS/MS模式下, 对比采用H2, NH3/He和O2为反应气消除质谱干扰的效果, 确定了利用O2反应气消除质谱干扰。 Cd的LOD为2.03~13.4 ng·L-1, 选择111Cd为分析同位素获得的LOD最低。 所建立的方法具有操作简单、 分析速度快、 结果准确可靠的优势, 为婴幼儿谷类辅助食品中重金属Cd的控制与高通量检测提供了技术支持。
