浅部真菌感染中的抗真菌药物治疗进展
2022-08-31杨之辉李若瑜
杨之辉 李若瑜
(北京大学第一医院皮肤性病科 北京大学真菌和真菌病研究中心 皮肤病分子诊断北京市重点实验室 国家皮肤与免疫疾病临床医学研究中心 国家药品监督管理局化妆品质量控制与评价重点实验室,北京 100034)
浅部真菌感染是致病真菌侵犯皮肤的角质层、毛发和甲板所导致的感染,困扰着世界约25%的人口,导致患者生活质量下降[1-3]。浅部真菌感染可由皮肤癣菌、念珠菌属、马拉色菌属等引起,而尤以皮肤癣菌最为常见。临床上以足癣最为常见,其次为体癣、股癣以及甲真菌病[4]。除此之外,外阴阴道念珠菌病(vulvovaginal candidiasis,VVC)也是常见的由念珠菌属引起的真菌感染,约75%的女性在其育龄期至少经历过一次VVC[5]。
目前临床上可用的抗真菌药物较为有限:系统性用药选择主要包括多烯类(如两性霉素B和制霉菌素)、唑类(如氟康唑、伊曲康唑、伏立康唑和泊沙康唑)、棘白菌素类(如卡泊芬净、阿尼芬净和米卡芬净)及丙烯胺类抗真菌药(如特比萘芬和萘替芬),其他较少使用的系统性用药及外用药物有氟胞嘧啶、环吡酮胺、tavaborole、阿莫罗芬、布替萘芬、灰黄霉素、托萘酯和那他霉素等[6]。由于抗真菌药物存在毒性、耐受性、药物相互作用等问题,且近年来多药耐药菌不断出现,临床亟需新的敏感度高、毒性低的抗真菌治疗选择。本文将对目前浅部真菌感染中的抗真菌药物治疗进展进行综述,包括系统性用药(包括新型化合物及原有化合物的新剂型)、外用药物及其他处于临床前期的具有抗真菌活性的化合物。
1 系统性抗真菌用药进展
该组药物包括研发用于甲真菌病及VVC的oteseconazole、用于甲真菌病的阿巴康唑及fosravuconazole以及用于VVC的ibrexafungerp(见表1)。

表1 浅部真菌感染中的系统性抗真菌用药进展总结Tab.1 Advancements in systematic antifungal agents for superficial fungal infections
1.1 oteseconazole (VT-1161)
oteseconazole(VT-1161)是一种可口服及静脉给药的四唑类抗真菌药,能够有效抑制真菌14 α-脱甲基酶细胞色素P450(CYP51),而不对人类CYP51产生明显影响,因而oteseconazole具有药物相互作用少、不良反应少的优势,且其半衰期久,在复发性VVC及甲真菌病的维持期治疗中或可采用每周1次的给药方式[7]。
VT-1161抗菌谱广,可覆盖念珠菌属(包括氟康唑敏感及耐药菌株)、根霉属、毛癣菌属及球孢子菌属[8]。在Act1-/-小鼠模型中(该种小鼠缺乏IL-17受体,因而对白念珠菌引起的口腔感染易感),VT-1611在治疗氟康唑敏感及耐药菌株引起的口咽黏膜念珠菌病中均有较高疗效[7]。
在一项纳入了259例中、重度甲真菌病患者的Ⅱ期随机、盲法、安慰剂对照的多中心临床研究中(NCT02267356),治疗组分别采取口服VT-1611 600 mg/d共2周(负荷剂量),继以600 mg/周共10周或22周;或口服VT-1611 300 mg/d共2周(负荷剂量)继以300 mg/周共10周或22周的治疗方案。试验第48周时治疗组的有效率为32%~42%,而安慰剂对照组为0[9]。在另一项Ⅱ期随机、双盲、安慰剂对照的临床研究中(NCT02267382),纳入的215例处于急性发作期的复发性VVC患者在经氟康唑治疗、急性感染控制后,治疗组分别采取口服VT-1611 300 mg/d共1周(负荷剂量),继以300 mg/周共11周或23周;或口服VT-1611 150 mg/d共1周(负荷剂量)继以150 mg/周共11周或23周的治疗方案。试验第48周时治疗组急性VVC的复发率为0~7%,而安慰剂组为52%[10]。两项临床试验均显示VT-1611治疗耐受性佳,治疗组未见明显肝功能或心电图异常。目前另有三项针对复发性VVC的Ⅲ期临床试验正在进行中(NCT03561701、NCT02267382、NCT03562156)。
1.2 阿巴康唑(albaconazole,UR-9825)
阿巴康唑属于三唑类抗真菌药,同样通过抑制真菌CYP51发挥作用,现有口服及外用两种剂型,具有广谱抗真菌作用。体外实验中,阿巴康唑对于念珠菌属的抑制活性高于氟康唑及伊曲康唑,其90%最小抑菌浓度(90% minimum inhibitory concentration,MIC90)在≤0.0002~0.12 μg/mL之间[11];而针对丝状真菌,除茄病镰刀菌及柱顶孢霉属之外,阿巴康唑的体外活性明显高于两性霉素B,尤其对于烟曲霉及淡紫拟青霉,阿巴康唑的MIC90仅为0.125 μg/mL[12]。此外,阿巴康唑对于马拉色菌属也具有抗菌活性,且其体外抗菌活性类似于氟胞嘧啶、氟康唑、 酮康唑、伊曲康唑及伏立康唑[13]。在动物模型中,阿巴康唑也被证实对于侵袭性曲霉病、念珠菌病、隐球菌病、赛多孢霉病及Chagas病的治疗均有效[14]。
阿巴康唑口服吸收快,在Ⅰ期临床试验中,阿巴康唑于2~4 h后在人体内达血药峰浓度(Cmax)。在一项纳入了584例远端甲下型甲真菌病患者的Ⅱ期、随机、双盲、安慰剂对照的临床研究中,治疗组分别接受口服阿巴康唑100 mg/周共36周、200 mg/周共36周、400 mg/周共36周及400 mg/周共24周治疗,试验第52周时治疗组21%~54%的患者90%及以上的甲板达到治愈,而安慰剂组仅为1%(P<0.001)。各组治疗相关不良反应出现率均≤3%,且均为轻中度,其中较为常见的不良反应有头痛(3%)、恶心(3%)、腹泻(3%)、上呼吸道感染(2%)、转氨酶ALT升高(2%)及肌酸激酶升高(2%)[15]。一项荟萃了40项临床试验的Meta分析中,阿巴康唑400 mg(每周1次)被认为是趾甲甲真菌病最有效的治疗方式,其次为泊沙康唑200~400 mg(每日1次)及特比萘芬250~350 mg(每日1次)[16]。
1.3 fosravuconazole(F-RVCZ)
fosravuconazole (F-RVCZ)全称为fosravuconazole L-赖氨酸乙醇,是ravuconazole(RVCZ)的前体药物,为具有广谱抗菌活性的新型三唑类药物,其抗菌谱覆盖毛癣菌属、念珠菌属、曲霉属及隐球菌属。F-RVCZ的系统生物利用度为RVCZ的2~4倍,且血药浓度高、半衰期长,其优异的口服吸收性及全身生物利用度使得3个月的短疗程疗法治疗重度甲真菌病成为可能[17]。
一项日本的Ⅲ期多中心、双盲、随机、安慰剂对照临床研究显示,在153例趾甲甲真菌病患者中,口服F-RVCZ 100 mg/d治疗12周的完全治愈率(于第48周评估)为59.4%、病原学治愈率为82.0%,而安慰剂组完全治愈率为5.8%、病原学治愈率为20.0%(P<0.001);治疗组药物不良反应发生率为23.8%,均为轻中度,常见不良反应有腹部不适(4.0%)及肝功能异常,包括谷酰胺转移酶γ-GT(15.8%)、谷丙转氨酶ALT(8.9%)及谷草转氨酶AST(7.9%)的升高[18]。此外,RVCZ对肝代谢酶CYP3A4抑制作用小,因而药物相互作用少[18],可以安全地应用于老年人群。在一项面向≥65周岁的老年重度甲真菌病患者的单中心前瞻性研究中,37例老年患者口服F-RVCZ 100 mg/d共12周,第48周时患者受累甲板的面积平均由86.6%改善至28.1%(P<0.01),83.3%的患者的受累甲板得到了40%及以上的缓解,29.7%的患者得到完全治愈;其中21.6%的老年患者出现了γ-GT升高,但均可自行缓解[17]。目前亦有采用口服F-RVCZ 100 mg/d共12周的方法成功治愈毛癣菌所致成人头癣的案例报道[19]。
1.4 ibrexafungerp (SCY-078)
ibrexafungerp属于三萜糖苷烯衍生物,因其具有独特的三萜类结构而成为首个“-fungerp”类抗真菌药物[20],可口服及静脉给药[8]。从作用靶点上讲,ibrexafungerp与棘白菌素类药物相似,均通过抑制细胞壁1,3-β-D-葡聚糖的合成而起到抗真菌作用。但不同于棘白菌素类药物,由于其独特的三萜类结构,ibrexafungerp对多种念珠菌属(包括对棘白菌素、唑类药物耐药的光滑念珠菌及耳念珠菌;因fks1和fks2点突变而发生棘白菌素类药物耐药的念珠菌)、曲霉属以及其他真菌病原体均表现出体外活性[20]。其中ibrexafungerp对于白念珠菌(MIC50:0.03~0.25 μg/mL)、耳念珠菌(MIC50:0.5~1 μg/mL)、光滑念珠菌(MIC50:0.125~1 μg/mL)及热带念珠菌(MIC50:<0.03~1 μg/mL)的抗菌活性均优于氟康唑[20]。
一项针对中、重度VVC治疗的Ⅱ期随机、评估者单盲的临床研究中,70名受试者平均分为3组,分别接受氟康唑150 mg顿服、ibrexafungerp 口服1 250 mg负荷剂量,继而750 mg/d共2 d或共4 d的治疗。试验第24天时3组的临床治愈率分别为55.0%、70.8%和69.2%。在随访第120天时,3组患者的持续临床治愈率分别为65.0%、79.1%和80.7%[21]。
两项Ⅲ期随机、双盲、安慰剂对照的临床试验进一步验证了ibrexafungerp 在急性VVC中的治疗效果。其中,VANISH-303(NCT03734991)纳入了376例来自美国的患者,试验中分别予患者ibrexafungerp 300 mg或安慰剂每日2次口服共1天,试验第25天时治疗组与对照组的临床治愈率分别为51%及29%,病原学清除率分别为50%及19%[22]。VANISH-306(NCT03987620)的试验设计与VANISH-303完全一致,但纳入的患者来自美国及欧洲,试验第25天时治疗组与对照组的临床治愈率分别为63%及44%,病原学清除率分别为59%及30%[23]。另一项安慰剂对照的Ⅲ期临床研究目前正在进行中,以评估ibrexafungerp在复发性VVC患者中的疗效(NCT04029116)。
此外,在临床试验中,ibrexafungerp也被证实可用于侵袭性念珠菌病的口服降阶梯治疗、侵袭性耳念珠菌感染及侵袭性肺曲霉病的治疗中[8]。目前,该药已于2021年6月于美国批准用于VVC的治疗,成为三萜系抗真菌药物中首个被批准用于临床的药物。
2 系统性用药中抗真菌化合物的新剂型
在系统性抗真菌药物中,除上述新型化合物外,不少学者对已有抗真菌药物进行了改良,以减少其毒性或提高生物利用度,本节将对超级生物利用度伊曲康唑及螺旋内两性霉素B进行介绍(见表2)。

表2 系统性用药中抗真菌药物新剂型的特点总结Tab.2 Characteristics of new formulations of existing antifungal agents for the systematic therapy of superficial fungal infections
2.1 超级生物利用度伊曲康唑(super bioavailability itraconazole,SUBA-ITZ)
伊曲康唑(itraconazole,ITZ)为广谱的三唑类抗真菌药物。传统ITZ口服胶囊在胃内释放药物,在与饭同服的情况下,其生物利用度约仅有55%,且在不同个体间差异大、受胃内pH值影响大。SUBA-ITZ在十二指肠释放药物,利用pH依赖的聚合物载体来增强其溶解及吸收。SUBA-ITZ的相对口服生物利用度升高至传统ITZ的173%,且其生物利用度在不同个体间的差异度降低了21%[24-26]。一项非盲、交叉、药代动力学的研究中,血中ITZ浓度(或羟基ITZ浓度)在口服SUBA-ITZ与传统ITZ药物后的比值在107%~118%之间[25]。同时,一项非盲、随机、交叉研究的结果表明SUBA-ITZ的血药浓度受进食的影响小[27]。
SUBA-ITZ目前已被美国食品与药物管理局(FDA)批准用于治疗芽生菌病、组织胞浆菌病及曲霉病(两性霉素B不耐受或抵抗的患者中)。目前临床应用的剂型为65 mg的口服胶囊,推荐与饭同服,负荷剂量为130 mg每日3次、共3日,维持剂量为130 mg每日1次[24]。目前另有一项对比传统ITZ与SUBA-ITZ在地方性霉菌病(endemic mycosis)中疗效的研究正在进行中(NCT03572049)。
2.2 螺旋内两性霉素B(encochleated amphotericin B/ amphotericin B cochleate,CAmB)
螺旋内两性霉素B(encochleated amphotericin B,CAmB)是多烯类抗真菌药物两性霉素B(amphotericin B,AmB)的口服新剂型。两性霉素B能够结合真菌细胞膜上的麦角固醇,在细胞膜上形成孔道导致单价离子(钾离子、钠离子、氢离子、氯离子)的快速流失进而导致真菌细胞死亡。在新剂型CAmB中,AmB与钙离子一起嵌入螺旋结构中的磷脂酰丝氨酸双层。该螺旋结构可以保护AmB不受胃肠道消化过程的影响,直至被吸收后螺旋结构被巨噬细胞所吞噬。由于螺旋结构内的钙浓度高于巨噬细胞胞浆内的钙浓度,钙离子冲出螺旋体并导致螺旋结构展开,AmB在巨噬细胞内得以释放[28]。简言之,螺旋体起到了稳定、保护AmB并将其运送至网状内皮细胞内的作用。因此,相比传统的AmB,口服CAmB后血浆循环中AmB的浓度低,AmB毒性所致的不良反应发生率低[8]。
一项Ⅱa期临床试验的初步结果(共4例患者)表明,针对唑类药物耐药的难治性黏膜皮肤念珠菌病,口服CAmB 400~800 mg/d可以改善50%~85%的临床症状,且其耐受性可,除恶心及头晕外,无其他药物相关毒性[29]。另一项Ⅱ期临床试验(NCT02971007)比较了口服单剂量CAmB 200 mg、CAmB 400 mg和氟康唑150 mg在治疗中重度VVC中的安全性及有效性,各治疗组均无严重不良事件的报道,但氟康唑的临床治愈率(75%)高于CAmB 200 mg(52%)和CAmB 400 mg(54%)[8,30]。此外,CAmB在隐球菌性脑膜脑炎中治疗效果的Ⅱ期临床试验也正在进行中(NCT04031833)。
3 外用抗真菌药物治疗进展
该组药物包括唑类药物艾氟康唑、卢立康唑、达帕康唑、防御多肽NP213及HXP124,以及其他新型外用药ME1111、DBI001(见表3)。其中艾氟康唑及卢立康唑已在部分国家上市应用于临床。
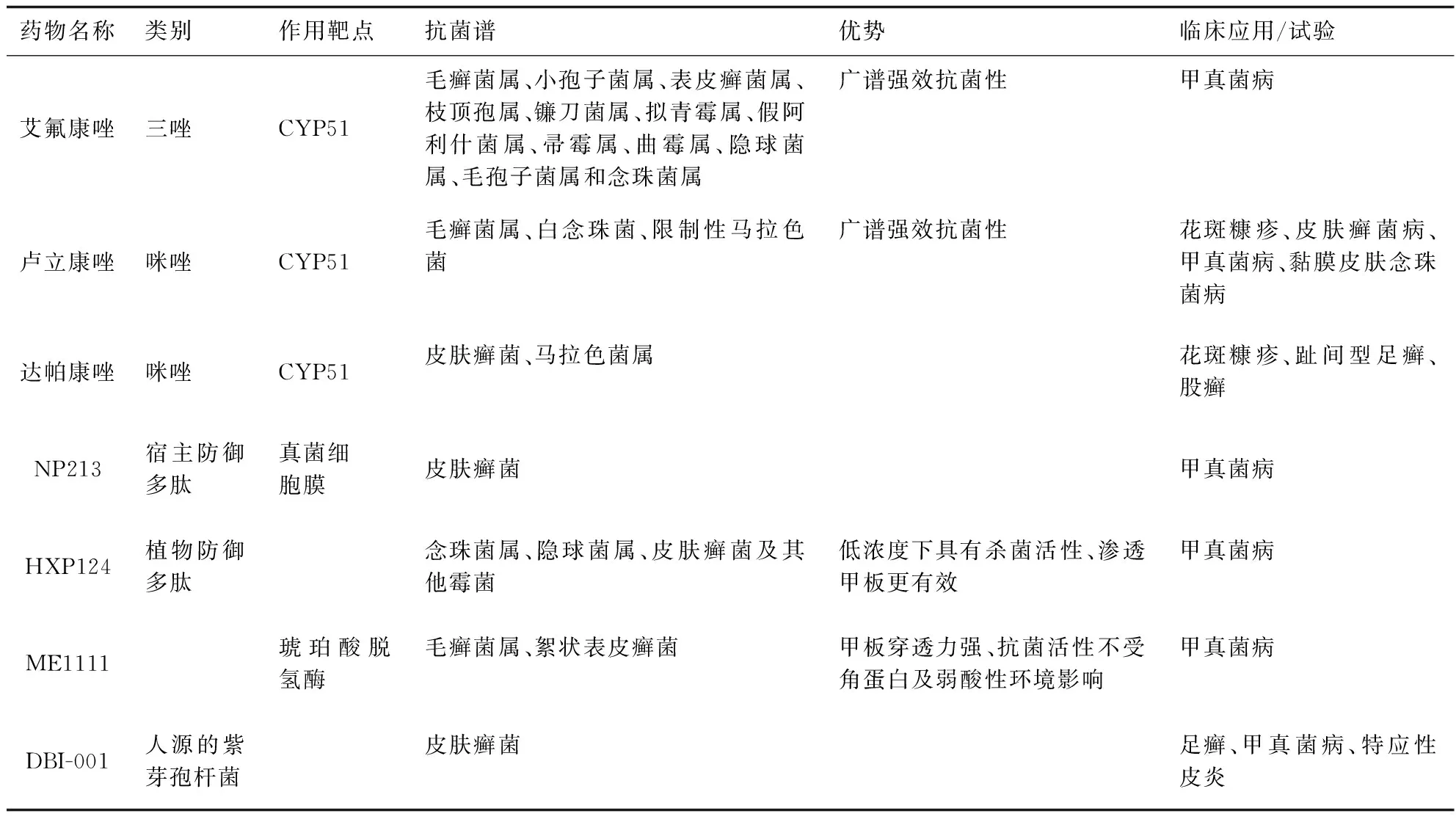
表3 浅部真菌感染治疗进展中的外用抗真菌药物总结Tab.3 Characteristics of recently approved or promising topical antifungal agents for superficial fungal infections
3.1 艾氟康唑(efinaconazole)
艾氟康唑为广谱的三唑类抗真菌药物,其通过抑制14α-脱甲基酶(CYP51)而阻断真菌细胞膜上麦角固醇的生物合成[31]。在体外试验中,艾氟康唑对毛癣菌属、小孢子菌属、表皮癣菌属、枝顶孢属、镰刀菌属、拟青霉属、假阿利什菌属、帚霉属、曲霉属、隐球菌属、毛孢子菌属和念珠菌属均有较强的抗菌活性[32]。其中针对趾间毛癣菌和红色毛癣菌的临床菌株,艾氟康唑的平均MIC为0.007 μg/mL,低于特比萘芬(0.011 μg/mL)、伊曲康唑(0.095 μg/mL)及氟康唑(12.77 μg/mL),但高于卢立康唑(0.0005 μg/mL)[33]。
在两项分别纳入了870例及785例趾甲远端侧位甲下型甲真菌病患者的Ⅲ期、多中心、双盲、随机临床试验中,治疗组外用10%艾氟康唑溶液每日1次共48周,在52周时其完全治愈率为15.2%~17.8%,而应用载体的对照组在52周时的完全治愈率为3.3%~5.5%(P<0.001),治疗组的病原学清除率也显著高于对照组(53.4%~55.2%),而不良反应在治疗组与对照组间相似(2%),主要为局部皮肤反应[34]。最新一项Ⅳ期非盲、多中心临床试验进一步针对艾氟康唑在6~16岁非成年远端侧位甲下型甲真菌病患者中的疗效进行了研究,纳入的62例患儿同样采取10%艾氟康唑溶液外用、每日1次共48周的治疗方案,其52周完全治愈率(65.0%)及病原学清除率(65.0%)均明显高于上述两项针对成人的研究结果[35]。虽然该发现可能和儿童自身特点(指甲生长更快、指甲长度更短、感染持续时间更短因而甲床损伤的风险相对低)有关,但亦可说明艾氟康唑溶液可能是适合甲真菌病患儿的治疗选择之一。
目前应用于甲真菌病的外用10%艾氟康唑溶液已在美国、加拿大及日本上市使用。
3.2 卢立康唑(luliconazole,NND-502)
卢立康唑属于咪唑类药物,同样通过抑制14α-脱甲基酶而阻断真菌细胞膜上麦角固醇的生物合成。在体外,针对毛癣菌属(包括红色毛癣菌、须癣毛癣菌及断发毛癣菌),卢立康唑较特比萘芬、利拉萘酯、丁替萘芬、阿莫罗芬、联苯苄唑等药物表现出更强的抗真菌活性,尤其针对红色毛癣菌,其MIC在≤0.00012~0.00024 μg/mL之间。卢立康唑对白念珠菌也有很高的活性(MIC:0.031~0.13 μg/mL),但弱于酮康唑、克霉唑、奈替康唑及咪康唑。此外,卢立康唑对限制性马拉色菌的MIC也很低(0.004~0.016 μg/mL)[36]。
在针对足癣的临床试验中,每日1次外用1%卢立康唑乳膏共2周,第4周时病原学(KOH镜检)转阴率在76.1%~79.7%之间[4];在针对体/股癣的临床试验中,每日1次外用1%卢立康唑乳膏共2周,第4周时完全治愈率(临床及病原学同时达到治愈)为95%[37];在仅针对股癣的临床试验中,每日1次外用1%卢立康唑乳膏共1周,其临床及病原学治愈率分别为24.2%及78.2%[38]。
目前,1%卢立康唑乳膏已在2005年于日本获批用于治疗皮肤浅部真菌感染,2013年11月被美国食物与药物管理局(FDA)批准用于治疗主要致病菌为红色毛癣菌、絮状表皮癣菌的成人趾间型足癣、股癣、体癣[4]。
上市后,有学者进一步针对卢立康唑在甲真菌病中的疗效进行了研究,一项纳入293例患者的Ⅲ期、随机、多中心、双盲临床试验显示,每日1次外用5%卢立康唑溶液共48周后,其完全治愈率(临床及病原学同时达到治愈)为14.9%,而载体对照组的完全治愈率为5.1%,治疗组及对照组病原学转阴率分别为45.4%及31.2%,试验中无严重的不良反应发生[39]。
3.3 达帕康唑(dapaconazole)
达帕康唑为新型咪唑类抗真菌药物。在健康志愿者中外用达帕康唑的耐受性及安全性好,在临床试验中被证实对花斑糠疹、足癣及股癣有效。
在一项纳入53例花斑糠疹患者的Ⅱ期、双盲、非劣效性临床试验中,患者分别采取2%达帕康唑甲苯磺酸盐(治疗组)或2%酮康唑乳膏(对照组)每日1次外用治疗共28 d,治疗组及对照组分别有92.6%及84.6%的患者临床及病原学均达到治愈,达到治愈的中位时间分别为21 d及23.5 d,而不良反应仅出现于酮康唑治疗组(13%),证实在花斑糠疹的治疗中达帕康唑的疗效并不劣于酮康唑[40]。
在针对趾间型足癣的一项纳入48例患者的Ⅱ期、双盲、非劣效性试验中(NCT02824926),研究者对双足均患有足癣的患者采取一足外用2%达帕康唑甲苯磺酸盐乳膏、另一足外用2%酮康唑乳膏每日2次连续14 d的治疗方法,治疗第14天达帕康唑及酮康唑治疗组的治愈率(临床及病原学同时达到治愈)分别为66.0%及68.1%,证实在足癣的治疗中达帕康唑的疗效并不劣于酮康唑,且其安全性与耐受性佳[41]。
针对股癣的一项纳入51例患者的Ⅱ期、双盲非劣效性试验(NCT03359070)亦表明,外用2%达帕康唑乳膏每日2次连续14 d的治疗效果不劣于咪康唑,达帕康唑及咪康唑治疗组分别有87%及92%的患者达到临床及病原学同时治愈[42]。
3.4 NP213(novexatin)
NP213是一种针对甲真菌病的外用治疗而研发的新型抗真菌药物,其根据人体甲板合成的内源性宿主防御多肽(host defense peptides,HDP)设计而成,具有水溶性,并能有效穿透人类甲板。NP213作用于真菌细胞膜,造成细胞膜溶解进而死亡。在体外NP213对于皮肤癣菌的MIC在<100~4 000 μg/mL之间,最低杀菌浓度(minimum fungicidal concentration,MFC)在500~4 000 μg/mL之间[43]。
在Ⅰ期临床试验中(EudraCT No. 2008-001496-29), 10%NP213溶液外用于8例志愿者的病甲后并不能在血浆中测出,提示无系统吸收。在一项纳入48例甲真菌病患者的随机、安慰剂对照的Ⅱa期临床试验中(EudraCT No. 2008-001496-29),治疗组患者每日外用10%NP213溶液共28 d,试验第180天时进行评估,治疗组84.6%的患者临床症状得到改善,38.4%的患者在症状改善的基础上同时培养转阴(至少1次阴性结果);而安慰剂组仅20%的患者得到临床缓解,10%的患者同时有至少1次的培养阴性结果。不良反应为局部皮肤轻度的短暂性红斑,且其出现率在治疗组及安慰剂组中一致,研究者怀疑不良反应的出现与治疗组及安慰剂组所用药中均含有20%尿素有关,于是他们选用不含尿素成分的NP213溶液及安慰剂进行了第二项Ⅱa期临床研究(共纳入47例轻中度甲真菌病患者),同样采用每日1次外用共28 d的给药方法,第28天时治疗组42.4%的患者趾甲培养转阴,第360天时56.5%的患者甲培养阴性,而安慰剂组无人培养阴性。试验中仅出现了1人次的治疗相关不良反应(腹痛)[44]。
3.5 HXP124
HXP124是一种具有半胱氨酸稳定、αβ基序结构(cysteine-stabilised αβ-motif structure)的新型植物防御多肽,对于临床上重要的人类致病菌具有广谱的杀菌活性,包括念珠菌属、隐球菌属、皮肤癣菌及其他丝状真菌。针对白念珠菌及毛癣菌属,HXP124的MIC与MFC值十分接近(均在13~30 μg/mL),提示HXP124在低浓度下即可展现出杀菌活性。并且,相比特比萘芬及艾氟康唑,HXP124能够更快、更有效地渗透入人类甲板,在甲板一侧外用HXP124后的7 d内,25%的所用药物可以穿透甲板,在甲板的另一侧被检测出来。在红色毛癣菌感染的病甲模型中,每日外用HXP124共7 d后,存活真菌的数量减少了95%以上[45]。
在一澳大利亚的Ⅰ/Ⅱa期临床试验中(ACTRN12618000131257),轻、中度甲真菌病患者每日外用HXP124或药物载体共6周,第12周时治疗组中37%的患者甲板受累面积减少达40%以上,而对照组仅18%的患者得到40%及以上的缓解[6]。
3.6 ME1111
ME1111为毛癣菌属琥珀酸脱氢酶的抑制剂[46],而该酶在线粒体呼吸电子转运链中发挥重要作用。体外药敏试验研究结果显示,ME1111针对皮肤癣菌(包括红色毛癣菌、须癣毛癣菌、断发毛癣菌及絮状表皮癣菌)的平均MIC50及MIC90均为0.25 μg/mL,这与目前常用的外用抗真菌制剂阿莫洛芬和环吡酮相一致。并且,ME1111在临床上可达到的浓度即能对皮肤癣菌呈现出杀菌活性,其针对红色毛癣菌和须癣毛癣菌的MFC90为8 μg/mL,这也与环吡酮相似[47]。但ME1111在人类甲板中的渗透性显著优于艾氟康唑、阿莫洛芬及环吡酮,且其抗菌活性在体外不受5%人类角蛋白影响[48]。目前,一项评估ME1111在轻、中度甲真菌病中有效性及安全性的Ⅱ期随机、双盲、载体对照、剂量范围临床试验正在进行中(NCT02022215)。
3.7 DBI-001
DBI-001为一种人源的紫芽孢杆菌(Janthinobacteriumlividum),而紫芽孢杆菌为一种需氧、革兰氏阴性、产生紫罗兰色素、具有抗病毒和抗真菌特性的变形杆菌[49]。在一项Ⅱb期临床研究中,DBI-001每日1次外用共28 d可显著减缓足癣的临床症状及体征,降低红色毛癣菌的真菌载量,改善微生态环境,且无安全性及耐受性问题。此外,DBI-001在特应性皮炎的治疗中也可以起到降低金黄色葡萄球菌载量及改善微生态的作用[50]。
4 其他处于临床前期的新型抗真菌药物
目前,有许多新型抗真菌药物尚处于进入临床试验前的药物研发阶段,现介绍吖啶酮、8-羟基喹啉衍生物、喹啉衍生物三种新型抗真菌化合物(见表4)。

表4 处于临床前期的新型抗真菌化合物特点总结Tab.4 Characteristics of novel antifungal agents at preclinical research stage
4.1 吖啶酮M14 (acridone M14)
吖啶类化合物是广泛存在于芸香科植物中的一类稀有生物碱。结构上,吖啶酮含有一个三环支架,在支架不同的位置上具有不同的基团,使其具有多种生物活性,如对癌症细胞的抗增殖作用和对一系列细菌、微藻和真菌的抗菌活性[51]。de Oliveira等[52]对17种吖啶酮生物碱的抗真菌活性进行了检测,只有一种新型吖啶酮(M14)对念珠菌属及皮肤癣菌属展现出较强的抑制活性。其中,对于试验纳入的皮肤癣菌(包括红色毛癣菌、须癣毛癣菌、断发毛癣菌、疣状毛癣菌、许兰毛癣菌及石膏样小孢子菌),M14的MIC范围为7.81~15.62 μg/mL,而氟康唑的MIC范围为4~64 μg/mL。对于除克柔念珠菌外的念珠菌属,M14也具有较好的抗真菌活性(MIC:7.81~31.25 μg/mL),但弱于氟康唑(MIC:≤0.12~16 μg/mL)。进一步的机制研究发现,M14在低于MIC的浓度时即可阻止白念珠菌生物膜的形成,并降低已形成的生物膜的活力。共聚焦激光扫描显微镜分析表明,在存在M14的环境中,白念珠菌菌丝的生长完全受抑,红色毛癣菌菌丝的生长也受到了严重抑制。同时,M14选择性作用于真菌细胞,而对人类的纤维母细胞毒性低。
4.2 8-羟基喹啉衍生物(8-hydroxyquinoline derivatives)
Pippi等[53]对8-羟基喹啉衍生物的抗真菌活性进行了探究。其中8-羟基喹啉-5-(N-4-氯苯基)磺胺(PH151)具有较强的抗真菌活性,对于念珠菌属(白念珠菌、光滑念珠菌、克柔念珠菌、近平滑念珠菌及热带念珠菌),其MIC为1.0~2.0 μg/mL,对于皮肤癣菌(犬小孢子菌、石膏样小孢子菌、须癣毛癣菌及红色毛癣菌),其MIC为1.0 μg/mL,但其体外抗菌活性均弱于阳性对照药物阿尼芬净。作为治疗甲真菌病的外用药物的研发新方向,研究进一步对PH151的纳米乳剂的抗菌活性进行了验证,其对念珠菌属的MIC为1.0~2.0 μg/mL,对皮肤癣菌属的MIC为0.5~2.0 μg/mL。山梨醇保护实验(sorbitol protection assay)和扫描电镜进一步显示8-羟基喹啉衍生物作用于念珠菌属和皮肤癣菌的细胞壁,抑制白念珠菌假菌丝的形成,提示8-羟基喹啉衍生物可能通过抑制真菌形态发生而起到抗菌作用。
4.3 喹啉衍生物(quinolines derivatives)
喹啉核(quinoline nucleus)在开发具有广谱生物活性的治疗药物中起到重要作用。目前已广泛应用的含有喹啉结构的药物包括:硝基喹啉(抗菌作用)、氯喹和羟氯喹(抗疟疾作用)和贝达喹啉(治疗耐多药结核病作用)等。Machado 等[54]评估了喹啉衍生物对念珠菌属和皮肤癣菌的抗真菌活性,发现喹啉类衍生化合物5具有较好的抗皮肤癣菌活性,对于试验纳入的皮肤癣菌(包括犬小孢子菌、石膏样小孢子菌、须癣毛癣菌及红色毛癣菌),其MIC范围为12.5~25.0 μg/mL。抗菌机制方面,喹啉类衍生化合物5在喹啉环的C-4位置有一个苯基取代基,这个基团可直接连接到细胞核上,成为其抗皮肤癣菌作用的基础。此外,其C-2位的甲基取代基可促进电子效应的发生并作用于目标生物。
5 结 论
由于浅部真菌感染病原耐药率不断升高、患者对现有抗真菌药物的耐受性有限等问题,临床对于新型抗真菌药物的需求不断提高。目前新型药物中口服的唑类药物对真菌的选择性更高、药物不良反应少,有望成为甲真菌病治疗中的新选择;三萜类药物对棘白菌素类药物耐药的菌株仍有效,且已在美国上市应用于临床外阴阴道念珠菌病的治疗;原有抗真菌药物的剂型也得到了改良,其中新剂型的伊曲康唑的口服生物利用度得到大幅提升,两性霉素B的口服新剂型的安全性也得到改善;新型外用药物,包括唑类药物及防御多肽等,有望独立应用于甲真菌病、体股癣及花斑糠疹的治疗中,成为治疗新选择;也有新型抗真菌药物正处于临床试验前的研发阶段,并在体外展现出较高的抗菌活性。随着临床中耐药菌株出现率的增高,未来仍需研究者不断探索具备高抗菌活性、高生物利用度、高安全性的新型抗真菌药物。
