前驱体结构及Cu含量对CuFe基催化剂CO2加氢制 C2+醇性能的影响
2022-08-25温月丽贾雅珍周森森
杨 晨,温月丽,王 斌,张 倩,贾雅珍,周森森,黄 伟,3
(1.太原理工大学 环境科学与工程学院,山西 太原 030024;2.太原理工大学 省部共建煤基能源清洁高效利用国家重点实验室,山西 太原 030024;3.山西太原理工煤转化技术工程有限公司,山西 太原 030024)
CO2是大气中主要的温室气体,极大地促进了全球气候的变化[1],而CO2资源化利用是实现碳减排的有效措施之一。在CO2的三大催化还原方式中,光催化和电催化的能效较低,而利用可再生能源生产的H2来热催化还原CO2是一个颇具节能前景的研究方向。与此同时,化石能源的短缺问题也日益严重,替代能源的开发迫在眉睫,而C2+醇作为一种清洁能源受到了研究者们的广泛关注。因此,将CO2催化加氢转化为C2+醇既能减少CO2的排放,尽早实现“双碳”目标,又能缓解化石能源枯竭的问题[2]。
目前,在用于CO2加氢合成低碳醇的催化剂体系中,改性的费托(Fischer-Tropsch)合成催化剂由于反应条件温和、价格低廉以及较高的低碳醇选择性等优点而备受关注。其中,CuFe基催化剂由于具有较高的活性以及C2+醇选择性,被视为CO2加氢制备C2+醇的候选催化剂之一。尽管目前对CuFe基催化剂的研究已较多,但较低的CO2转化率和C2+醇选择性等仍然是限制其发展的关键因素。GAO等[3]采用焙烧方式处理CuFeMg类水滑石前驱体后,得到了一种均匀且高分散的CuFe基催化剂。结果表明,活性物质的高度分散以及Cu、Fe物种之间的协同效应有利于催化剂活性和醇选择性的提高,Cu和Fe活性位点的均匀分布为H2和CO2的吸附提供了更多的不饱和配位中心,最终促进了目标产物的生成。宋镕鹏[4]采用溶胶-凝胶法制备了负载在TiO2载体上的CuCoFe催化剂,发现催化剂表面的碱性位点对C2+醇的生成有显著影响。由此可见,对于双金属或多金属催化剂,活性组分的均匀分散、强相互作用以及催化剂表面适当的碱性对催化剂的活性以及产物选择性具有关键作用[5-7]。因此,改善传统多组分催化剂中活性金属之间分散性差、相互作用不强等问题,制备对C2+醇具有高选择性的催化剂仍是一个充满挑战性的目标。
催化剂前驱体的性质将极大地影响多组分催化剂的分散及相互作用,从而影响催化剂性能。类水滑石(HTLC)是一类包含带正电荷的主层和可交换阴离子夹层的二维阴离子黏土[8-9]。由类水滑石衍生的复合金属氧化物(LDO)具有金属元素均匀分散、热稳定性高[10]以及离子之间相互作用力强等优点[3,11-12]。此外,LDO还含有强度不同的碱中心,其结构中活性金属充分暴露,具有比类水滑石更高的活性。将其用于CO2加氢合成C2+醇反应中,有望促进活性金属的分散,为催化剂提供适宜的碱性位点,促进反应物H2和CO2的吸附、活化和解离,从而改善催化剂的活性,提高CO2转化率和C2+醇的选择性,为新型高效CuFe基催化剂的研究奠定基础[13]。
本文首先制备了衍生自类水滑石的金属氧化物催化剂CuFeMg、CuFeZn和CuFeZnMg,考察前驱体结构以及催化剂表面碱性位强度对CO2加氢性能的影响。通过改变活性金属Cu含量(物质的量,下同)对催化剂进行调控,得到CuxFe1Zn2系列催化剂,并通过各种表征手段探究Cu含量的变化对催化性能及催化剂理化性质的影响。
1 实验部分
1.1 实验材料与试剂
硝酸铜(Cu(NO3)2·3H2O)、硝酸铁(Fe(NO3)3·9H2O)、硝酸锌(Zn(NO3)2·6H2O)、硝酸镁(Mg(NO3)2·6H2O)、氢氧化钠(NaOH)、碳酸钠(Na2CO3)和石英砂(SiO2)购买自天津市科密欧化学试剂有限公司;蒸馏水(DI)购买自太原理工大学中试基地(pH≈7)。H2(≥99.99%)、CO2(≥99.99%)、N2(≥99.99%)购买自太原市福江特种气体有限公司。
1.2 催化剂制备
通过并流共沉淀法制备了衍生自类水滑石的CuFeM(M=Mg,Zn)系列催化剂。将Cu(NO3)2·3H2O、Fe(NO3)3·9H2O和M(NO3)2·6H2O按n(Cu):n(Fe):n(M) =0.1:1.0:2.0溶于蒸馏水中,配制成c(Cu2+) +c(Fe3+) +c(M2+) =1.0 mol/L的混合溶液A1;以NaOH和Na2CO3的混合溶液(c(NaOH) =1.5 mol/L,c(Na2CO3) =2c(Fe3+))作为沉淀剂B1。在室温搅拌下将A1、B1两种溶液用蠕动泵同时滴加到盛有100 mL蒸馏水的烧杯中,过程中控制pH=9。滴加完毕后继续搅拌1 h,然后放入80 ℃的烘箱中老化12 h。将老化后的样品用蒸馏水抽滤洗涤至中性,然后在80 ℃的烘箱中干燥12 h后得到催化剂前驱体。将前驱体在马弗炉中空气气氛下350 ℃焙烧4 h,得到所需要的Cu0.1Fe1Mg2、Cu0.1Fe1Zn2和Cu0.1Fe1Zn1Mg1催化剂,分别简写为CuFeMg、CuFeZn和CuFeZnMg,压片造粒(40~60目)备用。
以CuFeZn催化剂为基础,通过改变Cu含量制备了CuxFe1Zn2系列催化剂。将Cu(NO3)2·3H2O、Fe(NO3)3·9H2O和Zn(NO3)2·6H2O按n(Cu):n(Fe):n(Zn) =x:1.0:2.0溶于蒸馏水中,得到溶液A2,依然以NaOH和Na2CO3的混合溶液(c(NaOH) =1.5 mol/L,c(Na2CO3) =2c(Fe3+))作为沉淀剂B2,后续步骤同CuFeM系列催化剂。最终得到不同Cu含量的Cu0.1Fe1Zn2、Cu0.3Fe1Zn2、Cu0.5Fe1Zn2和Cu0.7Fe1Zn2催化剂。
1.3 催化剂性能评价
催化剂的活性评价在连续性高压固定床反应装置上进行。首先将1 mL准备好的催化剂放在不锈钢反应管中(内径8 mm),反应管两端用10~20目的石英砂进行填充固定。反应开始前对催化剂进行预还原:以2 ℃/min的升温速率升温至350 ℃,在常压下用总流速80 mL/min的H2/N2混合气(V(H2):V(N2) =1:4)将催化剂进行预还原(活化),还原完成后使反应管冷却至室温。然后切换为总流速120 mL/min的CO2/H2反应气体(V(CO2):V(H2) =1:3),以2 ℃/min的升温速率升温至310 ℃,在反应压力4 MPa条件下对催化剂进行活性评价。
反应所产生的尾气采用低温冷却液循环泵进行气液分离,气相产物每24 h之内均匀时段检测3次,液相产物每隔24 h通过集液管收取1次。采用南京伽诺有限公司生产的GC-950N高效气相色谱仪对CO2+H2反应所生成的所有产物进行分析。CO和CO2等经TDX-01型填充柱分离后由热导检测器(TCD)分析测定(柱温120 ℃);醇类、烃类以及液相产物经PEG-20M型填充柱分离后由氢火焰离子检测器(FID)分析测定(柱温165 ℃)。CO2转化率及产物选择性计算公式如下:

式中,XCO2代表CO2的转化率,%;Si代表组分i的选择性,%;i为气相和液相产物中除CO2外的所有含C化合物;nCO2,out为出口气体中CO2的物质的量,mol;ni,g是出口气体中物质i的碳原子的物质的量,mol;ni,l是液相中物质i的碳原子的物质的量,mol。
1.4 催化剂表征
X射线衍射(XRD)采用日本理学公司生产的DX-2700型X-ray衍射仪进行测试,辐射源采用Cu靶Kα射线,扫描范围2θ=5°~85°,扫描速率为8 (°)/min。N2物理吸/脱附分析采用美国康塔公司生产的Quanta Chrome QDS-30型物理吸附仪进行测试,取0.15 g催化剂样品在200 ℃下脱气4 h后采用N2吸附法在液氮中进行测定,比表面积采用Brunauer-Emmett-Teller(BET)法计算,孔容、孔径采用Barret-Joyner-Halenda(BJH)法计算。H2程序升温还原(H2-TPR)在天津先权生产的TP-5000型吸附仪上进行,将0.05 g催化剂在氦气中150 ℃下吹扫30 min,温度降至50 ℃后切换为混合还原气(5%H2+95%N2),吸附30 min后,以10 ℃/min的速率升温至800 ℃,最后用热导检测器检测信号。扫描电镜(SEM)采用Quanta 400FEG型场发射电子显微镜进行测试,催化剂表面的元素分布情况采用EDS-mapping来分析。电感耦合等离子体-发射光谱表征(ICP-OES)采用Agilent ICP-OES720型电感耦合等离子光谱仪进行测试,测试前先将样品加热至220 ℃进行消解处理,消解后的样品使用水相滤膜滤出后用蒸馏水定容至25 mL。X射线荧光光谱(XRF)利用Epsilon1型X荧光光谱仪进行测试,测试元素范围Na~Am,靶材为Ag靶,检测器为SDD5。X射线光电子能谱(XPS)在赛默飞科技公司生产的ESCALAB 250型光谱仪上进行,辐射源为Al Kα,仪器工作电压12.5 kV,灯丝电流16 mA,真空度8×10-10Pa,以结合能为284.6 eV的C 1s为标准进行校正。
2 结果与讨论
2.1 不同前驱体的CuFeM系列催化剂
2.1.1 活性评价结果分析
表1和表2为催化剂的活性评价结果。CuFeMg和CuFeZnMg催化剂的催化性能较差,产物中CO选择性分别为69.02%和52.72%,总醇选择性分别为8.10%和7.36%,且醇产物中绝大部分为甲醇,可能是因为添加Mg后催化剂碱性太强,不利于C2+醇的生成。而CuFeZn催化剂则具有较好的催化性能,总醇选择性高达31.56%,且醇产物中94%以上为C2+醇,C2+醇的时空收率高达37.22 mg/(mL·h)。

表1 CuFeM系列催化剂的活性评价结果Table 1 Activity evaluation results of CuFeM catalysts

表2 CuFeM系列催化剂的醇分布Table 2 Alcohol distribution of CuFeM catalysts
2.1.2 XRD分析
为了探究催化剂前驱体的结构,对焙烧前的CuFeMg、CuFeZn和CuFeZnMg催化剂前驱体进行了XRD表征,如图1所示。CuFeMg前驱体在2θ=11.69°、23.36°、34.19°、38.80°、46.17°、59.63°和60.97°处均出现了衍射峰,归属于水滑石的特征峰,分别对应水滑石的(003)、(006)、(012)、(015)、(018)、(110)和(113)晶面,可见已成功制备出CuFeMg类水滑石前驱体。而CuFeZn和CuFeZnMg前驱体均未出现类水滑石的特征衍射峰。从文献[14-16]中得知,Zn2+、Fe3+生成氢氧化物沉淀的pH值相差较大,很难在同一体系中形成类水滑石结构,这可能是CuFeZn和CuFeZnMg前驱体未能形成类水滑石结构的原因。
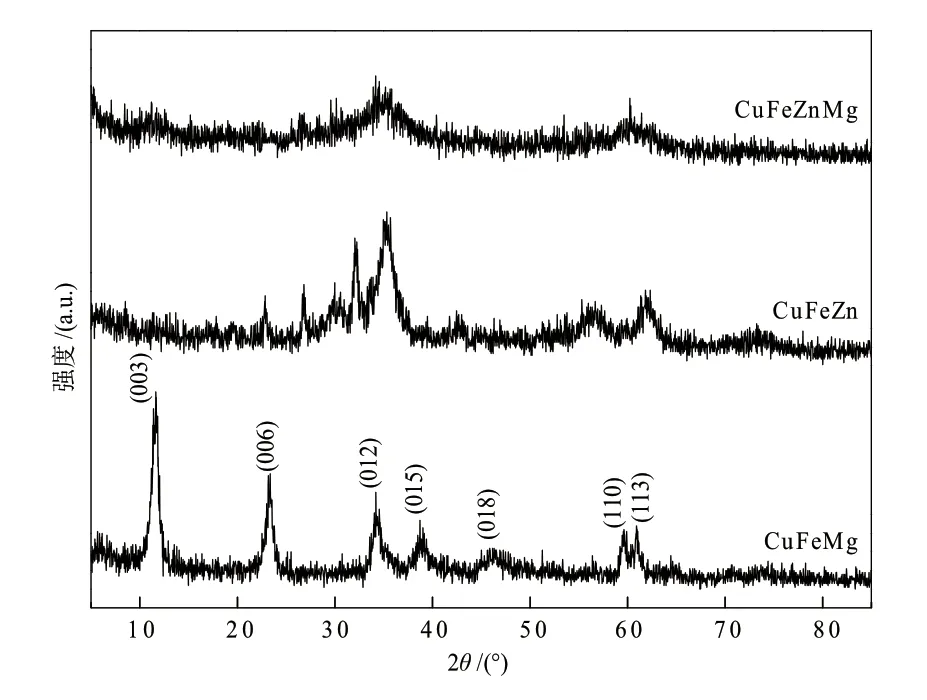
图1 CuFeM系列催化剂前驱体的XRD谱图Fig.1 XRD patterns of CuFeM catalyst precursors
2.1.3 CO2-TPD分析
为了探究催化剂表面的碱性强弱及其分布,对该系列催化剂进行了CO2-TPD表征,如图2所示。根据脱附温度的不同定义催化剂的碱性强度,将50~200 ℃、200~400 ℃和400~700 ℃范围内的CO2脱附峰分别定义为弱碱中心(α)、中强碱中心(β)和强碱中心(γ)。对谱图进行了分峰拟合,并对不同类型的碱性位占比进行了计算,结果如表3所示。CuFeMg催化剂中存在大量的中强碱和强碱性位,弱碱性位只占16.83%;而CuFeZn催化剂中绝大部分为弱碱性位(71.71%),中强碱和强碱性位占比相对较少;CuFeZnMg催化剂则介于两者之间。这说明碱金属Mg的加入会使催化剂中产生大量的强碱中心,而过渡金属Zn的加入则使催化剂产生大量的弱碱中心。结合催化剂的活性数据推测,中强碱和强碱性位有利于CO和烃的生成,而弱碱性位有利于目标产物C2+醇的生成。
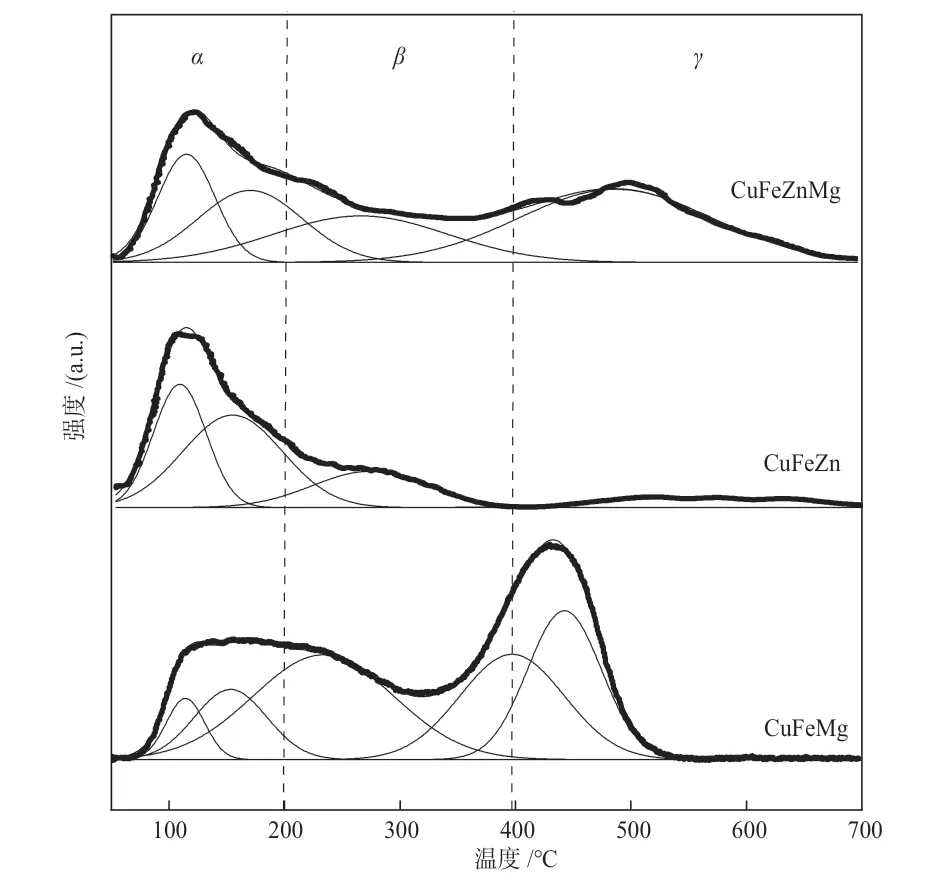
图2 CuFeM系列催化剂的CO2-TPD谱图Fig.2 CO2-TPD spectra of CuFeM catalysts

表3 CuFeM系列催化剂碱性位分布Table 3 Basic site distribution of CuFeM catalysts
2.1.4 N2吸/脱附分析
图3为催化剂反应前后的N2吸/脱附曲线,图4为催化剂反应前后的孔径分布。根据国际纯粹与应用化学联合会(IUPAC)分类,反应前所有催化剂均呈现IV型等温线,说明均为介孔材料,但其回滞环的形状却有比较大的差异。CuFeMg催化剂呈现H2(b)型回滞环,说明该催化剂为孔“颈”相对较宽的“墨水瓶”形介孔材料[10]。CuFeZn催化剂呈现H3型回滞环,说明该催化剂为平板狭缝介孔结构。CuFeZnMg催化剂呈现H2(a)型回滞环,说明该催化剂为孔“颈”相对较窄的“墨水瓶”形介孔材料。反应后,所有样品的回滞环形状明显变小,均呈现为H3型回滞环,说明反应后催化剂孔结构发生变化,比表面积大大减小,可能是因为反应过程中孔结构坍塌或者堵塞导致吸附容量变小。

图3 反应前(a)和反应后(b) CuFeM系列催化剂的N2吸/脱附曲线Fig.3 N2adsorption/desorption isotherms of CuFeM catalysts before (a) and after (b) reaction
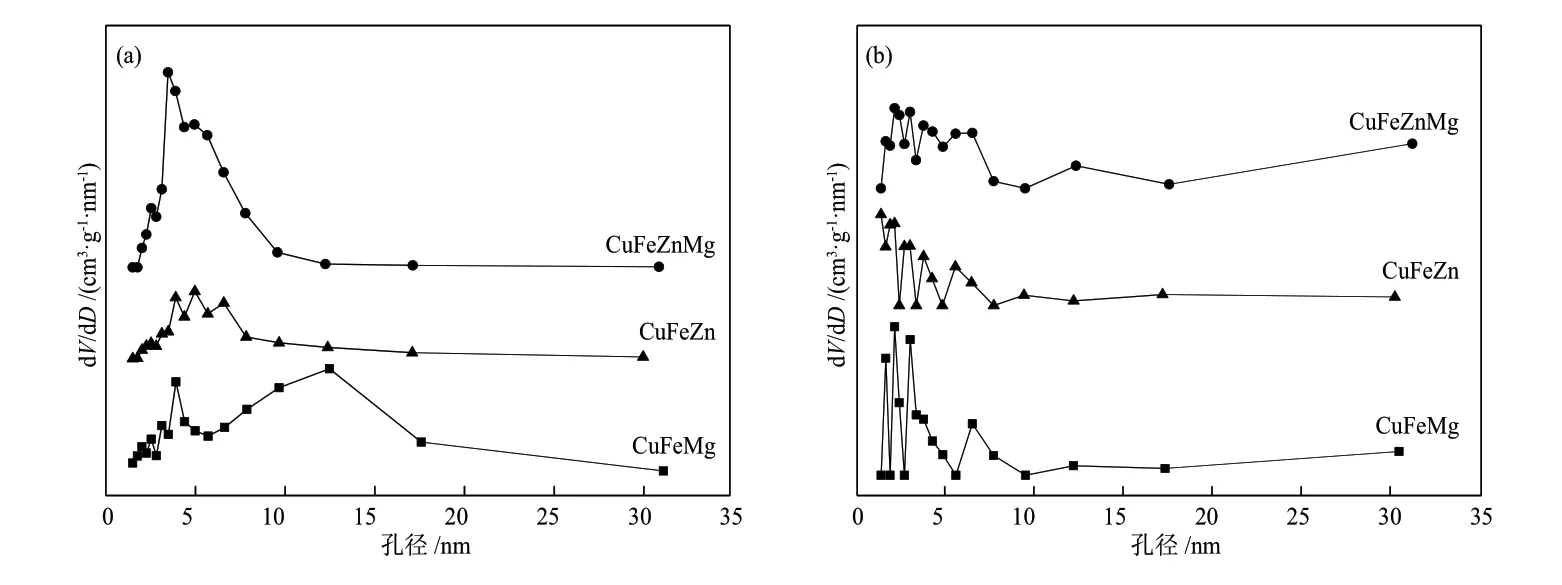
图4 反应前(a)和反应后(b) CuFeM系列催化剂的孔径分布Fig.4 Pore size distribution of CuFeM catalysts before (a) and after (b) reaction
表4列出了催化剂反应前后的织构参数。反应前,CuFeMg和CuFeZnMg催化剂的比表面积相差不大,均达到160 m2/g以上。可明显看出,CuFeZn催化剂的比表面积和孔容最小,但结合活性评价数据(表1、表2),该催化剂却拥有最好的催化性能,这说明比表面积和孔容不是影响该系列催化剂催化性能的关键因素。反应后,所有催化剂的比表面积、孔容和孔径均明显下降,可能是孔结构坍塌或者堵塞导致的,这也是催化剂稳定性不佳的原因之一。

表4 CuFeM系列催化剂反应前后的织构参数Table 4 Texture parameters of CuFeM catalysts before and after reaction
2.1.5 H2-TPR分析表征
图5为催化剂的H2-TPR结果。催化剂均在100~800 ℃的范围内出现两组还原峰,较低温度的还原峰归属为Cu物种的还原(Cu2+→Cu0);较高温度的宽峰,归属为Fe物种的还原(Fe3O4→FeO→Fe)[17-19]。含有Zn的CuFeZn和CuFeZnMg催化剂中Cu物种的还原峰略微向高温方向发生偏移,说明Zn的添加使Cu物种较难还原,可能是由于Zn和Cu之间存在一定的相互作用所致,而且添加Zn之后Cu物种还原峰的峰面积和峰形都有不同程度的变化,也充分说明了Cu物种的结合态发生了改变;同时,CuFeZn和CuFeZnMg催化剂中Fe物种的还原峰均向低温方向发生偏移,特别是CuFeZn催化剂中相应峰发生了较大幅度的移动,这说明Zn的添加使得Fe物种更容易被还原,催化剂中可能会因此产生更多的低价Fe物种,而结合课题组前期的研究结果,低价Fe有利于C2+醇的生成[20]。

图5 CuFeM系列催化剂的H2-TPR谱图Fig.5 H2-TPR spectra of CuFeM catalysts
2.2 不同Cu含量的CuxFe1Zn2系列催化剂
在CuFeM系列催化剂中,CuFeZn催化剂显示出优越的C2+醇合成性能,但CO2转化率仍然较低,故以CuFeM系列中催化性能最优的CuFeZn三元金属为基础,对其进行进一步优化。在本催化体系中,Cu、Fe物种为CO2加氢制低碳醇反应的催化剂的活性中心,其中Cu有利于CO2的吸附和H2的解离,能有效促进CO2转化[21],因此,为了进一步提高CO2转化率和C2+醇选择性,本文在Cu0.1Fe1Zn2催化剂的基础上进行了Cu含量的调控,考察Cu含量的变化对催化剂的微观组成、结构及活性金属价态等一系列物理化学性质的影响,探索催化剂理化性质与催化性能之间的构效关系,以期得到更佳的CO2加氢制备C2+醇性能。
2.2.1 活性评价结果分析
表5为CuxFe1Zn2系列催化剂的活性结果对比,转化率和选择性数据取反应5天活性数据的平均值。随着Cu含量的增加,CO2转化率逐渐升高,烃类选择性逐渐下降,而总醇选择性呈现先升高后降低的趋势。Cu0.5Fe1Zn2催化剂的总醇选择性最高,C2+醇的时空收率也最高,催化性能最好。

表5 CuxFe1Zn2系列催化剂的活性评价结果Table 5 Activity evaluation results of CuxFe1Zn2catalysts
表6为CuxFe1Zn2系列催化剂的醇产物分布情况,该系列催化剂的C2+醇占比均达到90%以上,且绝大部分的醇产物均为乙醇。
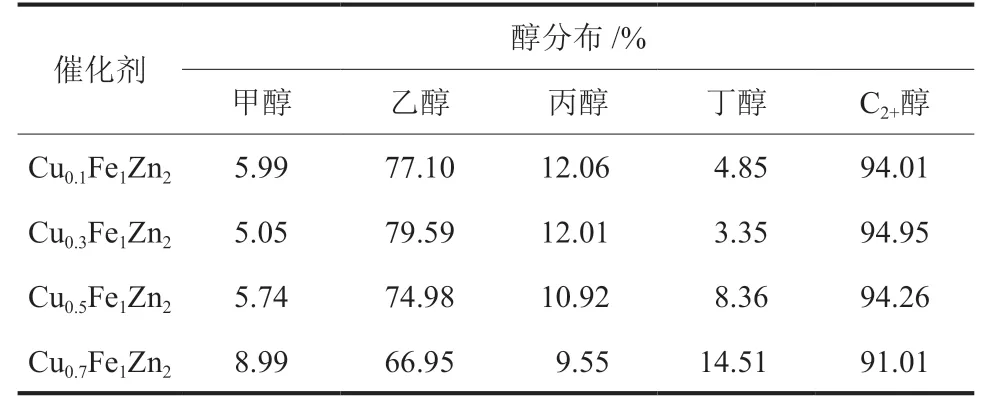
表6 CuxFe1Zn2系列催化剂的醇分布Table 6 Alcohol distribution of CuxFe1Zn2catalysts
图6为CuxFe1Zn2系列催化剂反应120 h内的总醇选择性随时间变化。120 h内Cu0.5Fe1Zn2催化剂的总醇选择性始终最高;Cu0.7Fe1Zn2催化剂的总醇选择性随时间下降的最快,稳定性最差,说明Cu含量过高可能会使活性组分在反应过程中发生烧结,最终导致催化剂的稳定性下降。

图6 CuxFe1Zn2系列催化剂的稳定性评价Fig.6 Stability evaluation of CuxFe1Zn2catalysts
2.2.2 XRD分析
为了探究催化剂反应前后的物种组成,对CuxFe1Zn2系列催化剂进行了XRD表征,如图7所示。反应前,催化剂中出现了ZnO(PDF No.99―0111)、CuO(PDF No.89―5899)、CuFe2O4(PDF No.77―0010)、Fe3O4(PDF No.89―4319)的衍射峰。反应后,出现了Fe5C2(PDF No.89―7272)的衍射峰,其中C可能来自反应过程中CO2的分解。同时,CuO被还原为Cu(PDF No.89―2838),结合H2-TPR分析结果表明,在H2气氛350 ℃预还原之后,Cu活性物种主要以低价态形式存在。反应后,催化剂的衍射峰变得窄而尖锐,意味着各物种的结晶度升高,这可能是导致催化剂活性下降的原因之一。
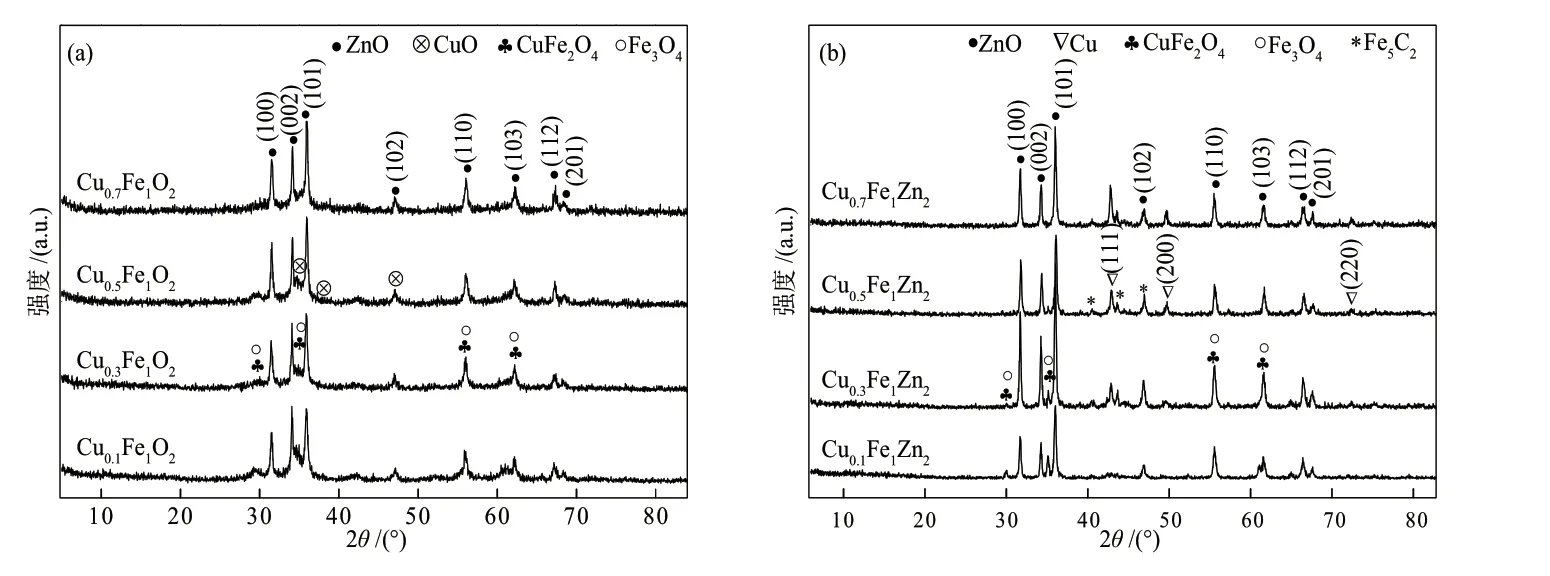
图7 反应前(a)和反应后(b) CuxFe1Zn2系列催化剂的XRD谱图Fig.7 XRD patterns of CuxFe1Zn2catalysts before (a) and after (b) reaction
根据谢乐公式计算了催化剂反应后的Cu0(111)晶面的晶粒尺寸,如表7所示。随着Cu含量的增加,Cu0(111)晶面的晶粒尺寸逐渐增大。据报道[22-23],这些较大且稳定的Cu颗粒促进了反应物形成乙醇。结合其活性数据推测,Cu物种在表面富集,全面增加了Cu活性位点的数量,从而有助于C2+醇的生成。Cu0.7Fe1Zn2催化剂的Cu0(111)晶面的晶粒尺寸最大,但其总醇选择性和C2+醇的时空收率却最低,说明最佳的Cu晶粒尺寸有一定范围,并不是越大越好。

表7 CuxFe1Zn2系列催化剂Cu0(111)晶面的晶粒尺寸Table 7 Grain sizes of Cu0(111) crystal plane of CuxFe1Zn2catalysts
2.2.3 H2-TPR分析
图8为CuxFe1Zn2系列催化剂的H2-TPR谱图。4种催化剂均显示有两组还原峰,分别归属为Cu物种的还原峰和Fe物种的还原峰。随着Cu含量的增加,Cu的还原峰面积逐渐增大,说明可还原性Cu物种逐渐增多。此外,Fe物种的还原峰逐渐向低温方向发生偏移,表明随着Cu活性物种的增加,Cu、Fe物种相互作用的几率增大,相互作用力增强,导致Fe物种更容易被还原,因而有更多的低价Fe物种产生。
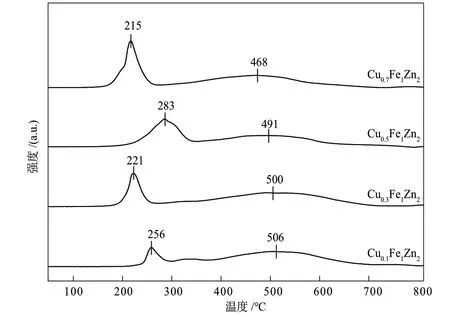
图8 CuxFe1Zn2系列催化剂的H2-TPR谱图Fig.8 H2-TPR spectra of CuxFe1Zn2catalysts
2.2.4 XPS分析
图9(a)为反应后催化剂的Fe 2p XPS谱图,结合能约为711 eV和725 eV处的两个峰分别对应于Fe 2p3/2和Fe 2p1/2。

图9 反应后CuxFe1Zn2系列催化剂的Fe 2p XPS光谱(a)和Fe 2p3/2分峰拟合图(b)Fig.9 Fe 2p XPS spectra of CuxFe1Zn2catalysts after reaction (a) and peak fitting spectra of Fe 2p3/2(b)
将Fe 2p3/2分峰拟合成以710.6 eV和712.9 eV为中心的两个峰(图9(b)),分别归属为Fe2+和Fe3+物种[24]。703.8 eV处的弱峰归属为Fe5C2物种[25-26],进一步证实了Fe3O4、CuFe2O4和Fe5C2不同Fe物种的共存,这与XRD表征结果一致。不同Fe物种的积分峰面积占比如表8所示。低价Fe(Fe5C2和Fe2+)的占比先增大后减少,在Cu0.5Fe1Zn2催化剂中达到最大,这与H2-TPR表征结果中Cu的增加使Fe物种更容易被还原保持一致。而较高比例的低价Fe有利于醇类,尤其是C2+醇的形成,这可能是影响该系列催化剂性能的关键因素,此结论与本课题组前期的研究结果一致[20]。

表8 反应后CuxFe1Zn2系列催化剂中Fe 2p3/2积分峰面积占比Table 8 Proportion of integral peak area of Fe 2p3/2in CuxFe1Zn2catalysts after reaction
2.2.5 SEM和EDS-mapping分析
对催化性能最好的Cu0.5Fe1Zn2催化剂进行了SEM和EDS-mapping表征,结果如图10所示。从图10(a)和图10(b)可以看出,催化剂呈现为大小均匀的球状纳米颗粒。从图10(c)~图10(f)可以看出,各个元素均匀分布,没有发生团聚现象,这可能是该催化剂活性较好的原因之一。

图10 Cu0.5Fe1Zn2催化剂的SEM照片((a)~(b))和EDS-mapping元素分布图((c)~(f))Fig.10 SEM photos ((a)~(b)) and EDS-mapping digrams ((c)~(f)) of Cu0.5Fe1Zn2catalysts
2.2.6 元素成分分析表征
为了探究催化剂中活性金属的实际含量和比例,对Cu0.5Fe1Zn2催化剂进行了XRF和ICP测试,如表9所示。经过计算,XRF与ICP测试结果均接近n(Cu):n(Fe):n(Zn) =0.5:1.0:1.8。已知XRF测试是一种近表层的分析方法,检测深度达到几十微米,而ICP测试可以检测催化剂体相的金属含量,两者的检测结果保持一致,说明催化剂近表面的各金属含量与体相的含量一致,活性金属在整个催化剂体系中均匀分布。

表9 Cu0.5Fe1Zn2催化剂的XRF和ICP测试结果Table 9 XRF and ICP test results of Cu0.5Fe1Zn2catalysts
3 结论
本文用类水滑石的制备方法制备了CuFeM系列催化剂的前驱体,考察了前驱体结构、催化剂碱性强弱和Cu含量对催化剂组成、形貌及低价Fe物种含量的影响,并关联了其在CO2加氢制备C2+醇中的构效关系,得出以下结论。
(1)由类水滑石前驱物焙烧生成的CuFeMg催化剂,产物中总醇选择性只有8.10%,且主要为甲醇,C2+醇占比只有35.40%;相反,CuFeZn催化剂的前驱体虽然不具有类水滑石结构,但由其衍生而来的复合金属氧化物催化剂却展示出良好的催化性能(总醇选择性为31.56%,总醇中C2+醇占比为94.01%),这说明类水滑石前驱体结构不是影响该反应的关键因素。而催化剂表面碱性强度对CO2加氢活性有显著影响,弱碱性位有利于目标产物C2+醇的生成,中强和强碱性位有利于CO和烃的生成。
(2)Cu活性物种有利于活化H2和CO2,能在一定程度上抑制烃类的生成。适当提高Cu含量可以有效提高总醇的选择性和C2+醇的时空收率,但Cu含量过高会导致催化剂的稳定性下降,不利于C2+醇的生成。当n(Cu):n(Fe):n(Zn) =0.5:1.0:2.0时催化剂中各元素分布均匀,活性金属相互作用,低价Fe含量较高,从而展现出良好的催化性能(总醇选择性为37.78%,C2+醇的时空收率为46.08 mg/(mL·h))。反应后,催化剂中各物种的结晶度升高,晶粒发生聚集,比表面积、孔容和孔径均大幅度减小。
