金刚石微粉表面的纳米硅烷化改性及其抗氧化性能
2022-08-17庞爱红董欣然董俊言沈方韧谭素玲贾晨超董书山毛青青吴增凤
庞爱红,董欣然,董俊言,沈方韧,谭素玲,贾晨超,董书山,毛青青,吴增凤
(1.河南厚德钻石科技有限公司, 河南 商丘476000)
(2.吉林大学, 超硬材料国家重点实验室, 长春 130000)
(3.塞默飞世尔科技公司, 上海 200000)
金刚石作为硬度高、耐磨性好的超硬材料,常与金属、陶瓷、树脂等结合剂联合烧结,制备成切削、磨削、抛光等用途的超硬工具[1-5]。金刚石工具发挥作用的核心要素是金刚石磨粒,其在持续的工作过程中能够被结合剂胎体牢固把持而保证使用寿命;同时,也必须保持合适的出露高度以保证工具锋利度。但由于金刚石表面的化学惰性,使得结合剂难以有效润湿并把持金刚石,金刚石磨粒常因结合剂胎体的把持力不足而过早脱落失效,影响工具效能的充分发挥。另外,在烧结制备金属/陶瓷结合剂工具时,较高的烧结温度易使金刚石表面氧化及石墨化;并且,工具在使用过程中往往会产生高热,使金刚石磨粒强度下降,影响工具的工作效率等[6-8]。
为了改善工具性能,对粒径为300~425 μm的中粗粒度的金刚石表面进行金属化处理,即在其表面包覆一层Ti、Cr、Ni、W等亲碳金属且与金刚石表面反应形成碳化物,可有效提高基体对金刚石的把持力,并可提高金刚石的高温热稳定性[9-10]。而大量应用于陶瓷/树脂结合剂磨具的细颗粒金刚石微粉,因其表面的金属化处理受到包覆技术、工艺、质量、效率及成本等多种因素的影响,在规模化工程应用中受到限制。特别是在金刚石用量极大的常规树脂/陶瓷结合剂磨具中,大都采用不经表面包覆处理的金刚石微粉裸料,导致树脂/陶瓷结合剂对金刚石微粉的把持力较差,磨具的使用寿命较短。因此,研究开发一种适用于金刚石微粉表面的非金属化改性技术,在金刚石微粉表面包覆一层致密的非金属薄膜,使其可与树脂/陶瓷基体成分反应从而提高基体对金刚石的把持力,还可有效提高金刚石微粉的高温抗氧化性能以及树脂/陶瓷结合剂对金刚石的把持能力,对于提高以金刚石微粉为磨料的高性能树脂/陶瓷结合剂金刚石工具性能有重要的工程应用意义。
对纳米/亚微米粒度的金刚石微粉表面进行硅烷化改性包覆处理,即以硅烷偶联剂为原料,采用溶胶-凝胶技术在金刚石表面包覆一层氧化硅薄膜,可有效提高超细颗粒金刚石在液态基质中的分散性和抗沉降性[11]。
硅烷偶联剂是一种分子中含有能与有机物和无机物同时反应的有机硅化合物,可用于制备无机-有机纳米复合材料[12-13],无机相可以是金属、陶瓷、氧化物、半导体等,有机相可以是塑料与橡胶等高分子材料。利用硅烷偶联剂对金属表面进行改性处理时,加入一些纳米粒子(如铈离子、纳米二氧化硅等)可以增加改性膜层的厚度和均匀性,有利于提高金属表面的抗腐蚀性[14]。
纳米/亚微米金刚石微粉由于其比表面积大、表面含有相当数量的功能基团而极易吸附团聚,在使用过程中难以有效分散,尤其是在制备抛光液时,金刚石颗粒容易在液态基质中沉降团聚而影响应用。为了有效提高细颗粒金刚石的分散性,业界开展了金刚石表面硅烷化包覆改性处理研究,以在金刚石表面形成连续的氧化硅膜或非连续的氧化硅球状颗粒。WAN等[15]用硅烷偶联剂的醇水溶液和甲苯溶液对金刚石微粉进行改性,用红外光谱分析了改性后金刚石表面的化学基团,证明硅烷偶联剂可在金刚石微粉表面形成一层凝胶膜,增强树脂结合剂与金刚石间的结合力,但并未对凝胶膜自身的物质结构进行进一步的分析与表征。此外,将硅烷偶联剂作为硅源,以聚乙烯吡咯烷酮(polyvinyl pyrrolidone,PVP)为偶联剂,还可在金刚石微粉表面附着一些分散分布的球状氧化硅颗粒[16-17],有利于改善金刚石在液态基质中的分散性。但这种非连续的氧化硅颗粒不能对金刚石表面形成全致密包覆,无法有效隔绝环境气氛,因而也难以改善金刚石的抗氧化性能。
金刚石的抗氧化性能主要和以下2个因素有关:(1)环境温度和气氛。对于晶型完整的金刚石颗粒,其在空气中的初始氧化温度约为800 ℃[18-19];(2)金刚石粒度。粒度越细,比表面积越大,在空气中加热时就越容易产生氧化烧蚀,其高温抗氧化性能越差。而对于采用机械破碎法制备的金刚石微粉,由于其含有更多的棱角与界面,初始氧化温度可以降至500 ℃左右[20]。
所以,对金刚石表面实施金属化包覆处理,可隔绝金刚石与外界氧源的接触而保护金刚石,提高金刚石在高温环境下的抗氧化性能[19];而对金刚石表面进行硅烷化改性处理,在金刚石表面形成一层氧化硅膜来隔离外界氧源,也可提高金刚石的抗氧化性能。但氧化硅膜必须覆盖完整、连续、致密,且在高温加热过程中不产生裂解,才能对金刚石起到有效的隔离保护作用。
在以往的金刚石表面硅烷化包覆处理研究报道中,均借助于甲苯、PVP等不同种类的反应助剂在金刚石表面包覆连续氧化硅膜或非连续的氧化硅颗粒。而本研究在不添加任何反应助剂的中性条件下,采用常见的硅烷偶联剂-正硅酸乙酯(TEOS)作为反应原料,通过调控反应体系的醇-水摩尔比,对金刚石微粉表面进行纳米膜包覆处理,并用X射线衍射(XRD)、透射电镜(TEM)及扫描电镜(SEM)等分析表征覆膜的物相结构,采用差示扫描量热法(DSC)分析覆膜金刚石的高温抗氧化能力。且为了进一步改善覆膜质量,还在硅烷膜中添加纳米硅粉,研究其增加后覆膜的厚度及均匀性变化情况。
1 实验材料与方法
金刚石微粉的粒度越细,就越容易发生团聚,在使用过程中则常常会因其分散性差而影响工程应用效果。为此,在工程应用过程中,为防止金刚石微粉发生团聚,对金刚石微粉特别是对超细的纳米/亚微米级的金刚石颗粒进行有效分散,是超细金刚石微粉发挥作用的一个重要条件。为了提高细粒度金刚石微粉的分散有效性,业界开展了许多采用硅烷偶联剂对金刚石微粉进行表面改性的研究[15,21],并取得了良好的应用效果。
1.1 实验原料
所用金刚石微粉用机械破碎法制备,其粒度尺寸为0.1~5.0 μm;所用纳米硅粉的主粒度尺寸为5.0~20.0 nm,纯度为99.9%;所用硅烷偶联剂为正硅酸乙酯(TEOS),纯度为99.9%。
1.2 金刚石微粉表面的硅烷化处理
硅烷化处理流程为:(1)将5 mL TEOS加入无水乙醇和水的混合溶液中,无水乙醇与水体积比为4∶1,混合溶液的总体积为200 mL;(2)将混合溶液放在磁力搅拌器上充分混合均匀,在50 ℃下水解1~3 h得到TEOS的水解溶液;(3)称取2 g金刚石微粉,将其加入水解溶液中,在50~100 ℃条件下搅拌2~4 h,得到纳米非晶氧化硅包覆的改性金刚石微粉的悬浊液;(4)将悬浊液在室温下静置沉淀,蒸发24~48 h,直至水完全蒸发,得到干燥的包覆膜层的微粉,其增加质量为金刚石原料质量的20.0%。为了进一步增加非晶氧化硅包覆膜厚度,在过程(3)中和金刚石一起一同加入质量分数为3.0%的纳米硅粉,其余处理步骤相同,得到的包覆膜层的增加质量为金刚石原料质量的45.0%。
1.3 测试与表征
将原料金刚石微粉(以下简称“D-Ⅰ”)、覆膜中不含纳米硅粉的改性金刚石微粉(以下简称“D-Ⅱ”)及覆膜中添加纳米硅粉的改性金刚石微粉(以下简称“D-Ⅲ”)在MAGELLAN 400扫描电镜下对比观察样品形貌,并使用扫描电镜能谱分析仪(EDS)对金刚石的表面纳米膜层组分进行测试,测试时信息深度为1 μm。
分别将差热分析前/后的覆膜改性金刚石微粉在Rigaku D/Max-2500型转靶X射线衍射仪上进行XRD测试,分析确定金刚石表面包覆膜层在加热处理前后的物相组成。测试采用铜靶,扫描范围(2θ)为10~90°,扫描速度(2θ)为20°/min。
采用JEM-2200FS透射电镜对改性金刚石微粉的表面覆膜形貌进行观察,并利用透射电镜能谱仪对覆膜成分及其分布状态进行表征。
在空气条件下,采用Rigaku TG-DTA 8120型热分析仪分别对D-Ⅰ、D-Ⅱ及D-Ⅲ进行热重分析(TG)和差式扫描量热分析(DSC),对比考察金刚石微粉在改性前后的抗氧化性能。测试时最高温度为800 ℃,升温速率为10 ℃/min。
2 实验结果与讨论
2.1 TEOS包覆反应机理及分析
在金刚石表面改性覆膜的反应机理包含水解和缩合2个过程,其中的缩合反应包括脱水缩合和脱醇缩合2种反应类型,其反应方程式为:

整个水解反应过程是TEOS在醇水溶液中与水发生反应,水电离出的 OH-取代TEOS中的—OC2H5(简称“—OR”)基团,与硅原子形成Si—OH键,被取代的—OR基团和水中剩余的H+结合形成乙醇。式(1)给出了TEOS中的—OR基团被水中 OH-一次取代的过程,生成的水解产物为Si(OR)3OH。实际上,TEOS的4个—OR基团根据实际反应条件皆可被 OH-取代,最终水解产物为 Si(OR)(4-n)(OH)n,其中的n可以是1,2,3或4,表明最终产物可能会随着n的变化而不同,其他研究也报道了类似的结果[22-23]。
TEOS在水解反应前处于体系能量较低的稳定状态,在—OR基团第一次被取代后,水解产物Si(OR)3OH中的取代羟基(—OH)基团不利于稳定硅原子的正电荷,所以在随后的水解反应过程中每一个—OR基团被取代的难度都将逐渐增加,这意味着在水解反应过程中随着n值从1到4,水解产物 Si(OR)(4-n)(OH)n也将从低能态的稳定相向高能态的过渡相转变,转变所需的活化能增加。因此,可以通过改变反应条件来获得具有不同n值的水解产物。
通过上述水解反应得到的水解产物Si(OR)(4-n)(OH)n可以脱水或脱醇形成聚合物,这种反应称为缩合反应。根据式(2),水解产物中的—OH基团之间相互反应,一个水解产物分子脱掉羟基中的H+,另一个水解产物分子脱掉一个—OH,这2个水解产物分子再反应形成Si-O-Si键,脱掉的H+和—OH反应形成H2O分子,就被称为脱水缩合。
根据式(3),水解产物中的—OH基团和—OR基团相互反应,一个水解产物分子脱掉一个—OR基团,另一个水解产物中的—OH脱掉一个H+,这2个水解产物同样可以形成Si—O—Si键,脱掉的H+和—OR基团反应生成乙醇,所以被称为脱醇缩合。
基于上述反应机理,可以得知影响水解产物结构的因素有水的含量和TEOS的含量;而水解产物的结构会影响下一步的缩合产物,最终影响金刚石表面凝胶膜的物相与形态。为了在金刚石表面形成具有交联网络结构的凝胶膜,可以通过改变反应条件,如水和TEOS的添加比例及反应工艺条件,来控制金刚石表面凝胶膜的结构与形态,由此,既可在金刚石表面获得连续膜结构,也可获得球状凝胶颗粒。
当水与TEOS的摩尔比≤5时[24],溶液中初始添加的水作为反应物不足以在反应开始时完成与所有TEOS分子的水解反应,需要缩合反应生成的水来继续后续的水解反应,所以每个TEOS分子只能水解取代一个—OR基团,其水解产物是 Si(OR)3OH,该水解产物可以脱水形成连续的线性链状聚合物。之后,生成的链状聚合物互相交叉连接,在金刚石表面形成带有电荷的三维连续网状膜,将金刚石颗粒分散隔离。但与此同时,在持续的凝缩过程中这种网状膜也易将多颗金刚石缠绕包裹在一起,形成金刚石-凝胶团聚体,导致金刚石颗粒的分散性变差。
当水与TEOS的摩尔比>5时[23,25],水解速率比缩合速率快得多,水解反应在缩合的初始阶段就基本完成,因此水解产物倾向于形成 Si(OR)2(OH)2。缩合反应沿多维方向进行,形成三维短链交联结构,进而形成孤立的凝胶颗粒聚集体[26],在此条件下,易在金刚石表面获得分立的球状凝胶颗粒。此外,也可以通过改变催化剂的类型和浓度而在金刚石表面获取颗粒状的水解产物。如用碱作催化剂时[27],整个溶液体系中的 OH-增加,水解产物倾向生成 Si(OR)(OH)3和Si(OH)4,缩合产物为分离的颗粒状SiO2聚集体。但当TEOS或碱的浓度过高时,过大的聚集体颗粒会导致静电斥力增加,最终无法形成凝胶膜。
在工程化烧结制备金刚石工具时,希望硅烷化改性的金刚石微粉具有良好的分散性与表面化学反应活性,亦即希望在金刚石颗粒表面获得一层连续致密且有活性反应基团的覆膜结构。由此,既可避免金刚石颗粒团聚,又可提高其高温抗氧化性能;同时,还能改善其与树脂/陶瓷结合剂间的化学反应能力,而提高烧结时基体对金刚石的把持力。
综上,要求在单颗粒金刚石表面形成一层连续完整的凝胶膜而非分立的球状凝胶颗粒,同时也避免形成金刚石-凝胶团聚体,使覆膜改性的金刚石颗粒具有良好的分散性、高温抗氧化性能及表面反应活性。本研究开发了一种新的金刚石表面硅烷化覆膜工艺,即采用高摩尔比的混合溶液系统(水与TEOS的摩尔比远大于5)对金刚石进行改性处理,在单颗粒金刚石表面获得含活性氧基团的SiO2纳米凝胶膜。这层覆膜可依靠自身的交联收缩应力而连续、致密包覆在金刚石颗粒表面,即可有效分散金刚石,又可在金刚石表面隔离空气而形成保护层,提高金刚石的高温抗氧化能力。
实验发现,单单依靠TEOS醇-水溶液反应体系所获得的覆膜厚度有限,难以满足工程应用的实际需求,需要采取其他的技术措施来增加覆膜厚度。在覆膜时添加纳米硅粉,其可与TEOS的水解产物缩合而成二氧化硅,使硅/氧比增加,凝胶膜增厚变匀,对金刚石的覆盖保护能力增强,进一步提高改性金刚石D-Ⅱ微粉的初始氧化温度。
2.2 SEM及EDS分析
分别将0.1 g的 D-Ⅰ或D-Ⅱ金刚石微粉加入3 mL的无水乙醇中超声5 min进行分散处理,并对其进行SEM对比分析。图1为D-Ⅰ和D-Ⅱ微粉SEM形貌及其表面EDS能谱。从图1a和图1b可以看出:金刚石改性前后的形貌没有明显改变,难以看出表面是否包覆有凝胶膜。从图1c和图1d可以看出:D-Ⅰ金刚石表面是100.00%的C元素,而D-Ⅱ金刚石表面覆膜中除C元素外还存在Si和O元素,且Si∶O原子数比为1∶8,说明D-Ⅱ凝胶膜中含有富余的活性氧基团。

图1 分散处理后的D-Ⅰ和D-Ⅱ微粉SEM形貌及其表面EDS能谱Fig.1 SEM morphologies and surface EDS spectra of dispersed D-Ⅰ and D-Ⅱ powders
在TEOS的醇-水溶液中对金刚石微粉进行改性处理,能够在金刚石表面获取厚度极薄的非晶纳米膜(在后文中有论述)。在工艺条件不变的条件下,若要进一步增加膜厚,难度较大。为此,在改性覆膜时加入纳米硅粉,通过纳米硅粉的表面聚合作用来增加覆膜厚度。图2为D-Ⅲ微粉表面SEM形貌及选区EDS能谱。

图2 D-Ⅲ微粉表面SEM形貌及选区EDS能谱Fig.2 SEM morphology and selected area EDS spectroscopy of D-Ⅲ micropowder surface
由图2a可以看出:球状的纳米硅粉颗粒黏附于氧化硅膜层中,覆膜层粗糙增厚。图2b表明:表面覆膜中除C外还测出了O和Si 2种元素,与图1的D-Ⅱ金刚石相比,Si元素的原子质量分数增大,其Si∶O原子比明显上升,从图1的1∶8升至1∶5,这说明添加的纳米硅粉可以被包裹在凝胶膜中,提升了Si的原子占比。所添加的纳米硅颗粒,可以在加热处理过程中与覆膜中的活性氧基团发生反应,促进覆膜致密化收缩。
2.3 XRD分析
图3分别是D-Ⅰ和D-Ⅱ金刚石微粉的XRD图谱。从图3可以看出:与D-Ⅰ的衍射图谱一致,改性后的D-Ⅱ金刚石的XRD谱图中只在衍射角2θ为43.935°和75.305°位置出现了金刚石衍射峰,分别对应金刚石的(111)和(220)晶面,并没有出现其他相的特征峰。但图1d的EDS结果证明了D-Ⅱ金刚石微粉表面凝胶膜的存在,这说明金刚石表面改性膜的厚度很薄,且可能呈非晶态形式存在。

图3 D-Ⅰ和D-Ⅱ金刚石微粉的XRD图谱Fig.3 XRD spectra of D-Ⅰ and D-Ⅱ diamond powders
图4为D-Ⅲ金刚石微粉和纳米硅粉的XRD图谱。如图4所示:D-Ⅲ金刚石微粉的谱图中(图4a)除出现金刚石的特征峰外,同时也出现了单质硅与二氧化硅的特征峰,单质硅的存在来源于覆膜中所添加的纳米硅粉。将D-Ⅲ的XRD谱图(图4a)和纳米硅粉的XRD谱图(图4b)做对比,可明显看出D-Ⅲ中出现了纳米硅粉的(111),(220),(311),(422)晶面,这几个晶面对应纳米硅粉衍射强度较强的衍射峰,纳米硅粉剩余晶面由于添加的纳米硅粉量较少,所以无法从背底中识别出来;而二氧化硅(110)晶面的衍射峰是一个典型的非晶峰包,表明凝胶膜中的二氧化硅是非晶相。同时,图3中的D-Ⅱ未出现二氧化硅的衍射峰,表明其金刚石表面覆盖的二氧化硅膜厚度不足且是非晶相。因此,在其他实验条件不变时,在覆膜中添加一定数量的纳米硅粉后,图4a中出现了明显的二氧化硅非晶衍射峰。由此表明,添加纳米硅粉可以增加金刚石表面凝胶膜的厚度,当膜厚增加到一定程度时,XRD便可检测出二氧化硅的非晶衍射峰。此外,二氧化硅的来源也可能是TEOS的水解产物与纳米硅粉发生缩合反应生成的,但目前尚无定论,需要后续的研究论证。

图4 D-Ⅲ金刚石微粉和纳米硅粉的XRD图谱Fig.4 XRD spectrum of D-Ⅲdiamond powers and nano-Si powders
2.4 TEM分析
图5是D-Ⅱ及D-Ⅲ金刚石微粉的TEM、HRTEM及TEM能谱分析结果。由图5可以看出:未添加纳米硅粉时,金刚石表面黏附着一层粗糙的覆膜(图5a);金刚石的棱角变得圆润模糊,凝胶膜表面没有具有晶体特征的晶格条纹(图5b),这说明金刚石表面包裹了一层非晶膜;金刚石边缘处所附着的膜由Si和O组成,由于膜层的厚度太薄,仅为2~10 nm,所以,在非边缘区域的能谱图中仍可检测到膜层下方的金刚石(图5c)。而D-Ⅲ金刚石表面的凝胶膜覆盖得更加均匀,能够清晰看出金刚石和凝胶膜之间的交界(图5d);此凝胶膜依旧由Si和O组成,但凝胶膜的厚度却显著增加至20 nm以上(图5e),由此可得到图4的非晶二氧化硅凝胶膜的XRD衍射峰。

图5 D-Ⅱ及D-Ⅲ金刚石微粉的TEM、HRTEM及TEM能谱分析结果Fig.5 TEM, HRTEM and TEM energy spectrum analysis results of D-Ⅱ and D-Ⅲ diamond powders
2.5 金刚石微粉的差热分析
分别对D-Ⅰ、D-Ⅱ及D-Ⅲ金刚石微粉进行差热分析,对比考察不同结构的改性覆膜层对金刚石微粉抗氧化性能的影响。
2.5.1 D-Ⅰ金刚石微粉
图6是D-Ⅰ金刚石微粉的TG及DSC测试结果,其中TG曲线上的起始氧化温度按照TG曲线开始偏离基线点的温度来确定。由于机械破碎法制备的金刚石微粉有很多破碎棱角与台阶面,颗粒表面积大且有大量sp3悬键,其在空气中容易吸附少量水分,所以图6的TG曲线在70 ℃左右有一个较小的失重,而与之对应的DSC曲线上则有一个较小的吸热峰,这可能是缘于金刚石微粉中表面吸附水的蒸发。根据图6的TG曲线,金刚石微粉在500~750 ℃间产生很大的氧化失重。与粒度代号为40/45等的粗粒度金刚石单晶不同,细颗粒金刚石微粉的棱边/棱面较多,与空气接触面积大,氧化活性较高,因而其起始氧化温度要明显低于粗粒度金刚石的,从500 ℃左右开始逐渐氧化失重,而相对应的DSC曲线则在714 ℃有一个较强的金刚石氧化放热峰。在此温度下,金刚石微粉被快速氧化烧蚀,此温度点也为金刚石氧化速率最大的温度点,此时的金刚石样品剩余质量占比为44.8%。经过800 ℃测试完毕后的样品剩余质量占比为21.5%,亦即有占比为78.5%的金刚石微粉被氧化烧蚀掉。
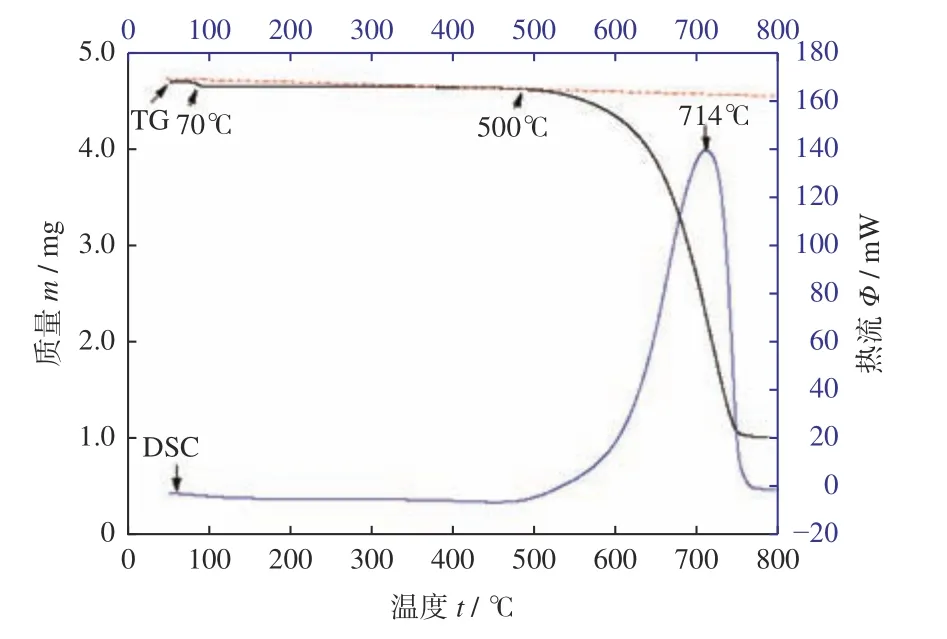
图6 D-Ⅰ金刚石微粉的TG及DSC测试结果Fig.6 TG and DSC results of D-Ⅰ diamond powders
2.5.2 D-Ⅱ金刚石微粉
图7为D-Ⅱ金刚石微粉的TG及DSC测试结果。根据图7的TG曲线,样品在550~750 ℃间发生氧化失重,起始氧化温度为550 ℃,相比于D-Ⅰ 金刚石的提升了50 ℃。这是由于D-Ⅱ 金刚石微粉表面包覆了一层凝胶膜,隔离了空气中的氧气,因而提高了其起始氧化温度。此时样品剩余质量占比为97.8%,烧蚀损失的2.2%来源于凝胶膜的脱水失重。相应的DSC曲线则在680 ℃出现一个较强的氧化放热峰,较图6中DSC曲线的峰值温度降低了34 ℃。这表明金刚石表面凝胶膜中的富氧基团的化学反应活性高于空气中氧的,可直接作用于金刚石表面而加快金刚石的氧化烧蚀速度。在此温度下,样品剩余质量占比为63.6%,比D-Ⅰ金刚石在氧化速率最大峰值温度点714 ℃时的剩余质量占比提升了18.8%。

图7 D-Ⅱ金刚石微粉的TG及DSC测试结果Fig.7 TG and DSC results of D-Ⅱ diamond powders
金刚石颗粒上覆膜的目的是为了增强其抗氧化能力,尽可能减少金刚石的氧化烧蚀量。所以在计算金刚石的氧化烧蚀量时,要去除凝胶膜的占比,只对差热分析前后的金刚石剩余质量进行比较来考察样品的抗氧化性,金刚石的剩余质量占比越多,其保护效果越好。差热分析后的金刚石剩余质量占比可按下式计算:

式中:Ws为差热分析后剩余金刚石的质量占比,WT是温度为T时TG曲线所测量的剩余样品的质量占比,Wm为剩余样品中凝胶膜的质量占比(扣除凝胶膜在加热过程中的脱水失重),Wo为初始样品中金刚石的质量占比。
考虑到初始D-Ⅱ样品是由质量分数分别为80.0%的金刚石(Wo)和20.0%的凝胶膜组成,在680 ℃峰值温度点D-Ⅱ样品的剩余质量占比WT为初始样品的63.6%,其中,凝胶膜的剩余质量占比Wm为初始样品的17.8%(扣除其2.2%的脱水失重),金刚石的剩余质量占比为初始样品的45.8%。将数据代入式(1)中,可得最终D-Ⅱ样品的剩余金刚石质量占比Ws为57.3%,比D-Ⅰ样品的剩余质量占比44.8%上升了12.5个百分点。这是由于在达到680 ℃之前,D-Ⅱ金刚石表面可能仍被完整的凝胶膜所覆盖而隔绝外界氧气,此时只有凝胶膜中的活性氧基团与金刚石发生氧化反应。但活性氧基团数量有限,所以金刚石剩余质量得以提升,说明覆膜对金刚石的保护作用增强。但是,当温度超过680 ℃后,金刚石表面的凝胶膜可能会因烧蚀而裂解,无法完整覆盖金刚石表面,而使空气中的氧也与金刚石表面接触而对金刚石产生氧化作用。此时在覆膜中的活性氧及空气中的氧的双重作用下,D-Ⅱ金刚石的氧化失重加速,所以在差热测试后,样品的剩余质量占比WT为28.4%。考虑到D-Ⅱ金刚石表面的TEOS覆膜增重的变化,最终测试样品中剩余金刚石质量占比Ws为13.3%,比D-Ⅰ金刚石的烧蚀残余质量占比21.5%还要少。
2.5.3 D-Ⅲ金刚石微粉
图8为D-Ⅲ金刚石微粉的TG及DSC测试曲线。D-Ⅲ金刚石分别是由质量分数为55.0%的金刚石(Wo)和45.0%的凝胶膜组成,根据图8的TG曲线,在50~610 ℃温度区间内样品的质量缓慢下降,可能缘于凝胶膜中结合水的加热析出;在610 ℃后样品开始加速氧化失重,此时样品剩余质量占比为96.2%,亦即样品中凝胶膜脱水失重率为3.8%。而在DSC曲线的50~610 ℃温度段内,分别在170 ℃和570 ℃出现2个吸热峰。在此温度段内的TG失重和DSC吸热现象主要来源于凝胶膜中的二氧化硅结合水的析出,而二氧化硅结合水则有2种来源途径:(1)根据前述脱水缩合反应方程式(2),TEOS水解后与自身缩合而形成二氧化硅网状膜,在此过程中会产生部分结合水,此部分结合水可能会在170 ℃脱除挥发;(2)在570 ℃时,TEOS水解产物与纳米硅粉缩合形成二氧化硅,在此缩合过程中也可产生结合水的分解挥发而出现吸热峰。

图8 D-Ⅲ金刚石微粉的TG及DSC测试结果Fig.8 TG and DSC results of D-Ⅲ diamond powders
从图8的TG曲线可以看出:样品在610~800 ℃出现明显的金刚石氧化烧蚀失重,起始氧化温度为610℃,比D-Ⅱ金刚石的又提高了60 ℃,测试样品的剩余质量占比WT为82.3%,样品中凝胶膜脱水后失重的质量占比Wm为41.2%,所以代入金刚石剩余质量占比公式(1)中可得D-Ⅲ样品中金刚石剩余质量占比Ws为74.7%,与相对应的D-I的44.8%和D-II的57.3%相比,D-Ⅲ金刚石剩余量显著提升,而金刚石的烧蚀损失量(占比为25.3%)显著减少,亦即,覆膜对金刚石的保护作用增强。这是由于纳米硅粉和凝胶膜中的活性氧基团之间的反应,可以消耗掉大部分活性氧而生成具有保护效果的二氧化硅,相应地减少了活性氧基团对金刚石的氧化烧蚀,从而显著提升了金刚石的高温抗氧化性能。
综上,通过采用TEOS对金刚石微粉进行改性处理,可以在金刚石微粉表面获取连续、致密且含有活性氧基团的纳米非晶二氧化硅膜层。膜层既可在金刚石表面形成隔离保护层,提高金刚石的高温抗氧化性能,又可提供具有足够活性的氧基团。这种活性氧基团可以在低温烧结时与树脂结合剂中的—OH基团反应而提高二者间的结合强度,由此可有效提高树脂结合剂对金刚石的固结把持能力,为开发高性能树脂结合剂金刚石工具提供良好的物质条件。同时,在TEOS改性覆膜中添加纳米硅粉后,还可显著提高改性金刚石在800 ℃时的高温抗氧化性能,有效防止金刚石微粉的高温氧化,这为采用细颗粒金刚石微粉在高温条件下烧结制备陶瓷结合剂金刚石工具提供了有益的材料基础,从而有助于开发高性能的陶瓷结合剂金刚石工具。
2.6 差热分析后样品的XRD分析
为了进一步分析不同改性处理的金刚石微粉的性能,对差热分析后的覆膜改性金刚石微粉样品进行XRD分析,以确定加热氧化处理后残余样品的物相组成。差热分析在空气条件下进行,加热速率为10 ℃/min,测试最高温度为800 ℃。图9为差热分析后的D-Ⅱ及D-Ⅲ样品的XRD图谱。
从图9的特征衍射峰可以看出:2种样品皆由晶体二氧化硅和金刚石组成。将图9a与图3中的D-Ⅱ金刚石微粉的XRD图谱对比,可以看出图9a中出现了晶体二氧化硅衍射峰,这表明TEOS覆膜中的氧化硅在加热过程中出现了由非晶结构向晶态结构的转变。将图9b与非加热处理的D-Ⅲ金刚石微粉图4a比较,可以看出图9b中二氧化硅的半峰宽减小,表明覆膜中的氧化硅由非晶相转化为晶体相的比例显著提高;同时,图9b中单质硅的特征峰消失,这是由于纳米硅粉会在高温下被覆膜中的富余活性氧基团氧化而全部转化为二氧化硅晶体所致。
通过对比分析图9的差热样品可知:差热测试后D-Ⅲ金刚石微粉的剩余质量明显高于D-II金刚石微粉的,表明D-Ⅲ金刚石表面覆膜层可有效提高其对金刚石的抗氧化保护能力,这得益于膜层中的纳米硅粉消耗了凝胶膜中的活性氧基团,消解了其对金刚石在高温下的氧化损伤。D-Ⅲ的XRD谱图中无纳米硅衍射峰,取而代之的是二氧化硅的衍射峰,这也证明了纳米硅在高温下可以和膜层中的活性氧基团反应形成二氧化硅而有效保护金刚石,从而显著提升金刚石微粉的抗氧化性能。

图9 差热分析后的D-Ⅱ及D-Ⅲ样品的XRD图谱Fig.9 XRD patterns of D-Ⅱ and D-Ⅲ samples after differential thermal analysis
3 结论
(1)采用TEOS对金刚石微粉表面进行改性处理,可在金刚石颗粒表面形成2~10 nm的具有活性氧基团的非晶二氧化硅纳米凝胶膜,加热至一定的温度后,凝胶膜中的二氧化硅可由非晶相向晶体相转变。
(2)金刚石微粉在空气中的初始氧化温度从原料金刚石的500 ℃提升到TEOS覆膜改性后的550 ℃。
(3)在TEOS覆膜中添加纳米硅粉后,金刚石微粉在空气中的初始氧化温度可进一步提升至610 ℃;且经过800 ℃的热处理后,样品剩余质量比原料金刚石处理后的剩余质量大幅度提升,表明TEOS覆膜中添加纳米硅粉后可以显著提高金刚石的高温抗氧化性能。
(4)TEOS覆膜中富含的活性氧基团能与树脂/陶瓷结合剂间产生化学反应,有利于提高结合剂基体对金刚石的把持力,可为制备高性能的树脂/陶瓷结合剂金刚石工具提供良好的功能化改性原材料。
