5种新型聚酰亚胺的合成及光谱学性能研究
2022-08-16徐山祖王甫鹏杨艳华
徐山祖,李 先,王甫鹏,杨艳华
(昆明学院 化学化工学院,云南 昆明 650214)
芳香型聚酰亚胺由于具有低介电性能和强机械强度等特性,已被广泛应用于微电子领域.然而,在电场作用下,聚酰亚胺分子链中存在从二胺单体到二酐单体的电荷转移复合物,致使聚酰亚胺呈现深棕色或紫褐色,限制了其在光学器件领域的应用.一般情况下,通过引入柔性链接、不对称结构基团或空间体积较大的芳香基团[1],影响电荷转移效应,从而起到改善聚酰亚胺光学性能的作用.我们前期的工作[2-4]主要聚焦于聚酰亚胺结构对电稳态存储性能的影响,在此基础上,我们采用相同的合成方法制备取代基不同的聚酰亚胺,进一步探讨结构对核磁和光学性能的影响.因此,本文拟通过引入不同电荷特性的芳基取代基团,调控聚酰亚胺分子的光谱学性能,旨在为获得适合制造光学器件的聚酰亚胺材料提供参考依据.
1 实验部分
1.1 试剂和仪器
N,N-二甲基乙酰胺(DMAc)购自南京化学试剂有限公司,加入KOH减压蒸馏后除水备用;所有芳基硼酸和有机试剂均购自阿拉丁试剂(上海)有限公司,所有试剂和溶剂均为分析纯.
Bruker Avance II-400型核磁共振仪测试化合物的1H NMR和13C NMR;日本岛津UV-2450/2550型紫外-可见分光光度计测试化合物的光谱图.根据之前的研究[2-4]结果,合成化合物1、2和3.
1.2 实验步骤
1.2.1 二胺单体的合成
根据之前的研究[4]结果,以4-氨基-N-(4-氨基苯基)-N-(2-溴苯基)苯甲酰胺(化合物3)为底物,经Suzuki偶联反应进行结构修饰,合成路线如图1所示,反应涉及的物质的量完全相同,此处不再赘述.
二胺单体4a(C26H23N3O):1H NMR(400 MHz,DMSO-d6,δ):7.52(d,1H,J=8.0 Hz,ArH),7.40(d,3H,J=8.0 Hz,ArH),7.30~7.23(m,2H,ArH),7.18(d,3H,J=8.0 Hz,ArH),6.99(d,2H,J=12.0 Hz,ArH),6.52(d,2H,J=8.0 Hz,ArH),6.30(d,4H,J=8.0 Hz,ArH),5.40(s,2H,-CH2-),5.01(s,2H,-NH2),4.85(s,2H,-NH2).13C NMR(101 MHz,DMSO-d6,δ):170.1,150.5,147.2,141.4,140.8,136.0,133.2,131.0,130.1,129.4,128.7,128.2,127.9,127.5,127.1,123.0,114.3,112.5,51.6.
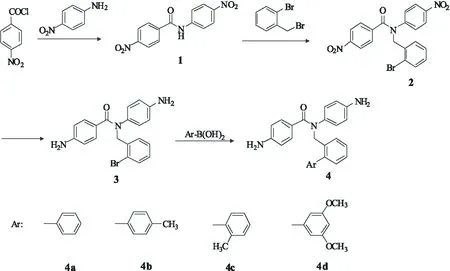
图1 二胺单体的合成路线
二胺单体4b(C27H25N3O):1H NMR(400 MHz,DMSO-d6,δ):7.50(d,1H,J=8.0 Hz,ArH),7.36(t,1H,J=4.0 Hz,ArH),7.29(t,1H,J=8.0 Hz,ArH),7.21(d,2H,J=8.0 Hz,ArH),7.13(d,1H,J=8.0 Hz,ArH),7.06(d,2H,J=8.0 Hz,ArH),6.99(d,2H,J=8.0 Hz,ArH),6.53(d,2H,J=8.0 Hz,ArH),6.30(d,4H,J=8.0 Hz,ArH),5.40(s,2H,-CH2-),5.01(s,2H,-NH2),4.85(s,2H,-NH2),2.34(s,3H,-CH3).13C NMR(101 MHz,DMSO-d6,δ):170.2,150.5,147.3,141.3,137.9,136.7,136.0,133.2,131.0,130.1,129.3,129.3,128.3,128.2,127.8,127.7,127.0,123.1,114.3,112.5, 51.6,21.2.
二胺单体4c(C27H25N3O):1H NMR(400 MHz,DMSO-d6,δ):7.54(d,1H,J=8.0 Hz,ArH),7.39(t,1H,J=8.0 Hz,ArH),7.29(s,1H,ArH),7.26(d,2H,J=4.0 Hz,ArH),7.20~7.16(m,1H,ArH),7.03(q,3H,J=4.0 Hz,ArH),6.88(d,1H,J=8.0 Hz,ArH),6.51(d,2H,J=8.0 Hz,ArH),6.31(q,4H,J=4.0 Hz,ArH),5.41(s,2H,-CH2-),5.03(s,2H,-NH2),4.62(q,2H,J=12.0 Hz,-NH2),1.85(s,3H,-CH3).13C NMR(101 MHz,DMSO-d6,δ):170.1,150.5,147.3,140.6,140.3,136.3,135.7,133.3,131.0,130.3,129.6,129.5,128.1,127.9,127.9,127.5,126.9,126.0,123.0,114.3,112.5,51.6,20.0.
二胺单体4d(C28H27N3O3):1H NMR(400 MHz,DMSO-d6,δ):7.48(d,1H,J=8.0 Hz,ArH),7.37(t,1H,J=8.0 Hz,ArH),7.28(t,1H,J=8.0 Hz,ArH),7.15(d,1H,J=4.0 Hz,ArH),6.98(d,2H,J=8.0 Hz,ArH),6.53(d,2H,J=8.0 Hz,ArH),6.47(s,1H,ArH),6.30(d,6H,J=12.0 Hz,ArH),5.40(s,2H,-CH2-),5.01(s,2H,-NH2),4.88(s,2H,-NH2),3.73(s,6H,-OCH3).13C NMR(101 MHz,DMSO-d6,δ):170.2,160.6,150.5,147.2,142.9,141.4,136.0,133.1,131.0,129.8,128.3,128.0,127.0,123.1,114.2,112.5,107.5,99.7,55.7,51.3.
1.2.2 聚合物的合成
根据之前的研究[4]结果,合成所有聚酰亚胺化合物,并进行核磁氢谱表征.
聚酰亚胺3-PMDA((C30H16BrN3O5)n):1H NMR(400 MHz,DMSO-d6,δ):8.30(s,2H,ArH),7.95~7.22(m,12H,ArH),5.20(s,2H,-CH2-).
聚酰亚胺4a-PMDA((C36H21N3O5)n):1H NMR(400 MHz,DMSO-d6,δ):8.31~8.15(m,2H,ArH),7.70~7.03(m,17H,ArH),5.10(t,2H,J=28.0 Hz,-CH2-).
聚酰亚胺4b-PMDA((C37H23N3O5)n):1H NMR(400 MHz,DMSO-d6,δ):8.29(t,2H,J=28.0 Hz,ArH),7.67~6.83(m,16H,ArH),5.09(d,2H,J=28.0 Hz,-CH2-),2.36(s,3H,-CH3).
聚酰亚胺4c-PMDA((C37H23N3O5)n):1H NMR(400 MHz,DMSO-d6,δ):8.30~8.21(m,2H,ArH),7.85~7.55(m,4H,ArH),7.44~7.21(m,8H,ArH),7.16~6.83(m,4H,ArH),4.86(d,2H,J=32.0 Hz,-CH2-),1.88(s,3H,-CH3).
聚酰亚胺4d-PMDA((C38H25N3O7)n)在氘代二甲亚砜中溶解度太差,未能测出核磁氢谱.
2 结果与讨论
2.1 核磁表征
化合物3经Suzuki偶联反应后,分别引入苯基、对甲基苯基、邻甲基苯基和3,5-二甲氧基苯基等基团,得到二胺单体4a,4b,4c和4d.以上物质分别与均苯四甲酸二酐经化学酰亚胺法得到聚酰亚胺3-PMDA,4a-PMDA,4b-PMDA,4c-PMDA和4d-PMDA.二胺单体和聚酰亚胺的核磁氢谱特征峰化学位移值(δ)如表1所示.二胺单体4a,4b,4c和4d的-CH2-化学位移值分别为5.40,5.40,5.41和5.40,相比较于化合物3的5.45,δ减小,向高场方向移动.同时二胺单体4a,4b,4c和4d的-NH2化学位移值相比较化合物3的5.06和4.94,δ减小,也向高场方向移动,说明引入芳基修饰的二胺单体,增加了分子中π电子的流动性,产生感应磁场,影响了分子的各向异性效应,-CH2-和-NH2恰好处于屏蔽区,δ都向高场移动[5].

表1 聚酰亚胺及其二胺单体结构式与光谱学数据

表1(续)
聚酰亚胺4d-PMDA在氘代试剂中的溶解性太差,未能测试核磁氢谱.聚酰亚胺4a-PMDA,4b-PMDA和4c-PMDA中-CH2-的δ分别为5.10,5.09和4.86,相比较于3-PMDA的5.20,δ变小,都向高场方向移动,说明分子中的各向异性效应影响了-CH2-的δ.然而,4b-PMDA和4c-PMDA中-CH3的δ分别为2.36和1.88,相比较于4b和4c的2.34和1.85,δ偏大,向低场方向移动,说明两种物质中的-CH3处于去屏蔽区.同时所有聚酰亚胺中-CH2-的δ都比二胺单体的偏小,说明-CH2-处于屏蔽区,δ都向高场移动.
2.2 聚酰亚胺的紫外-可见光谱测试
测试紫外-可见光谱(UV)试剂为二氯甲烷,溶液浓度为5×10-5mol/L.将测试结果进行归一化处理后,得到的5种聚酰亚胺UV图谱,如图2所示,最大吸收波长数据如表1所示.

λ/nm
5种聚酰亚胺的UV图谱中,只有一个位于290~320 nm区间的最大吸收波长,这是由电子供体(二胺部分)与电子受体(二酐部分)间的分子内电荷转移导致的[2].在250~275 nm波长范围内有两个很弱的吸收峰,这是由分子内含有的杂原子多重键生色团(C=O)的n→π*跃迁导致的,这种跃迁符合轨道重叠禁阻和对称性禁阻的条件,所以吸收强度很弱[6].相较于聚酰亚胺3-PMDA的最大吸收波长值310 nm,经Suzuki偶联反应引入的芳基基团不同,导致每个聚酰亚胺分子的最大吸收波长值间存在差异.
虽然聚酰亚胺4a-PMDA在结构上只比4b-PMDA少了一个对甲基基团,但是相较于4a-PMDA的最大吸收波长值308 nm,4b-PMDA的为311 nm,波长红移,说明4b-PMDA含有对-CH3基团中C-H键的电子与整个分子中的π电子重叠,产生超共轭效应,使得π电子的离域空间增加,降低了分子的π*轨道能量,导致UV光谱发生红移.相较于4a-PMDA的UV光谱,3-PMDA最大吸收波长红移2 nm,说明-Br连接在共轭体系上后,形成了p-π共轭效应,使π电子的离域范围增大,导致光谱发生红移[5].
4c-PMDA和4d-PMDA的最大吸收波长值分别为298,296 nm,波长蓝移,说明4c-PMDA中的邻-CH3基团和4d-PMDA中的两个-OCH3基团,增加了分子间的空间位阻效应,减弱了分子的刚性和平面性,使得分子中的π电子离域性减弱,提升了分子的π*轨道能量,导致UV光谱发生蓝移.
3 小结
综上所述,本研究合成了5种具有均苯四甲酸二酐部分的聚酰亚胺,由于Suzuki偶联反应引入的芳基基团电荷特性不同,不仅导致聚酰亚胺分子中存在各向异性效应,而且扰乱了分子的共轭体系,致使聚酰亚胺特征峰在核磁氢谱中的化学位移存在差异,以及紫外-可见光谱图谱发生红移或蓝移.此外,由于聚酰亚胺的取代基不同,还可能会影响聚酰亚胺薄膜的吸水性、热稳定性能和透明性等性质,对于该问题我们将在后续的工作中继续深入研究.
