认识非常规氢键
2022-08-15赵继海刘懿梅
赵继海 刘懿梅
(1.广东深圳科学高中 2.广东深圳红岭中学)
1 问题的提出
氢键是高考化学的常见考点,但2020年的一道高考题却使人耳目一新,也让不少考生叫苦,因为涉及了不同于正常氢键的双氢键.
例1(2020 年全国Ⅲ卷,节选)氨硼烷(NH3BH3)分子中,与N 原子相连的H 呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-).与NH3BH3原子总数相等的等电子体是_________(写分子式),其熔点比NH3BH3_________(填“高”或“低”),原因是在NH3BH3分子之间存在________,也称“双氢键”.
从考后的反馈来看,最后的解释原因这一问,考生得分率较低,因为对双氢键感到陌生,但也说明很多考生并未真正理解氢键的本质.其实题目中是有提示的,考虑到氢键的电性本质,显然是因为Hδ+和Hδ-之间产生了静电作用.目前的高三复习往往把重点放在氢键理论的模式化应用上,即用模板化的语言解释物质的性质表现,而忽略了对氢键本质的认识.
2 氢键的本质
高中教材将氢键表示为X—H…Y,X、Y 代表F、O、N 等原子,强极性的X—H 键中正电性的H 原子与Y 原子的孤对电子之间产生静电作用而形成氢键.这一类氢键是高中师生所熟悉的,可视为常规型氢键.
物质世界是丰富多彩的,在化合物中,键的极性强弱并非一成不变,而是要受到与键相连原子的影响.例如CH4分子本来难以形成氢键,但在三氯甲烷分子中,由于受到3个吸电子的Cl原子的作用,使得C—H 键的极性增强,H 原子有了强正电性,就能够与负电性强的原子形成氢键,例如三氯甲烷与丙酮可以形成分子间氢键,如图1所示.可见,氢键的本质是正电性的H 原子与负电性微粒之间的作用,那么在X—H…Y 结构中,只要H 原子的正电性和Y 的负电性达到一定程度,就可以产生明显的电性相互作用,这就是非常规氢键产生的原因.
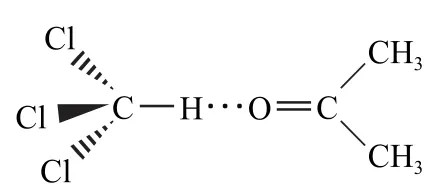
图1
3 常见的非常规氢键
除了正常氢键外,人们早已发现了多种类型的非常规氢键,二氢键是其中的研究热点.
3.1 二氢键
2020年全国Ⅲ卷高考题中所提到的氨硼烷(NH3BH3)的特殊性质是二氢键理论的起源.与NH3BH3原子总数相等的等电子体是CH3CH3,其相对分子质量(30)与NH3BH3(31)相似,范德华力的大小接近,然而实验表明,CH3CH3的熔点是-181 ℃,而NH3BH3的熔点是+104 ℃,相差285 ℃.这说明在NH3BH3晶体中,分子间存在不寻常的强烈相互作用.为解释这种作用,化学家提出了二氢键的观点.
NH3BH3的结构可表示为H3N→BH3,由H3N提供孤电子对给缺电子的B 原子,形成了配位键.H3N—BH3分子中不再有孤电子对,也就不能形成常规的氢键.但由于电负性的差异,N—H 中的H 表现正电性,而B—H 中的H 表现负电性,因此存在着B—Hδ-…Hδ+—N 的电性作用,这就是二氢键(如图2).
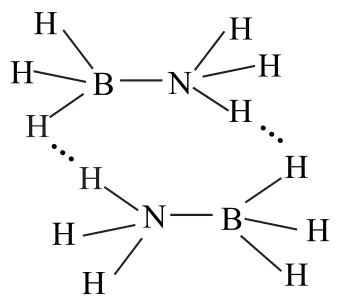
图2
二氢键可以表示为X—Hδ-…Hδ+—Y.显然,X应是电负性较小的原子,而Y 则是电负性比H 大的原子.现已在很多物质中发现了二氢键,甚至稀有气体的氢化物也能产生二氢键(如图3).
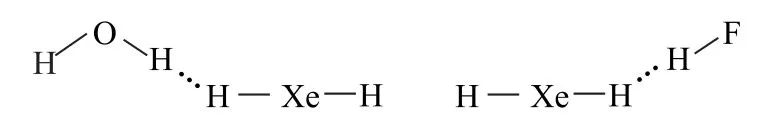
图3
3.2 芳香氢键
例2(2003年全国化学竞赛题)氯仿在苯中的溶解度明显比1,1,1-三氯乙烷的大,请解释原因.
分析苯环具有离域π 键体系,电荷密度较大,可以想象,如果Hδ+靠近π键的电子云时,两者必然产生电性作用.这种作用是离域π 键作为质子的接受体,称为芳香氢键(如图4).由于芳香氢键的存在,使得三氯甲烷与苯的结合力增强,溶解度变大.不仅是芳环上的离域π键,其他一些物质如乙炔中的碳碳三键由于电荷密度较高,也能与Hδ+产生类似的电性作用.这种类型的氢键可以统称为X—H…π型氢键.

图4
本题是化学竞赛中第一次考查非常规氢键,此后非常规氢键在各类竞赛题中多次出现,2020年则扩展到高考题中.这也体现了当前高考化学的走向——考查学科本质,并且与化学新课程追求基础性和时代性相统一的目标是相适应的.
3.3 金属氢键
一些过渡金属的原子由于价电子数较多,形成了富电子体系.研究发现,这些富电子的过渡金属原子也可以与正电性的H 原子产生电性作用.这种作用力与常规氢键类似,可用X—H…M 表示,只是用富电子的金属原子如Pt等代替了含有孤电子对的F、O、N等原子,因而被称为金属氢键.
3.4 单电子氢键
研究还发现,带有单电子的自由基也可以与卤化氢、水等形成氢键.这种氢键是自由基中的单电子作为质子受体,吸引分子中带正电的H 而形成的,因此称为单电子氢键.例如甲基自由基与Hδ+—F的氢键.单电子氢键也与常规氢键类似,只是将孤电子对与Hδ+的作用变为了单电子与Hδ+的作用,因此如果其他分子能够提供Hδ+,这种氢键就可以形成.例如乙炔分子中的碳原子是sp杂化,电负性较大,使得与之相连的H 原子正电性增强,也可以作为质子供体与甲基的单电子作用,形成单电子氢键(如图5).
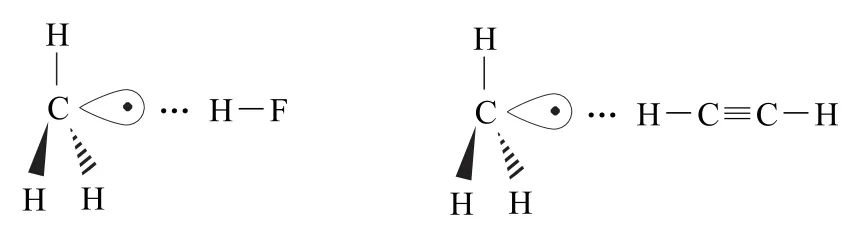
图5
4 氢键的新定义
随着对物质结构研究的深入,化学家将介于强相互作用的化学键和范德华力之间的各种键力统称为次级键,氢键就是最具代表性的次级键.新物质、新现象的层出不穷,各种各样的非常规氢键陆续被发现,使人们对氢键的认识不断深化,原有的X—H…Y 型概念已经无法满足表征各类氢键的要求.因此,IUPAC于2011年3月给出了有关氢键的最新定义.
该定义规定:氢键就是键合于一个分子或分子碎片X—H 上的H 原子与另一个原子或原子团之间的吸引力,有分子间氢键和分子内氢键之分,X—H 中X的电负性比H 原子强.氢键可表示为X—H…Y—Z,Y 可以是分子或离子,也可以是一个分子片段,可以与Z成键,但必须是富电子的(例如具有未成键电子对或者π键).
新定义表明,正常氢键与非常规氢键是统一的,其实质是正电性原子与负电性原子的作用.因此,我们不能局限于知识点的重复训练,应增进对化学本质的理解,提高化学核心素养,这也正是高考追求的目标.
(完)
