基于美国FAERS数据库的利那洛肽不良事件信号挖掘与分析
2022-08-08王浩阳丽刘小英陈力成都市新都区人民医院药剂科成都60500四川大学华西第二医院药学部成都6004四川大学华西第二医院循证药学中心成都6004出生缺陷与相关妇儿疾病教育部重点实验室成都6004
王浩,阳丽,刘小英,陈力(. 成都市新都区人民医院药剂科,成都 60500;2. 四川大学华西第二医院药学部,成都 6004;3. 四川大学华西第二医院循证药学中心,成都 6004;4. 出生缺陷与相关妇儿疾病教育部重点实验室,成都 6004)
肠易激综合征(IBS)是一种全球范围内常见的、以腹痛/腹胀或腹部不适为主要症状的功能性肠病,排便后症状多有改善,常伴有排便习惯(频率和/或性状)的改变[1]。若腹部症状+便秘反复不断,则很有可能是IBS 的一种主要亚型便秘型肠易激综合征(IBS-C)[2]。我国IBS 患病率为6.5%[1],其中IBS-C 占比达15.1%[3]。利那洛肽是一种鸟苷酸环化酶C 受体(GC-C)激动剂,它与肠道GC-C 结合后,一方面使细胞内和细胞外环磷酸鸟苷(cGMP)浓度升高,可刺激肠液分泌,加快胃肠道蠕动,从而增加排便频率;另一方面细胞外cGMP 浓度升高可降低痛觉神经信号传导,缓解腹痛症状[4-5]。2013年2月,利那洛肽在美国获批准上市,用于IBS-C 和慢性特发性便秘患者的治疗。作为全球首个获批用于便秘治疗的鸟苷酸环化酶C 激动剂,它的上市填补了IBS-C 患者仅能选择症状改善类药物而无针对性治疗药物的空白。2019年1月 15日国家药品监督管理局(NMPA)批准该药正式在中国上市。作为我国专门治疗成人IBS-C 的处方药物,将填补我国成人IBS-C 治疗的空白,为广大国内患者带来福音。随着利那洛肽的广泛使用,真实世界的药物不良事件(ADE)报告也逐渐增多。本文通过对美国FDA ADE 报告系统(FAERS)收集到的数据进行挖掘和筛选,分析利那洛肽可疑的ADE 信号,以期为国内临床安全合理用药提供参考。
1 资料与方法
1.1 数据来源
选取FAERS 数据库中2016年第一季度至2021年第二季度共22 个季度的数据,用MySQL进行分析,去重处理后得到首要怀疑药物为利那洛肽的ADE 报告。
1.2 数据筛选
以利那洛肽的通用名“Linaclotide”和商品名“LINZESS”为关键检索词在数据库中进行检索,得到包括人员信息、药物信息、ADE 和原发疾病等数据资料,删除重复和存疑数据,形成研究ADE 的原始数据。
1.3 数据处理
采用《国际医学用语词典》 MedDRA 23.0 更新版(MedDRA)中药物不良反应(ADR)术语集的首选系统器官分类(SOC)和首选术语(PT)对ADE 进行分类和表达,并完成相应的中英文映射。
1.4 数据分析
选用在ADE 监测中广泛应用的比值失衡测量法中的报告比值比法(ROR)[6]和综合标准法(MHRA)[7]分别计算ROR 值和比例报告比值(PRR),筛选潜在信号(见表1、2)。目标药物相关风险信号的检测阈值设定为ROR 中95%的可信区间(95%CI)下限大于1 且报告数不少于3 例,以及MHRA 中PRR ≥2、χ2≥4 且报告数不少于3 例[8]。
1.5 严重ADE
严重ADE 系指使用药物引起下列情况之一:导致死亡;危及生命;致畸、致癌、致缺陷;导致显著或永久的人体伤残或器官功能损伤;导致住院或住院时间延长;导致其他重要医学事件,如不进展治疗可能出现上述情况(如成瘾性)。
2 结果
2.1 ADE 报告的基本情况
2016年第一季度至2021年第二季度的ADE背景信号共22 137 402 个,其中经删除重复数据后得到首要怀疑药物为利那洛肽的ADE 报告共16 730 份,报告数1088 个。在6560 例患者的报告中,可发现女性占大多数(61.20%),患者主要为18 岁及以上人群(34.59%),而美国是报告数最多的国家(94.38%),2016 至2020年每年报告数差距不大,具体报告基本信息见表1。

表1 利那洛肽相关ADE 报告基本信息Tab 1 Basic information of linaclotide ADE reports
2.2 不良反应信号分析结果
对利那洛肽为首要怀疑药品的ADE 信号进行筛选,经ROR 法和MHRA 法筛选后最终获得的利那洛肽ADE 信号数为102 个,报告总计数为11 623 份,经删除存疑信号后,得到ADE 相关信号75 个,报告总计数为7577 份。在有信号的PT 中,以报告数排序的前50 位如表2所示。其中,较为常见的未在说明书中提及的ADE 为腹泻(1943 例)、腹胀(434 例)、腹痛等(318 例)等。
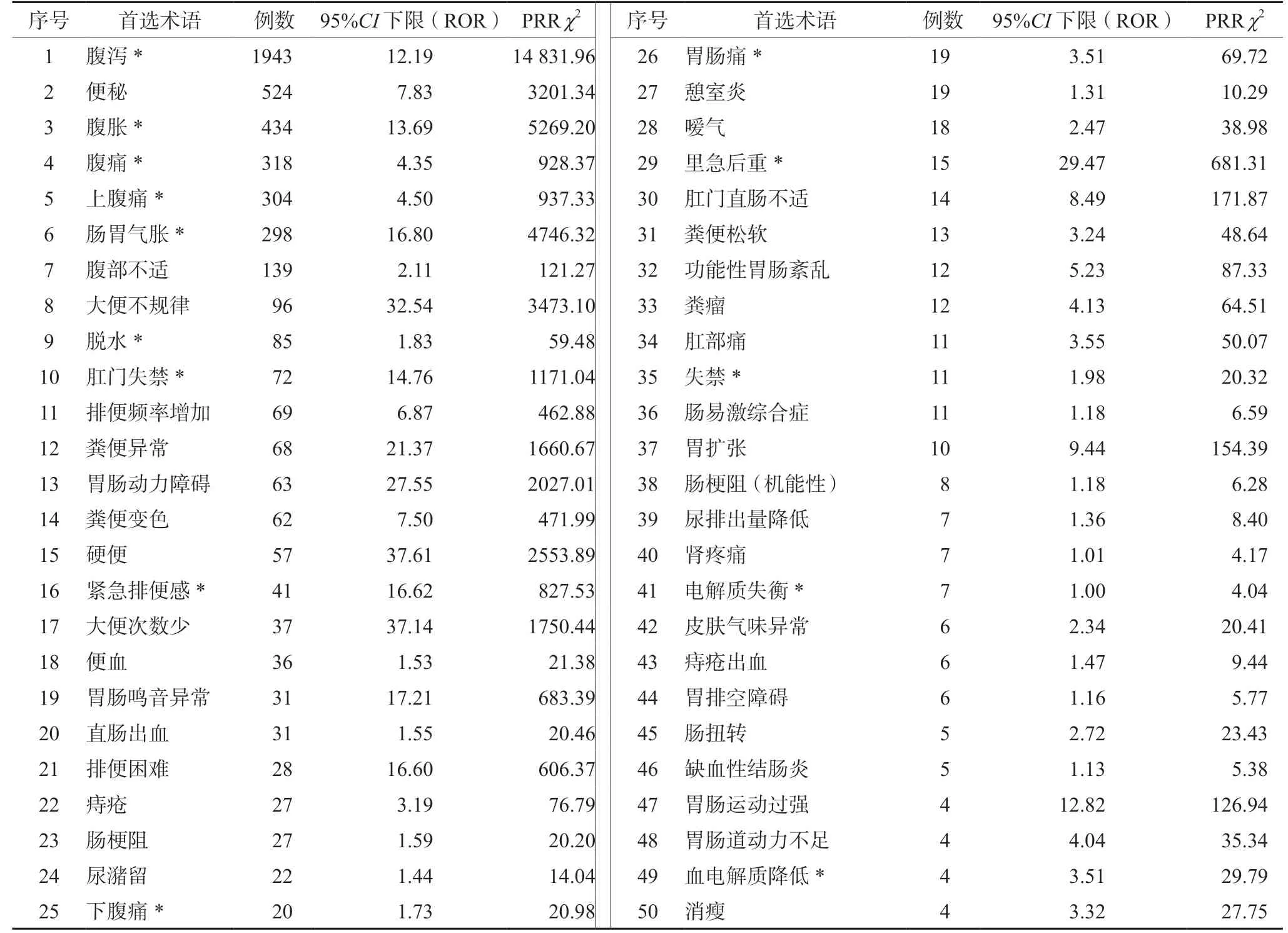
表2 利那洛肽报告数排名前50 位的ADE 信号Tab 2 Top 50 ADE signals of linaclotide in descending order of reports
2.3 SOC 分类ADE 报告及信号分类
根据MedDRA 对有信号的PT 进行SOC 分类排序,可发现有信号的SOC 11 个,具体见图1。其中,胃肠系统疾病(64.99%)、全身性疾病及给药部位各种反应(32.04%)的报告例数相对较多。
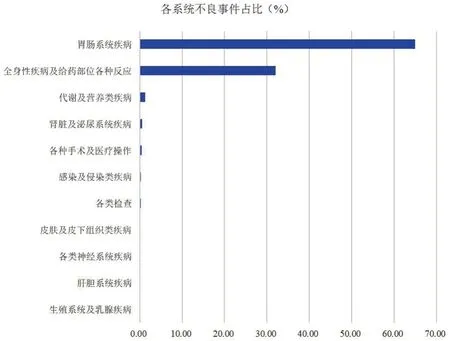
图1 各SOC 项下不良事件信号的报告例数占比Fig 1 Percentage of ADE signal detection of each SOC
2.4 严重的ADE
严重的 ADE 主要体现在胃肠系统和肾脏及泌尿系统两大类。其中在胃肠系统主要表现为肛门失禁、便血、直肠出血、肠梗阻等,而在肾脏及泌尿系统疾病主要表现为尿潴留、失禁等(见表3)。
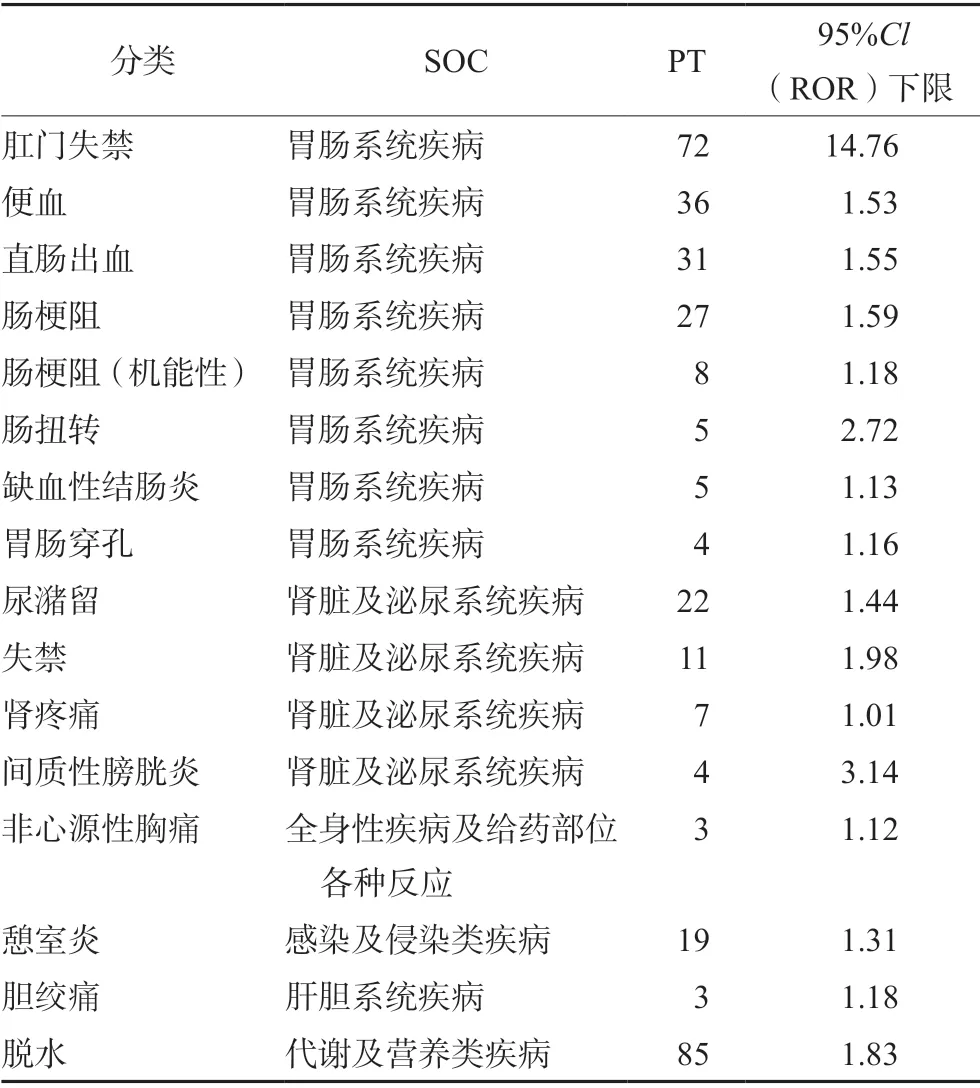
表3 严重的 ADE 信号Tab 3 Severe ADE signal
3 讨论
通过ROR 法和MHRA 法挖掘到的ADE 信号与利那洛肽说明书记录及用药警示信息基本一致,主要表现为胃肠系统疾病、全身性疾病及给药部位各种反应。
3.1 常见的ADE 信号
一项关于利那洛肽治疗IBS-C 的meta 分析发现利那洛肽的主要不良反应为胃肠道反应,以腹痛、腹泻较为常见[9]。结合表2和图1可发现,胃肠系统疾病这一SOC 的ADE 报告数占比最高,主要信号包括腹泻、腹胀、腹痛等。在慢性便秘患者的两项大型Ⅲ期试验中,最常见和剂量相关的ADE 是腹泻,导致两个利那洛肽治疗组中 4% 的患者停止治疗[10]。一项利那洛肽在对合并便秘的IBS 患者的Ⅱb 期研究中发现有至少3%的利那洛肽使用者发生了腹泻,且腹泻发生率跟剂量成正相关,大多数为轻度或中度,也有部分患者出现较为严重的腹泻,从第一次服用研究药物到首次出现腹泻的中位天数为4 d[11],可能与利那洛肽主要作用于胃肠道有关,提示临床使用过程中如果发生持续(如超过1 周)或重度腹泻,应考虑暂停利那洛肽直至腹泻缓解,同时因持续性或严重腹泻可能导致水、电解质紊乱,对有水、电解质紊乱倾向及耐受性差的患者(如老年人、心血管疾病患者、糖尿病和高血压)应谨慎使用。一项为期12 周的临床随机对照试验发现,有7 例接受利那洛肽的患者在治疗结束时血清碳酸氢盐水平低于正常下限,但这些患者均未报告腹泻为或其他被认为与低碳酸氢盐水平有关的不良反应[12],提示利那洛肽使用者虽未出现腹泻但依然有酸碱失衡的风险。对于上述情况,应考虑检查电解质及酸碱平衡。除说明书记载的常见胃肠道不良反应,此次研究还检测到粪便变色、胃肠鸣音异常、肠梗阻、便血、肠扭转、胃肠穿孔等少见的胃肠道ADE 信号,提示在治疗过程中发生此类疾病需考虑是否具有相关性,在存在高危因素尤其有肠梗阻的患者应避免使用。而仅次于胃肠系统疾病的全身性疾病及给药部位反应,主要信号包括药物无效、对非适应证用药无效、治疗反应减弱,提示临床在使用过程中注意观察药品效应,出现上述情况应考虑重新调整用药方案。
3.2 其他少见的ADE 信号
虽然在安全性上,利那洛肽几乎不进入血液循环,与其他药物基本无相互作用[13],但在本次研究中发现尚有少量非胃肠系统的新的 ADE 信号的报告,主要包括尿排出量降低、肾疼痛、皮肤气味异常等,具体原理和机制尚不明确。说明书中病毒性胃肠炎、头晕、头痛是常见的ADE,但在本次研究前50 位中却未被发现,此处与说明书提示存在差异,临床需注意。
3.3 严重的ADE 信号
通过表3可以发现利那洛肽严重ADE 信号中肛门失禁、脱水较其他严重ADE 信号计数多,可能是因腹泻是利那洛肽常见的ADE,严重腹泻及腹泻持续时间较长时容易导致患者肛门失禁、脱水,且肛门失禁信号强度较大,提示于药物使用的相关性较强。此外,其他严重ADE 虽然发生较少但可能会导致患者住院或危及生命,提示在使用过程中应密切监测,出现以上严重 ADE时应立即停药,并做相应处理。
3.4 小结
即使有如此大样本的数据,本研究仍存在一定的局限性。首先,由于FAERS 是自发呈报系统,存在漏报、错报等情况;其次,尽管ROR 法和MHRA 法两种方法同时使用,但仍不能完全排除假阳性信号的出现;另外,在使用MedDRA术语集时,使用比PT 更高级别的术语可能出现统计上不同的结果[14];最后,定量信号检测方法产生的ADE 信号是基于报告的数量关联而非生物学关联[15]。综上,本研究无法精确定义利那洛肽的ADE 真实发生率,最终结果仍需进一步的研究证实。
4 结论
基于美国 FAERS 数据库,利用ROR 法和MHRA 法对利那洛肽上市后的ADE 进行分析,挖掘出更加真实完整的药品安全信息,发现了如便秘、大便不规律、胃肠动力障碍、粪便变色、硬便、便血、胃肠鸣音异常、直肠出血、肠梗阻、尿潴留、憩室炎、嗳气、胃扩张、尿排出量降低、肾疼痛、皮肤气味异常等新的ADE,同时还观察到利那洛肽在胃肠系统、全身性疾病及给药部位各种反应方面的ADE 相对较多,这在一定程度上弥补了药品上市前临床试验的不足,可为临床合理用药提供参考。当然,利那洛肽的ADE 还需在真实世界中不断地被探索和研究,以更好地为患者的生命健康保驾护航。
