离子液体催化热解纤维素制备左旋葡萄糖酮的研究
2022-08-01徐安邦冉景煜唐广川杨仲卿秦昌雷曹景沛
徐安邦 ,黄 鑫,* ,冉景煜 ,唐广川 ,杨仲卿 ,秦昌雷 ,曹景沛
(1. 重庆大学 低品位能源利用技术及系统教育部重点实验室, 重庆400044;2. 中国矿业大学 煤炭深加工与洁净利用教育部重点实验室, 江苏 徐州 221116)
生物质是世界上储量最丰富的有机碳资源[1],其作为化石资源的潜在替代品在生产液体燃料和精细化学品等方面引起了广泛的关注[2,3]。目前,生物质热化学转化技术主要包括燃烧、气化、液化、水解和热解等[4-6]。其中,热解因其简单的工艺流程和所得生物油中含有多种化学品而受到学者的广泛研究[7]。左旋葡萄糖酮(levoglucosenone,LGO),是来源于纤维素催化热解的主要产物之一,是一种高附加值的平台化合物。由于LGO独特的化学结构,它被认为是一种极具潜力的手性合成原料,在燃料、药物中间体和高分子材料等方面表现出了独特的优势[4-7],但LGO并未规模化生产,产量有限,这极大限制了LGO的应用。
在纤维素或生物质的常规热解过程中,LGO的产率很低。研究人员发现,当在热解过程中引入合适的酸催化剂,能够选择性地促进LGO 的生成。文献[8,9]表明,在极性溶剂(四氢呋喃、γ-戊内酯和二甲亚砜)中,热解纤维素可以得到较高产率的LGO,这些极性溶剂可稳定纤维素的羟基,抑制初次热解产物中左旋葡萄糖(LGA)的再聚合,并且在无机酸(硫酸或磷酸)的作用下促使LGA脱水转化生成LGO。在用硫酸作为催化剂,四氢呋喃为溶剂条件下,纤维素在210 ℃热解时LGO产率达到最大值,约为51%[9]。此外在四氢呋喃溶剂中,LGA也可在丙基磺酸酸化过的二氧化硅上进行脱水作用生成LGO,其最优选择性为59%,但是该固体酸稳定性较差,在反应过程中因吸附产生的水而快速失活[10]。澳大利亚CIRCA公司[11]使用环丁砜为溶剂磷酸为催化剂将生物质样品进行热解可以得到大约6%的LGO收率,但是由于环丁砜和LGO的沸点接近,分离提纯困难,同时涉及到使用高浓度的磷酸,造成设备投资大能耗高。相对于直接对纤维素进行热解,用无机酸预处理过的纤维素作为原料对其热解也可以有效的提高LGO的产率。Dobele等[12,13]研究了磷酸负载和磷酸预处理纤维素的热解规律,考察了热解参数如磷酸浓度和热解温度对LGO生产的影响,表明高磷酸浓度和较高热解温度有利于LGO的生成。将无机酸替换成无机酸的盐类化合物也可在一定程度上获得更高的LGO产率,Zhang等[14]指出,在相同的条件下硫酸铁盐比硫酸或者磷酸催化纤维素热解可获得更高产率的LGO。
固体酸催化剂也可有效地促进纤维素在氮气气氛下热解生成LGO。不同的固体酸对LGO呈现出了不同的选择性,效果较好的是用硫酸或者磷酸浸泡过的金属氧化物或者活性炭[15-18]。陆强等[19,20]研究表明,用固体超强酸等和纤维素机械混合后进行热解,固体酸可以有效的降低纤维素热解温度,极大促进LGA脱水生成LGO。他们还将不同比例的磷酸活化过的活性炭催化剂和纤维素机械混合,将混合物分别进行Py-GC/MS和小型实验室固定床热解实验,研究发现,在热解温度为300 ℃,催化剂和纤维素混合比为1∶3时,可以得到LGO的最大产率分别为18.1%和14.7%[15]。
此外,离子液体催化剂也可以有效的促进纤维素热解转化为LGO。Kudo等[21-24]研究了不同类型的离子液体对纤维素催化热解制备LGO的影响。结果表明,阴离子的类型对催化作用有显著影响,含磺酸根阴离子的离子液体可以显著提高LGO的产率。离子液体在选择性地促使糖苷键断裂形成LGO的同时也降低了反应温度,并且抑制了结焦。但由于离子液体是阴阳离子共同组成的,阳离子对离子液体的性能也可能有着重要的影响。Sun等[25]研究发现,1-烷基-3-甲基咪唑氯盐型离子液体中,当烷基侧链碳原子数为奇数时,离子液体几乎不能溶解纤维素;然而当碳原子数为偶数时,溶解纤维素能力却很强,这说明阳离子对于纤维素的转化过程也有非常重要的影响。
因此,本研究着重考察了1-烷基-2,3-二甲基三氟甲烷磺酸咪唑离子液体的阳离子侧链官能团(丁基、辛基、十二烷基和十六烷基)对纤维素催化热解制备LGO的影响因素,并通过密度泛函理论(DFT)对LGO生成的最佳路径进行计算。纤维素热解后产生的焦炭也被用于比表面积和孔容分析。
1 实验部分
1.1 材料
本研究所用到的化学品均为分析纯样品。纤维素和LGO购买于Sigma-Aldrich公司,LGA购买于Carbosynth公司,甲醇购买于Aladdin公司,1-丁基-2,3-二甲基三氟甲烷磺酸咪唑、1-辛基-2,3-二甲基三氟甲烷磺酸咪唑、1-十二烷基-2,3-二甲基三氟甲烷磺酸咪唑和1-十六烷基-2,3-二甲基三氟甲烷磺酸咪唑离子液体购买于上海成捷化学有限公司,为方便表述,分别简写为丁基(Butyl)、辛基(Octyl)、十二烷基(Dodecyl)和十六烷基(Cetyl)。
1.2 实验方法
纤维素快速热解装置如文献[26]所示,该热解反应器是具有高加热速率的下坠床石英管式反应器。首先将纤维素和离子液体以质量比1∶1混合后装入进样瓶中,然后用管式炉将通有N2(200 mL/min)保护的石英管加热到设定温度,以0.1 g/min的进料速率将样品加入石英管中。进料完成后,在设定温度保持10 min,直到无明显热解气体析出。热解产生的挥发分通过冷阱收集,热解气在经过气溶胶滤筒过滤后用气袋收集。实验完成后,用甲醇洗涤冷阱收集的生物油样品,收集后进行GC和GC/MS定性及定量分析。热解后的离子液体和焦炭的混合物放入过量甲醇溶液中使离子液体溶解,充分搅拌后过滤分离离子液体甲醇溶液和焦炭,将甲醇蒸发以及在110 ℃过夜干燥后称量即得到离子液体的回收率和焦炭的产率。
1.3 分析方法
离子液体的热重分析实验在瑞士梅特勒-托利多ESI-0910型同步热分析仪进行。实验条件为:10 mg离子液体,Ar气氛,流量50 mL/min。初始温度为室温,然后升温到105 ℃保持10 min,最后升温到700 ℃,升温速率为10 ℃/min。热解产生的生物油通过GC、GC/MS和FT-IR进行分析, GC/MS配备安捷伦HP-5MS 色谱柱(cross-link 5% PH ME siloxane, 30 m ×0.25 mm × 0.25 μm)。升温程序为初温 60 ℃,停留5 min,以 5 ℃/min 升至 250 ℃,保持 10 min。用面积内标法对LGA和LGO进行定量分析,内标物为二乙二醇二甲醚,生物油中其他化合物的定量分析是根据LGA或者LGO为基础进行计算的。LGO和LGA的产率以纤维素中碳元素为基准表示(%-C)。FT-IR分析是采用赛默飞Nicout iS5型红外光谱仪,以KBr压片, 分辨率40 cm-1,累积扫描32次,测量为4000-400 cm-1。对焦炭进行比表面积和表面形貌分析。比表面积测定采用北京金埃谱生产的V-4800TP 型比表面积测定仪,在液氮(77 K) 条件下测定样品的N2吸附-脱附等温曲线并用BET方法得到比表面积曲线。利用蔡司GeminiSEM 500场发射扫描电子显微镜 (SEM) 对热解后焦炭的表面形貌进行表征。
1.4 DFT计算
采用Gaussian 09W 程序包,使用B3LYP-D3(BJ)泛函和6-311G(d, p)基组[27,28],对离子液体的静电势面以及LGA转化为LGO反应路径中的反应物、中间体、过渡态以及产物进行几何结构优化和频率计算。通过频率计算确定反应物、中间体和产物无虚频,过渡态有唯一虚频。随后进行内禀反应坐标(IRC)计算进一步确定过渡态的正确性。离子液体阴阳离子间的相互作用能采用Counterpoise方法计算。
2 结果与讨论
2.1 离子液体电荷和热重分析
离子液体的结构和静电势面如图1所示。正电荷集中在咪唑环,负电荷集中在氧周围,较短侧链的电荷受到咪唑环的影响而呈现微弱的正电荷,较长侧链则呈现电中性。通过Counterpoise方法计算出丁基、辛基、十二烷基和十六烷基离子液体阴阳离子间的相互作用能分别是-361.2、-359.1、-358.6和-358.5 kJ/mol。随着烷基侧链长度增加,阴阳离子间的相互作用能逐渐减弱,表明侧链增加使离子液体扩散增强。
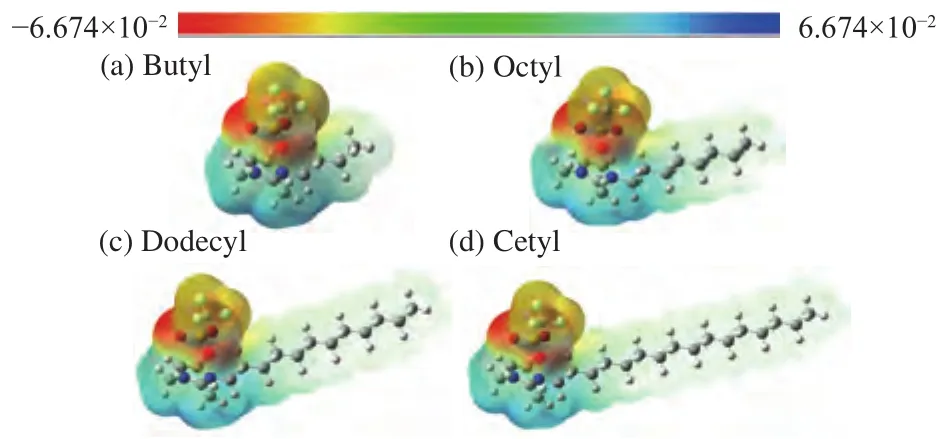
图1 1-烷基-2,3-二甲基三氟甲烷磺酸咪唑Figure 1 1-Alkyl-2,3-dimethylimidazolium triflate
图2描述了四种离子液体在加热速率为10 ℃/min的热重分析结果。结果表明,四种离子液体表现出了相同的热失重规律,从DTG质量损失速率来看,四种离子液体的分解主要发生在370-470 ℃,此时离子液体的损失率高于90%,主要原因是高温破坏了离子液体的化学键,导致其分解。在温度低于350 ℃时,离子液体几乎不发生分解,此时离子液体损失率低于2%。在四种离子液体中,丁基离子液体具有最好的稳定性。考虑到离子液体在温度高于350 ℃后会受热分解,本实验所采用的热解温度为300和350 ℃。
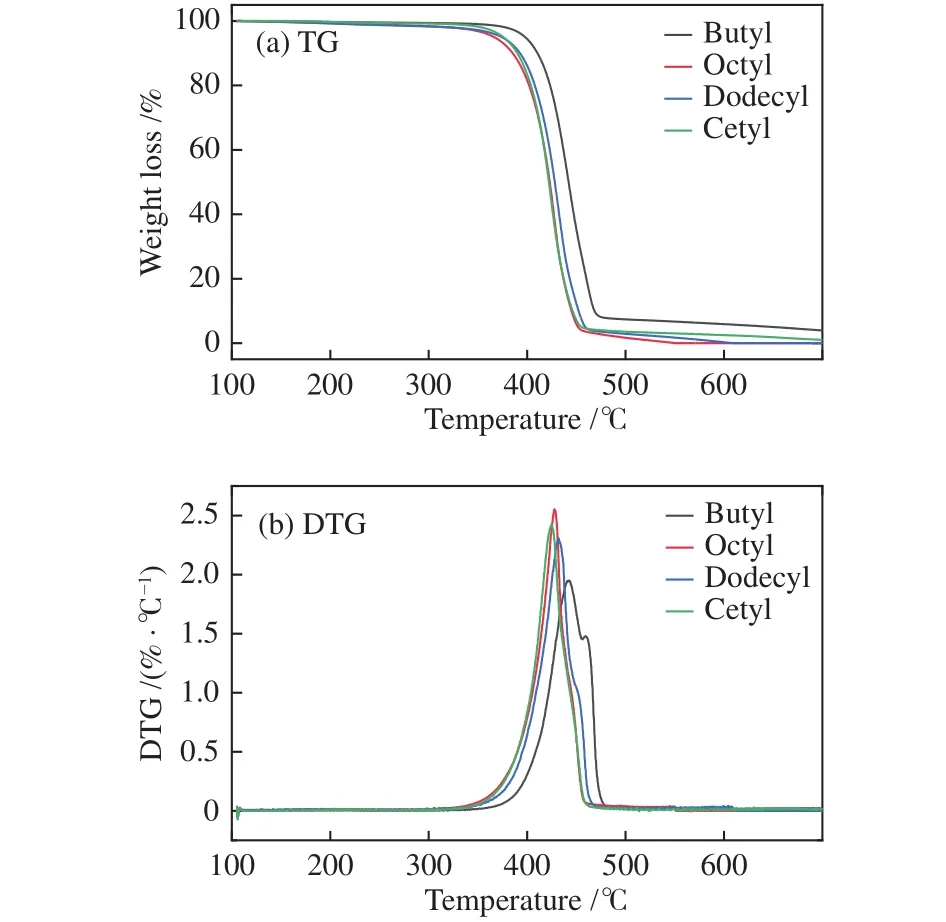
图2 离子液体的热重分析Figure 2 Thermogravimetric analysis of the ionic liquids
2.2 热解产物分析
离子液体催化纤维素热解得到的气、液、固三相产物质量平衡如图3所示。其质量平衡均在90%以上,表明了实验的准确性。对比非催化实验结果表明,离子液体催化剂可以对结焦和焦炭产生显著影响。非催化热解的结焦产率在300 ℃时达到18.2%,而在加入离子液体之后,结焦的产率明显降低,尤其是丁基催化热解产物中结焦产率仅有1.4%。因此,离子液体的作用下可有效减少热解过程中大分子产物的生成。在温度升高至350 ℃后,丁基的生物油产率由31.1%提高至34.3%,十二烷基生物油则由31.4%提高至47.9%。生物油产率随着温度的升高而有较大提高,主要原因是温度升高有利于纤维素中挥发分的析出;另一方面,离子液体在高温下可以被分解为小分子物质,进而被收集在生物油中,这一现象随着离子液体烷基侧链的增长而增强。相比于非催化热解,催化热解的焦炭产率普遍较高,这是因为离子液体烷基侧链导致的[29,30],较强的电荷作用促使纤维素分子产生聚集,较长的烷基侧链导致阳离子的聚集加强和阴离子的扩散减弱,由于离子液体侧链的聚集作用会进一步促使纤维素分子产生聚集,这种聚集不利于热解产物的析出,还会促进一次热解产物发生二次反应生成焦炭。在300 ℃时,最高焦炭产率为十二烷基的14.1%。当温度提高至350 ℃后,最高焦炭产率为丁基的13.1%,而十二烷基的焦炭产率下降至10%。原因是温度的升高有利于纤维素充分热解,加速挥发分析出,同时减少挥发分的二次聚合反应,减少了焦炭的生成。

图3 热解产物产率分析Figure 3 Analysis of pyrolysis product yields
热解产生的气体成分分析如图4所示。由图4可知,纤维素的非催化热解产物主要是H2,以及少量的CO2和CO。这是因为纤维素中有丰富的氢键,热解会首先使纤维素分子中的氢键断裂,然后是碳氧键断裂或重排生成CO2和CO。在加入离子液体后,纤维素催化热解的气体产物主要是CO2和CO,以及少量H2这说明离子液体的加入促进了纤维素的碳氧键断裂和重排反应。随着温度的升高,气体产物中CO2和CO产率升高,并且出现了还原性气体CH4,这表明温度升高有助于挥发分二次反应生成小分子物质[31]。由此可以看出,离子液体的催化作用促使纤维素分子中的羟基转化和不稳定双键的脱除以及酸类物质的脱羰反应生成CO2和CO[32]。四种离子液体热解气体产物中CO2和CO并没有明显差距,说明离子液体烷基侧链对CO2和CO的生成作用不强。图4表明,丁基离子液体有着最高的CH4产率,这说明丁基离子液体会更好的促进纤维素中C-C键断裂生成小分子物质。
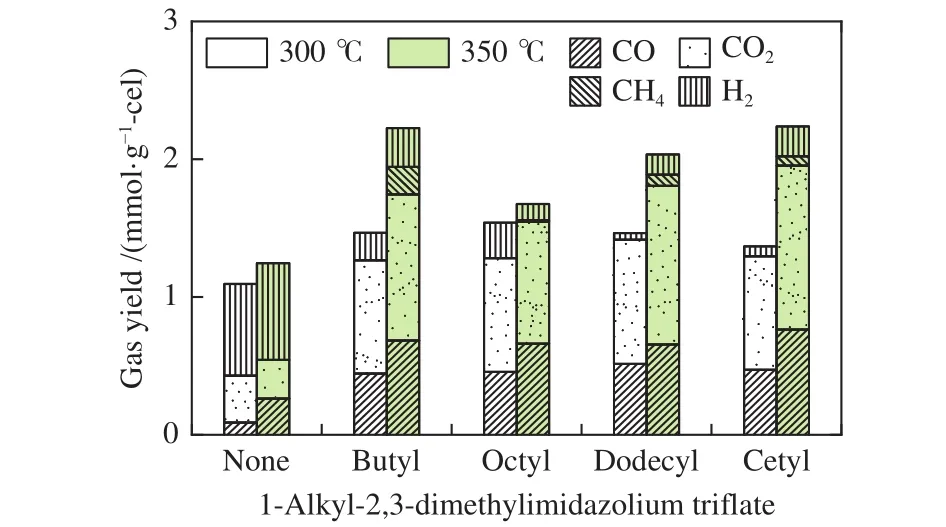
图4 气体产物组成分析Figure 4 Analysis of gas composition
2.3 LGA和LGO产率分析
将纤维素和离子液体以1∶1混合后在300和350 ℃热解,考察丁基、辛基、十二烷基和十六烷基四种离子液体对LGA和LGO产率的影响规律,其结果如图5所示。在非催化热解所得生物油中主要成分是LGA,随着热解温度从300 ℃提高到350 ℃,LGA的碳产率从21.1%-C增加到28.4%-C,其原因是纤维素在较高温度下热解反应更加充分,这和纤维素直接热解的热重分析曲线一致。
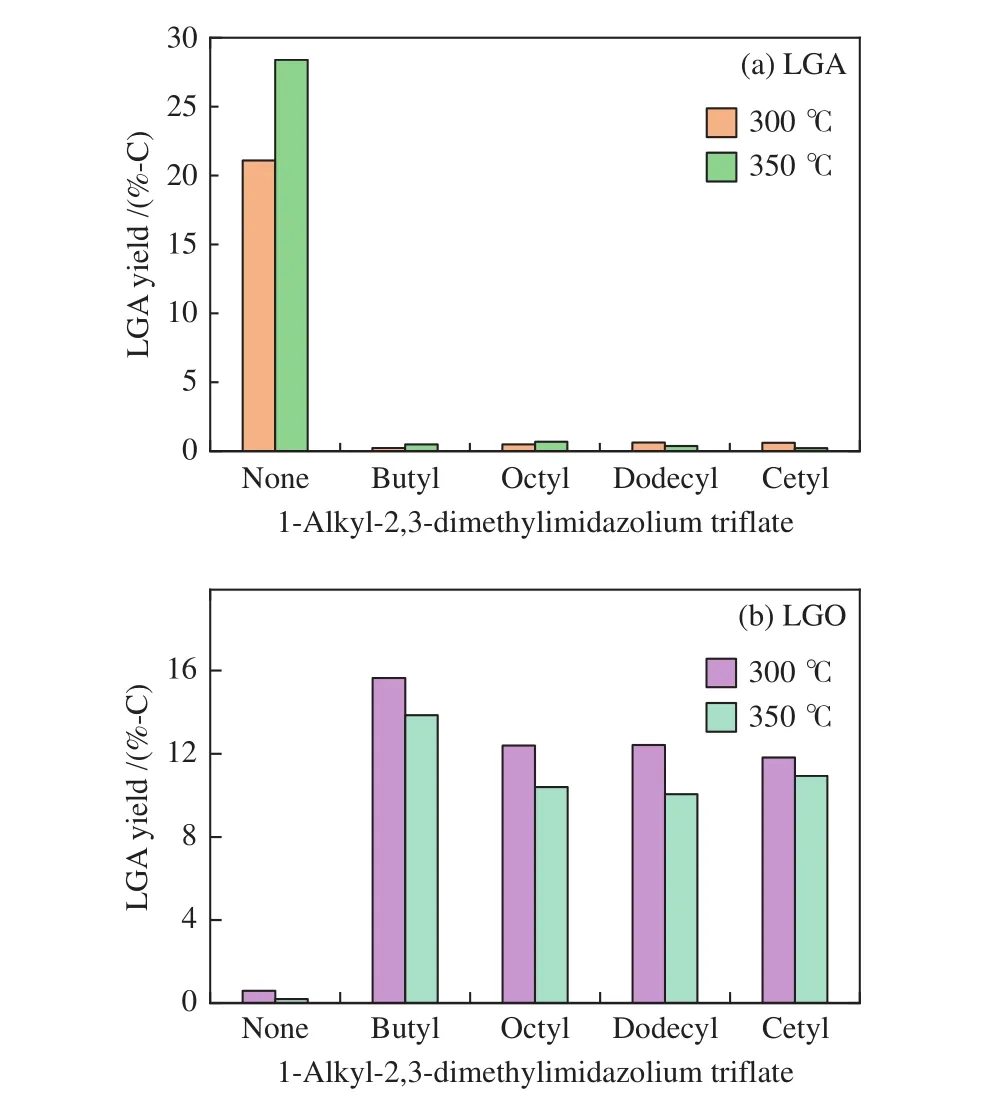
图5 离子液体对LGA和LGO的产率影响Figure 5 Influence of the ionic liquids on the yields of LGA and LGO
在加入离子液体催化剂后,生物油的主要成分变为LGO,其产率为10.1%-15.6%-C,表明这四种离子液体催化剂都可以很好地促进纤维素热解转化为LGO。Wang等[30]研究结果表明,较长的烷基侧链会显著增强阳离子的聚集而减弱阴离子的扩散。在四种离子液体中,丁基离子液体的侧链长度最短,有利于阴离子的扩散,使丁基离子液体与纤维素接触更充分,从而获得最高产率的LGO。值得注意的是,LGA是LGO的前驱体,在非催化条件下,LGA的产率明显高于LGO的产率,而催化热解的LGO最大选择性为54.9%,说明在离子液体的催化作用下,LGA将不仅转化为LGO,还会转化为其他形式的化学品。
2.4 生物油分析
热解后生物油的FT-IR分析如图6所示。由图6可知,纤维素催化热解所得生物油都有着相似的吸收特征峰,表明生物油中含有类似的官能团组成。在3400 cm-1附近的吸收峰很强且宽,是由有机酸和醇类的O-H的氢键伸缩振动形成的[33]。在2780和3000 cm-1附近的吸收峰对应醛类化合物中的C-H振动。在1500-1800 cm-1出现强吸收峰,这对应于C=O伸缩振动的灵活性,表明生物油中存在羧酸、酮和醛类化合物。在1135、1080和 1040 cm-1处的伸缩振动可以分别归因于伯醇和仲醇的C-O-C糖苷键拉伸、C-O-C环骨架振动和C-O-H 拉伸[33,34]。此外,通过FT-IR还可以观察到两种重要的化学物质:LGA的特征吸收峰为2900和930-1170 cm-1,LGO的特征吸收峰为2976和1700 cm-1。根据吸收峰的强度判断,无催化剂条件下C = O的伸缩振动较弱,说明生物油中几乎不含LGO,而加入离子液体催化剂后,C = O的伸缩振动明显增强,表明了LGO的存在,这一结论和GC/MS的分析结果呈现出了良好一致性。
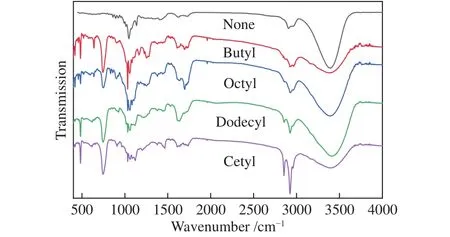
图6 生物油的FT-IR谱图Figure 6 FT-IR analysis of the bio-oils
除了LGA和LGO外,生物油中还有大量其他化合物,采用GC/MS对其进行定性和定量分析,得到的总离子流如图7所示,其具体组成见表1。从图7中可以看出,纤维素非催化热解后主要生成LGA (峰14);在离子液体的作用下,LGA峰几乎全部消失,然而LGO的峰强度(峰8)显著增强,说明了离子液体具有良好的催化效果。此外,在离子液体的作用下,糠醛、5-甲基糠醛、3-甲基环戊-2-烯酮和LAC的产率都在一定程度上提高,结合2.3中LGO最大选择性(54.9%),说明离子液体也可促使LGA转化为这些化合物。值得注意的是,加入离子液体后并未检测到AGF,说明AGF在离子液体作用下较容易转化,其转化的产物可能是LGO,也可能是一些其他小分子的化合物,需要值得更加深入的研究。此外,DH来自于LGO和热解产生的水反应,文献表明,该反应在低温下即可进行。Krishna等[35]研究了LGO和水反应生成DH的影响因素。结果表明,该反应在125 ℃可以很快的促进DH生成。然而,在350 ℃并未检测到DH,是由于LGO在高温下的热不稳定性造成的。

图7 生物油总离子流图Figure 7 Total ion chromatogram of the bio-oils

表1 GC/MS检测到的化合物的定量分析(mg/g-纤维素)Table 1 Quantitative analysis of compounds detected by GC/MS (mg/g-cellulose)
2.5 焦炭分析
选取300 ℃离子液体和纤维素混合热解后的焦炭进行N2吸附-脱附分析,结果如图8所示,焦炭的比表面积、孔容和平均直径见表2。丁基和辛基得到的焦炭的吸附-脱附曲线对应吸附类型I曲线,表明这两种焦炭的比表面积较高,分别为389.4和281.2 m2/g。十二烷基和十六烷基得到的焦炭的吸附-脱附曲线对应吸附类型II曲线,说明这两种焦炭拥有较小的比表面积和不含微孔。
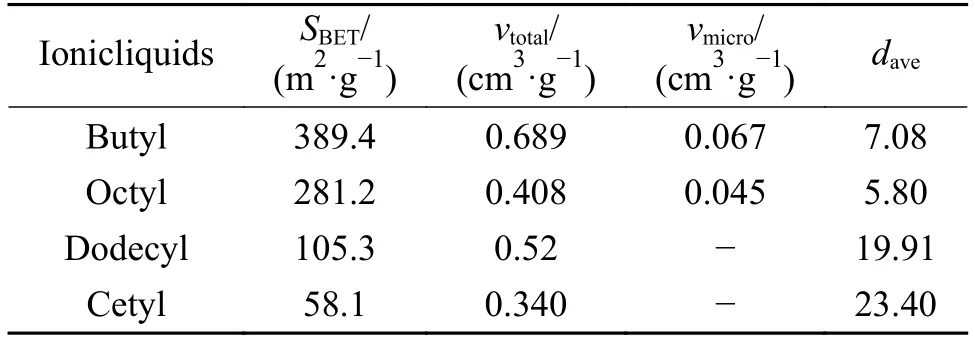
表2 焦炭的比表面积、孔容和平均直径Table 2 Analysis of the specific surface area,pore volume and average diameter of char
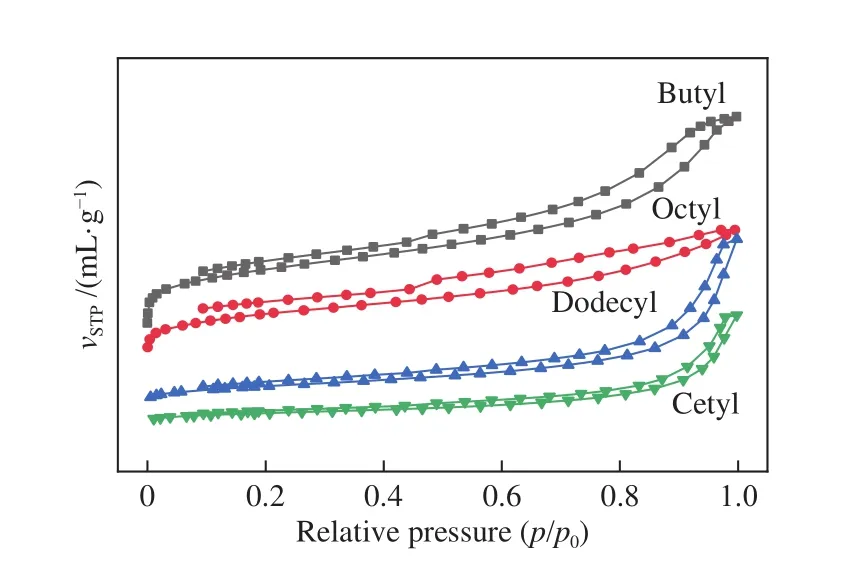
图8 N2吸附-脱附等温曲线Figure 8 N2 adsorption-desorption curves
从表2可以看出,丁基离子液体催化纤维素热解后所得焦炭具有较大的总孔容,最高可达0.689 cm3/g,然而微孔含量却很低,说明纤维素在离子液体作用下热解后得到的焦炭主要拥有中孔或者大孔结构。原因是更长的烷基侧链会使阴离子的扩散减弱[29,30],也可能是由于较长的烷基侧链因空间位阻使离子液体形成不均一的有机基团造成的。丁基离子液体的烷基侧链长度最短,不会形成较大的基团,因此,其生成的焦炭有更高的比表面积和孔容。在热解过程中,纤维素会聚集在离子液体基团表面,由于烷基侧链的聚集作用使空间位阻增加导致离子不能更好的进入纤维素内部,不利于微孔的形成。十六烷基等离子液体因较长的烷基侧链会使电荷密度升高,束缚较多的阴离子而形成的较大基团,使得到的焦炭的孔径更大。
丁基和十六烷基的焦炭的SEM分析见图9。由图9可知,焦炭的表面有大量的凹槽且孔道的结构比较稀疏,呈现出蜂窝状的蓬松样貌,表明焦炭中含有大量的孔结构,这与N2吸附-脱附的表征结果一致。

图9 焦炭的SEM分析Figure 9 SEM analysis of the chars
2.6 离子液体回收
在300 和350 ℃两种温度条件下进行热解实验后的离子液体回收数据如图10所示。由图10可知,离子液体的回收率随着侧链长度的增加而下降,说明侧链长度对离子液体稳定性有较大的影响。当实验温度提高至350 ℃时,离子液体的回收率有着较大的下降。十六烷基离子液体在350 ℃实验后仅有80.2%的回收率,低于丁基离子液体的95.9%。这说明离子液体的侧链在高温下会分解转化,使离子液体的回收率下降。

图10 离子液体回收率Figure 10 Recovery rate of the ionic liquid
由图5可知,丁基离子液体对催化热解纤维素制备LGO的效果最好。因此,选取丁基离子液体进行多次回收实验以探究回收离子液体对LGO产率的影响,其结果如图11所示。在350 ℃下,丁基离子液体在三次回收后,LGO的产率从13.8%-C轻微下降到12.5%-C,回收率从95.9%下降到67.5%,而生物油的产率在三次回收实验中从73.2%增加到85.8%,说明离子液体在经过多次实验后更容易分解,但总体来说离子液体催化效果保持稳定。

图11 离子液体回收利用对LGO产率的影响Figure 11 Effect of repeated use of the ionic liquid on LGO yield
2.7 机理分析
为深入了解LGA向LGO的转化过程,对LGA向LGO转化的路径进行了预测[36],如图12所示。通过DFT计算得出其能垒图,如图13所示。路径3中第一次脱水的能垒254.1 kJ/mol低于路径1和2中第一次脱水的能垒271.5 kJ/mol,表明外侧的羟基更容易脱水。路径1的第二步脱水反应是在烯醇结构转化成羰基之后进行的,降低了反应难度,此时反应能垒为232.5 kJ/mol。路径2和路径3的第二步脱水反应的能垒分别为301.8和346.0 kJ/mol,这表明路径2和路径3的二步脱水反应较难发生,而且4→LGO的反应能垒较低,最高只有66.5 kJ/mol,说明路径2和路径3中的结构4不稳定。综述分析,路径1为LGA向LGO转化的最佳路径。
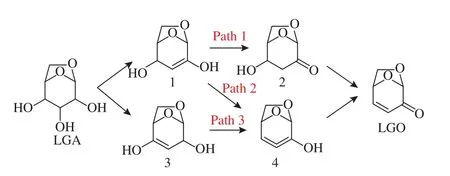
图12 LGA转化为LGO的反应路径示意图Figure 12 Reaction paths of LGA conversion to LGO

图13 LGA转化为LGO的能垒示意图Figure 13 Energy barriers of LGA conversion to LGO
3 结 论
本研究考察了离子液体的烷基侧链长度对纤维素催化热解制备LGO的影响规律,GC/MS和FT-IR结果表明,所有离子液体可有效地促使纤维素热解生成LGO,其中,丁基离子液体因其最短侧链而有较弱的聚集作用,有利于离子液体的扩散,从而对LGO有最好的催化效果。在300 ℃热解时,LGO的最高产率可达15.6 %-C,较低的热解温度有利于LGO的生成和离子液体的回收。离子液体重复利用三次后LGO的产率从13.9%-C轻微下降到了12.5%-C,保持了较好的催化效果。利用DFT对LGO的生成过程进行了计算,确定了路径1为LGA向LGO转化的最优路径。此外,离子液体也可显著提高纤维素热解后焦炭的孔特性,其最高比表面积和孔容分别为389.4 m2/g和0.689 cm3/g。本研究为探究离子液体在生物质的应用方面提供一定的指导作用。
