血同型半胱氨酸与老年2型糖尿病肾病的相关性
2022-07-11宋全全冯珊珊张英辉李夏平王智慧梁蓉袁良
宋全全, 冯珊珊, 张英辉*, 李夏平, 王智慧, 梁蓉, 袁良
(1.广元市精神卫生中心防保科, 广元 628000; 2.甘肃中医药大学公共卫生学院, 兰州 730000)
糖尿病肾病(diabetic kidney disease,DKD)是糖尿病微血管病变主要并发症之一,也是2型糖尿病(T2DM)患者主要的死亡原因,严重影响中老年患者生活质量[1-2]。有研究显示,中国是世界上糖尿病患病人数最多的国家,预计到2030年中国糖尿病患病人数将增至1.68亿[3]。同型半胱氨酸(homocysteine, Hcy)是一种具有良好化学反应性的含硫氨基酸,其主要代谢产物为Hcy-硫内酯,该产物可通过引起活性蛋白质变性,从而导致细胞毒性、炎性损伤、血栓形成及血管钙化等[4]。
众多研究结果表明,Hcy是动脉粥样硬化、高血压、脑梗塞等心脑血管疾病的危险因素[5]。冯珊珊等[6]研究发现老年T2DM患者血胆红素及超氧化物歧化酶(superoxide dismutase,SOD)水平降低或HbA1C水平升高,均是引发DKD的独立危险因素。何小魁等[7]研究表明,在肾功能不全患者中Hcy水平呈上升趋势,尤其是慢性肾脏病患者,高同型半胱氨酸血症(HHcys)的发生率高达90%。已有研究表明血Hcy不仅与DKD患者肾功能水平有关,而且与DKD临床分期显著相关[8]。但目前有关Hcy与T2DM患者肾功能相关性的研究大多是根据白蛋白尿分期方式进行,综合考虑白蛋白尿和肾小球滤过率因素的研究鲜见,且样本量较小[7, 9]。此外,有关老年人群T2DM患者Hcy水平与慢性肾脏疾病关系的研究较少。为此,回顾性收集360例老年T2DM患者临床资料,通过分析T2DM患者Hcy水平与肾功能的关系,探究血Hcy水平对DKD的影响,进而为DKD的防治提供新的思路及理论依据。
1 对象与方法
1.1 研究对象
回顾性收集2017年1月—2020年12月期间广元市第四人民医院内分泌科收治的符合诊断标准且病例资料完整的T2DM患者360例为研究对象,其中单纯T2DM 患者120例,DKD患者240例。纳入标准:性别不限、年龄≥60岁;T2DM诊断采用《中国2型糖尿病防治指南(2017年版)》,而单纯T2DM患者指不伴有任何急性或慢性并发症的T2DM患者。 排除标准:研究资料不全;T2DM合并感染、恶性肿瘤、休克及其他严重疾病;存在原发性肝、肾功能不全;近期服用叶酸、维生素B12等药物。所有研究对象均签署知情同意书,且本研究获得广元市第四人民医院院伦理委员会审核批准。
1.2 研究方法
收集各组基本信息,包括性别、年龄、体质指数BMI、收缩压/舒张压、糖尿病病程等。采集研究人群空腹静脉血,利用Mindray全自动生化分析仪BS-280及其配套试剂盒(由深圳迈瑞公司提供)依次检测丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、血肌酐(Cr)、血尿酸(UA)、β2微球蛋白(β2-MG)、空腹血糖(GLU)、糖化血红蛋白(HbA1c)、血脂[总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)]及Hcy等水平。收集患者晨起后第一次小便样本检测尿白蛋白/肌酐(urine albumin/creatinine,UACR)。肾小球滤过率(glomerular filtration rate,eGFR)估算参照White等[10]研究结果。
1.3 诊断标准及分组
DKD诊断标准:符合《2021年版糖尿病肾脏疾病临床诊疗中国指南》[11],由T2DM导致的两次及多次非同日随机检测eGFR<60 mL/min/1.73 m2和UACR≥30 mg/g,且持续超过3个月,需同时满足以上标准。HHcys诊断标准:Hcy>15 μmol/L。
根据预估eGFR及UACR水平,将DKD患者分为4组:即无慢性肾脏病(NADKD)[eGFR≥60 mL/min/1.73 m2且UACR<30 mg/g]、白蛋白尿伴肾功能未受损(ALB-NADKD)组[eGFR≥60 mL/min/1.73 m2且UACR≥30 mg/g]、正常白蛋白尿伴肾功能损伤(NAALB-DKD)组[eGFR<60 mL/min/1.73 m2且UACR<30 mg/g]和白蛋白尿伴肾功能受损(ALB-DKD)组[eGFR<60 mL/min/1.73 m2且UACR≥30 mg/g]。
1.4 统计方法
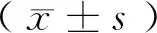
2 结果
2.1 研究人群一般特征资料比较
表1显示了研究对象的一般特征,120例单纯T2DM患者中,性别比例相当,平均年龄(66.39±7.00)岁,平均糖尿病病程(4.38±1.23)年,DKD组每个亚组60例,平均年龄(64.48±6.78)岁。与单纯T2DM组相比,DKD组BMI、收缩压、糖尿病病程、ALT、AST、Cr、UA、GLU、UACR、血脂水平TG、β2-MG、HbA1c及Hcy随DKD严重程度的增加逐渐升高,而eGFR、HDL、叶酸水平则随DKD严重程度的增加反而降低,其中NAALB-DKD组和ALB-DKD组指标变化最为显著(P<0.05)。与NADKD组相比,NAALB-DKD组、ALB-DKD组平均糖尿病病程、UA、UACR及Hcy明显升高(P<0.05),eGFR显著下降,但NAALB-DKD组eGFR的下降无统计学差异(P>0.05)。此外,各DKD组在年龄、性别及舒张压等指标上的变化均无明显差异(P>0.05)。
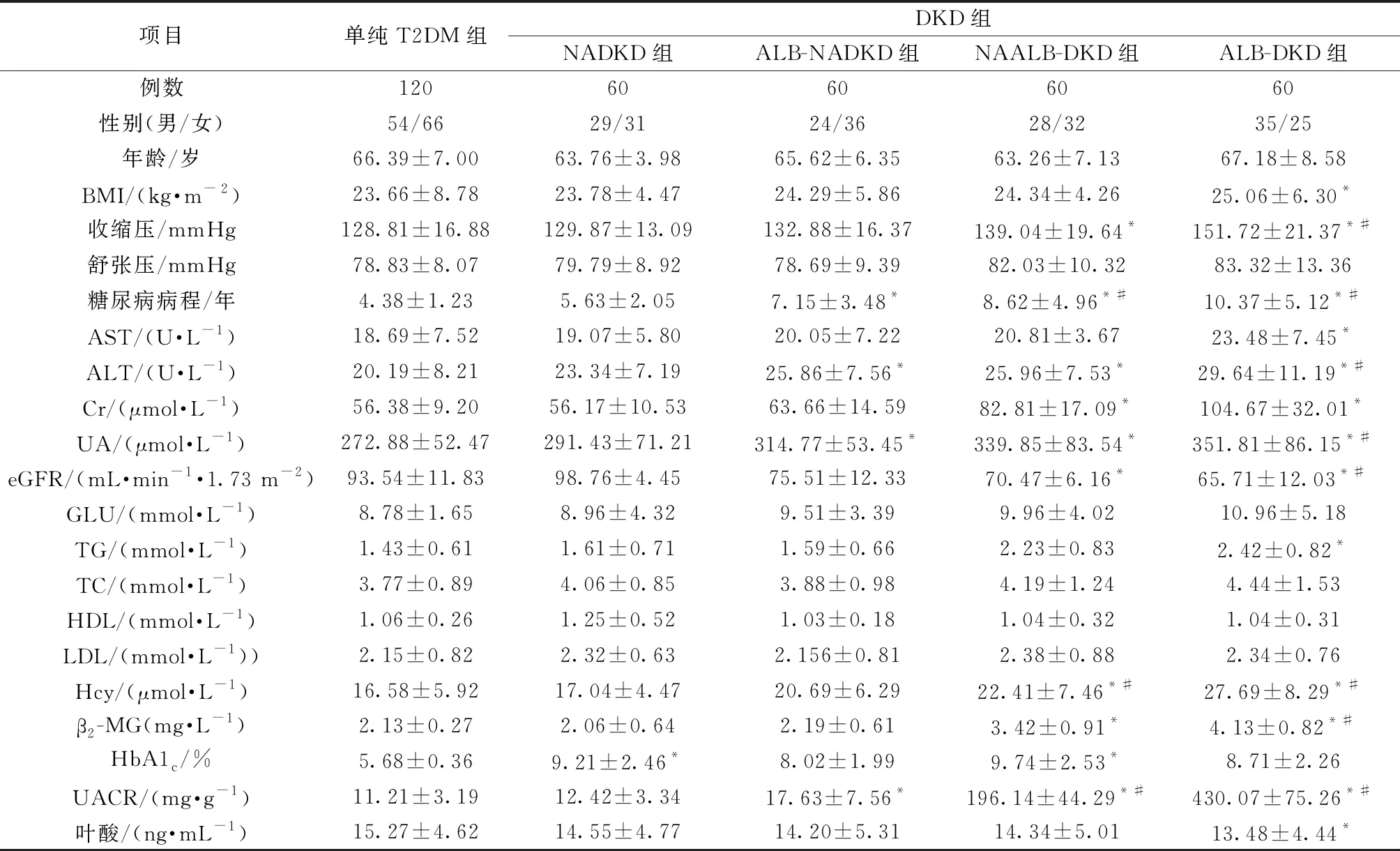
表1 各组研究对象基线资料比较
2.2 各组高同型半胱氨酸血症、肥胖及高血压患病率比较
ALB-DKD组、NAALB-DKD组HHcys发生率、高血压患病率显著高于NADKD组和单纯T2DM组(P<0.05);ALB-NADKD组HHcys发生率明显高于NADKD组,高血压患病率显著高于单纯T2DM组(P<0.05);与单纯T2DM组和NADKD组比较,ALB-DKD组肥胖患病率显著升高,且差异具有统计学意义(P<0.05),如表2所示。

表2 各组HHcys、肥胖发生率及高血压患病率的比较
2.3 DKD各组Hcy与eGFR、UACR之间的关系
图1显示了DKD各组Hcy与eGFR、UACR之间的关系,总体上随着DKD病情的增加,Hcy呈明显上升趋势,eGFR呈明显下降的趋势,且UACR与Hcy水平变化趋势较为一致。可见,Hcy与eGFR、UACR之间存在明显的剂量反应关系,指标之间下降或上升的趋势彼此相关。

图1 各组Hcy水平与eGFR、UACR之间的关系
2.4 DKD各组Hcy与一般资料、临床指标的相关性分析
Spearman秩相关分析结果如表3所示,单纯T2DM组Hcy与收缩压呈正相关关系,与eGFR呈负相关关系(P<0.05);DKD组Hcy与年龄、收缩压、平均糖尿病病程、Cr、UA、β2-MG、UACR均呈正相关关系,与舒张压、eGFR、HDL、叶酸呈负相关关系,然而,ALB-DKD组Hcy与收缩压、年龄、UACR、eGFR、HDL及叶酸相关性最为显著(P<0.05)。其余组Hcy与BMI、AST、ALT、GLU(空腹血糖)、TC、LDL均呈一定的正相关关系,但差异无统计学意义(P>0.05)。DKD组Hcy与eGFR水平呈显著负相关关系,而与UACR水平呈显著正相关关系,如图2所示。
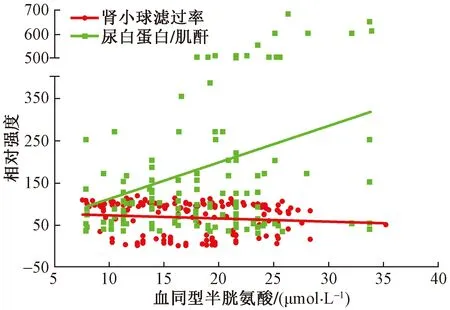
图2 DKD组Hcy与eGFR、UACR的相关性

表3 各组Hcy水平与一般资料、临床指标相关性分析
2.5 Hcy对CKD各组影响的多元Logistic回归分析
多元Logistic回归结果显示,未调整混杂因素后,Hcy是单纯T2DM患者发展为ALB-NADKD组、NAALB-DKD组及ALB-DKD组的独立危险因素(P<0.001)。由于临床上血肌酐Cr、β2-微球蛋白β2-MG分别是影响eGFR和UACR的重要因素,因此模型1调整了除Cr和β2-MG外其他与肾功能有关的基线资料及临床检测指标,结果显示Hcy可增加T2DM患者发生DKD的风险,且对DKD严重程度的影响进一步加大(P<0.001)。模型2对Cr和β2-MG进行回归,结果显示Hcy对不同程度DKD的发生发展均没有影响(P>0.05)。由此可以推测,Hcy可能通过影响T2DM患者Cr和β2-MG水平,从而对不同程度DKD的发生发展产生影响,如表4所示。

表4 Hcy对CKD各组影响的多元Logistic回归分析
3 讨论
Hcy是靶细胞在去甲基化过程中产生的一种高生物活性的含硫非必需氨基酸,该氨基酸在细胞内的代谢路径众多,主要参与一碳单位/叶酸循环、蛋氨酸循环和含硫氨基酸的形成[4]。流行病学研究表明,Hcy来源增多或代谢障碍造成的Hcy水平异常升高往往是动脉粥样硬化、高血压、血栓、冠心病、免疫功能缺陷等疾病的主要诱发因素,其机制可能与引起血管动脉内-中膜厚度的增加有关[12-14]。肾脏是Hcy消除和代谢的主要器官,在肾功能不全患者中Hcy水平明显升高,而2型糖尿病患者中也同样发现Hcy与肾功能之间密切相关[15]。因此,Hcy水平异常可能与糖尿病微血管并发症等系列疾病的发生发展有一定的关联,有必要对其相关机制作进一步分析。
Friedman等[16]通过多因素分析发现,Hcy是T2DM患者发生DKD的强预测因子,Hcy水平每升高1 μmol/L,DKD发生率增加1~2倍,也有研究表明,血Hcy不仅与 DKD患者的肾功能水平有关,而且与DKD的分期有关[8]。
研究结果显示,DKD组Hcy水平及肾功能相关指标Cr、UA、UACR、β2-MG、Hb A1c等均明显高于单纯T2DM组,其中Hcy水平随着肾功能损伤程度的增加逐渐升高,这与吴娟[8]、Nigwekar等[17]的研究结果相似,这说明Hcy可能与T2DM患者慢性肾损伤程度有关。此外,DKD组Hcy与收缩压、UACR呈明显正相关,而与eGFR呈显著负相关,这与张艳霞等[18]研究结果一致,这可能与血液中高浓度的Hcy会通过释放血管收缩因子、炎症因子及免疫相关因子导致血管内皮损伤、血管平滑肌增生、促进血栓形成等有关。研究发现Hcy在生成蛋氨酸和半胱氨酸过程中一旦所需的酶或辅酶等因子缺乏时,容易引起机体Hcy的累计[4],因此,临床上多通过补充叶酸、维生素的方式来降低Hcy,本研究则发现,即使T2DM患者叶酸含量处在正常范围内,其水平与Hcy存在明显的负相关关系,故而推测T2DM患者中叶酸的轻微波动也会对Hcy水平造成一定影响。
可以看出,ALB-DKD组、NAALB-DKD组HHcys发生率、高血压患病率显著高于单纯T2DM组或NADKD组,这与何小魁等[7]、Deng等[19]的研究结果相似,说明HHcys与肾功能损伤程度呈正向关系。分析其可能的原因,Hcy在细胞内代谢过程中产生大量活性物质Hcy-硫内酯,该物质能介导胰岛素信号传导通路发生障碍[20],从而诱导胰岛素抵抗,影响糖代谢过程,使血糖及HbA1c升高。这与本研究Hcy与T2DM患者血糖、HbA1c水平呈正相关结论相似。也有研究显示Hcy-硫内酯与HDL水平呈明显的负相关[21],但是未发现血脂与Hcy之间显著的相关性,这可能研究对象均是老年人,其身体各方面机能、吸收功能下降,体内脂肪水平较低有关。Hcy水平与血压和肥胖相互关联,肥胖可能通过影响Hcy代谢关键辅酶——亚甲基四氢叶酸还原酶,从而造成HHcys的发生,而Hcy可通过多种通路造成血管内皮结构和功能紊乱,从而使体循环阻力增加,升高血压[22]。多元Logistic回归分析结果显示,Hcy是单纯T2DM患者发展为ALB-NADKD组、NAALB-DKD组及ALB-DKD组的独立危险因素,提示Hcy可能间接通过影响T2DM患者Cr和β2-MG水平,从而参与DKD的发生发展。
Hcy异常升高导致DKD发生发展的可能机制:①肾小球血管硬化是导致DKD发生的主要因素,持续HHcys状态可增加血脂、NO、NT-1等因子在肾小球微血管内皮细胞积累,使肾小球内皮功能受损,引起肾小球血管厚度增加、管壁硬化[23];②氧化应激状态的升高可能是早期DKD发生的独立因素,机体大量的Hcy在消除过程中容受氧化酶刺激,产生较多活性氧(ROS),从而使抗氧化酶活性的降低,导致肾小球细胞损伤和肾功能障碍[14];③促进炎症反应,Hcy可以激活核因子κβ、LR4/CD14等相关炎性反应信号通路,促进全身性血管炎症和微血管硬化的发生[24];④血栓形成,Hcy可通过抑制内皮细胞的抗凝血能力,使机体凝血系统和纤溶系统动态平衡紊乱,促使血液长期处于高凝状态[25],容易诱导血栓形成。
4 结论
HHcy在一定程度上可作为T2DM患者发生DKD的强预测因子,临床上不仅将早期检测血Hcy水平作为评估和预防心血管疾病的主要指标,同时也要作为早期评估T2DM患者肾功能损伤及DKD严重程度的必要指标,并及时精准干预,以极大程度减少DKD的发生。
