毛裂蜂斗菜中的1个新的倍半萜化合物
2022-06-17李炳李医明朱维良
李炳,张 勇 ,贾 琦*,李医明,朱维良
1.上海中医药大学中药学院,上海 201203
2.中国科学院新疆理化技术研究所,中国科学院干旱区植物资源化学重点实验室,省部共建新疆特有药用资源利用国家重点实验室培育基地,新疆 乌鲁木齐 830011
3.中国科学院上海药物研究所,新药研究国家重点实验室,中科院受体结构与功能重点实验室,上海 201203
4.中国科学院大学,北京 100049
毛裂蜂斗菜Petasites tricholobusFranch.是菊科(Compositae)千里光族(Senecioneae Cass.)蜂斗菜属PetasitesMill.的多年生草本植物[1]。蜂斗菜属植物全球共有18种,分布于欧洲、亚洲、北美洲,我国有6个品种,分别是蜂斗菜P.japonicus(Seib.et Zucc.) Maxim、掌叶蜂斗菜P.tatewakianusKitam.、盐源蜂斗菜P.versipilisHand.Mazz、台湾蜂斗菜P.formasanusKitam.、长白蜂斗菜P.rubellus(J.F.Gmel.) Toman和毛裂蜂斗菜P.tricholobusFanch.,其广泛分布于东北、华东和西南部[2]。毛裂蜂斗菜具有清热解毒、散瘀消肿功效,民间常用于治疗扁桃体炎、毒蛇咬伤、解毒去痰等病症[3]。现代研究表明,毛裂蜂斗菜具有丰富的药理活性,如神经保护、抗氧化、抗过敏、抗脑缺血、抗炎等[4-8]。本课题组前期对毛裂蜂斗菜95%乙醇提取物中化学成分进行了系统的研究,从中分离得到多个酚类化合物[9]和2个特征性的倍半萜硫酸酯类化合物[10]。近期,本课题组从该植物50%乙醇提取物中分离得到5个倍半萜类化学成分(图1),其中化合物1为新化合物,命名为毛裂蜂斗菜素(petatricholide),其余4个化合物均为倍半萜螺内酯类化合物,分别为bakkenolide IIIb(2)、monoketone(3)、japonipene C(4)和petatewalide A(5),化合物2~5均为首次从毛裂蜂斗菜中分离得到。
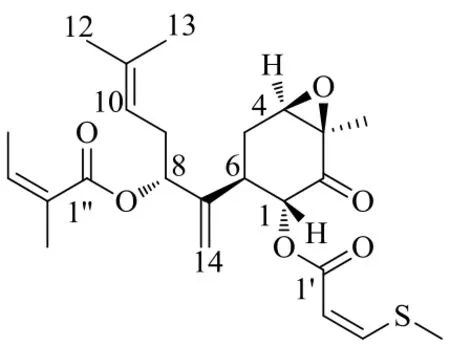
图1 化合物1的结构Fig.1 Structure of compound 1
1 仪器与材料
ESI-MS由Agilent G6520 Q-TOF LC-MS型质谱仪测定;EI-MS由Thermo DFS型质谱仪测定;旋光用Autopol VI 90079型旋光仪测定;红外光谱用Thermo nicolet 6700型红外光谱仪测定;1H、13C和2D NMR用Bruker Avance III 500型核磁共振仪测定,ROESY用Varian vnmrs 400型核磁共振仪测定,以TMS为内标。300~400目硅胶、H硅胶(国药集团化学试剂有限公司);ODS-A-HG 12 nm S-50 μm(日本YMC公司);Sephadex LH-20型凝胶(瑞典GE Healthcare Bio-Sciences AB公司);微孔树脂(MCI GEL CHP20P,日本三菱化学株式会社);硅胶GF254预制薄层色谱板(烟台化学工业研究所),显色剂(硫酸-香兰素显色剂);所用试剂甲醇、乙醇、醋酸乙酯、正丁醇、石油醚、环己烷、二氯甲烷等试剂均为分析纯,由国药集团化学试剂有限公司提供。
本实验药材毛裂蜂斗菜全草于2009年10月采自重庆,经上海中医药大学中药研究所吴立宏研究员鉴定为菊科蜂斗菜属植物毛裂蜂斗菜P.tricholobusFanch.,标本(FDC-20091029)保存于上海中医药大学中药学院中药化学教研室。
2 提取与分离
干燥的毛裂蜂斗菜全草(6.5 kg),粉碎后采用95% 乙醇加热回流提取3次,药渣采用50%乙醇100 ℃回流提取2次,收集2次滤液浓缩得到50%乙醇提取浓缩液。50%乙醇提取液依次采用醋酸乙酯和正丁醇等体积多次萃取,依次得到醋酸乙酯和正丁醇萃取液,减压浓缩后分别获得醋酸乙酯萃取物(21 g)、正丁醇萃取物(153 g)和萃取后水层3个部位。随后采用薄层色谱(TLC)方法对醋酸乙酯和正丁醇萃取物中主要特征性成分进行初步分析,根据倍半萜类化合物在显色剂(硫酸-香兰素显色剂)下的显色特征,优选醋酸乙酯萃取物进行后续的分离纯化。
醋酸乙酯萃取部位(21 g)采用300~400目硅胶,以二氯甲烷-甲醇体系梯度洗脱(15∶1、9∶1、6∶1、4∶1、1∶1),得到4个组分(Fr.1~4)。Fr.1(5.3 g)经H硅胶柱色谱分离,以石油醚-醋酸乙酯体系进行梯度洗脱(40∶1、20∶1、9∶1、6∶1、4∶1、2∶1),得到4个组分(Fr.1.1~1.4)。Fr.1.1(1.6 g)经Sephadex LH-20柱色谱进行纯化,二氯甲烷-甲醇等度洗脱(1∶1),得到Fr.1.1.1(960 mg)。Fr.1.1.1经ODS柱色谱,甲醇-水(0∶100、20∶80、40∶60、60∶40、75∶25)梯度洗脱,得到化合物1(2.5 mg)、4(24.9 mg)、5(7.1 mg)。Fr.1.3(812 mg)经Sephadex LH-20柱色谱二氯甲烷-甲醇等度洗脱(1∶1),洗脱后主成分采用ODS柱色谱二次纯化,甲醇-水梯度洗脱(0∶100、20∶80、40∶60、60∶40、80∶20)后得到化合物2(16.7 mg)。Fr.2(2.1 g)经300~400目硅胶柱色谱,以石油醚-醋酸乙酯(30∶1、15∶1、10∶1、6∶1、4∶1、1∶1)梯度洗脱,得到3个组分(Fr.2.1~2.3)。Fr.2.2(163 mg)经Sephadex LH-20柱色谱,二氯甲烷-甲醇等度洗脱(1∶1),洗脱后主成分采用MCI柱色谱,甲醇-水梯度洗脱(0∶100、20∶80、40∶60、50∶50、70∶30)分离纯化,得到化合物3(2.9 mg)。
3 结构鉴定
根据化合物1的HR-ESI-MSm/z471.181 1 [M+Na]+(计算值471.181 7,C24H32O6SNa),确定该化合物的分子式为C24H32O6S,相对分子质量为448,不饱和度为9。IR光谱中1732 cm−1和 1647 cm−1处的特征吸收峰表明其结构中含有α,β-不饱和酯。1H-NMR数据显示(表1),高场区有6个甲基信号δH2.41 (3H, s), 1.98 (3H, m), 1.89 (3H, t,J= 1.5 Hz),1.71 (3H, brs), 1.66 (3H, brs) 和1.42 (3H, s);δH7.35(1H, d,J= 10.2 Hz), 5.76 (1H, d,J= 10.2 Hz) 信号提示结构中含有1组顺式不饱和烯氢质子。13C-NMR数据(表1)显示该化合物含有24个碳信号,结合DEPT135图谱信息显示δC24.6, 19.4, 17.6,16.7, 14.7, 13.7为6个甲基信号,δC112.6, 31.9和31.3为3个亚甲基信号,δC154.4, 138.3, 119.1, 110.7,75.2, 74.5, 64.3, 44.0为8个次甲基信号,δC201.7,166.9, 165.3, 147.9, 134.1, 127.8, 61.3为7个季碳信号。δC201.7信号提示结构中含有1个酮式结构,δC166.9和165.3显示结构中含有2个酯键,δC154.4,147.9, 138.3, 134.1, 127.8, 119.1, 112.6, 110.7则显示结构中含有8个不饱和碳信号。上述特征信号与化合 物 1α-(3′-ethyl-cis-crotonoyloxy)-8-angeloyloxy-3β,4β-epoxy-bisabola-7(14),10-diene[11]类似,主要差异在于化合物1的C-1位取代基是甲基硫代丙烯酰氧基(methylthioacryloyloxy),而已报到化合物C-1位是乙酰基取代。化合物1的平面结构通过HSQC与HMBC谱做进一步的确定,在HMBC谱(图2)中H-1 (δH5.72, 1H) 和C-1′ (δC165.3) 相关,显示甲基硫代丙烯酰氧基与C-1相连;H-8 (δH5.21, 1H)和 C-1′′(δC166.9) 相关,显示当归酰氧基(angeloyloxy) 与C-8相连;H-14 (δH5.27, 1H;δH5.16, 1H) 和C-7 (δC147.9), C-8 (δC75.2), C-6 (δC44.0) 相关,H-8 (δH5.21, 1H) 和C-7 (δC147.9) 相关,H-6 (δH2.94, 1H) 和C-7 (δC147.9), C-14 (δC112.6) 相关,上述信号显示C-7位是连接C-14、C-8和C-6位的关键位点;H-12 (δH1.71, 3H) 和C-11 (δC134.1), C-10 (δC119.1) 相关,H-13 (δH1.66, 3H) 和C-11 (δC134.1) 相关,上述信号显示12和13位甲基与C-11相连;H-15 (δH1.42, 3H) 和C-3 (δC61.3),C-4 (δC64.3), C-2 (δC201.7) 相关,显示15位甲基与C-3相连;H-4′ (δH2.41, 3H) 和C-3′ (δC154.4) 相关,显示4′位甲基与C-3′相连;H-4′′ (δH1.98, 3H) 和C-3′′ (δC138.3), C-2′′ (δC127.8) 相关,H-5′′ (δH1.89,3H) 和C-1′′ (δC166.9), C-2′′ (δC127.8), C-3′′ (δC138.3) 相关,上述信号显示4′′和5′′甲基分别与C-3′′和C-2′′相连。1H-1H COSY谱(图2)进一步证实,H-1 (δH5.72, 1H) 和H-6 (δH2.94, 1H) 相连,H-6 (δH2.94, 1H) 和H-5 (δH2.61, 1H;δH2.16, 1H) 相连,H-5 (δH2.61, 1H;δH2.16, 1H) 和H-4 (δH3.55, 1H)相连;H-8 (δH5.21, 1H) 和H-9 (δH2.42, 2H) 相连,H-9 (δH2.42, 2H) 和H-10 (δH5.11, 1H) 相连;H-2′(δH5.76, 1H) 和H-3′ (δH7.35, 1H) 相连;H-3′′ (δH6.16, 1H) 和 H-4′′ (δH1.98, 3H) 相连。结合1H-NMR、13C-NMR、HSQC、HMBC及1H-1H COSY谱,化合物1的平面结构确定为1-(cis-methylthioacryloyloxy)-8-angeloyloxy-3,4-epoxy-bisabola-7(14),10-diene。

表1 化合物1的1H和13C-NMR数据 (500/125 MHz, CD3OD)Table 1 1H and 13C-NMR data of compound 1 (500/125 MHz, CD3OD)
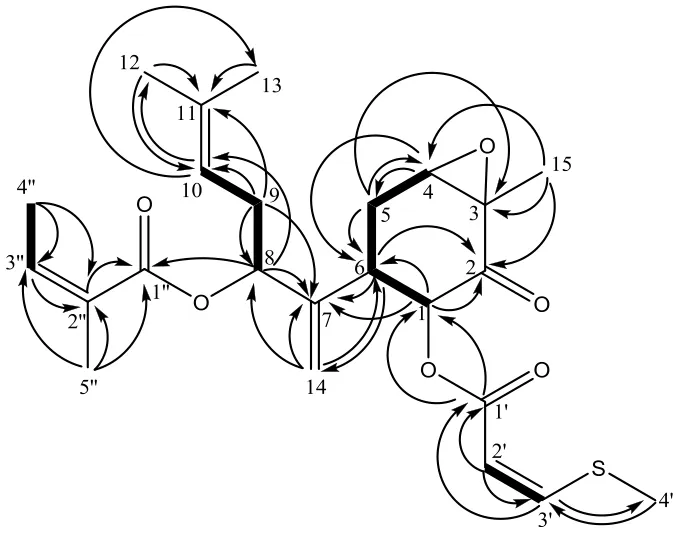
图2 化合物1的HMBC (H→C) 和1H-1H COSY (▬) 关键相关信号Fig.2 Key HMBC (H→C) and 1H-1H COSY (▬)correlations of compound 1
ROESY谱(图3)显示,H-4与H-15相关,H-1与H-8相关,H-4与H-1、H-8均没有相关信号。参考文献已报到的相似倍半萜骨架[12],将H-6定义为α-H,根据J1,6值 (12.8 Hz) H-1则为β-H,H-8同样为β-H;由于H-4与H-1无相关,且参考J4,5偶合常数值 (4.3 Hz),H-4则为α-H,H-15同样为α-H。综上,化合物1的相对构型确定为1α-(cismethylthioacryloyloxy)-8α-angeloyloxy-3β,4β-epoxybisabola-7(14),10-diene,经文献及数据库检索确定为新化合物,命名为毛裂蜂斗菜素。
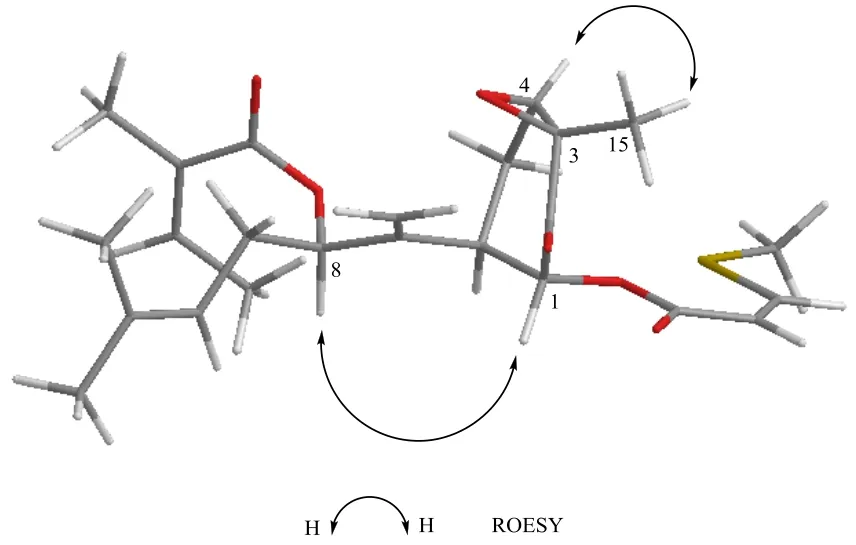
图3 化合物1的ROESY关键相关信号Fig.3 Key ROESY correlations of compound 1
化合物2:白色无定形粉末(甲醇);EI-MSm/z:466 [M-H]+;1H-NMR (500 MHz, CDCl3)δ: 7.09(1H, d,J= 10.2 Hz, H-3′′), 6.93 (1H, d,J= 10.0 Hz,H-3′), 5.83 (1H, d,J= 11.4 Hz, H-9), 5.81 (1H, d,J=10.2 Hz, H-2′′), 5.53 (1H, d,J= 10.0 Hz, H-2′), 5.19(1H, s, H-13a), 5.14 (1H, s, H-13b), 5.14 (1H, dt,J=11.5, 5.3 Hz, H-1), 4.65 (2H, brs, H-12), 2.74 (1H, dd,J= 11.4, 5.1 Hz, H-10), 2.39 (3H, s, H-4′′), 2.35 (3H,s, H-4′), 2.23 (1H, d,J= 14.3 Hz, H-6a), 1.94 (1H, d,J= 14.3 Hz, H-6b), 1.83 (1H, m, H-2a), 1.79 (1H, m,H-2b), 1.66 (1H, m, H-3a), 1.57 (1H, m, H-4), 1.34(1H, dddd,J= 16.5, 13.3, 13.3, 4.3 Hz, H-3b), 1.10(3H, s, H-15), 0.89 (3H, d,J= 6.6 Hz, H-14);13C-NMR (125 MHz, CDCl3)δ: 177.9 (C-8), 165.7(C-1′), 165.2 (C-1′′), 153.3 (C-3′′), 151.9 (C-3′), 147.9(C-11), 113.0 (C-2′), 112.4 (C-2′′), 108.0 (C-13), 80.6(C-9), 70.7 (C-12), 70.1 (C-1), 55.0 (C-7), 51.9(C-10), 45.7 (C-6), 43.2 (C-5), 35.4 (C-4), 29.5 (C-3),26.8 (C-2), 19.6 (C-15), 19.2 (C-4′, 4′′), 15.6 (C-14)。以上数据与文献报道基本一致[13],故鉴定化合物2为bakkenolide IIIb。
化合物3:白色无定形粉末(甲醇);ESI-MSm/z:287.1 [M+Na]+, 550.9 [2M+Na]+;1H-NMR (500 MHz, CD3OD)δ: 5.30 (2H, dt,J= 16.3, 2.3 Hz,H-13), 4.86 (2H, dt,J= 13.9, 2.3 Hz, H-12), 4.58 (1H,d,J= 11.2 Hz, H-9), 2.91 (1H, dd,J= 11.2, 1.3 Hz,H-10), 2.70 (1H, m, H-3a), 2.27 (1H, m, H-3b), 2.09(1H, m, H-4), 2.06 (2H, brs, H-6), 1.96 (1H, m, H-2a),1.68 (1H, dddd,J= 17.9, 13.7, 4.5, 4.4 Hz, H-2b),1.08 (3H, s, H-15), 1.02 (3H, d,J= 6.7 Hz, H-14);13C-NMR (125 MHz, CD3OD)δ: 212.8 (C-1), 179.9(C-8), 148.7 (C-11), 106.0 (C-13), 85.1 (C-9), 70.7(C-12), 67.1 (C-10), 57.9 (C-7), 45.9 (C-6), 45.4(C-5), 38.1 (C-3), 36.9 (C-4), 31.0 (C-2), 19.4 (C-15),14.3 (C-14)。以上数据与文献报道基本一致[14],故鉴定化合物3为monoketone。
化合物4:白色无定形粉末(甲醇);ESI-MSm/z:473.2 [M+Na]+;1H-NMR (500 MHz, CDCl3)δ: 7.04(1H, d,J= 10.0 Hz, H-3′), 5.77 (1H, d,J= 11.1 Hz,H-9), 5.62 (1H, d,J= 10.0 Hz, H-2′), 5.21 (1H, s,H-13a), 5.17 (1H, s, H-13b), 5.15 (1H, dt,J= 12.2,4.9 Hz, H-1), 4.68 (2H, s, H-12), 2.75 (1H, dd,J=11.1, 4.8 Hz, H-10), 2.39 (3H, s, H-4′), 2.25 (1H, d,J= 14.3 Hz, H-6a), 2.14 (2H, m, H-2′′), 2.06 (1H, m,H-3′′), 1.95 (1H, d,J= 14.3 Hz, H-6b), 1.80 (1H, m,H-2a), 1.72 (1H, m, H-2b), 1.66 (1H, m, H-3a), 1.58(1H, m, H-4), 1.38 (1H, m, H-3b), 1.11 (3H, s, H-15),0.95 (6H, d,J= 6.5 Hz, H-4′′, 5′′), 0.90 (3H, d,J= 6.7 Hz, H-14);13C-NMR (125 MHz, CDCl3)δ: 177.5(C-8), 171.9 (C-1′′), 165.6 (C-1′), 152.5 (C-3′), 147.9(C-11), 112.5 (C-2′), 108.2 (C-13), 80.5 (C-9), 70.4(C-12), 70.3 (C-1), 54.7 (C-7), 51.9 (C-10), 46.2(C-6), 43.3 (C-2′′), 43.3 (C-5), 35.2 (C-4), 29.5 (C-3),26.7 (C-2), 25.1 (C-3′′), 22.5 (C-5′′), 22.4 (C-4′′), 19.5(C-15), 19.2 (C-4′), 15.5 (C-14)。以上数据与文献报道基本一致[15],故鉴定化合物4为japonipene C。
化合物5:白色无定形粉末(甲醇);ESI-MSm/z:413.2 [M+Na]+;1H-NMR (500 MHz, CDCl3)δ: 5.76(1H, d,J= 11.2 Hz, H-9), 5.45 (1H, brs, H-2′), 5.20(1H, brs, H-13a), 5.17 (1H, brs, H-13b), 5.09 (1H, dt,J= 12.1, 4.9 Hz, H-1), 4.67 (2H, m, H-12), 2.74 (1H,dd,J= 11.2, 4.9 Hz, H-10), 2.24 (1H, d,J= 15.0 Hz,H-6a), 2.14 (3H, brs, H-5′), 2.02 (3H, s, H-2′′), 1.95(1H, d,J= 15.0 Hz, H-6b), 1.84 (3H, brs, H-4′), 1.79(2H, m, H-2), 1.67 (1H, m, H-3a), 1.57 (1H, m, H-4),1.36 (1H, m, H-3b), 1.11 (3H, s, H-15), 0.91 (3H, d,J= 6.6 Hz, H-14);13C-NMR (125 MHz, CDCl3)δ:177.7 (C-8), 170.0 (C-1′′), 165.5 (C-1′), 157.1 (C-3′),147.8 (C-11), 115.9 (C-2′), 108.3 (C-13), 80.9 (C-9),70.6 (C-12), 69.5 (C-1), 54.9 (C-7), 51.7 (C-10), 45.8(C-6), 43.3 (C-5), 35.4 (C-4), 29.6 (C-3), 27.4 (C-4′),26.8 (C-2), 21.2 (C-2′′), 20.1 (C-5′), 19.6 (C-15),15.6 (C-14)。以上数据与文献报道基本一致[16],故鉴定化合物5为petatewalide A。
4 讨论
本实验从毛裂蜂斗菜50%乙醇提取物中分离并鉴定了5个倍半萜类化合物,包括1个新化合物(1)以及4个首次从该植物中分离得到的螺内酯类化合物(2~5)。本课题组通过文献检索发现,具有与化合物1相同骨架的特征型环氧倍半萜类结构仅从菊科植物厚敦菊属[17]、冬泉菊属[18]、款冬属[11,19]和橐吾属[20]植物中分离得到,本研究证实菊科蜂斗菜属植物同样存在特征型的环氧倍半萜类化合物。由于菊科植物在外部形态方面存在严重的同塑性演化,且菊科千里光族亚族内各属系统位置及亲缘关系的划分依然是学术界争论的焦点[21],本研究在丰富蜂斗菜属植物倍半萜类化合物类型的同时,可从植物次级代谢产物合成生源途径方面为千里光族亚族群的划分提供参考。
利益冲突所有作者均声明不存在利益冲突
