重庆市临床试验机构研究协调员培训现状分析
2022-05-16曹丽亚陈勇川谢江川潘辛梅谢林利
曹丽亚,陈勇川,谢江川,潘辛梅,谢林利
(中国人民解放军陆军军医大学第一附属医院,重庆 400038)
临床研究协调员(CRC)是研究者、申办者和受试者间的纽带,在研究中心协助研究者进行非医学性判断的事务工作,其专业化水平的高低直接影响临床试验的质量[1]。目前,暂无统一的CRC 资格认定或行业准入标准,不同公司CRC 的专业水平参差不齐,高质量的培训显得尤为重要。本研究中调查了CRC 的培训现状和需求,并分析了存在的不足,旨在为开展CRC 的高质量培训提供参考。现报道如下。
1 资料与方法
1.1 调查对象
以重庆市22家临床试验机构在研临床试验项目中的CRC为调查对象,于2019年3月至9月对其发放问卷调查表,对回收问卷进行流水编号,录入问卷数据库,并对其进行统计与分析。
1.2 问卷内容
问卷设置单选题和多选题。针对调查对象,内容包括被调查对象的年龄、学历、专业、工作经历、单位性质等基本信息;针对培训现状,内容包括参加岗前培训的形式、时间、上岗要求及胜任程度,上岗后培训的形式、频率、是否考核、满意度等;针对培训需求,内容包括工作难点、效率影响、欠缺的培训内容、最实用的方式、影响参加培训的原因等。
2 结果
2.1 被调查对象基本情况
共发放问卷140 份,回收有效问卷110 份,有效回收率为78.57%。被调查对象基本情况见表1。
2.2 CRC 培训现状
岗前培训:CRC 岗前培训形式和时间见表2,CRC认为岗前培训能胜任的工作量见表3,CRC 独立上岗的要求见表4。
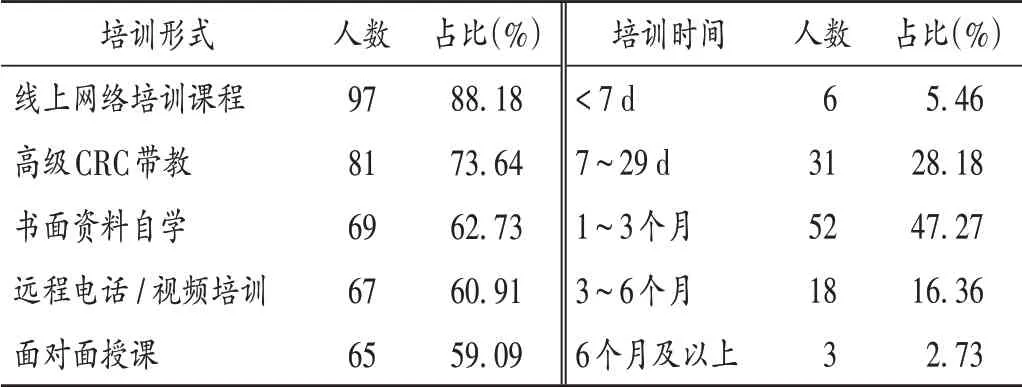
表2 CRC岗前培训形式和时间(n =110)Tab.2 Model and time of the pre-job training for CRC(n=110)

表3 CRC认为岗前培训能胜任的工作量(n=110)Tab.3 Amount of work that CRC believes they can do after the pre-job training(n=110)
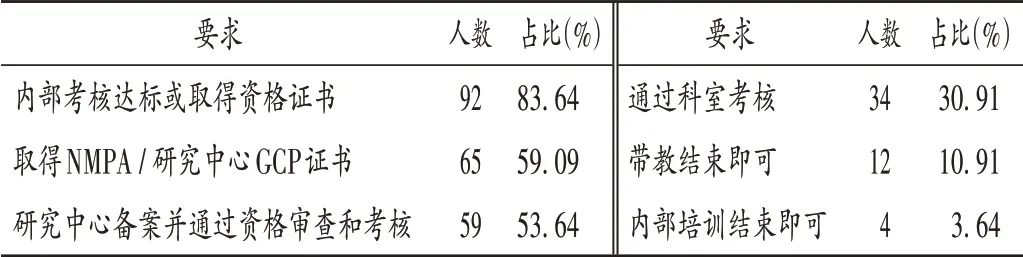
表4 CRC独立上岗的要求(n=110)Tab.4 Requirements for independent employment of CRC(n=110)
上岗后培训:CRC 上岗后培训的主要来源见表5。CRC 上岗后接受所在公司继续教育培训的频率为每1~2 周1 次的占45.45%(50/ 110),每月1 次的占39.09%(43/ 110),3 个月以上或新项目启动时才培训的占15.46%(17/110);仅65.45%(72/110)的CRC 表示继续教育后会进行考核。

表5 CRC上岗后培训的主要来源(n=110)Tab.5 Primaiy sources of the post-job training for CRC(n=110)
2.3 CRC 培训需求
满意度调查:CRC 对本单位培训满意和很满意的占61.82%(68/ 110),不满意的占38.18%(42/ 110),不满意的原因包括培训内容实用性不强、培训过于简单等;85.45%(94/110)的CRC 表示没有固定频率参加 其他单位组织的培训,对其他单位或组织的培训满意和很满意的CRC 占70.91%(78/ 110)。影响CRC 参加其他单位或组织培训的原因中,64.55%(71/110)表示工作太忙而没时间和精力,42.73%(47/110)表示地点太远而无法协调,36.36%(40/ 110)表示培训机会少;89.09%(98/110)表示本单位组织的业务培训最实用,其次是研究中心机构内部的培训和申办方项目组的培训,分别占75.45%(83/110)和64.55%(71/110)。
欠缺的培训内容:见表6。
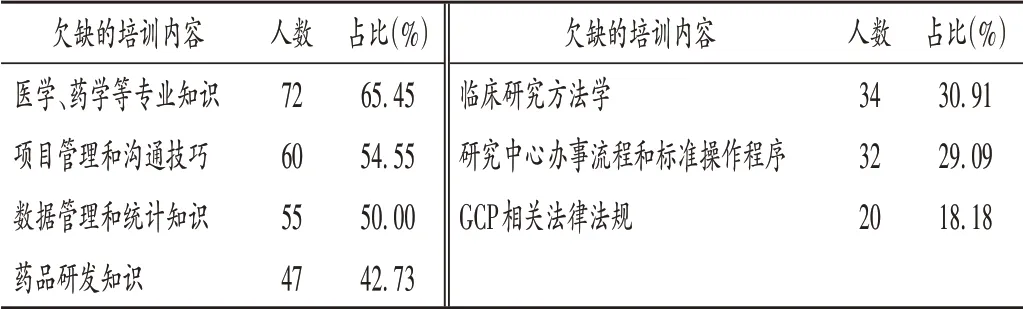
表6 CRC认为欠缺的培训内容(n=110)Tab.6 Training content deemed insufficient by CRC(n=110)
工作难点:排在前3位的分别为与研究者和医技等辅助科室合作、项目更换交接、协调安排各中心访视,分别占50.00%(55/ 110)、44.55%(49/ 110)、39.09%(43/110)。
3 讨论
3.1 CRC 属新兴行业且尚无统一准入标准
由表1 可知,CRC 从业人员年龄多为20~30 岁(87.27%),对学历、专业和既往工作背景要求不严格,行业准入门槛不高,且由其他行业转行做CRC的比例较高(10.00%),这主要与我国临床试验开展的数量增加和质量要求提高有关。CRC 主要工作场所在医院,但绝大多数CRC 来自合同研究组织(CRO)或临床机构管理组织(SMO),占93.64%,不同公司的准入门槛和管理能力参差不齐,目前并无统一的行业准入标准[2]。工作中偶有发现CRC无医药相关背景,甚至没有经过系统培训被派遣到临床试验机构开展工作,这将给受试者、临床试验机构和申办方带来巨大风险。
建议逐渐为CRC 职业设定专业人才培养机制,如在本科教育中开设相关专业或课程,或将临床试验的相关知识融入临床医学、药学、护理学、生物学等专业的本科教育中,促进CRC 的规范化培养与高等教育的交叉融合;依托研究机构和企业建立联合培养机制,培养专业的CRC 人才。目前,其他城市已有高校与医院、企业合作,在传统药学专业课程中加入CRC 相关课程,结合实践带教,探索校、医、教协同视域下的CRC 联合培养机制[3]。同时,建议设定统一的行业准入标准,明确CRC 的教育程度、培训内容和时长,并进行模拟实践等,全部达标后,方可获得行业准入资格。
3.2 尚无统一的CRC 培训体系
由表2可知,各公司或单位培训形式多样,不同公司CRC独立上岗前培训的形式和时长不一,但总的培训时间较短,培训时间少于3 个月的占80.91%,多数培训由CRC 所在公司完成,说明岗前培训的强度和内容不够。在当前行业发展背景下,快速上岗已成为临床试验参与各方的迫切需求,内部考核、机构培训、实践带教等方式可在一定程度上帮助CRC快速上岗,但不同公司和研究机构对CRC 的培训内容和强度不一。除取得《药物临床试验质量管理规范》(GCP)证书外,目前尚无统一的资质规定,仅有GCP 证书并不能达到具体工作要求。上岗后的继续教育培训是更新专业知识和提高业务能力的重要组成部分。由表5可知,CRC的上岗后培训主要由其所在公司或申办方项目组组织,国家药品监督管理局、医院或相关组织每年组织的学习班或研修班受时间、精力、成本等因素影响,培训强度和效果参差不齐。
本调查结果显示,CRC 认为其所在SMO 公司、研究中心和申办方的培训最实用,侧面反映相关监管部门或其他具有公信力的组织对CRC 的培训不够,缺乏权威、系统的培训体系。目前,由临床研究专业协会(ACRP)及社会临床研究组织(SoCRA)提供的CRC 培训及资格认证服务获业界广泛认可[4];其他城市已有高校、医院和组织探索CRC 的规范化培训,创建适合中国的CRC 规范化培训和认证体系,但尚未建立官方或行业协会性质的CRC培训及认证标准[5]。
3.3 CRC 培训需求大且内容广
在临床试验中,CRC 负责试验药品管理、物资管理、协调访视、协助研究者进行医学资料收集、安全事件上报等工作[6]。在我国专职临床研究人员极其缺乏的现状下,CRC 除具备良好的沟通协调能力外,还需掌握医学、药学、统计学等专业知识,具有良好医药背景的CRC在与研究者和受试者沟通协作时优势明显[7]。CRC通常被认为从事大量事务性工作,培训内容主要包括GCP 相关法律法规、伦理、受试者保护等基础内容,以及项目开展的具体事务工作要点,而针对医学、药学等专业知识的深度教育较欠缺。除专业技能的培训外,作为申办方、研究者、受试者和临床试验机构、伦理各方的纽带,协调能力和沟通技巧等方面的培训也较欠缺,加之绝大多数CRC 为第三方公司派遣到医院开展工作,在与研究者、临床试验机构、伦理和医技科室沟通协作时易产生孤立无援的感觉。故培训中应增加职业教育,增强其工作自信心和职业归属感。此外,本次调查结果还显示,临床试验机构培训的实用性仅次于所在公司,但其对CRC 的培训仅占30.91% ,说明临床试验机构对于CRC的培训和管理还有待加强。
3.4 小结
重庆市医药研发事业正处于大力发展阶段,已出台多项相关政策鼓励新药研发,临床试验是其中至关重要的一环[8]。配备足量、高水平的CRC,保证临床试验及时、有效实施,已成为医药研发的迫切需求。规范化培训是提升行业认知和提高从业人员整体水平的有效途径。规范化的CRC 培训系统需要政府引导、临床试验机构落地实施和临床研究行业的协同与支持,多方协作建立满足临床试验开展需求的培训体系,促进重庆市乃至全国新药临床研究事业的发展。本研究中尚存在一些不足,如调查区域较单一,培训内容受相关政策或法规影响,问卷设计未涉及相关内容,故其结论有一定局限性,后续将进一步研究。
