脑卒中病灶对多频EIT 边界电压谱特性的影响研究
2022-04-22赵志博曹新生文治洪王春晨高志军
赵志博,代 萌,付 峰,曹新生,文治洪,王 航,代 静,王春晨,高志军,刘 洋,杨 琳*
(1.空军军医大学基础医学院,西安 710032;2.空军军医大学军事生物医学工程学系,西安 710032;3.空军军医大学航空航天医学系,西安 710032)
0 引言
脑卒中(分为缺血性脑卒中和出血性脑卒中)具有发病急、病情凶险等特点,已成为我国居民的第一位死亡原因,同时也是导致我国成人残疾的首位病因[1]。临床实践表明,早期检测和治疗是改善脑卒中预后的关键[2]。目前,CT 和MRI 是诊断脑卒中的临床金标准,但因设备体积庞大且价格昂贵,无法用于基层社区医疗单位或急救车等院前急救,患者只有到达医院后方可行CT 或MRI 检查,往往错失最佳治疗时机[3]。据统计,目前仅有3%~5%的缺血性脑卒中患者能在“时间窗”内得到溶栓治疗[4]。因此,临床上迫切需要一种在院前急救阶段便能够开展快速检测与鉴别脑卒中的诊断技术。
多频电阻抗断层成像(electrical impedance tomography,EIT)是EIT 的一种成像模式,其基于人体组织的阻抗随频率变化的特性(阻抗频谱特性),利用在同一时刻、多种频率的测量数据重构人体内的阻抗分布,又被称为准静态EIT[5]。与传统的动态EIT 相比,多频EIT 具有不需要其他时刻数据作为参考的特点,在一次性快速检测脑卒中方面极具潜力,有望成为快速检测脑卒中的成像技术[6]。
由于多频EIT 的独特优势,利用多频EIT 快速检测脑卒中引起了众多学者的关注。诸多研究小组分别在组织阻抗频谱测量[7]、多频EIT 数据采集系统[8]和成像算法[9]等方面开展了研究,为多频EIT 检测脑卒中奠定了良好的基础。截至目前,多频EIT 尚无法应用于实际,制约其研究进程的一个重要原因是脑卒中病灶对多频EIT 边界电压谱特性的影响情况尚不清晰,致使无法深入开展具有针对脑卒中检测的特异性研究。为此,本文在课题组前期建立的人头三维模型基础上,系统性仿真不同位置、不同体积以及不同性质的脑卒中病灶对多频EIT 边界电压谱的影响,并量化分析多频EIT 边界电压谱特征,获得检测和鉴别脑卒中的最优频率段,以期为未来多频EIT 检测脑卒中研究奠定良好的数据基础。
1 材料与方法
1.1 真实人头模型的构建
基于真实人脑CT 图像,依次采用图像重建软件Mimics、计算机辅助设计(computer aided design,CAD)和SolidWorks 软件对人头进行真实边界的重建,真实人头模型包含头皮层、颅骨层、脑脊液层、脑组织层和脑室5 个部分,具体构建方法见课题组前期研究[10-11],模型如图1(a)所示。其次,在COMSOL Multiphysics 多物理场仿真软件中,模拟脑卒中病灶,并分别根据人头各种组织的电阻抗频谱特性[电导率谱和介电虚部谱如图1(b)和(c)所示]依次设置相应组织,从而构建具有真实组织阻抗频谱特性的人头模型。最后,依据电磁场求解方法,完成多频EIT边界电压谱的仿真计算。正常脑组织和脑卒中组织的阻抗频谱不但实部成分(电导率)有明显的不同,而且虚部成分(介电虚部)也存在特异性差异[7],因此,本研究采用了电导率和介电虚部分别定义人头模型中各组织的电特性,以期综合分析脑卒中组织对多频EIT 边界电压谱的影响。

图1 人头模型和人头组织阻抗频谱特性
1.2 脑卒中病灶的模拟
采用如下方案模拟不同类型、不同体积和不同位置的脑卒中病灶。为了模拟不同位置的脑卒中病灶,根据临床颅脑解剖结构,将颅内区域划分为额区、颞区和枕区,在每个区的轴向上,从边缘逐渐靠近颅脑中心,即远、中、近3 个位置分别设置病灶;为了模拟临床中不同体积的脑卒中病灶,根据临床脑卒中病灶体积范围,以整个脑体积的0.5%、2.5%和5%区域作为病灶体积,例如,图2 表示位于枕区、靠近颅脑中心的3 种体积的病灶;为了模拟不同类型的脑卒中病灶,所有病灶都分为出血性和缺血性2 种情况。简言之,共模拟3 个区(额、颞、枕区)×3 个位置/区(远、中、近)×3 种体积/区/位置(0.5%、2.5%、5%)×2 种类型(缺血、出血)=54 种病变的情况。
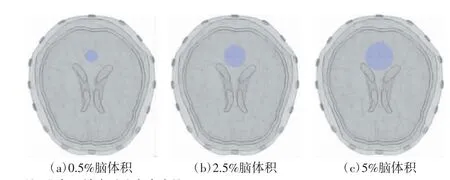
图2 位于枕区的距颅脑中心最近侧位置的病灶
1.3 多频EIT 边界电压谱的仿真计算
为了全面评估脑卒中病灶对多频EIT 边界电压谱的影响,分别仿真计算在10 Hz~1 MHz 内16 个频率下的EIT 边界电压,频率分别为10 Hz、20 Hz、50 Hz、100 Hz、200 Hz、500 Hz、1 kHz、2.5 kHz、5 kHz、10 kHz、25 kHz、50 kHz、100 kHz、200 kHz、500 kHz和1 MHz。
人头模型的皮肤表面共设置16 个电极(电极直径为1 cm),为了保证计算的准确性,所有条件下的模型剖分单元数均大于350000。由于具有高阻抗的颅骨会对电流形成屏蔽作用,激励电流难以到达颅内,所以采用对向激励-相邻测量模式实施EIT数据仿真,以增强颅内的敏感性[6]。仿真电流大小为500 μA。理论上,对向激励-相邻测量模式产生的1 帧EIT 数据包含了256 个通道电压(16×16),但在实际中我们无法准确测量激励电极与皮肤之间的接触阻抗,因此,将激励电极作为测量电极的通道电压去除,共64 个通道电压(16×4),可获得192 个有效通道电压。
EIT 边界电压谱仿真计算方法如下:(1)计算无病灶情况下的边界电压谱。将10 Hz 处各种人头组织的阻抗分别设置对应组织的电特性,包括电导率和介电虚部,并将激励频率设置为10 Hz,然后开展EIT仿真,可获得1 帧10 Hz 处的EIT 边界电压,包括实部和虚部两部分;以此类推,分别将20 Hz、50 Hz、100 Hz、200 Hz、500 Hz、1 kHz、2.5 kHz、5 kHz、10 kHz、25 kHz、50 kHz、100 kHz、200 kHz、500 kHz 和1 MHz处各种人头组织的阻抗分别设置对应组织的电特性,并将激励频率设置为相应的频率,然后依次开展EIT 仿真[11],可分别获得相应频率处的边界电压。通过以上计算,可获得16 种频率处的边界电压,并将其定义为无病灶情况下的EIT 边界电压谱。(2)分别计算54 种病变情况下的边界电压谱。仿真计算方法与无病灶情况相同,在设置完病灶的属性(位置和大小等)后,分别以不同频率处的人头组织和病灶的阻抗定义相应的人头组织与病灶的电特性,以及设置相应的激励频率,然后实施EIT 仿真,可分别获得所有病变情况下的EIT 边界电压谱。
1.4 数据分析
通过以上仿真计算,可获得无脑卒中病灶和54种存在脑卒中病灶情况的EIT 边界电压谱。因为人头模型中各种组织的阻抗分为实部和虚部两部分,所以获得的EIT 边界电压也分为实部和虚部两部分。以Vreal和Vimg表示1 帧EIT 边界电压的实部和虚部,可通过将所有通道的测量电压求和获得,具体计算公式为

本研究采用对向激励-相邻测量的模式,因此有192 个有效测量通道[14]。通过计算所有频率处的Vreal和Vimg,可获得EIT 边界电压谱。依据此方法,可计算出所有存在脑卒中病灶情况下的EIT 边界电压谱。然后,分别对比分析发生脑卒中前后以及不同类型脑卒中引起的多频EIT 边界电压谱,以获得用于检测脑卒中病灶和鉴别脑卒中类型的最优频率段。
1.4.1 定量分析脑卒中发生前后的多频EIT 边界电压谱变化
为了达到利用多频EIT 检测脑卒中的目的,首先需要从正常组织中识别出脑卒中病灶。为此,提出边界电压谱变化指数(boundary voltage variation index,BVVI)分析脑卒中发生前后的多频EIT 边界电压谱在所有频率处的差异,BVVI 包括实部BVVIreal和虚部BVVIimg两部分,具体计算公式如下:
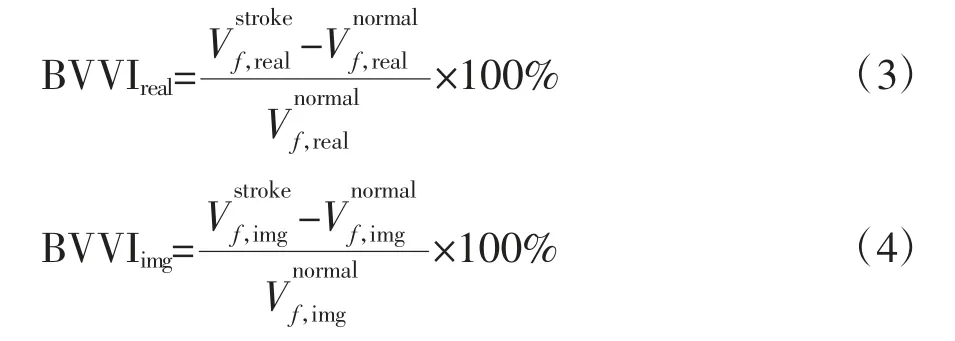
根据BVVI 可获得脑卒中发生前后多频EIT 边界电压变化最大的频率范围,即区分正常组织和脑卒中组织的最优频率段。
1.4.2 定量分析不同类型脑卒中的多频EIT 边界电压谱差异
在脑卒中发作早期,不但要从正常脑组织中检测出脑卒中,而且需要鉴别脑卒中类型,因此,需要进一步考察2 种不同类型脑卒中引起的EIT 边界电压谱差异。为此,将测量频段划分为3 个频段:低频段(10 Hz~<1 kHz),中频段(1 kHz~<100 kHz)和高频段(100 kHz~1 MHz),并提出利用频差变化指数(frequency difference change index,FDCI)分别对比出血性病灶和缺血性病灶引起的多频EIT 边界电压谱在3 个频率段内的差异。FDCI 包括实部FDCIreal和虚部FDCIimg两部分,具体计算公式如下:

式中,f0表示在各频段内的最低频率,在低频段内f0=10 Hz;在中频段内,f0=1 kHz;在高频段内,f0=100 kHz。
FDCI 表示存在病变组织的EIT 边界电压谱变化减去无脑卒中组织的EIT 边界电压谱变化,等效为脑卒中病变对应的边界电压谱变化减去等体积的正常脑组织对应的边界电压谱变化。由于2 种脑卒中(出血性和缺血性)病灶都与正常脑组织相比较,所以FDCI 可一定程度上反映2 种脑卒中病灶的EIT 边界电压谱差异。
2 结果
2.1 脑卒中发生前后的多频EIT 边界电压谱差异
缺血性和出血性脑卒中发生前后的多频EIT 边界电压谱变化如图3 所示。图3(a)和(b)为缺血性脑卒中发生前后的多频EIT 边界电压谱变化的实部BVVIreal和虚部BVVIimg。整体上,BVVIreal随频率升高而降低,变化范围为0.61%(10 Hz,颞区,5%脑体积,距颅脑中心最远处)至0.001%(1 MHz,枕区,0.5%脑体积,距颅脑中心最近处,因表中数据保留小数点后2 位,故0.001%在表1 中对应值为0.00%)。另外,相同体积的缺血性病灶,BVVIreal随着病灶与颅脑中心之间距离的增大而增大,例如,位于额区、5%脑体积的缺血性病灶、10 Hz 处,近、中、远处的BVVIreal分别为0.47%、0.51%和0.57%。此外,缺血性病灶引起的BVVIimg在10~100 Hz 范围内的变化小于1.00%,而在100~500 Hz 内迅速增加,最大值可达8.30%(500 Hz,颞区,5%脑体积,距颅脑中心最远处)。而且,针对同一病灶,BVVIimg明显大于BVVIreal,例如,位于颞区、距颅脑中心最远处、5%脑体积的缺血性病灶,BVVIimg和BVVIreal分别为8.30%和0.61%。详见表1。
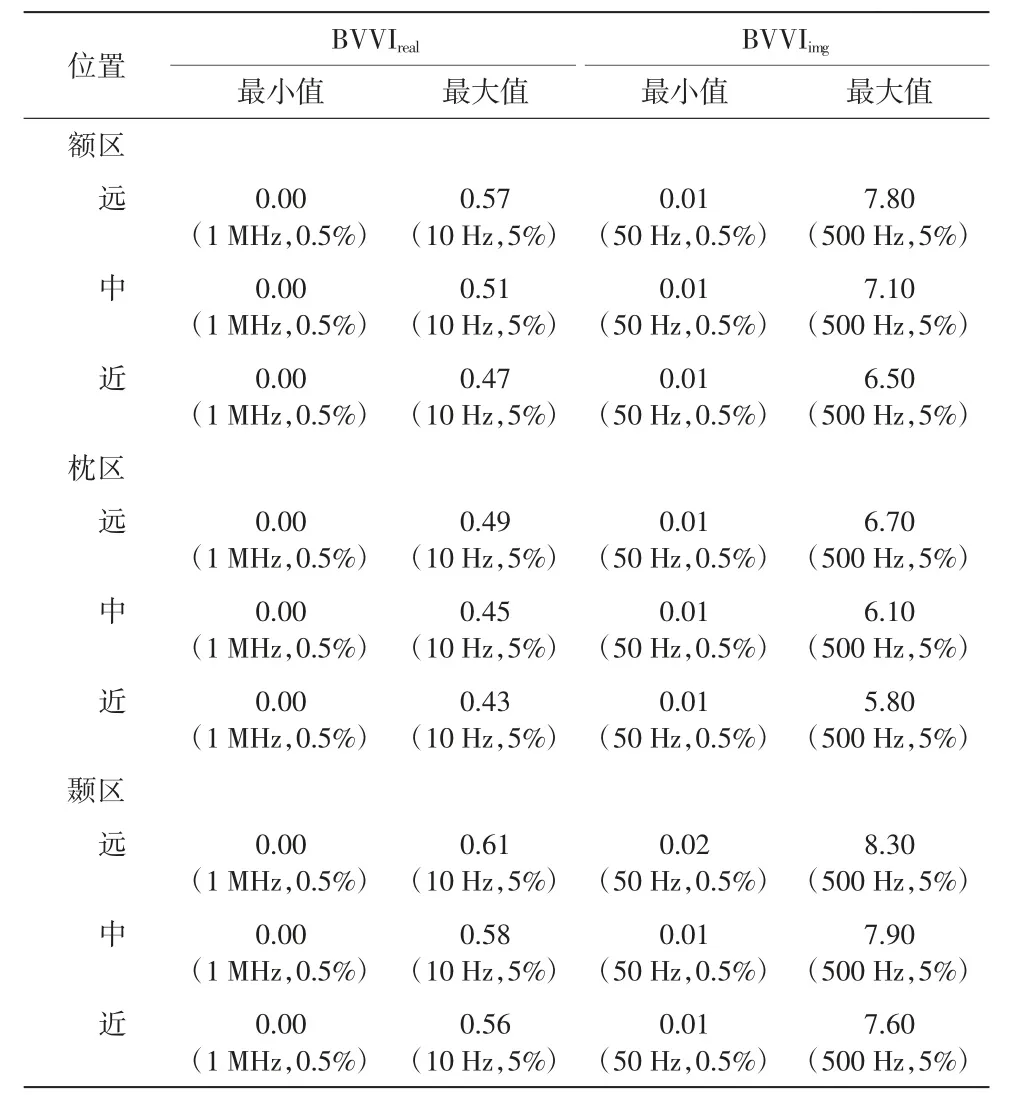
表1 缺血性脑卒中病灶引起的多频EIT 边界电压谱变化 单位:%
图3(c)和(d)为出血性脑卒中发生前后的多频EIT 边界电压谱变化的实部BVVIreal和虚部BVVIimg。在10 Hz~200 kHz 范围内,BVVIreal随频率升高而逐渐减低,变化范围为1.3%(10 Hz,颞区,5%脑体积,距颅脑中心最远处)至0.07%(200 kHz,额区,0.5%脑体积,距颅脑中心最近处);但在200 kHz~1 MHz 范围内,BVVIreal迅速升高,最大值为1.7%(1 MHz,颞区,5%脑体积,距颅脑中心最远处)。BVVIimg在100 Hz~2.5 kHz范围内升高,然后降低至0.01%(100 kHz,颞区,0.5%脑体积,距颅脑中心最远处),继而随频率升高而迅速升高,在1 MHz 处达到最大值,BVVIimg的范围为5.50%(1 MHz,枕区,5%脑体积,距颅脑中心最近处)至7.20%(1 MHz,颞区,5%脑体积,距颅脑中心最远处)。详见表2。

表2 出血性脑卒中病灶引起的多频EIT 边界电压谱变化 单位:%
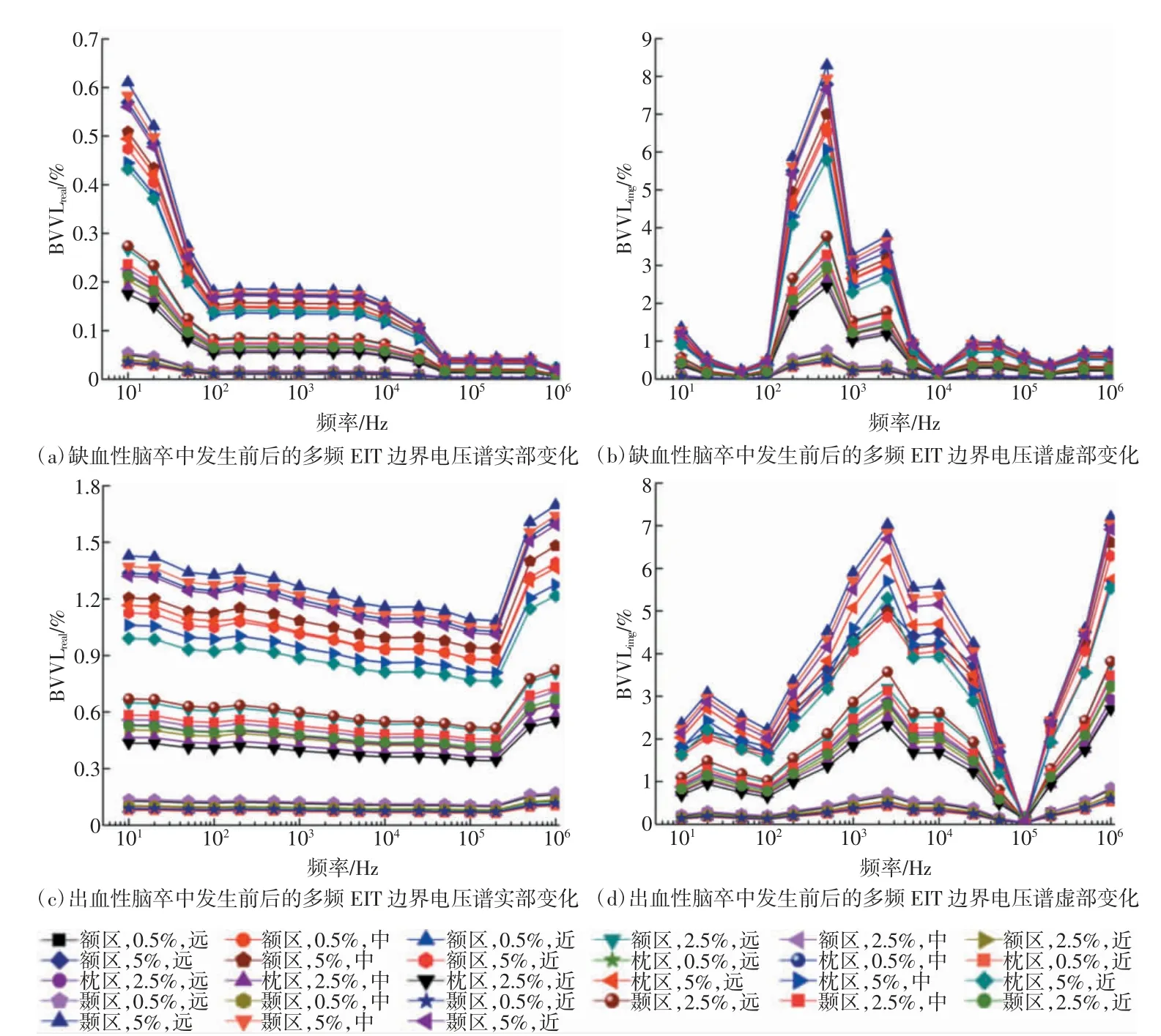
图3 缺血性和出血性脑卒中发生前后的多频EIT 边界电压谱变化
2.2 不同类型脑卒中引起的多频EIT 边界电压谱差异
缺血性和出血性脑卒中病灶引起的多频EIT 边界电压谱FDCI 如图4 所示。图4(a)和(b)为缺血性脑卒中病灶引起的多频EIT 边界电压FDCI 的实部和虚部。整体上,处于低频段的FDCIreal明显大于处于中频段和高频段的FDCIreal。在低频段内,FDCIreal先随着频率的升高而升高,于100 Hz 处达到峰值,然后逐渐降低;FDCIreal在100 Hz 处的最大值范围为0.28%(枕区,5%脑体积,距颅脑中心最近处)至0.42%(颞区,5%脑体积,距颅脑中心最远处)。在中频段内,FDCIreal随频率升高而降低,最大值为0.13%(颞区,5%脑体积,距颅脑中心最远处;颞区,5%脑体积,距颅脑中心中等距离处;额区,5%脑体积,距颅脑中心最远处)。在高频段内,FDCIreal基本无变 化,FDCIreal值 均 为0.02。FDCIimg在3 个频段内均先随频率升高而升高,然后随频率升高而降低。FDCIimg在低频段内的最大值位于100 Hz 处,范围为0.30%(枕区,5%脑体积,距颅脑中心最近处)至0.45%(颞区,5%脑体积,距颅脑中心最远处)。在中频段和高频段内的最大值均小于0.2%。详见表3。
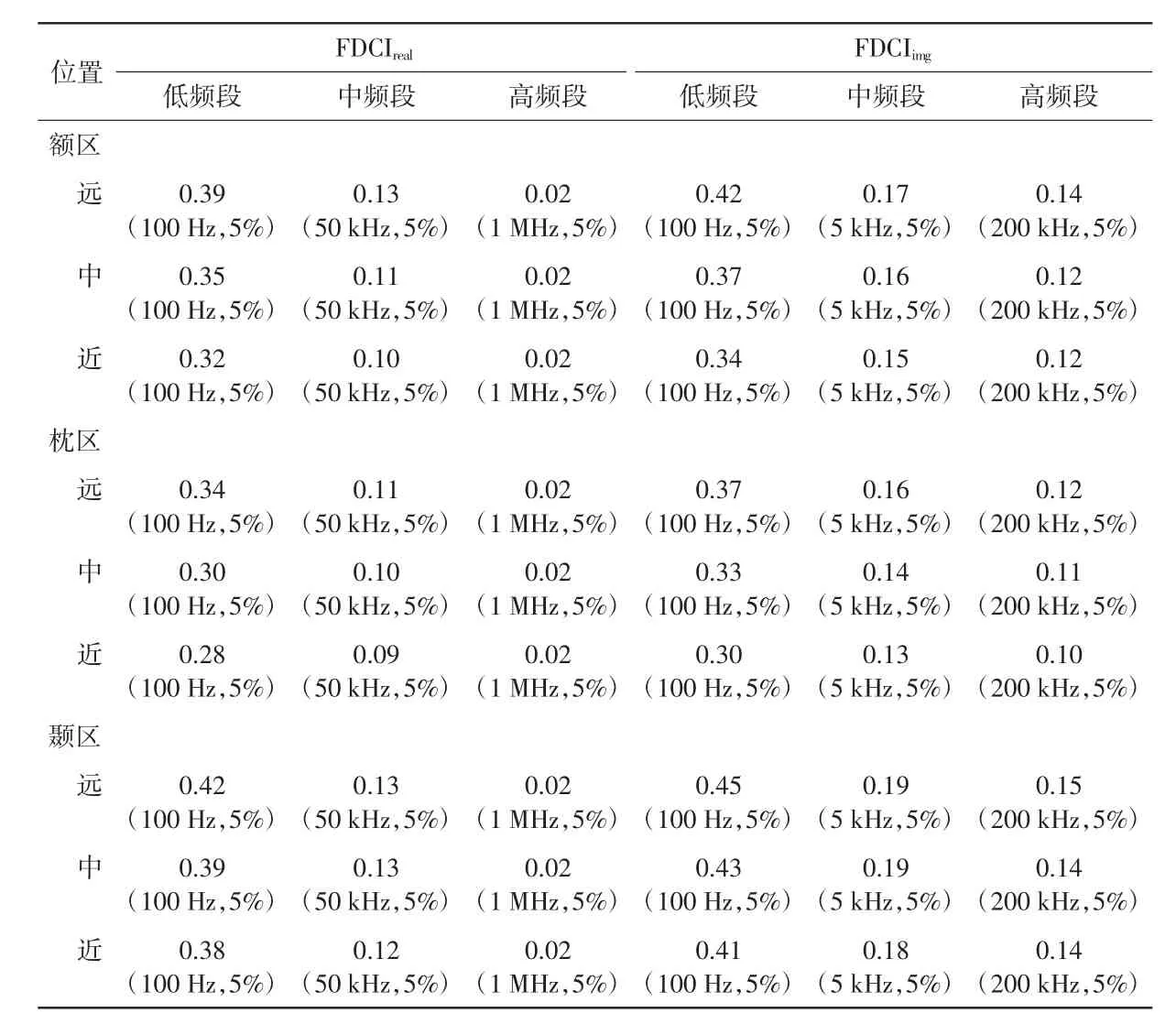
表3 缺血性脑卒中病灶引起的多频EIT 边界电压谱FDCI 单位:%
图4(c)和(d)为出血性脑卒中病灶引起的多频EIT 边界电压谱FDCI。FDCIreal在3个频段内均随频率升高呈增加趋势,但在高频段内FDCIreal变化(最大值为0.57%,颞区,5%脑体积,距颅脑中心最远处)明显大于在中频段内变化(最大值为0.17%,颞区,5%脑体积,距颅脑中心最远处)、低频段内变化(最大值为0.14%,颞区,5%脑体积,距颅脑中心最远处)。此外,FDCIimg在高频段内变化(最大值为1.50%,颞区,5%脑体积,距颅脑中心最远处)远大于在中频段内变化(最大值为0.32%,颞区,5%脑体积,距颅脑中心最近处)和低频段内变化(最大值为0.42%,颞区,5%脑体积,距颅脑中心最近处)。详见表4。
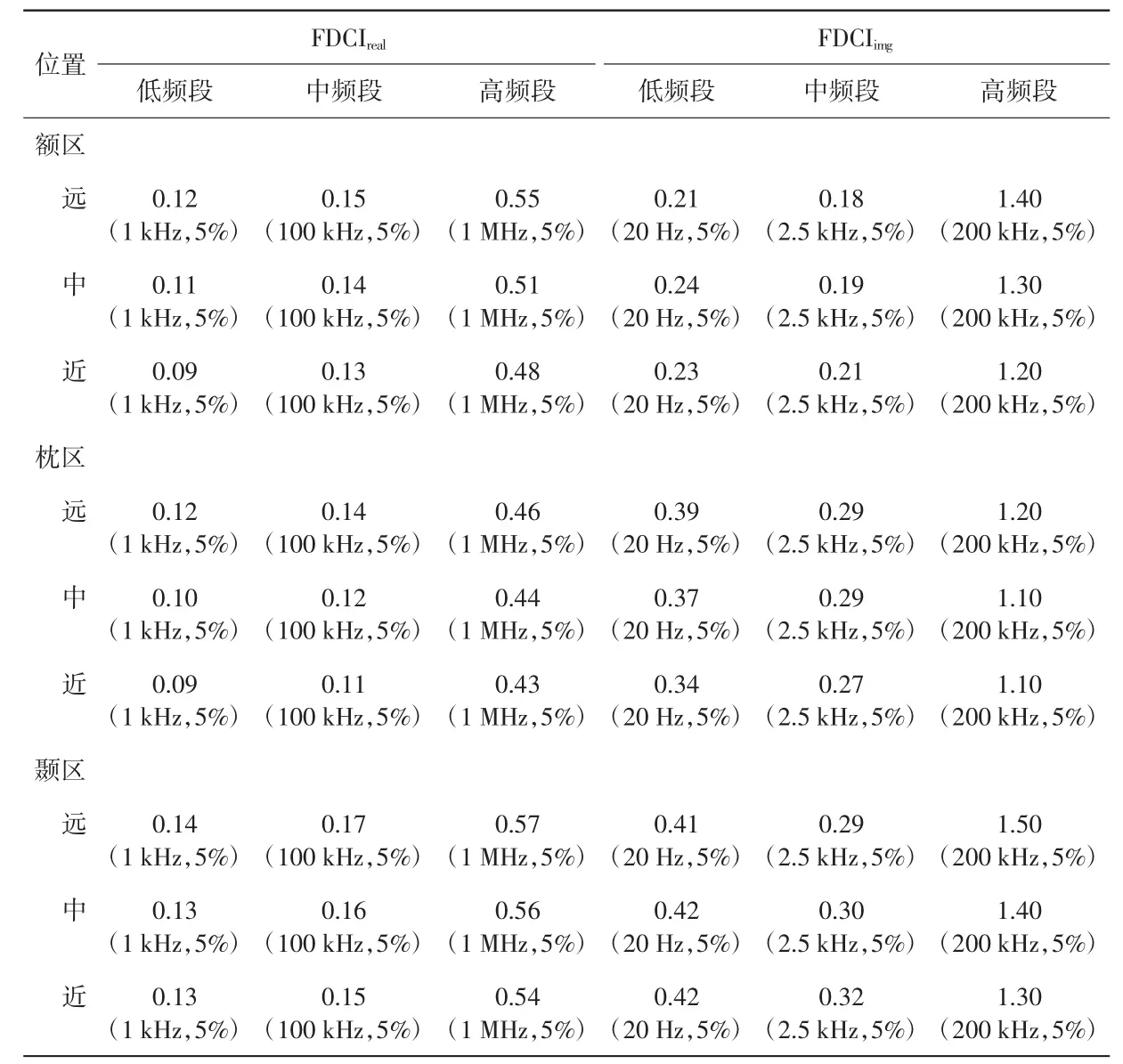
表4 出血性脑卒中病灶引起的多频EIT 边界电压谱FDCI 单位:%
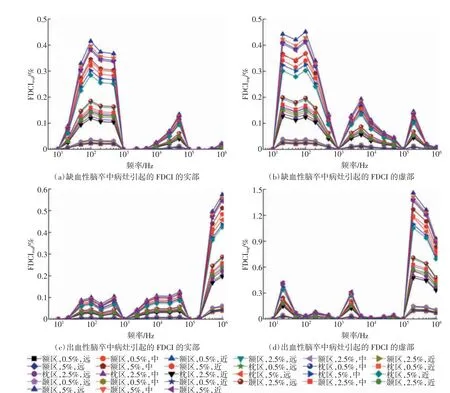
图4 缺血性和出血性脑卒中病灶引起的多频EIT 边界电压谱FDCI
3 讨论
从BVVI 的结果可知,缺血性脑卒中病灶在10 Hz~100 kHz范围内的BVVIreal较大,最大值约为0.6%,而BVVIimg在100 Hz~<10 kHz 范围内较大,最大值约为8%,说明在10 Hz~<100 kHz 频段内,缺血性脑卒中病灶与正常脑组织具有明显的阻抗差异。因此,利用10 Hz~100 kHz 频段内的多频EIT 边界电压谱信息有利于区分缺血性病灶和正常脑组织,其中,应着重关注10~100 Hz 的EIT 边界电压谱实部、100 Hz~<1 kHz 的EIT边界电压谱虚部。对于出血性脑卒中病灶,BVVIreal在200 kHz~1 MHz 范围内变化较大,最大值可达1.7%,并且BVVIimg同样在此频段内变化较大,表明在200 kHz~1 MHz 范围内的EIT 边界电压谱包含了区分出血性病灶和正常脑组织的重要信息。
从FDCI 的结果可知,缺血性脑卒中引起的FDCIreal和FDCIimg均在低频段(10 Hz~<1 kHz)变化最明显,FDCIreal最大值约为0.4%,FDCIimg最大值约为0.5%。但是,出血性脑卒中引起的FDCIreal和FDCIimg均在高频段(100 kHz~1 MHz)变化最明显,FDCIreal最大值约为0.6%,FDCIimg最大值约为1.5%。因此,同时利用低频段(10 Hz~<1 kHz)和高频段(100 kHz~1 MHz)的EIT 边界电压谱有助于鉴别缺血性脑卒中和出血性脑卒中。
本研究构建的真实人头模型中的脑组织尚未被进一步细分为脑灰质和脑白质,未来将通过图像分割技术,从真实人头CT 图像中获得白质区域和灰质区域,从而建立更加逼真的人头模型(包括逼真的解剖结构和逼真的电阻抗特性分布),进一步提高模型的准确性。另外,根据本研究的结果,课题组将优化前期提出的利用多频EIT 检测脑卒中的成像算法[15],进一步提高成像算法的性能。而且,本研究获得的最优脑卒中病灶检测频率和最优的脑卒中病灶鉴别频率也可为多频EIT 数据采集系统的设计提供重要的数据参考,以及在以后的研究中可更加注重系统在最优频率段的性能,如系统的检测精度和频带。
综上所述,本文首先构建了具有真实人头阻抗频谱分布的三维人头模型,然后仿真了由不同位置、不同体积和不同性质的脑卒中病灶引起的EIT边界电压谱,并量化分析了多频EIT 边界电压谱特征,为未来开展多频EIT 检测脑卒中研究(包括数据采集系统研发和成像算法设计)奠定了坚实的数据基础。
