阿奇霉素微生物限度检查方法适用性验证
2022-04-11钱良友伍冰冰向大位
钱良友 伍冰冰 向大位
摘要:目的 建立阿奇霉素微生物限度检查方法。方法 按《中国药典》2020版四部生物检查法进行试验。加入铜绿假单胞菌等5个试验菌,测定回收率。结果 需氧菌总数采用薄膜过滤法,霉菌和酵母菌总数采用倾注法,各试验菌回收率均在0.5~2.0范围,控制菌检查方法可行。结论 本试验建立的方法可用于阿奇霉素微生物限度检查。
关键词:阿奇霉素、方法适用性、回收率、薄膜过滤法、倾注法
【中图分类号】 F763 【文献标识码】 A 【文章编号】2107-2306(2022)06--02
ABSTRACT OBJECTIVE: To establish a method for microbial limit test of azithromycin. METHODS:The test was carried out according to the biological examination method of the fourth part of the 2020 edition of Chinese Pharmacopoeia principles. The recovery rate was determined by adding 5 experimental bacteria such as Pseudomonas aeruginosa.RESULTS:The total number of aerobic bacteria was membrane filtration method, and the number of mold and yeastwas pouring method. The recovery rate of each test bacteria was in the range of 0.5~ 2.0. The method of controlbacteria examination was feasible.CONCLUSION: The established method can be used for the microbial limit test of azithromycin.
KEYWORDS Azithromycin; Method applicability recovery; Membrane fitration;Pour method
阿奇霉素属于大环内酯类的第二代抗生素[1],抗菌谱广泛,尤其对需氧菌和厌氧菌的抗菌能力更加显著,为临床应用带来了活力[2-3]。用于治疗化脓性链球菌引起的急性咽炎或者是扁桃体炎或者是敏感细菌引起的鼻窦炎、中耳炎、急性支气管炎以及慢性支气管炎急性发作时的一种药物[4]。阿奇霉素因具有强力杀灭病原微生物的作用在临床治疗中广泛应用,对其治疗机制的分析和探讨发现,阿奇霉素一方面通过杀灭病原微生物来降低感染引起的炎症反应、平息免疫活化,表现出对先天免疫系统中性粒细胞趋化和巨噬细胞极化的影响,另一方面以某种机制对后天免疫系统的 T 细胞活化和细胞因子表达有显著调节作用[4]。随着阿奇霉素在临床上的应用越来越广泛,为使临床用药更加安全有效,实施微生物限度检查是确保药品卫生质量的重要途径。
本研究参考《中国药典》2020年版四部生物检查法[5],建立了阿奇霉素的微生物限度检查方法,该方法可为其他大环内酯类抗生素药物微生物限度检查法的建立提供参考,同时为药品检验机构及生产企业建立品种2020年版药典微生物限度检查法提供借鉴。
1. 仪器和材料
1.1仪器
YXQ-LS-100G立式压力蒸汽灭菌器(上海博迅医疗生物仪器股份有限公司);生物安全柜(苏净安泰空气技术有限公司);BSP-150生化培养箱(上海博迅医疗生物仪器股份有限公司);BMJ-400C霉菌培养箱(上海博迅医疗生物仪器股份有限公司)。
1.2供试品
阿奇霉素(批号:C08-202101001、C08-202101003、C08-202109001)生产商为黄石世星
1.3菌种
金黄色葡萄球菌[CMCC(B)26003]、铜绿假单胞菌[CMCC(B)10104]、枯草芽孢杆菌[CMCC(B)63501]、大肠埃希菌[CMCC(B)44102]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003],以上菌种均购自中国食品药品检定研究院。
1.4培养基
pH7.0无菌氯化钠-蛋白胨缓冲液,批号2001092;胰酪大豆胨琼脂培养基,批号190827;胰酪大豆胨液体培养基,批号190815;沙氏葡萄糖琼脂培养基,批号190509;沙氏葡萄糖液体培养基,批号2010092;麦康凯琼脂培养基,批号201223;麦康凯琼液体培养基,批号2018042。(以上培养基均来源于北京三药技术有限责任公司。)
2. 实验方法
2.1菌液的制备
参照2020年版《中國药典》四部通则1105微生物计数法项下方法制备。将阳性菌菌液稀释10-3~10-7倍,使菌落数不大于100cfu/ml。
2.2 供试液的制备
取阿奇霉素10g,加入pH7.0氯化钠-蛋白胨缓冲液100ml中,混匀,即得供试液Ⅰ(100mg/ml);再用pH7.0无菌氯化钠-蛋白胨缓冲液稀释,别配制成供试液Ⅱ(20mg/ml)、供试液Ⅲ(10mg/ml)、供试液Ⅳ(5mg/ml),备用。
2.3 計算公式及接受标准
试验组比值=(试验组菌落数-供试品对照组菌落数)/菌液对照组菌落数。
所得比值均应在0.5~2.0范围内。
2.4微生物总数计数方法验证
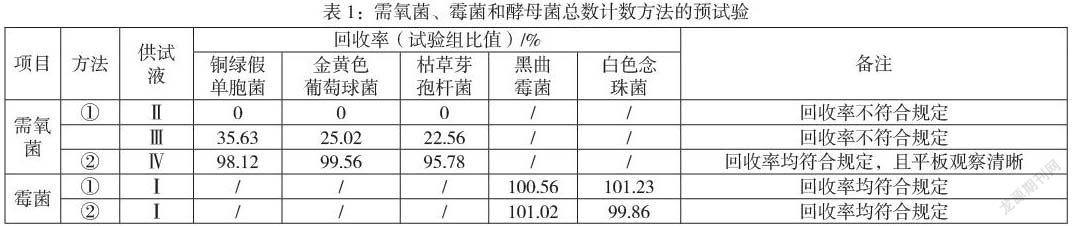
2.4.1需氧菌总数计数(预试验):分别取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌为试验菌,分别对供试液进行处理。①分别取供试液Ⅱ和Ⅲ各1ml,用0.1%无菌蛋白胨水溶液冲洗1000ml,每次100ml。②取供试液Ⅳ1ml,加置100ml 0.1%无菌蛋白胨水溶液中,全量通过一次性薄膜过滤器后,再用0.1%无菌蛋白胨水溶液冲洗400ml,每次100ml,冲洗最后100ml时加入菌悬液。
2.4.2霉菌和酵母菌总数计数(预试验):以黑曲霉菌和白色念珠菌为试验菌,分别采用2种方法对供试品进行试验。①取供试液Ⅰ1ml平皿法测定;②取供试液Ⅰ1ml,采用0.1%无菌蛋白胨水溶液500ml薄膜过滤冲洗,冲洗最后100ml时加入菌悬液。结果见表1:
2.5微生物计数方法适用性
通过预试验,确认需氧菌总数计数使用方法②,霉菌和酵母菌总数计数使用方法①。根据此结论进行三次平行试验[5]确认。
2.5.1试验组:需氧菌总数取供试液Ⅳ1ml,加置100ml 0.1%无菌蛋白胨水溶液中,全量通过一次性薄膜过滤器后,再用400ml 0.1%无菌蛋白胨水溶液冲洗4次,每次100ml,冲洗最后100ml时加入小于100cfu菌悬液的1ml,冲洗后取出贴膜于胰酪大豆胨琼脂培养基平板上,每株试验菌平行制备两个平皿,置30~35℃培养3~5天;霉菌和酵母菌总数取供试液Ⅰ1ml,置无菌平皿中,注入15~20ml温度不超过45℃溶化的沙氏葡萄糖琼脂培养基,混匀,凝固,每株试验菌平行制备两个平皿。置20~25℃培养5天,逐日观察结果。
2.5.2供试品对照组:取不加入菌液的供试液,同法测定其微生物数。
2.5.3菌液对照组:取稀释液代替供试液,同法操作加入试验菌液并进行微生物回收试验。
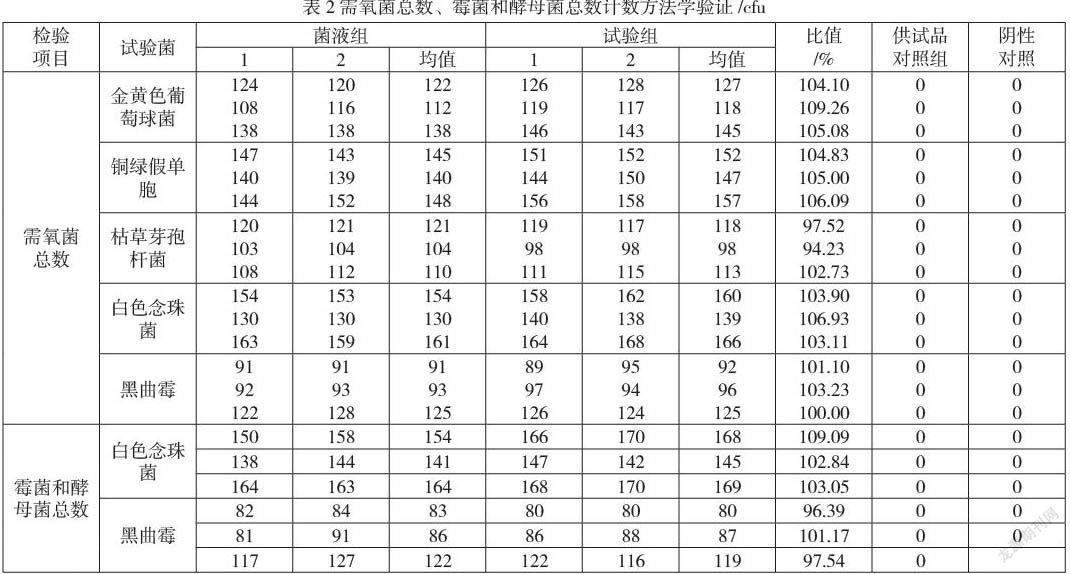
结果:5株需氧菌、2株真菌的回收比值均在0.5~2之间,符合药典规定,因此可照此方法进行阿奇霉素胶囊的需氧菌总数、霉菌和酵母菌总数计数。见表2。
2.6控制菌检查方法的验证
根据《中国药典》2020年版要求,控制菌检查只需检查大肠埃希菌。
试验组:取供试液Ⅰ 10mL,用微生物限度检验仪立即过滤,再用500ml的0.1%无菌蛋白胨水溶液冲洗5次(100ml/次),在最后一次冲洗液中加入不大于100cfu的大肠埃希菌菌悬液1ml,过滤后,取出滤膜接种至100ml的胰酪大豆胨液体培养基中。
菌液对照组:取不大于100cfu的大肠埃希菌,接种至100ml的胰酪大豆胨液体培养基中。
阴性对照组:取0.1%无菌蛋白胨水溶液500ml薄膜过滤冲洗后,滤膜接种置100ml胰酪大豆胨液体培养基中。均按药典方法培养。
结果:控制菌选用稀释10-6倍的大肠埃希菌,三批供试品进行三次平行验证,结果为试验组和阳性组均检出大肠埃希菌生长,而阴性组均未检出,表明适用性试验符合药典标准。
3 讨论
通过上述一系列试验,验证阿奇霉素对真菌无抑制作用,因此,采用倾注法进行霉菌和酵母菌总数测定。试药对细菌生长有强抑制作用,对于抑菌作用较强的供试品,应尽量选用薄膜过滤法进行试验[6]。阿奇霉素对金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、大肠埃希菌都较敏感,因此本次验证中需氧菌总数通过提高稀释倍数+薄膜过滤来进行验证(取1︰200的供试液1mL,每膜冲洗500mL,100mL/次)。经过验证,大肠埃希菌检查采用薄膜过滤法(每膜冲洗500mL,100mL/次),可有效消除供试品自身杀菌和抑菌作用,与不加供试液的阳性对照比较,生长正常。
检查方法中干扰因素较多,易影响计数结果,如培养条件、培养基、加菌浓度及加菌量等[7-8]。采用薄膜过滤法试验时,先将供试液加至100ml冲洗液中,可使含量均匀,避免药液中少量沉淀而堵塞滤膜导致过滤困难,更有利于供试液中微生物的回收。
参考文献:
[1] 阿奇霉素的免疫治疗机制[J].中国免疫学杂志 2021 年第 37 卷1768-1771.
[2]许银芝,申超宇. 大环内酯类抗生素应用的调查分析 [J].中国药业, 2002, 11(2): 63.
[3]刘素霞.阿奇霉素的药理及其临床应用观察[J].甘肃科技,2014,30(21):129-130.
[4]国家药典委员会.中国药典(四部)[S].北京:中国医药科技出版2020.
[5] SHI J,LIU Y,ZHANG Y,et al. PA5470 counteracts antimicro‐bial effect of azithromycin by releasing stalled ribosome in pseudo‐monas aeruginosa[J]. Antimicrob Agents Chemother.2018,62(2)
[6] 陈伟盛, 关倩明, 朱荣峰, 等. 药品微生物限度检查中微生物污染的鉴定和溯源分析 [J]. 药物分析杂志, 2014, 34(1):58-63.
[7] 殷建国. 微生物限度检查应注意的若干问题 [J]. 中国药事,2004, 18(7): 456.
[8] WEINBERGER M,LESSER D. Diffuse panbronchiolitis:A progressive fatal lung disease that is curable with azithromycin,butonly if diagnosed[J].Pediatr Pulmonol,2019,54(4):457-462. DOI:10. 1002/ ppul. 24226.
