减盐增鲜的豌豆肽美拉德反应产物制备及其风味分析
2022-03-30于静洋崔和平夏书芹张晓鸣
严 方, 于静洋, 崔和平, 夏书芹, 张晓鸣
(江南大学 食品学院,江苏 无锡 214122)
食盐是饮食中不可缺少的调味品,摄入过多则带来很多健康问题[1],减盐已经被全球公认为最具有成本效益的慢性病干预策略之一。 受到传统饮食文化等因素的影响, 我国居民食盐摄入量居高不下。 通过低钠饮食改善国民健康现状、提高人民生活质量已经成为全社会关注的热点问题。 虽然人们在低钠盐开发方面进行了积极探索,却由于其牺牲食品口味的代价而难以从根本解决国民食盐摄入过量的问题。 提出“科学减盐、技术减盐”的有效方法,是我国社会亟待解决的重要民生问题,也是食品行业技术创新的必然要求。
为了实现科学减盐,人们采用其他金属元素的无机盐取代钠盐[2],以氯化钾和硫酸镁为添加剂的低钠盐已在市场流通,但其成本高、后苦味重,很难被消费者广泛接受, 并且钾离子增加心脏负担,对心脏病、肾功能不全、高血钾等病症患者并不适用[3]。近年来,有关咸味肽的研究逐渐成为风味领域的关注热点,为食盐替代物的研发开辟了新的方向[4]。
虽然小分子咸味肽可以作为咸味强化剂用于食品的减盐增咸,但是通过提取或合成法来制备特定小肽过程复杂、成本较高。 研究表明,采用酶解技术将食源性蛋白质水解为肽, 再添加至食品中,对食品风味具有显著的改善作用[5],为了兼顾食品鲜味、醇厚味和整体香气的提升,可以将蛋白质酶解产物进行美拉德反应,得到挥发性小分子香气物质及改善醇厚味的美拉德肽[6-8]。 目前,国内外生产美拉德反应产物 (Maillard reaction products,MRPs)的主要原料是动植物蛋白。 动物蛋白原料成本高、冷链运输和储藏过程中内源酶活性不稳定,导致产品质量难以标准化,且随着出口食品安全性要求的提高, 已开始限制以动物源为原料生产的热反应产品。 植物蛋白则来源广泛、价格低廉,质量稳定可靠。
与常见的大豆、玉米等蛋白质相比,豌豆蛋白作为新型植物基原料,具有非过敏原、非转基因的优点。 同时,豌豆蛋白是豌豆淀粉工业化生产而得的副产物,主要用于饲料生产。 为提高豌豆蛋白附加值,实现植物蛋白资源综合利用,以豌豆蛋白作原料,利用酶解技术对豌豆肽进行定向制备,以水解度(degree of hydrolysis,DH)和固形物溶出率为参数对酶解工艺进行优化,以豌豆蛋白为反应物进行美拉德反应, 研究美拉德反应初始pH 对MRPs 褐变程度、增味效果(咸味、鲜味和醇厚味)及挥发性风味成分的影响,为减盐增鲜风味产品的研发提供了指导。
1 材料与方法
1.1 材料与试剂
豌豆蛋白(蛋白质质量分数80%):烟台东方蛋白科技有限公司产品;复合蛋白酶、氨肽酶:安徽强旺调味食品有限公司产品;甲醛、氢氧化钠、盐酸、葡萄糖、L-半胱氨酸、1,2-二氯苯:中国医药集团上海化学试剂公司产品;谷胱甘肽:上海源叶生物科技有限公司产品;食盐、味精:市售食品级。
1.2 仪器与设备
AL204 电子天平、酸度计:上海梅特勒有限公司产品;集热式恒温热磁力搅拌器:巩义予华仪器有限责任公司产品;PAL-1 手持式折光仪: 广州ATAGO 科学仪器有限公司产品;高效液相色谱:沃特世科技(上海)有限公司产品;A360 型紫外可见分光光度计:上海翱艺仪器有限公司产品;SA402B 电子舌:日本INSENT 公司产品。
1.3 实验方法
1.3.1 豌豆肽的制备 称取8.0 g 豌豆蛋白于酶解罐中,加适量去离子水,调节底物质量浓度为80 g/L,于95 ℃下热处理20 min 使豌豆蛋白变性。 冷却后用6 mol/L 的 NaOH 溶液调节酶解液 pH 到 8.0,加入适量复合蛋白酶,在60 ℃条件下酶解一定时间,冷却后再向酶解液中加入适量氨肽酶, 在50 ℃条件下酶解一定时间。 反应结束后,立即置于沸水浴中灭酶10 min, 冷却后于10 000 r/min 转速下离心10 min,上清液即为豌豆蛋白肽溶液。
1.3.2 美拉德反应产物的制备 取10 g 豌豆蛋白肽溶液(相当于0.1 g 豌豆肽),加入0.15 g 葡萄糖和0.10 g L-半胱氨酸, 用 6 mol/L 的 NaOH 溶液调节混合液 pH 分别至 6.4、7.4、8.4, 然后转移到 50 mL 反应瓶中,加磁力搅拌子,旋紧密封,在油浴锅中120 ℃条件下反应1 h 后,立即冰浴终止反应。
1.3.3 水解度的测定 利用甲醛滴定法[9]测定。 水解度(DH)由样品量与滴定消耗NaOH 体积计算得到。

式中:c 为氢氧化钠标准溶液浓度,mol/L;V1为样品溶液在加甲醛后滴定至终点所消耗的NaOH 标准溶液的体积,mL;V2为空白溶液在加甲醛后滴定至终点所消耗的NaOH 标准溶液的体积,mL;V 为酶解上清液的体积,mL;m 为初始豌豆蛋白质量,g;n为豌豆蛋白原料中蛋白质质量分数,%;8 为每克豌豆蛋白中肽键毫摩尔数,mmol/g。
1.3.4 固形物溶出率的测定 参照NY/T 2637—2014 测定固形物质量分数,计算固形物溶出率。

式中:W 为固形物溶出率,%;P 为离心后上清液的固形物质量分数,%;m1为离心后上清液的质量,g;m 为样品质量,g。
1.3.5 氨基酸质量浓度的测定 采用高效液相色谱法测定。 ODS Hypersil 色谱柱(250 mm×4.6 mm),柱温 40 ℃,检测波长 338 nm,流量 1.0 mL/min。 流动相 A:0.06 mmol/L 乙酸钠,B:0.15 mmol/L 混合液(乙酸钠、乙腈、甲醇体积比为 1∶2∶2)。
1.3.6 相对分子质量的测定 采用凝胶渗透色谱法进行测定。 TSKgel 2000SWXL 色谱柱 (300 mm×7.8 mm),柱温 30 ℃,检测波长 220 nm,流量0.5 mL/min;流动相:乙腈、水、三氟乙酸体积比为40∶60∶0.1。标准曲线采用以下标准品分析绘制:细胞色素C(相对分子质量12 500)、抑蛋白酶肽(相对分子质量6 500)、杆菌肽(相对分子质量1 450)、四肽GGYR(相对分子质量451)和三肽GGG(相对分子质量189)。
1.3.7 褐变程度的测定 将样品加水稀释5 倍,用分光光度计在420 nm 处测定吸光度。
1.3.8 电子舌分析 以5 g/L 盐溶液为对照, 样品溶液配制时,保证其中盐质量浓度为5 g/L,再分别加入5 g/L MRPs 样品,混合均匀。 然后将配制好的溶液直接倒入电子舌专用测定杯中, 于室温下测定。 每个样品测定4 次,第一次测定后仪器趋于稳定,取后3 次信号数据的平均值作为样品味觉信号强度。
1.3.9 感官评定 感官评定小组由12 名经验丰富的感官评定员(23~55 岁,8 女 4 男)组成,在实验前, 每个小组成员需要先对参照品进行感官评定,以熟悉各项感官指标。 将美拉德产物以5 g/L 添加到5 g/L 盐溶液中,分别对样品溶液的咸味、鲜味和醇厚味3 项指标在0~6 分内打分,分数越高表明该滋味越强。 为避免顺序效应,样品以随机3 位数标记,并随机呈送给每个感官评定员品尝。 各滋味参照溶液及其强度评分:5 g/L 盐溶液 (咸味,3 分);5 g/L 味精溶液(鲜味,3 分);30 mmol/L 谷胱甘肽溶液(醇厚味,3 分)。 每个样品重复 3 次,取平均值为最终得分。
1.3.10 挥发性风味物质分析 采用顶空固相微萃取(HS-SPME)结合气相色谱串联质谱技术(GCMS)分析。 HS-SPME 条件:取 3.0 g MRPs 于顶空瓶中, 加入 10 μL 的 0.015 g/L 1,2-二氯苯甲醇溶液做内标,加入磁力搅拌子,迅速封盖。 插入老化过的萃取头,50 ℃下萃取30 min 后进样, 进样口温度250 ℃,解吸 7 min。 GC-MS 条件:采用 DB-WAX 毛细管柱(30 m×0.25 mm×0.25 μm),参照文献[8]测定。
1.3.11 数据分析 采用SPSS 22.0 通过Duncan 多重检验对数据进行显著性分析,P<0.05 表示存在显著性差异。
2 结果与分析
2.1 豌豆蛋白的酶解参数优化
2.1.1 复合蛋白酶的添加量 为了提高酶解效率,采用双酶分步酶解的方法水解豌豆蛋白。 首先采用复合蛋白酶(内切酶)迅速降低大分子蛋白质的相对分子质量,然后采用氨肽酶(外切酶)从肽的链端逐一水解肽键,形成游离氨基酸。 酶的添加量是影响DH 的重要因素, 通常酶的催化反应速率正比于酶的添加量, 加酶量的提高能够缩短酶解反应时间。 因此,首先考察复合蛋白酶添加量对豌豆蛋白的DH 和固形物溶出率的影响。 取8.0 g 豌豆蛋白,加水配制成80 g/L 溶液,分别加入2 000、2 500、3 000、3 500、4 000 U/g(以底物质量计)的复合蛋白酶,在 60 ℃和pH 8.0 下酶解 3 h,降温至 50 ℃后,加入300 U/g 的氨肽酶,继续酶解2 h,终止反应后测定不同加酶量条件下产物的DH 与固形物溶出率,结果见图1。
豌豆蛋白的DH 和固形物溶出率都随着复合蛋白酶加酶量的增加而增加。 加酶量越大,复合蛋白酶为底物提供的催化活性位点越多,酶促反应的最大速率越大,根据米氏方程可知,在相同底物质量浓度条件下,其酶解速率也越大。 酶解速率的提高促进蛋白质向肽的快速转化,因此在相同酶解时间条件下,加酶量越大则DH 越大。当加酶量从3 000 U/g 增加到 3 500 U/g 时,DH 增加了 2.22%,固形物溶出率增加了3.80%,增加速度最快。当加酶量超过3 500 U/g 底物时,DH 和固形物溶出率的增长速率变缓慢。 这是因为加酶量越大,酶解速率越快,底物消耗越快,根据米氏方程,底物质量浓度降低会引起酶解速率下降,最终达到平衡状态。 所以加酶量的增加虽然会加快酶解速率,同时也会加快平衡到来的时间,继续增加加酶量,DH 不会继续提高。 因此,选择3 500 U/g 为复合蛋白酶的最优添加量。 从图1 还可以看出,随着加酶量增加,DH 与固形物溶出率表现出相同的变化趋势,并且同时在3 500 U/g的加酶量下达到最大值,这是由于蛋白质或肽在水中的溶解度与其相对分子质量有密切的关系。 随着蛋白质水解的发生,大分子蛋白质逐渐变为相对分子质量较小的肽,极性基团尤其是氨基和羧基的数目增加,电荷密度增大,分散相的水溶性逐渐增加,导致酶解液的固形物溶出率逐渐提高。

图1 复合蛋白酶添加量对豌豆蛋白的DH 和固形物溶出率的影响Fig. 1 Effect of protamex protease concentration on DH and solid dissolution ratio of pea protein
2.1.2 复合蛋白酶的酶解时间 在复合蛋白酶添加量的优化基础上,进一步研究酶解时间对豌豆蛋白DH 和固形物溶出率的影响。 取8.0 g 的豌豆蛋白,加水配成80 g/L 溶液,加入3 500 U/g 的复合蛋白酶, 在 60 ℃和 pH 8.0 下分别酶解 1、2、3、4、5 h,降温至50 ℃后,加入300 U/g 的氨肽酶,继续酶解2 h,测定复合蛋白酶不同作用时间制得产物的DH 与固形物溶出率,结果见图2。
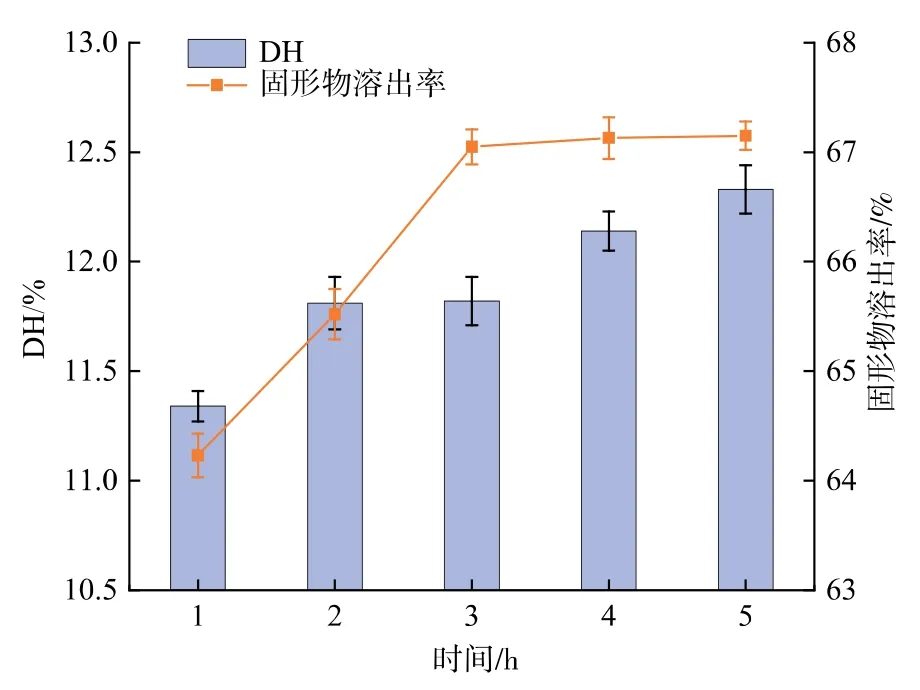
图2 复合蛋白酶的酶解时间对豌豆蛋白的DH 和固形物溶出率的影响Fig. 2 Effect of hydrolysis time by protamex protease on DH and solid dissolution ratio of pea protein
随着复合蛋白酶作用时间的延长,大分子蛋白质被逐渐水解形成相对分子质量较小的肽段,因此豌豆蛋白的DH 和固形物溶出率呈上升趋势。 DH在1~2 h 和3~4 h 时增速明显, 因为复合蛋白酶在酶解初始阶段活力较高,与底物结合充分,水解效率较高,而随着加热时间的延长,底物减少,产物质量浓度增加, 由于产物对蛋白质水解的抑制作用,使得酶活力下降, 导致酶解速率下降,DH 增速变慢。 另一方面,由于底物质量浓度远高于酶的质量浓度,在酶促反应早期可认为底物质量浓度为一个常数,酶促反应为零级反应,酶解速率不受底物质量浓度的影响;随着酶解的进行,底物质量浓度下降,反应逐渐遵循一级反应动力学,肽的形成速率随反应的进行而减小,这也会导致在水解反应后期豌豆蛋白DH 增速放缓。在酶解1~3 h 内,固形物溶出率增长迅速,在此之后趋于平稳,而3 h 后豌豆蛋白的DH 仍然持续增长。 这一结果说明酶解3 h 形成的豌豆肽即使进一步形成相对分子质量更小的肽,水溶性不再增加。 在酶解1~3 h 形成的肽,水溶性对其相对分子质量的变化更敏感。 综合考虑固形物溶出率和DH 的增长速率, 选择4 h 为复合蛋白酶的最优酶解时间。
2.1.3 氨肽酶的添加量 作为外切酶,氨肽酶对游离氨基酸的形成具有重要作用,因此进一步对氨肽酶添加量进行优化。 取8.0 g 豌豆蛋白, 加水配成80 g/L 溶液,按上述条件用复合蛋白酶酶解4 h 后,分别加入 250、300、350、400、450 U/g 的氨肽酶,在50 ℃下酶解2 h,测定不同加酶量条件下产物的DH与固形物溶出率,结果见图3。
对比图1 与图3 可知,氨肽酶在较低的加酶量水平下即可达到与复合蛋白酶相同的DH 提高幅度, 证实氨肽酶比复合蛋白酶具有更高的催化效率。 随着氨肽酶加酶量的增大,DH 随之上升。 而氨肽酶的添加量低于350 U/g 时, 固形物溶出率没有显著性变化,添加量从350 U/g 上升到400 U/g 时,固形物溶出率提高幅度最高,相比增加了2.37%。此时氨肽酶在复合蛋白酶的酶解作用基础上,持续切断肽链末端肽键,把肽彻底水解成氨基酸。 综合DH和固形物溶出率的结果, 选择400 U/g 为氨肽酶的最优添加量。
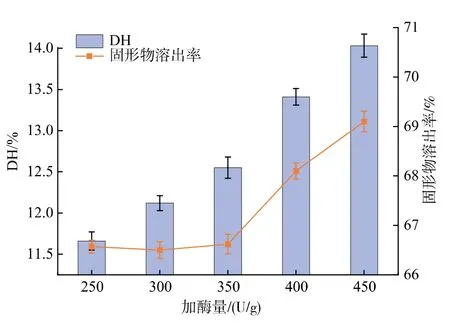
图3 氨肽酶添加量对豌豆蛋白的DH 和固形物溶出率的影响Fig. 3 Effect of aminopeptidase concentration on DH and solid dissolution ratio of pea protein
2.1.4 氨肽酶的酶解时间 取8.0 g 豌豆蛋白,加水配成80 g/L 溶液,按上述条件用复合蛋白酶酶解4 h 后,加入400 U/g 的氨肽酶,在50 ℃下分别酶解1、2、3、4、5 h,测定不同酶解时间下产物的 DH 与固形物溶出率,结果见图4。
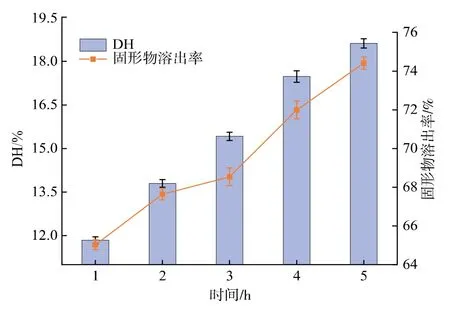
图4 氨肽酶的酶解时间对豌豆蛋白的DH 和固形物溶出率的影响Fig. 4 Effect of hydrolysis time by aminopeptidase on DH and solid dissolution ratio of pea protein
氨肽酶的酶解时间对DH 和固形物溶出率影响较大,随着酶解时间的延长,豌豆蛋白DH 与固形物溶出率显著提高。 与图2 比较可以看出,在相同的酶解时间内, 氨肽酶比复合蛋白酶对豌豆蛋白DH的提高作用更明显,并且5 h 内未达到平衡状态,表明随着酶解反应的进行与游离氨基酸的累积,产物的抑制作用并未出现, 因此在相同的酶解条件下,相比于大分子豌豆肽向小分子豌豆肽的转化平衡而言,小分子豌豆肽向氨基酸的转化平衡更难逆向移动。 此外,与复合蛋白酶酶解过程相比,随着氨肽酶酶解时间的延长,所得产物固形物溶出率的增加更为显著。 结合两步酶解过程固形物溶出率的变化规律可知,豌豆蛋白降解为大分子肽时,水溶性显著提高; 而大分子肽进一步降解为小分子肽时,在一定的相对分子质量范围内,不同相对分子质量豌豆肽的水溶性无显著差异;在小分子肽水解为游离氨基酸时,水溶性显著提高,游离氨基酸对豌豆蛋白水解产物水溶性的贡献最大。 在氨肽酶作用前2 h,豌豆蛋白的DH 增长较快,但固形物溶出率增长较慢。 延长水解时间到4 h 时,DH 和固形物溶出率增长速率均显著提高,虽然不及4 h 到5 h 的涨幅,但节约了时间成本。因此,选择4 h 为氨肽酶最优酶解时间。
综上可知,豌豆蛋白酶解最优工艺为:3 500 U/g复合蛋白酶酶解4 h,400 U/g 氨肽酶酶解4 h。 此时, 酶解液DH 达到17.48%, 固形物溶出率达到71.99%。 DH 在一定程度上也可以反映出小分子肽的质量浓度。 根据相对分子质量测定结果可知,酶解液中相对分子质量小于250 的组分占18.86%(质量分数), 相对分子质量 250 到 1 000 的组分占72.74%(质量分数), 相对分子质量大于1 000 的组分仅有8.40%(质量分数), 表明豌豆蛋白在此酶解参数下水解程度较高,大分子的蛋白质被深度水解成了小分子的氨基酸或肽类。 由表1 可知,豌豆蛋白酶解液中游离氨基酸占水解氨基酸的9.17%(质量分数), 而肽结合氨基酸占水解氨基酸的质量分数高达90.83%,肽结合氨基酸质量浓度远高于游离氨基酸,表明在酶解液中的氨基酸主要都以结合态的形式存在。 结合上述相对分子质量的结果分析可知,在此最优酶解工艺下,豌豆蛋白主要被水解为小分子肽,水解成游离氨基酸的比例较低。 有研究表明,相对分子质量低于1 000 的肽反应活性更强,与大分子肽相比,更容易发生美拉德反应[10]。

表1 豌豆蛋白酶解液的氨基酸质量浓度Table 1 Mass concentration of amino acids in pea protein hydrolysates
2.2 美拉德反应pH 对褐变程度的影响
美拉德反应过程复杂,时间、温度、pH、水分活度等参数都会对反应动力学产生影响。 其中,反应时间和温度是两个重要因素, 但前人对其报道较多,而关于反应pH 的研究较少,尤其是在产物的滋味方面。 根据前期实验可知,美拉德反应时间为1 h的产物减盐增鲜效果最佳, 随着加热时间延长到2 h 和3 h,MRPs 的减盐增鲜效果显著下降, 咸味值分别降低了4.98%和13.51%, 鲜味值分别降低了6.26%和12.98%, 因此后续研究都以1 h 为美拉德反应时间。
颜色变化是美拉德反应最直观的特征,反应液在420 nm 处吸光度可以表示反应后期类黑精等深色物质的形成程度。 由图5 可知,在相同温度下,随着初始pH 的升高,MRPs 的褐变程度呈现上升趋势,与孙方达等[11]的研究结果相符合。 pH 是影响美拉德反应路径的重要因素之一, 在酸性环境下,氨基处于质子化状态,阻碍氨基葡萄糖生成,从而抑制后续美拉德反应进行。随着初始pH 升高,美拉德反应速率变快, 加速了Amadori 重排产物及其下游褐变前体物的形成与积累,促进了类黑精生成。 而在碱性环境下, 二羰基化合物具有更强的反应活性,容易与豌豆肽侧链的胍基、氨基或咪唑基发生羰氨反应进而交联形成类黑精大分子。 此外,碱性条件有利于糠醛与α-羟基醛发生羟醛缩合引起环状呈色物质的形成。 碱性条件还可活化呋喃与吡咯的α 位碳的氢键,通过亲电取代反应引起呋喃醛或吡咯醛之间的聚合,这也是类黑精形成的重要途径。
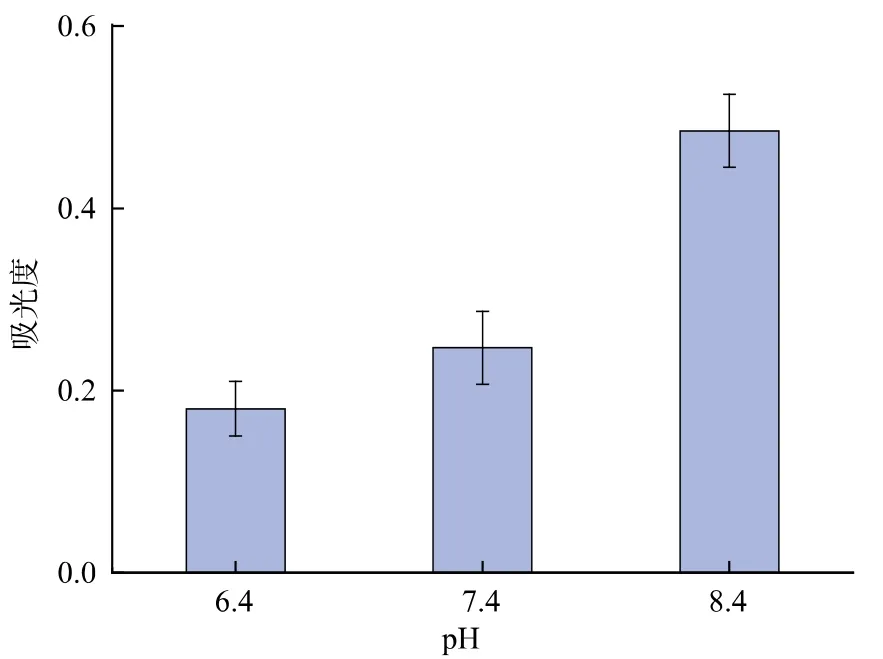
图5 反应pH 对MRPs 的褐变程度的影响Fig. 5 Effect of reaction pH values on the browning degree of MRPs
2.3 美拉德反应pH 对滋味的影响
MRPs 的主要呈味功能是增强咸味食品的醇厚味[12],同时作者发现豌豆肽MRPs 具有增咸和增鲜功能,为此,通过电子舌分析不同初始pH 下产物的咸味、鲜味增强效果,结果见表2。 与5 g/L NaCl 溶液对照组相比,加入5 g/L MRPs 后,溶液鲜味和咸味响应值都有了不同程度的提高, 这表明MRPs 具有增咸增鲜的效果。 同时,pH 越高,MRPs 的增咸和增鲜效果越佳,尤其是在pH 8.4 条件下,溶液的鲜味较另外两个样品分别增长了36.48%和21.27%,咸味较另外两个样品分别增长了57.30%和27.61%;与NaCl 对照组相比,咸味、鲜味分别提高了41.03%和303.39%。有研究表明,氨基酸或小分子肽具有滋味增强作用。 在提高初始pH 的情况下加速了氨基酸发生美拉德反应, 可能促进一些呈味肽的生成,进而促使产物增咸、增鲜的效果得到提升。 如从牛肉汤中分离出来的Alapyridaine[13]、从鱼露中分离出来的精氨酸二肽等[14]都曾被报道具有咸味或鲜味。此外, 在pH 8.4 的初始条件下进行美拉德反应,产物的最终pH 降到了7 左右,也避免了在低pH 下产生的酸涩味会对整体滋味起负面作用。

表2 电子舌测定的MRPs 增味效果Table 2 Taste enhancement of MRPs measured by electronic tongue
电子舌是一种模拟人的味觉感受机理研制出的智能检测系统,可以以数字化的形式快速对食品的多种基本滋味指标进行评价。 牛云蔚等利用感官评定和电子舌对樱桃酒的多种滋味进行比较,得出两者结果相关性很高[15]。 但并没有研究表明电子舌可以完全取代感官评价,且醇厚味是美拉德反应过程中形成的特征性滋味,电子舌无法测定,仅仅能通过感官评定法来分析。 感官评定结果表明(见表3), 随着初始 pH 的增加,MRPs 的增味效果都显著增加。 对于咸味和鲜味来说,感官评定与上述电子舌分析结果一致。 结合这两种滋味分析方法可知,在相同的盐质量浓度下, 添加一定量的MRPs 可以在不降低咸味的情况下,减少盐的摄入,达成“科学减盐”和“减盐不减咸”的目标。

表3 感官评定获得的MRPs 的增味效果Table 3 Taste enhancement of MRPs measured by sensory evaluation
2.4 美拉德反应pH 对挥发性风味物质的影响
挥发性风味物质的组成和质量分数在一定程度上共同决定了样品的香气特征,因此,通过GCMS 检测不同初始反应pH 下MRPs 的挥发性化合物,结果见表4。 3 个样品中检测到的挥发性风味物质分别为 69.78、82.71、125.94 ng/g,表明反应 pH 对美拉德产物的挥发性物质有着较大的影响。 提高反应pH 可以促进Amadori 化合物及氨基酸的降解、脱氧糖酮的环化与裂解等反应的发生,促进小分子挥发性物质的形成。 不同pH 条件下制备的豌豆肽MRPs 挥发性风味物质种类差别不大, 以酮类和醛类为主,还有少量含氮类和呋喃类化合物。

表4 不同初始pH 条件下制备的MRPs 挥发性风味物质的组成和质量分数Table 4 Composition and mass fraction of volatile flavor compoundsof MRPs prepared at different initial pH
醛类化合物在3 个样品中分别为41.47、44.52、92.40 ng/g,是主要的风味物质,且因为它的阈值较低,对样品风味的贡献程度比较大。 醛类主要是由脱氧糖酮逆醛化或氨基酸Strecker 降解产生的,在所有样品中均检出了己醛、壬醛和苯甲醛。 己醛和壬醛主要呈现出花果香味[16],而苯甲醛具有樱桃或苦杏仁香味[17]。
在美拉德反应中,含氮化合物由氨基酸羰氨缩合并进一步降解生成,氨基在较低的pH 下质子化,无法进行亲核进攻,因此较难形成含氮挥发性风味物质。 含有坚果、焙烤风味的吡嗪、2-甲基吡嗪只有在pH 大于7.4 时才生成, 含氮化合物总含量随着pH 的升高而增加,这与前人的研究结果一致[18]。 呋喃化合物具有水果、焦糖香,可能是由还原糖降解生成的,虽然其含量较低,但对美拉德产物整体香气也起到了一定的修饰作用[19]。 综上分析,初始pH的提高可以促进MRPs 挥发性风味物质释放, 在提高滋味的同时,使整体香气更浓郁。
3 结 语
以豌豆蛋白为原料,采用酶解技术与美拉德反应相结合的方法,制备了具有滋味(咸味、鲜味和醇厚味)增强及整体风味浓郁的产物。 优化后的豌豆肽制备工艺为双酶分步酶解: 先加入3 500 U/g 的复合蛋白酶,在60 ℃、pH 8.0 下酶解4 h,然后加入400 U/g 的氨肽酶,在50 ℃下继续酶解4 h,在此条件下得到的豌豆蛋白酶解液的DH 为17.48%,固形物溶出率为71.99%,酶解液中相对分子质量小于1 000 的组分占91.60%(质量分数), 肽结合氨基酸
占总氨基酸的90.83%(质量分数),酶解产物主要是小肽。 在美拉德反应中, 初始pH 分别调节到6.4、7.4 和 8.4, 发现 MRPs 的褐变程度随着 pH 的提高而提高。 由电子舌分析和感官评定法的共同结果可知, 在相同的盐质量浓度下,5 g/L 的MRPs 具有增强咸味、鲜味和醇厚味的作用,且pH 越高,增味作用越强, 这也意味着添加MRPs 可以达到一定的减盐不减咸效果。 GC-MS 结果表明,提高pH 可以加快美拉德反应速率,增加MRPs 挥发性风味物质。目前,由于美拉德反应的复杂性,MRPs 增加滋味的机理尚未明晰,后续可以从味觉受体和味觉感知生理学等方面进一步探究。
