指纹图谱、多成分定量分析及化学模式识别分析相结合的心安胶囊质量评价
2022-03-29李艳荣杜义龙沈莹吴哲王狄鑫赵胜男潘海峰
李艳荣 杜义龙 沈莹 吴哲 王狄鑫 赵胜男 潘海峰

中圖分类号 R286.0 文献标志码 A 文章编号 1001-0408(2022)06-0706-07
DOI 10.6039/j.issn.1001-0408.2022.06.10
摘 要 目的 建立指纹图谱、多成分定量分析和化学模式识别分析相结合的心安胶囊质量评价方法。方法 采用高效液相色谱(HPLC)法,结合《中药色谱指纹图谱相似度评价系统(2012版)》建立24批心安胶囊的指纹图谱,并进行相似度评价,确定共有峰;采用同一HPLC法测定心安胶囊中牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷和异槲皮素的含量;以指纹图谱共有峰峰面积为变量,采用MetaboAnalyst 5.0工具绘制聚类分析(CA)热图,采用SIMCA 14.1软件进行主成分分析(PCA)和偏最小二乘法-判别分析(PLS-DA)。结果 24批心安胶囊共有12个共有峰,相似度均大于0.97;指认出绿原酸、牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷和异槲皮素6个共有峰。牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷、异槲皮素检测质量浓度的线性范围分别为2.36~151.35、9.15~585.20、1.20~76.50、0.68~43.20、0.44~27.90 µg/mL(r均大于0.999);精密度、重复性、稳定性(24 h)试验的RSD均小于2.00%;平均加样回收率分别为95.80%(RSD=0.96%,n=6)、102.10%(RSD=0.93%,n=6)、103.26%(RSD=1.28%,n=6)、103.89%(RSD=0.73%,n=6)、102.09%(RSD=1.79%,n=6)。5种成分的含量分别为0.988 8~1.559 1、4.336 6~11.220 1、0.065 1~0.830 5、0.043 8~0.692 5、0.023 2~0.427 2 mg/粒。CA、PCA结果显示,24批样品可分成3类,S1~S15为一类,S16~S18为一类,S19~S24为一类;PLS-DA发现,6号峰对应成分和牡荆素葡萄糖苷(7号峰)、牡荆素鼠李糖苷(8号峰)、金丝桃苷(10号峰)、异槲皮素(11号峰)的变量重要性投影值均大于1。结论 所建立的HPLC指纹图谱、多成分定量方法简单、可行,结合化学模式识别分析可用于心安胶囊的质量控制;牡荆素葡萄糖苷、牡荆素鼠李糖苷等可能是影响各批样品质量的差异标志物。
关键词 心安胶囊;高效液相色谱法;指纹图谱;多成分定量分析;聚类分析;主成分分析;偏最小二乘法-判别分析;质量控制
Quality evaluation of Xin’an capsules by combination of fingerprint, multi-component quantitative analysis and chemical pattern recognition analysis
LI Yanrong1,DU Yilong1,SHEN Ying2,WU Zhe1,WANG Dixin1,ZHAO Shengnan1,PAN Haifeng1(1. Institute of Traditional Chinese Medicine/Key Laboratory of Traditional Chinese Medicine Research and Development of Hebei Province, Chengde Medical University, Hebei Chengde 067000, China; 2. Chengde Yushi Jindan Pharmaceutical Co., Ltd., Hebei Chengde 068150, China)
ABSTRACT OBJECTIVE To establish a method for quality evaluation of Xin’an capsule by combining fingerprint, multi-component quantitative analysis and chemical pattern recognition analysis. METHODS High performance liquid chromatography (HPLC) combined with Similarity Evaluation System of TCM Chromatogram Fingerprint (2012 edition) were used to establish the fingerprints of 24 batches of Xin’an capsules and evaluate the similarity. The common peaks were determined. The contents of glucosylvitexin, rhamnosylvitexin, vitexin, hyperoside and isoquercetin in Xin’an capsules were determined by the same HPLC method. Taking the common peak area of fingerprint as the variable, MetaboAnalyst 5.0 tool was used to draw the cluster analysis (CA) heat map. SIMCA 14.1 software was used to perform principle component analysis (PCA) and partial least squares-discriminant analysis (PLS-DA). RESULTS Twelve common peaks were identified with the similarity greater than 0.97. Six common peaks were identified as chlorogenic acid, glucosylvitexin, rhamnosylvitexin, vitexin, hyperoside and isoquercetin. The linear range of glucosylvitexin, rhamnosylvitexin, vitexin, hyperoside and isoquercetin were 2.36-151.35, 9.15-585.20, 1.20-76.50, 0.68-43.20, 0.44-27.90 µg/mL(all r>0.999). RSDs of precision, repeatability and stability (24 h) tests were all less than 2.00%. The average recoveries were 95.80% (RSD=0.96%, n=6), 102.10% (RSD=0.93%, n=6), 103.26% (RSD=1.28%, n=6), 103.89% (RSD=0.73%, n=6) and 102.09% (RSD=1.79%, n=6), respectively. The contents of the five components were 0.988 8-1.559 1, 4.336 6-11.220 1, 0.065 1-0.830 5, 0.043 8-0.692 5 and 0.023 2-0.427 2 mg/grain, respectively. The results of CA and PCA showed that 24 batches of samples could be divided into three categories, i.e. S1-S15, S16-S18 and S19-S24. PLS-DA showed that variable importance in projection values of the corresponding component of peak 6 and glucosylvitexin (peak 7), rhamnosylvitexin (peak 8), hyperoside (peak 10) and isoquercetin (peak 11) were greater than 1. CONCLUSIONS The established HPLC fingerprint and multi-component quantitative method are simple and feasible. Combined with chemical pattern recognition analysis, it can be used for the quality control of Xin’an capsules. Glucosylvitexin, rhamnosylvitexin and other components may be differentital markers affecting the quality of each batch of samples.
KEYWORDS Xin’an capsules; high performance liquid chromatography; fingerprint; multi-component quantitative analysis; cluster analysis; principal component analysis; partial least squares-discriminant analysis; quality control
心安胶囊是以山楂叶提取物为原料制成的胶囊剂,具有扩张冠状血管、改善心肌供血、降低血脂的作用,可用于临床治疗冠心病、心绞痛、高血压等心脑血管疾病[1]。现代研究表明,山楂叶的主要有效成分为黄酮类成分,包括牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷和异槲皮素等,具有调节脂质和糖代谢、护肝、抗氧化、扩张冠状动脉等多种药理活性[2-4]。现行标准仅通过测定总黄酮的含量来对心安胶囊进行质量控制[1],而已有文献则多集中于心安胶囊的指纹图谱研究和含量测定[5-7]。由此可见,现有质量研究尚不全面,数据分析方法较为单一,也未就质量差异原因进行分析,不能全面反映心安胶囊的内在质量和不同生产企业产品的质量差异。
中药色谱指纹图谱能体现中药成分的整体性和复杂性,强调共有峰归属和相似度评价,是目前符合中药特点的评价模式之一,但已知成分共有峰的含量难以确定[8-9],故在指纹图谱基础上进行多成分定量测定可弥补上述不足。基于中药化学成分的复杂性,指纹图谱技术结合化学模式识别分析能真实、形象地反映中药的质量差异,揭示其复杂成分之间的规律,已被广泛应用于药物的质量控制、差异标志物的筛选[10-11]。聚类分析(cluster analysis,CA)是根据样本特征进行分类的一种多元分析技术,常以指纹图谱为基础,对中药及其制剂进行区分鉴别[12]。主成分分析(principal component analysis,PCA)是一种利用降维技术将多个指标转化为少数几个具代表性的综合指标的无监督模式识别方法,可简单、直观地对样品进行分类[13-14]。偏最小二乘法-判别分析(partial least squares-discriminant analysis,PLS-DA)是一种有监督的模式识别方法,适用于区别两类或多类样品,在中药质量综合分析中有较广泛的应用[15-16]。鉴于此,本文采用高效液相色谱(high performance liquid chromatography,HPLC)法,建立了24批心安胶囊的指纹图谱,测定了其中牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷和异槲皮素5种黄酮类成分的含量,同时结合CA、PCA、PLS-DA等化学模式识别技术对样品数据进行深入分析,筛选差异标志物,以期为全面、客观、准确地评价其质量提供依据。
1 材料
1.1 主要仪器
本研究所用主要仪器有Agilent 1200型HPLC仪及配备的二极管阵列检测器(diode-array detector,DAD)、在线脱气机、四元泵、自动进样器、柱温箱(美国Agilent公司),KQ-700型超声波清洗器(昆山市超声仪器有限公司),AG-254十万分之一电子分析天平(瑞士Mettler Toledo公司)等。
1.2 主要药品与试剂
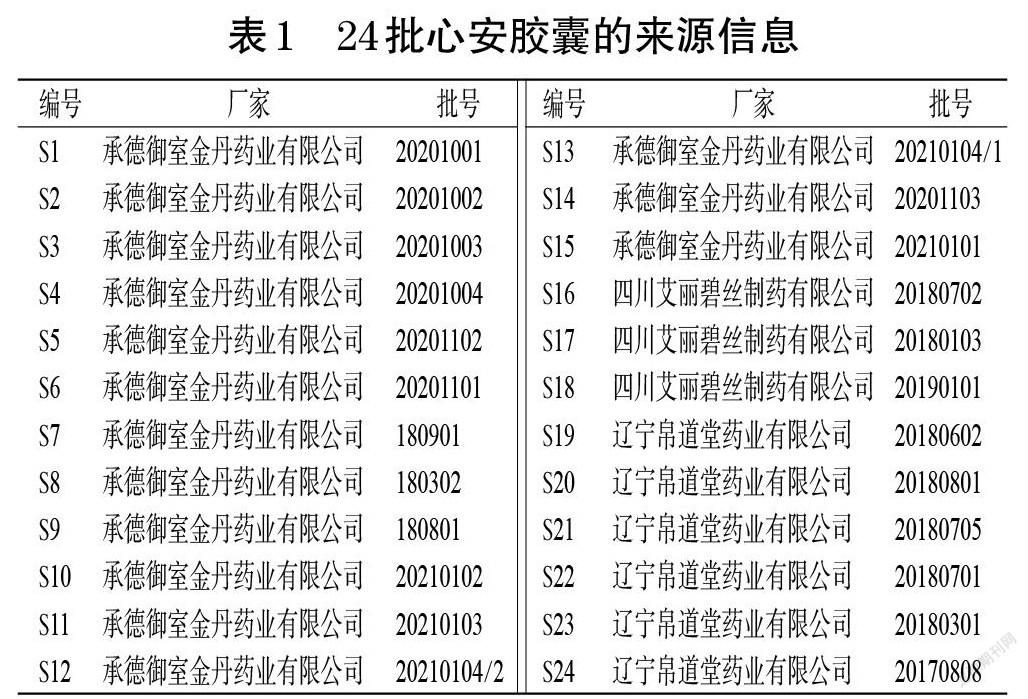
绿原酸对照品(批号18071907)、牡荆素葡萄糖苷对照品(批号20042305)、牡荆素鼠李糖苷对照品(批号18060103)、牡荆素对照品(批号16070601)、金丝桃苷对照品(批号19103001)、异槲皮素对照品(批号18062702)均购自成都普菲德生物科技有限公司,纯度均不低于98%。甲醇、乙腈为色谱纯,甲酸为分析纯,水为纯净水。24批心安胶囊由3家企业提供,规格均为每粒含总黄酮80 mg,其来源信息见表1。
2 方法与结果
2.1 色谱条件
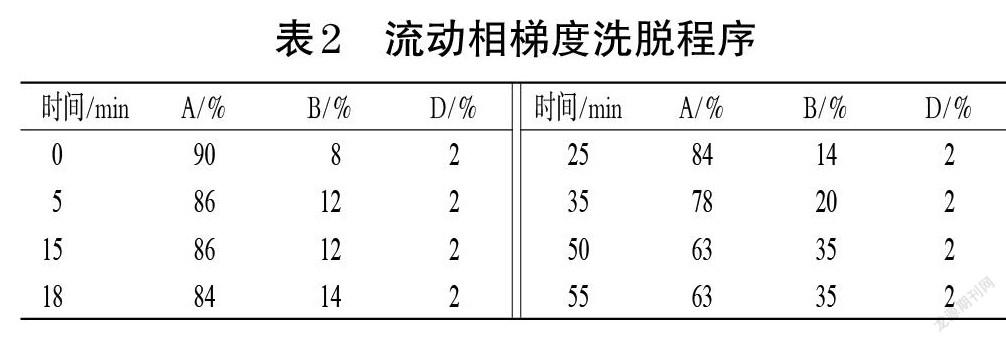
色谱柱为Agilent ZORBAX SB-C18色谱柱(4.6 mm×250 mm,5 μm);流动相为0.1%甲酸溶液(A)-乙腈(B)-四氢呋喃(D),梯度洗脱程序见表2;流速为1.0 mL/min;柱温为30 ℃;检测波长为340 nm;进样量为10 μL。
2.2 溶液的制备
2.2.1 混合对照品溶液 分别精密称取绿原酸、牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷、异槲皮素对照品适量,分别置于10 mL量瓶中,用甲醇溶解并定容,制成质量浓度分别为1.05、1.01、1.06、1.02、0.96、0.93 mg/mL的单一对照品贮备液。分别取上述各對照品贮备液适量,置于同一量瓶中,以50%甲醇为溶剂,制成绿原酸、牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷、异槲皮素质量浓度分别为38.44、75.40、294.30、38.25、21.60、13.95 μg/mL的混合对照品溶液。
2.2.2 供试品溶液 随机取10粒心安胶囊,称定其总质量。将胶囊内容物倒出,擦净胶囊壳,称定10粒胶囊壳总质量,计算平均粒重:平均粒重=(胶囊总质量-胶囊壳总质量)/10。将胶囊内容物研细,取细粉约0.5 g,精密称定,置于具塞三角瓶,精密加入60%甲醇25 mL,称定质量,超声(功率250 W,频率40 kHz,下同)30 min,放冷,再次称定质量,用60%甲醇补足减失的质量,取上清液,以12 000 r/min离心10 min,用0.45 μm微孔滤膜滤过,取续滤液,即得。
2.3 指纹图谱分析
2.3.1 精密度试验 取心安胶囊样品(编号S1),按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件连续进样6次,记录色谱图。以牡荆素葡萄糖苷色谱峰为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间的RSD均小于2.00%,相对峰面积的RSD均小于3.00%,表明方法精密度良好。
2.3.2 重复性试验 取心安胶囊样品(编号S1),按“2.2.2”项下方法平行制备供试品溶液,共6份,按“2.1”项下色谱条件进样测定,记录色谱图。以牡荆素葡萄糖苷色谱峰为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间的RSD均小于2.00%,相对峰面积的RSD均小于3.00%,表明方法重复性良好。
2.3.3 稳定性试验 取心安胶囊样品(编号S1),按“2.2.2”项下方法制备供试品溶液,分别于室温下放置0、2、4、8、12、24 h时按“2.1”项下色谱条件进样测定,记录色谱图。以牡荆素葡萄糖苷色谱峰为参照峰,计算各共有峰的相对保留时间和相对峰面积。结果显示,各共有峰相对保留时间的RSD均小于2.00%,相对峰面积的RSD均小于3.00%,表明供试品溶液在室温下放置24 h内稳定。
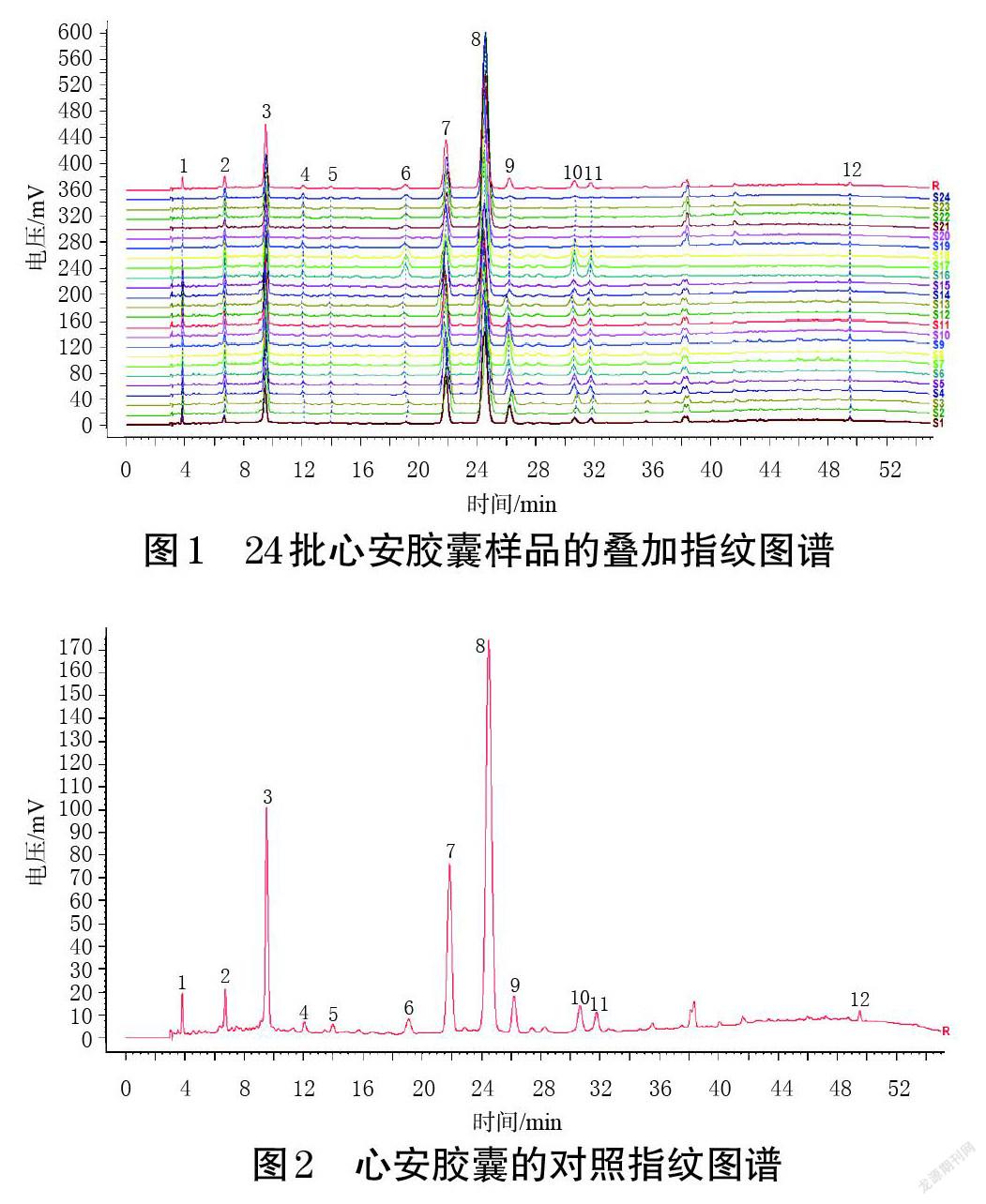
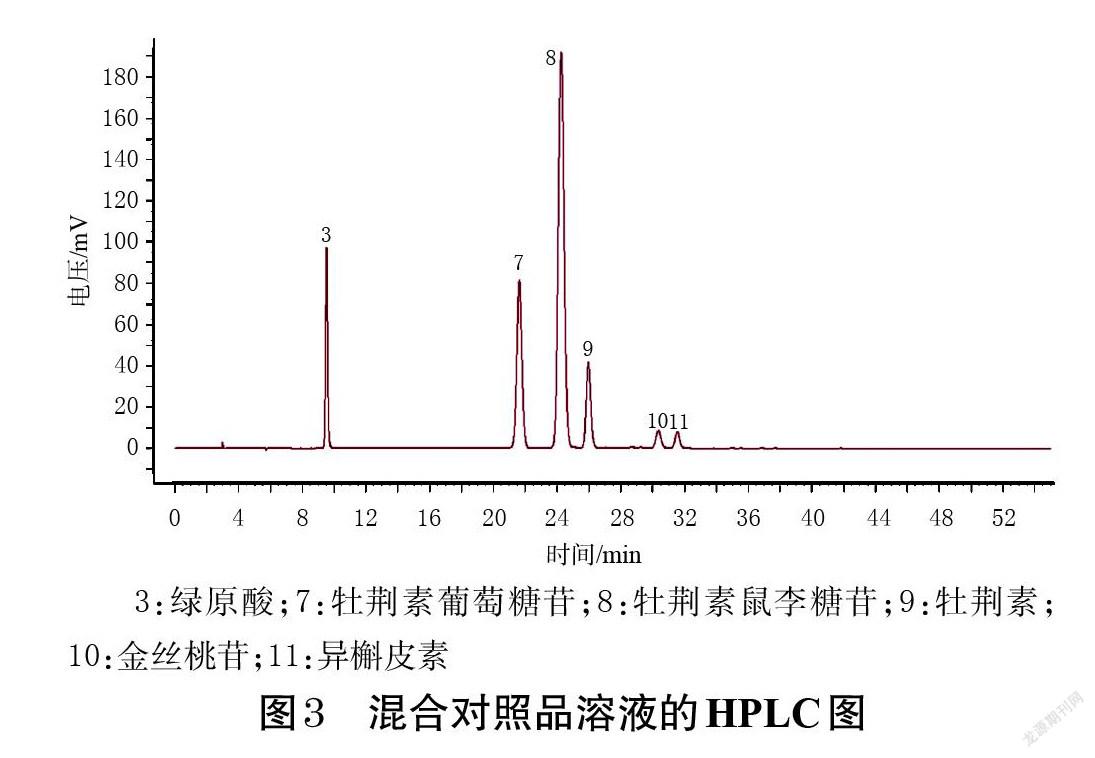
2.3.4 指纹图谱的建立、相似度评价及共有峰指认 取24批心安胶囊样品,分别按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,记录色谱图。将所得色谱图的“AIA”格式文件导入《中药色谱指纹图谱相似度评价系统(2012版)》进行分析,设S11图谱为参照图谱,采用中位数法自动匹配后生成24批心安胶囊样品的叠加指纹图谱和对照指纹图谱(图1、图2)。结果显示,24批心安胶囊样品有12个共有峰。24批心安胶囊样品图谱与对照指纹图谱的相似度分别为0.993、0.993、0.991、0.990、0.992、0.991、0.980、0.972、0.977、0.992、0.992、0.991、0.990、0.991、0.991、0.989、0.988、0.987、0.983、0.983、0.977、0.982、0.985、0.982,均大于0.97,提示样品图谱与对照指纹图谱具有较高的相似度,各批样品的化学成分整体类似。经与混合对照品色谱图(图3)比对,共指认出6个色谱峰,分别为绿原酸(3号峰)、牡荆素葡萄糖苷(7号峰)、牡荆素鼠李糖苷(8号峰)、牡荆素(9号峰)、金丝桃苷(10号峰)、异槲皮素(11号峰)。
2.4 多成分定量测定
2.4.1 专属性考察 取心安胶囊样品(编号S1),按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件对60%甲醇空白溶剂和供试品溶液进样分析。结果显示空白溶剂对供试品测定无干扰,表明方法专属性良好,具体图略。
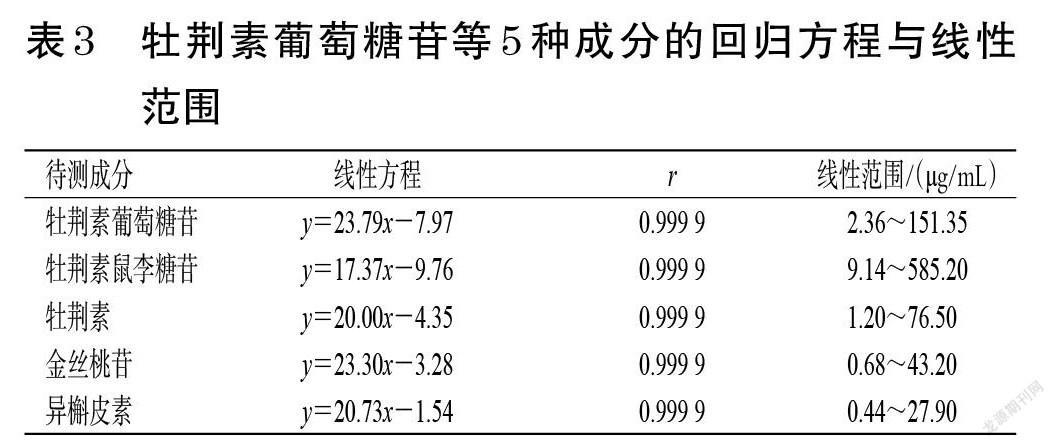
2.4.2 线性关系考察 精密量取“2.2.1”项下牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷、异槲皮素对照品贮备液各适量,以50%甲醇为溶剂,配制成上述成分质量浓度分别为151.35、585.20、76.50、43.20、27.90 μg/mL的混合对照品溶液Ⅰ。取上述混合对照品溶液Ⅰ,用50%甲醇倍比稀释,配制成牡荆素葡萄糖苷质量浓度分别为75.68、37.84、18.92、9.46、4.73、2.36 μg/mL,牡荆素鼠李糖苷质量浓度分别为292.60、146.30、73.15、36.58、18.29、9.14 μg/mL,牡荆素质量浓度分别为38.25、19.12、9.56、4.78、2.39、1.20 μg/mL,金丝桃苷质量浓度分别为21.60、10.80、5.40、2.70、1.35、0.68 μg/mL,异槲皮素质量浓度分别为13.95、6.98、3.49、1.74、0.87、0.44 μg/mL的系列线性溶液。取上述混合对照品溶液Ⅰ和系列线性溶液各适量,按“2.1”项下色谱条件依次进样测定,记录峰面积。以待测成分质量浓度(x)为横坐标、峰面积(y)为纵坐标进行线性回归,结果见表3。
2.4.3 精密度试验 取心安胶囊样品(编号S1),按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件连续进样6次,记录峰面积。结果显示,牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷和异槲皮素峰面积的RSD均小于2.00%,表明方法精密度良好。
2.4.4 重复性试验 取心安胶囊样品(编号S1),共6份,按“2.2.2”项下方法平行制备供试品溶液,按“2.1”项下色谱条件进样测定,记录峰面积并按外标法计算各成分含量。结果显示,牡荆素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷和异槲皮素含量的RSD均小于2.00%,表明方法重复性良好。
2.4.5 稳定性试验 取心安胶囊样品(编号S1),按“2.2.2”项下方法制备供试品溶液,分别于室温下放置0、2、4、8、12、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果显示,牡荊素葡萄糖苷、牡荆素鼠李糖苷、牡荆素、金丝桃苷和异槲皮素峰面积的RSD均小于2.00%,表明供试品溶液在室温下放置24 h内稳定。
2.4.6 加样回收率试验 精密称取已知含量的心安胶囊样品(编号S1)6份,每份约0.25 g,分别精密加入0.902 mg/mL的牡荆素葡萄糖苷溶液1 mL、0.930 mg/mL的牡荆素鼠李糖苷溶液4 mL、0.890 mg/mL的牡荆素溶液0.5 mL、 0.725 mg/mL的金丝桃苷溶液0.2 mL、0.610 mg/mL的异槲皮素溶液0.2 mL(按“2.2.1”项下方法配制),按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,记录峰面积并计算5种成分的加样回收率。结果显示,5种成分的平均加样回收率分别为95.80%、102.10%、103.26%、103.89%、102.09%,RSD均小于2.00%(n=6),表明方法准确度良好,结果见表4。
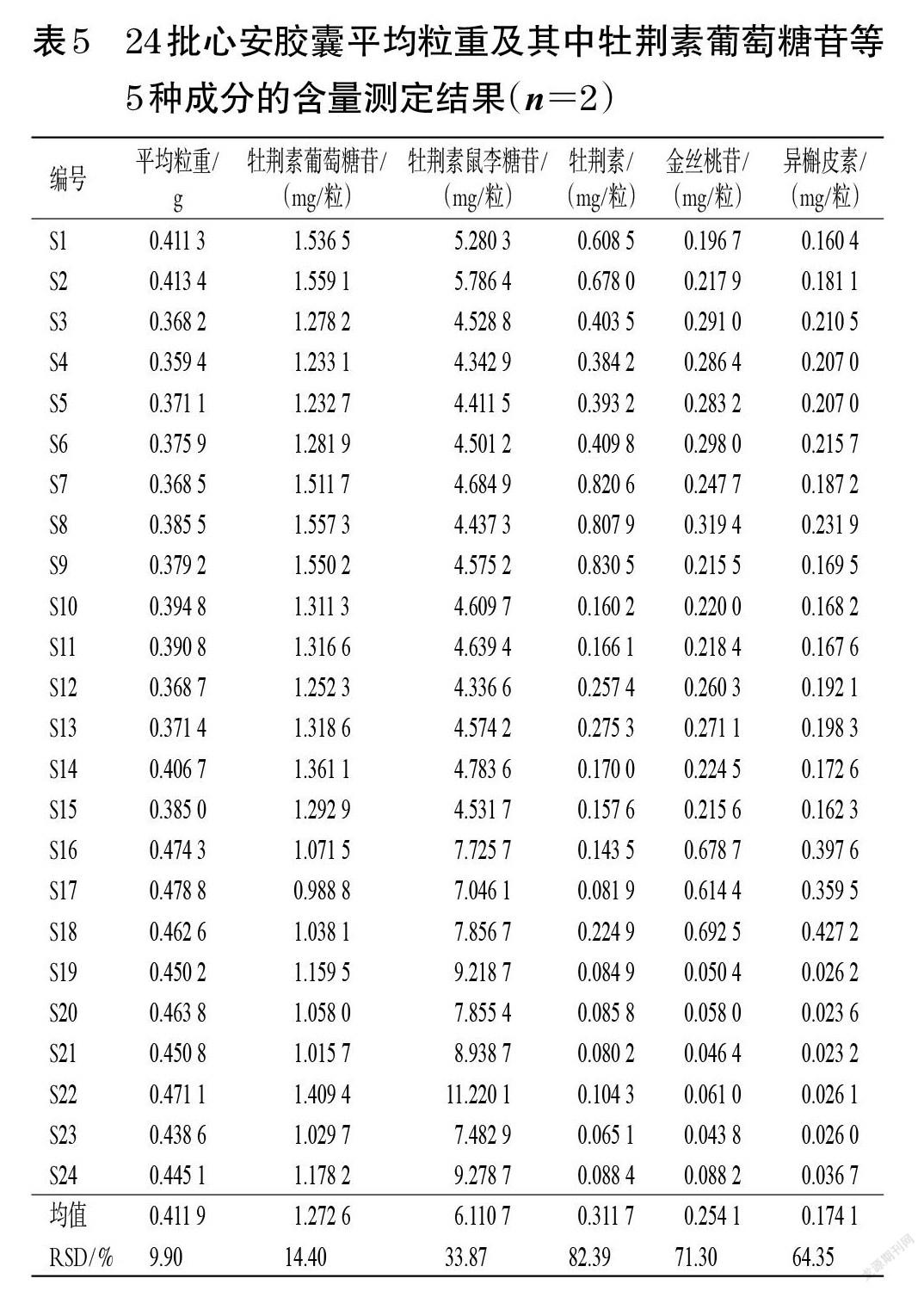
2.4.7 样品含量测定 取24批心安胶囊样品,按“2.2.2”项下方法测定平均粒重并制备供试品溶液,每批平行制备2份,按“2.1”项下色谱条件进样测定,记录峰面积,采用外标法计算各样品中牡荆素葡萄糖苷等5种成分的含量,结果见表5。
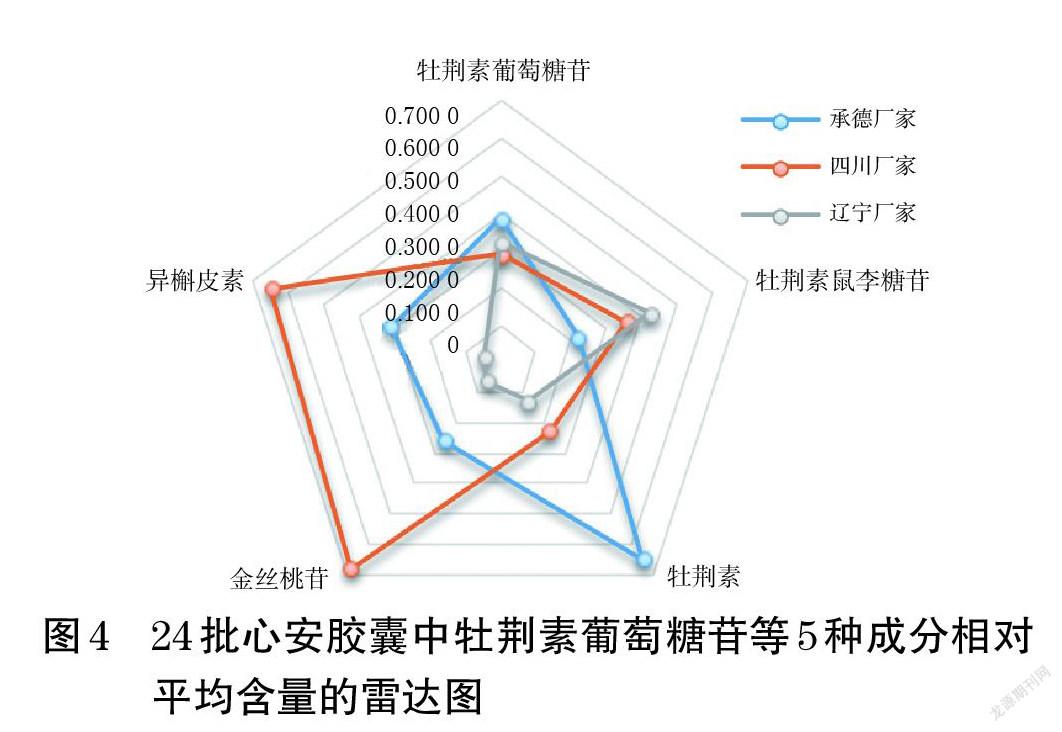
由于不同样品中各成分的含量差异较大,故按以下方法计算各已知成分的相对平均含量(用比值表示):相对平均含量=各厂家样品中每种成分的平均含量/各厂家样品中每种成分的平均含量之和。以上述相对平均含量为对象,采用Excel 2013绘制雷达图,结果见图4。由表5、图4可以观察出,同一厂家不同批次样品中5种成分的含量有一定差异;不同厂家样品之间各成分的含量差异较为明显,如承德厂家样品中牡荆素葡萄糖苷和牡荆素含量较高,牡荆素鼠李糖苷含量较低;四川厂家样品中金丝桃苷和异槲皮素含量较高;辽宁厂家样品中牡荆素鼠李糖苷含量较高,牡荆素、金丝桃苷和异槲皮素含量较低。
2.5 化学模式识别分析
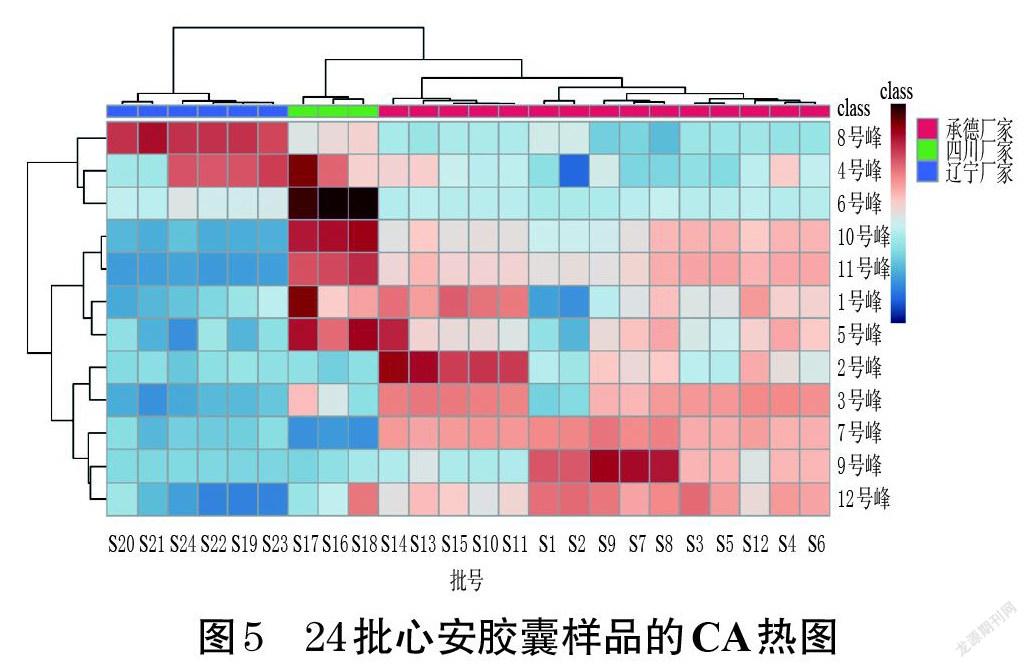
2.5.1 CA CA热图可对数据进行筛选、提取和降维,可通过横向聚类来反映样品的关系,通过纵向聚类来反映化学成分之间的关系[17]。该法以渐进的蓝红色条带来直观呈现数据结果,其颜色代表归一化后的含量数据,含量越高,条带颜色越红,反之条带颜色越蓝,可以此反映研究对象的差异变化[18]。将24批心安胶囊的12个共有峰峰面积导入MetaboAnalyst 5.0工具,选择“statistical analysis”模块,对数据进行筛选、归一化等操作后,输出CA热图,详见图5。由图5可知,24批样品可聚成3类:S1~S15聚为一类,S16~S18聚为一类,S19~S24聚为一类;承德厂家生产的15批心安胶囊样品中,除4、6号峰对应成分和牡荆素鼠李糖苷(8号峰)外,其余共有峰对应成分的含量整体较高;四川厂家生产的样品中,5、6号峰对应成分和金丝桃苷(10号峰)、异槲皮素(11号峰)的含量相对较高,且6号峰对应成分的含量明显高于承德厂家和辽宁厂家生产的样品;辽宁厂家生产的样品中,牡荆素鼠李糖苷(8号峰)的含量相对较高。结合CA热图中的条带颜色可知,6、7、8、10、11号峰是主要差异峰,不同厂家样品间的差异较为显著。
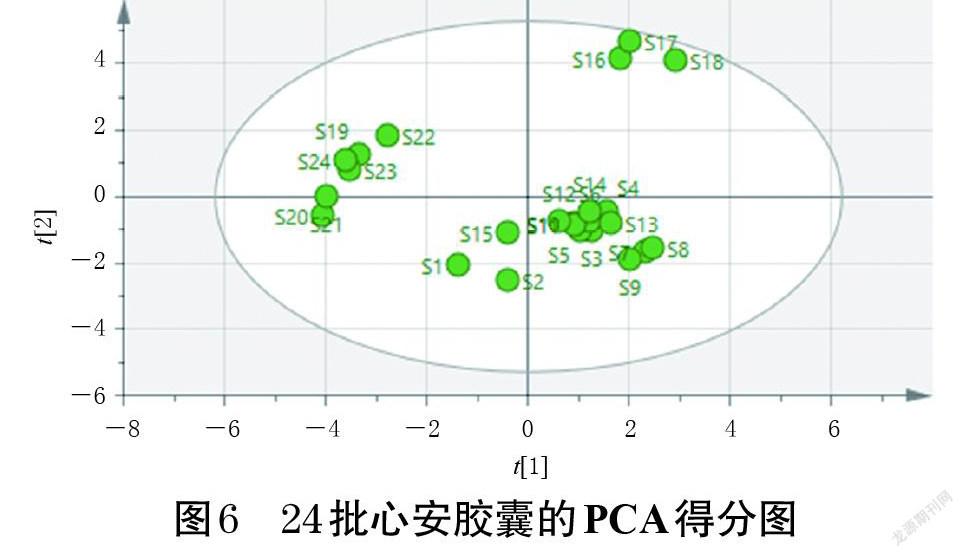
2.5.2 PCA 建立24批心安胶囊的12个共有峰峰面积矩阵,导入SIMCA 14.1软件中,以共有峰峰面积为变量,建立PCA模型并绘制PCA得分图。模型质量参数R 2X为0.953,预测能力参数Q 2为0.802,均高于0.5,说明该模型有较高的稳定性和预测力[19],PCA得分图见图6。由图6可知,3个厂家生产的心安胶囊样品分布在不同区域,说明其组间差异较明显,且分类结果与CA一致。
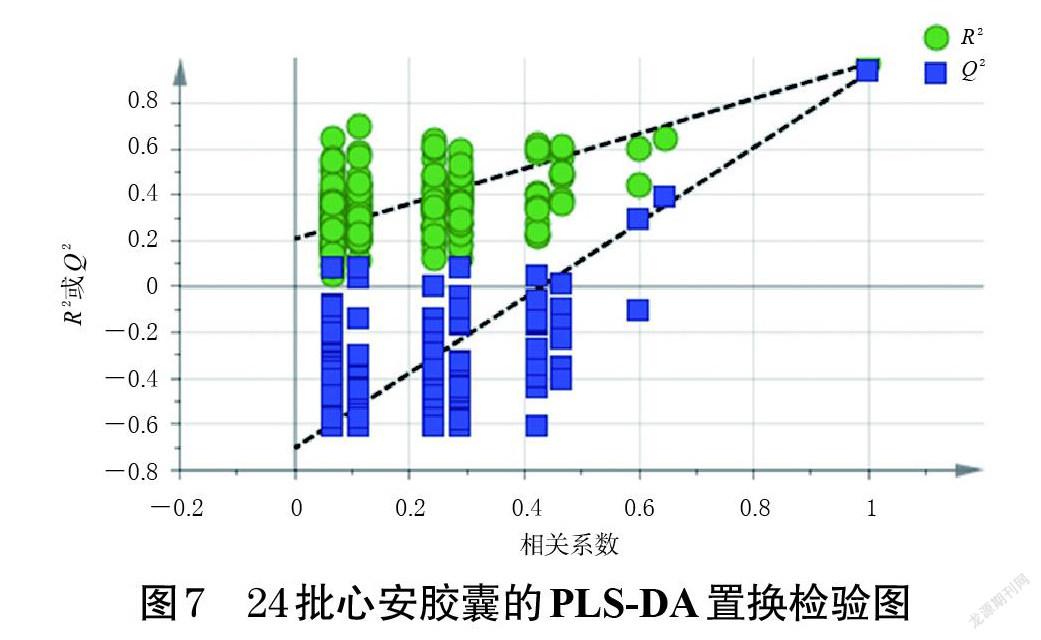
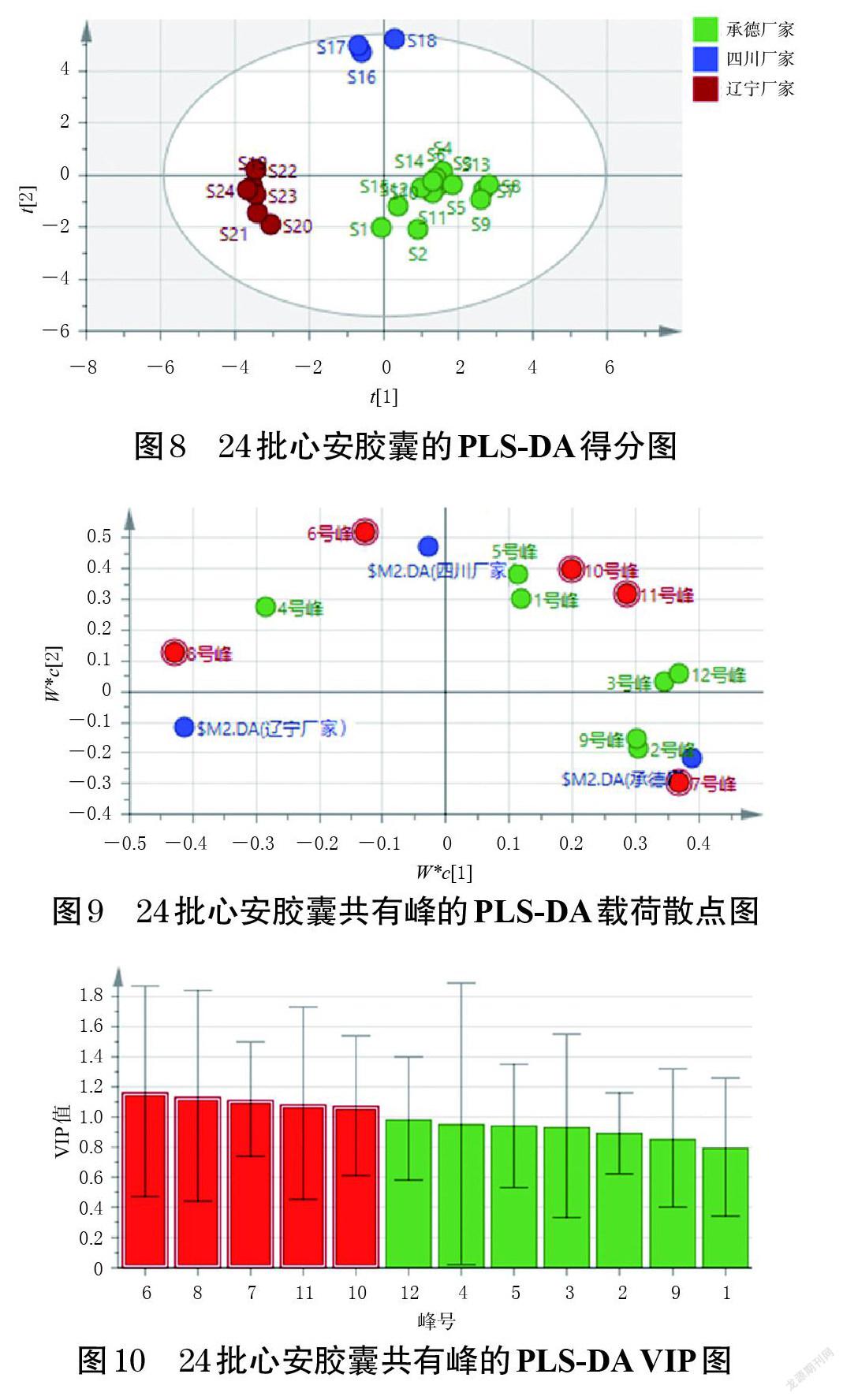
2.5.3 PLS-DA 为明确24批样品的组间差异及差异标志物,本研究在CA和PCA的基础上,将24批心安胶囊的12个共有峰峰面积导入SIMCA 14.1软件,建立PLS-DA模型。结果显示,自变量累积解释能力参数R 2X为0.967,因变量累积解释能力参数R 2Y为0.965,预测能力参数Q 2为0.919,均大于0.5,且R 2和Q 2两者差距小于0.2,说明所建模型具有较强的解释率和预测率[19]。设置分类Y矩阵随机排列200次并进行置换检验,置换检验图见图7。由图7可知,R 2拟合直线在Y坐标轴的截距为0.209(应小于0.30),说明所建立的模型可靠;Q 2拟合直线在Y坐标轴的截距为-0.703(应小于0.05),表明所建模型不存在过度拟合,可用于分析24批样品的组间差异[19]。PLS-DA得分图、载荷散点图和变量重要性投影(variable importance in projection,VIP)图分别见图8~图10。由图8可知,3个厂家生产的24批样品均分布在95%置信区间内,且不同厂家分布在不同区域,区分明显,分类结果与CA和PCA一致。由图9可知,离原点分散较远的色谱峰分别为6、7、8、10、11号峰,说明这些成分对样品组间差异的影响较大。结合VIP值筛选出能引起不同厂家心安胶囊质量差异的标志性成分,其中VIP值>1且其值越大,表明对质量差异的贡献越大,可作为差异标志物[20]。由图10可得出,6号峰对应成分和牡荆素葡萄糖苷(7号峰)、牡荆素鼠李糖苷(8号峰)、金丝桃苷(10号峰)、异槲皮素(11号峰)为差异标志物。
3 讨论
3.1 色谱条件的优化
本课题组前期考察了4种型号的色谱柱[Agilent ZORBAX SB-C18、Thermo AcclaimTM120 C18、Water Sunfire C18及Agilent 5 HC-C18(2),規格(4.6 mm×250 mm,5 µm)均相同]的分离效果,发现Agilent ZORBAX SB-C18的分离效果最佳。本课题组考察了流动相体系中不同体积分数甲酸溶液(0.05%、0.1%、0.2%)的分离效果,发现以0.1%甲酸溶液(A)-乙腈(B)-四氢呋喃(D)的分离效果最好,并对梯度洗脱程序进行了优化。本课题组对检测波长(320、340、350、363 nm)进行了筛选,发现340 nm波长下各色谱峰的响应值均较高,故将其作为检测波长。本课题组还对柱温(25、30、35 ℃)、流速(0.8、1.0、1.2 mL/min)进行了考察,发现当柱温为30 ℃、流速为1.0 mL/min时的分离效果最佳。
3.2 供试品溶液制备方法的考察
本课题组以指纹图谱信息的全面性和色谱峰的响应值为主要指标,比较了不同提取溶剂(50%甲醇、60%甲醇、70%甲醇)和不同超声提取时间(20、30、40 min)的提取效率。结果显示,以60%甲醇提取时,样品中杂质较少,提取效率较高;当超声提取时间为30 min时,提取效率最优,再延长提取时间,提取效率无明显变化,故最终确定以60%甲醇超声30 min作为供试品溶液的制备方法。
3.3 指纹图谱的化学模式识别分析
本研究结果表明,24批心安胶囊样品有12个共有峰,且各色谱图整体相似,与对照指纹图谱的相似度均大于0.97。比较24批样品的外观及其指纹图谱特征发现,承德厂家产心安胶囊样品(编号S1~S15)内容物呈棕灰色,颜色较浅,色谱图所示色谱峰较多且响应较强;四川厂家产心安胶囊样品(编号S16~S18)内容物呈灰黄色,颜色浅,色谱图所示色谱峰较多;辽宁厂家产心安胶囊样品(编号S19~S24)为深棕褐色,颜色较深,色谱图所示色谱峰较少。CA、PCA及PLS-DA均将24批样品分为3类,且均随厂家不同而明显区分,分类结果一致。PLS-DA指出,6号峰对应成分和牡荆素葡萄糖苷(7号峰)、牡荆素鼠李糖苷(8号峰)、金丝桃苷(10号峰)、异槲皮素(11号峰)为差异标志物,提示生产厂家在生产过程中应重点关注上述成分的含量,以提高心安胶囊的整体稳定性。笔者进一步分析了造成这种差异的原因,可能与厂家的生产工艺以及山楂叶原药材的生长环境、海拔、光照、采收期、储藏等因素有关,具体原因有待结合实际生产调研进一步确认。
4 结语
综上所述,本研究建立的HPLC指纹图谱、多成分定量方法简单、可行,可较全面地分析心安胶囊的成分信息,结合CA、PCA和PLS-DA可对该制剂进行综合评价,使分析结果更为科学、全面,可为完善心安胶囊的药品标准提供实验依据。后续本课题组将进一步加大样本量,通过液质联用技术对未知成分进行指认,进一步开展心安胶囊谱效关系、代谢组学研究,为全面评价心安胶囊的质量奠定基础。
参考文献
[ 1 ] 卫生部药典委员会.中华人民共和国卫生部药品标准:第3册:中药成方制剂[S].北京:中国医药出版社,1991:53.
[ 2 ] PAN H F,WANG X,DU Y L,et al. A simple and sensitive method for the simultaneous determination of six consti- tuents in hawthorn leaves[J]. Anal Methods,2014,6(18):7475-7483.
[ 3 ] XU B X,YANG M Y,DU Y L,et al. Fingerprint and multi-ingredient quantitative analyses for quality evaluation of hawthorn leaves and Guang hawthorn leaves by UPLC-MS[J]. Revista Brasileira De Farmacognosia,2018,28(3):369-373.
[ 4 ] 弓威.山楂叶有效成分提取分离及利用研究[D].北京:中国农业科学院,2015.
[ 5 ] 王领弟,徐宝欣,李艳荣,等.基于主成分和聚类分析的心安胶囊指纹图谱研究[J].中国药师,2017,20(1):35-37,45.
[ 6 ] 杨明宇,赵胜男,王领弟,等.反相高效液相色谱法测定不同厂家心安胶囊中6种成分的含量[J].承德医学院学报,2016,33(3):185-187.
[ 7 ] 张婷婷,张妍妍. HPLC测定心安胶囊中牡荆素鼠李糖苷的含量[J].中医药学报,2009,37(3):48-49.
[ 8 ] 何兵,刘艳,李春红,等.多指标定量指纹图谱在中药金银花质量评价中的应用[J].中国药学杂志,2015,50(14):1237-1242.
[ 9 ] 周昱杉,梁洁,信晨曦,等.中药复方制剂质量评价方法[J].中华中医药学刊,2019,37(3):589-592.
[10] 刘江,陈兴福,邹元锋.基于中药指纹图谱多维信息的化学模式识别研究进展[J].中国中药杂志,2012,37(8):1081-1088.
[11] 阿基业,何骏,孙润彬.代谢组学数据处理:主成分分析十个要点问题[J].药学学报,2018,53(6):929-937.
[12] 林林,于鳳蕊,徐丽华,等.女金丸HPLC指纹图谱建立及聚类分析和主成分分析[J].中国药房,2019,30(10):1339-1343.
[13] 孙磊,张超,田润涛,等.色谱指纹图谱结合化学计量学用于3种乳香的鉴别和质量评价[J].中国药学杂志,2015,50(2):140-146.
[14] 于新兰,包蓉,蔡磊,等.基于多波长检测和替代对照品法用于通滞苏润江制剂的综合质量控制[J].中国药学杂志,2018,53(18):1594-1602.
[15] 孙立丽,王萌,任晓亮.化学模式识别方法在中药质量控制研究中的应用进展[J].中草药,2017,48(20):4339- 4345.
[16] 陈粲文,宋粉云,李华,等.安胎丸UPLC指纹图谱及模式识别研究[J].药物分析杂志,2016,36(3):465-472.
[17] 张琳琳,张文婷,唐登峰,等.基于指纹图谱、多指标含量测定及化学计量学的宁心宝胶囊质量评价[J].中国药学杂志,2019,54(17):1425-1431.
[18] 杨正明,威则日沙,李学学,等.基于多元统计分析的川产道地药材江油附子和川乌中6种生物碱含量比较研究[J].中草药,2019,50(6):1461-1471.
[19] 李明月.心脉通胶囊的HPLC指纹图谱研究与化学模式识别[J].药物分析杂志,2020,40(6):1104-1112.
[20] 潘玄玄,宋粉云,林秀莲,等.沉香化气丸的UPLC指纹图谱与化学模式识别[J].中国实验方剂学杂志,2017,23(19):105-110.
(收稿日期:2021-10-28 修回日期:2022-01-23)
(编辑:曾海蓉)
