纳氏试剂分光光度法测定氨氮前处理方法的改进研究
2022-03-11周煜山东省日照生态环境监测中心山东日照276826
周煜(山东省日照生态环境监测中心,山东 日照 276826)
0 引言
在化学实验及化工研究时使用的检测氨氮测定方法中,HJ 535—2009 《纳氏试剂分光光度法》是最常用的方法之一,适用范围广,但干扰项也较多[1]。该方法规定了絮凝沉淀法和预蒸馏法两种前处理方式,在待测样品色度或浊度影响较大,以及钙镁等金属离子含量较高时,通常选择预蒸馏法进行前处理,可以保证准确的监测结果。根据方法要求,预蒸馏时使用20 g/L的硼酸溶液作为吸收液,但由于四硼酸盐-硼酸缓冲体系的存在,需使用氢氧化钠溶液将馏出液的pH值调至11左右才能保证硼酸被完全中和[2]。每个水样氨氮含量不同,馏出液的pH值也有差异,准确调整馏出液的pH值是整个预处理环节中较为繁琐的步骤,且国标及《水和废水监测分析方法》(第四版)中均未对馏出液的中和处理做出具体规定,在实际工作中多有不便。
在研究了HJ 536—2009 《水杨酸分光光度法》和HJ 533—2009 《环境空气和废气 氨的测定 纳氏试剂分光光度法》之后,发现上述两种方法均使用低浓度硫酸作为吸收液[3-4],在实际工作中也发现,纳氏试剂法测定氨气时,使用硫酸吸收液无需额外进行中和操作,纳氏试剂中的氢氧化钠完全可以中和多余的硫酸,而且几乎不影响最终结果。因此,为寻求操作更简便的预蒸馏方式,在参考了各项方法之后,本文选择0.005 mol/L的硫酸溶液作为蒸馏吸收液,采用实际样品加标回收、国家标准物质两种方式进行准确度和精密度试验,对硫酸替代硼酸作为吸收液的可行性进行了初步研究,为水中氨氮测定方法的前处理程序提供一点参考。
1 实验仪器与试剂
1.1 实验仪器
选用紫外可见分光光度计(TU1810);智能一体化蒸馏仪(ST106-3RW);电子天平(AL204)。
1.2 试剂
纳氏试剂:称取16.0 g氢氧化钠溶于50 mL水中,冷却至室温。称取7.0 g碘化钾和10.0 g碘化汞溶于水中,将此溶液在搅拌下加入上述50 mL氢氧化钠溶液中,用水稀释至100 mL。
酒石酸钾钠溶液(ρ=500 g/L):称取50.0 g酒石酸钾钠溶于100 mL水中,充分加热煮沸至体积减少1/2,冷却后使用无氨水稀释至100 mL。
溴百里酚蓝指示剂(ρ=0.5 g/L):称取0.05 g溴百里酚蓝溶于50 mL水中,加入10 mL无水乙醇,用水稀释至100 mL。
氢氧化钠溶液(ρ=40 g/L):称取4 g氢氧化钠溶于水中,稀释至100 mL。
轻质氧化镁:500 ℃加热处理。
硫酸吸收液(c(H2SO4)=0.005 mol/L):量取0.70 mL硫酸加入水中,稀释至250 mL,临用时再用水稀释 10 倍。
氨氮标准工作溶液(ρN=10 μg/mL):吸取10.00 mL氨氮标准贮备溶液(ρN=500 μg/mL)于500 mL容量瓶中,稀释至刻度。
实验室用水均为新鲜二级水,氨氮标准贮备溶液为环境保护部标准样品研究所的标准溶液。
2 实验过程及结果
2.1 校准曲线的测定
在8个50 mL比色管中,分别加入0.00、0.50、1.00、2.00、4.00、6.00、8.00和10.00 mL氨氮标准工作溶液,对应的氨氮含量分别为0.0、5.0、10.0、20.0、40.0、60.0、80.0和100 μg,加水至标线。加入1.0 mL酒石酸钾钠溶液,摇匀,再加入1.0 mL纳氏试剂,摇匀。放置10 min后,在420 nm波长下,使用2 cm比色皿,以水为参比,测量吸光度。以减去空白后的吸光度为纵坐标,以其对应的氨氮含量(μg)为横坐标,绘制校正曲线。得到回归方程y=0.001+0.006 92x,相关系数r=0.999 9,具体测定结果如表1所示。
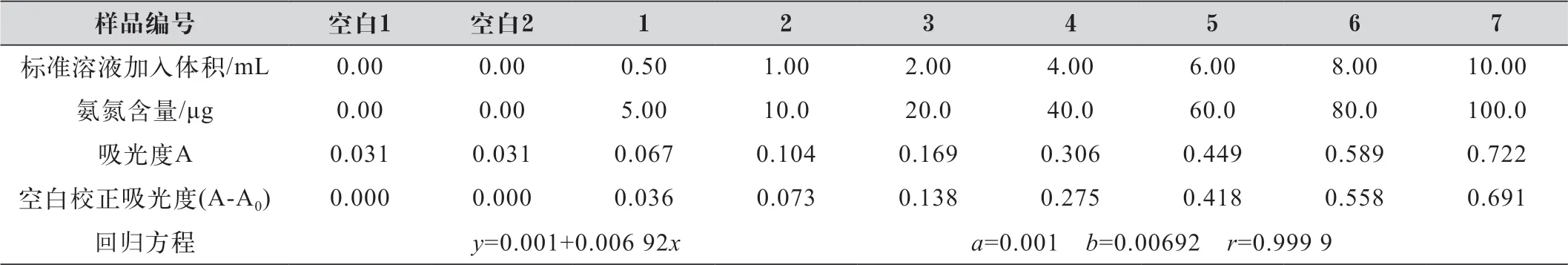
表1 氨氮校准曲线测定结果
2.2 实际样品加标回收率的测定
分别对来自河流断面1(样品1)、河流断面2(样品2)和某企业间接排放口(样品3)三个点位的实际样品进行6次平行测定,同时对加标样品进行6次平行测定,计算加标回收率,操作过程如下:向250 mL容量瓶内加入50 mL硫酸溶液,确保冷凝管出口在硫酸溶液液面之下;分取250 mL样品移入500 mL烧瓶中,加几滴溴百里酚蓝指示剂,使用氢氧化钠溶液调整pH至6.0(指示剂呈黄色)~7.4(指示剂呈蓝色),加入0.25 g轻质氧化镁及数粒玻璃珠,立即连接蒸馏器和冷凝管;加热蒸馏,控制馏出液速率约为10 mL/min,待馏出液达200 mL时,停止蒸馏,加水定容至250 mL;直接量取定容后的水样50 mL按与校准曲线相同的步骤测量吸光度,同时做2个吸收液空白,以吸收液空白校正后的吸光度进行计算,具体结果如表2所示。

表2 实际样品加标回收率测定结果统计
由表2可知,样品1的加标回收率为98.7%,实际样品和加标样品的相对平均偏差分别为2.2%、2.65%;样品2的样品1的加标回收率为104%,实际样品和加标样品的相对平均偏差分别为3.10%、1.23%;样品3的加标回收率为102%,实际样品和加标样品的相对平均偏差分别为2.65%、3.24%。3组样品的加标回收率均在95%至105%之间,相对平均偏差均在5%之内,满足实验室内样品准确度和精密度的要求[5]。
2.3 标准样品的测定
对环境保护部标准物质研究所的氨氮标样批号:2005131(标准样品1)、2005117(标准样品2)和2005119(标准样品3)按2.2中实验步骤进行6次平行测定,具体结果如表3所示。
由表3结果可知,标准样品2005131、2005117、2005119的6次平行及平均值均在保证值内,准确度满足质控要求;3组标准样品的相对平均偏差分别为0.93%、1.08%和1.19%,精密度满足质控要求。
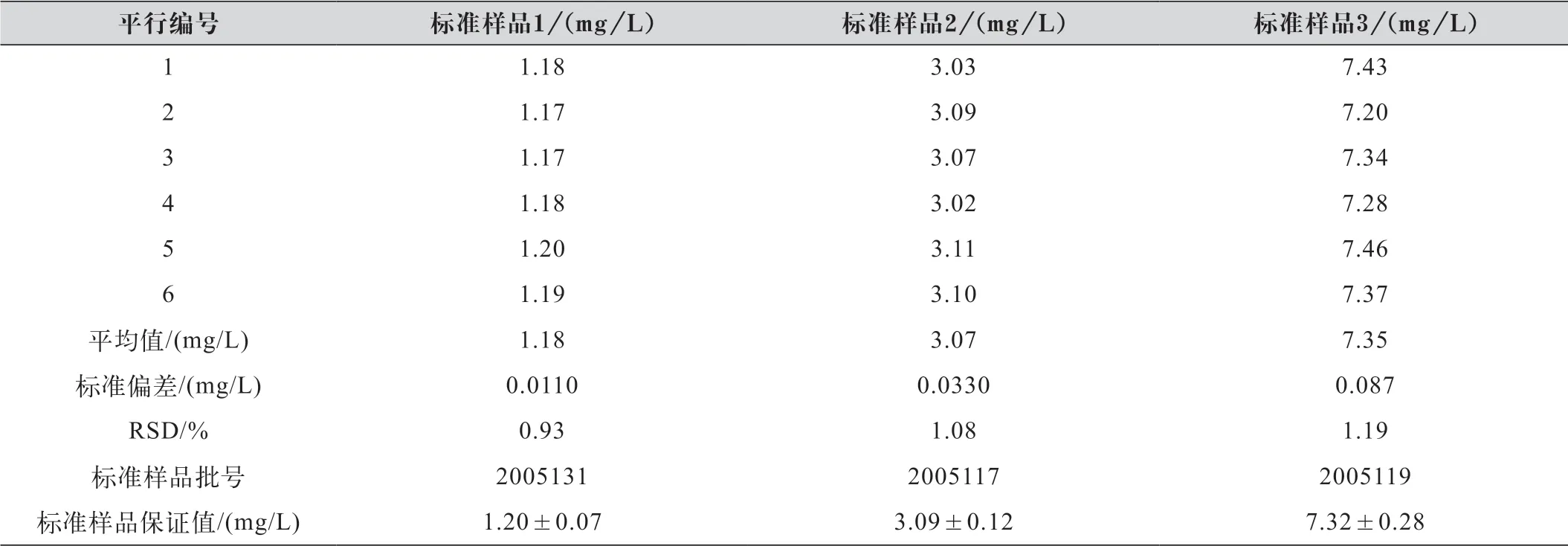
表3 标准样品结果统计
2.4 比对试验
对采自河流断面3(样品4)、河流断面4(样品5)和某企业间接排放口2(样品6)三个点位的实际样品,按照2.2实验步骤分别使用硼酸吸收液和硫酸吸收液进行6次平行测定,具体结果如表4~表6所示。
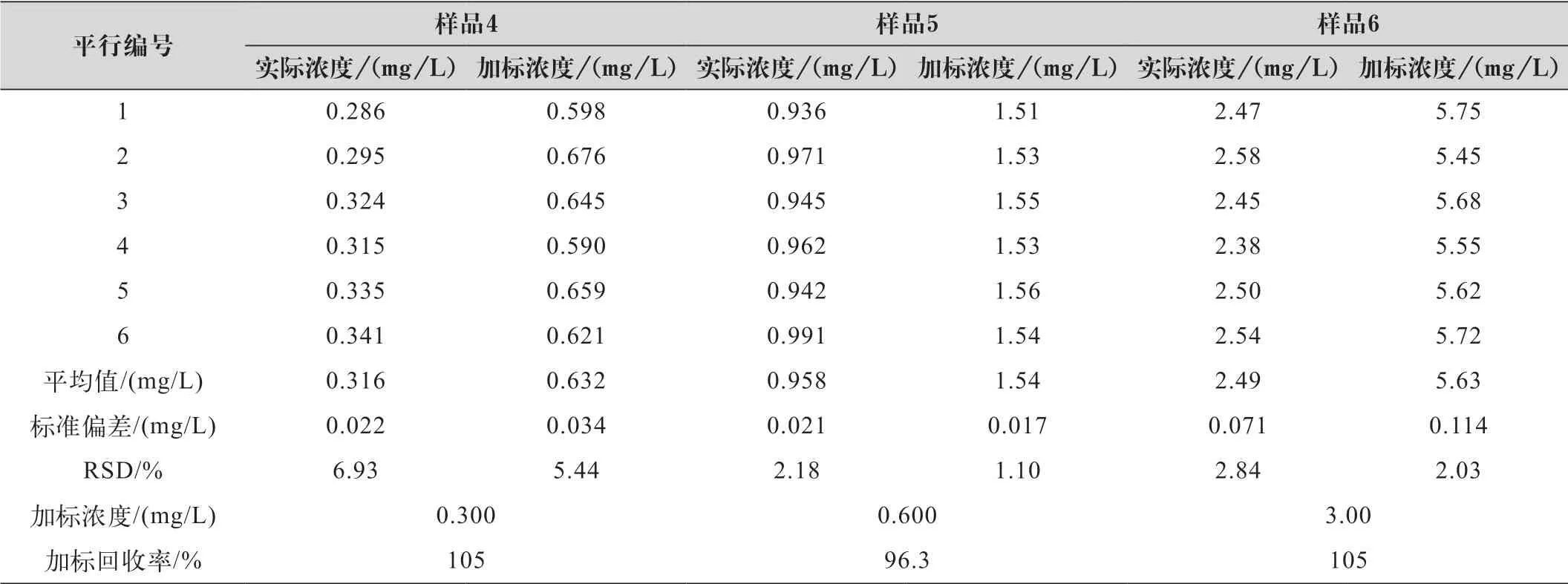
表4 实际样品测定结果统计(硼酸吸收液)
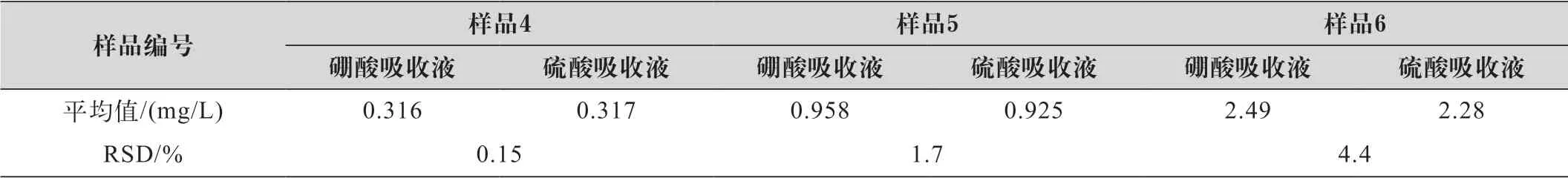
表6 实际样品比对结果统计
由表4、表5可知,使用硼酸吸收液测定样品4、样品5和样品6得到了较好的结果,三组样品的相对平均偏差在1.1%~6.9%之间,加标回收率在96.3%~105%之间,精密度和准确度均满足质控要求;使用硫酸吸收液测定样品4、样品5和样品6,相对平均偏差在1.45%~3.59%之间,加标回收率在96.7%~103%之间,精密度和准确度也满足质控要求。总体上看,在高中低三个浓度的样品中,使用硼酸吸收液和硫酸吸收液的样品平均值基本一致,加标回收率也基本在同一水平,两组之间无明显差异,平均相对偏差在0.15%~4.40%之间,符合国控采测分离作业指导书中精密度要求(样品浓度≤1.00 mg/L时,相对平均偏差≤10%;样品浓度>1.00 mg/L时,相对平均偏差≤5%);在低浓度样品中,使用硼酸吸收液测得样品4及样品4加标的相对平均偏差分别为6.93%和5.44%,使用硫酸吸收液测得样品4及样品4加标的相对平均偏差分别为3.9%和2.18%,使用硼酸吸收液测得的样品精密度略差于硫酸吸收液;在高浓度样品中,使用硼酸吸收液测得样品6及样品6加标的相对平均偏差分别为2.84%和2.03%,使用硫酸吸收液测得样品4及样品4加标的相对平均偏差分别为1.66%和1.45%,同样发现使用硼酸吸收液测得的样品精密度略差于硫酸吸收液。
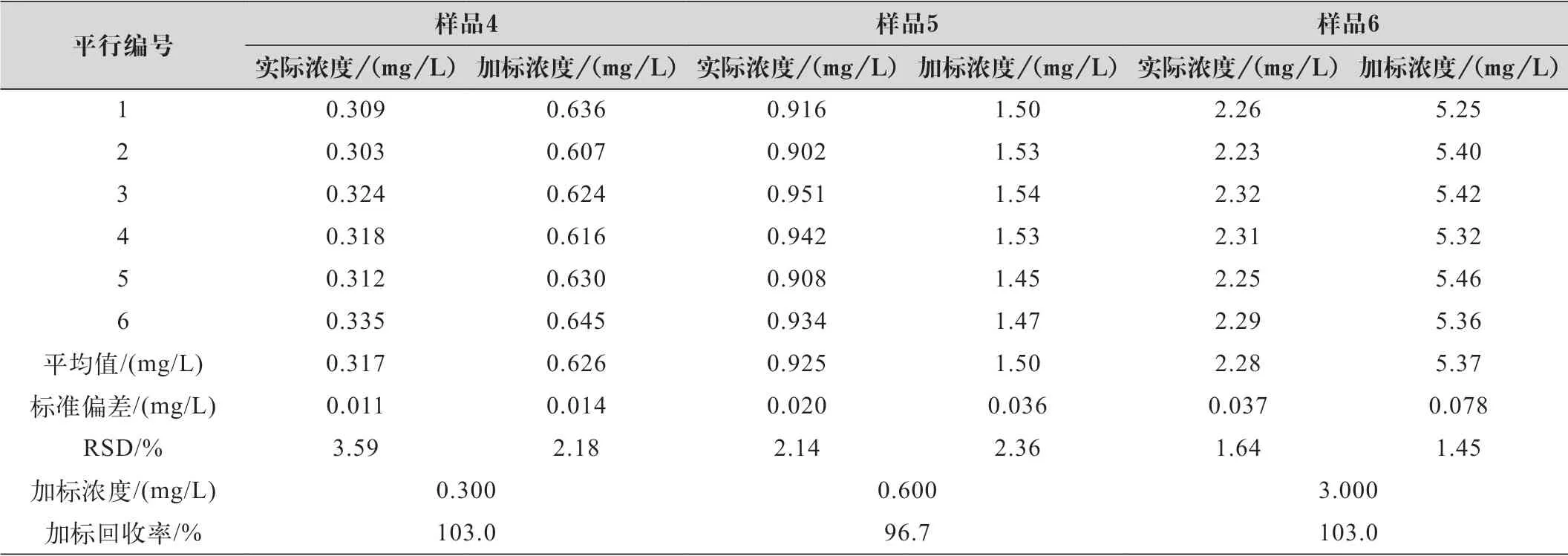
表5 实际样品测定结果统计(硫酸吸收液)
因此,通过使用2种吸收液进行实际样品测定发现,使用2种吸收液均能达到较好的试验结果,硫酸吸收液测定的样品精密度和准确度上和硼酸吸收液基本保持一致水平,可以满足质控要求,并在低浓度样品中精密度更能取得较好的结果,数据离散水平低于硼酸吸收液,可以替代原标准中的硼酸吸收液使用。
3 结果分析
硫酸作为强酸,相比硼酸可以更快地吸收蒸馏出的氨,而氨极易溶于水,因此硫酸溶液在理论上完全可以作为蒸馏吸收液使用;此外,每份比色体积50 mL的0.005 mol/L硫酸吸收液中含有H+0.25 mmol,1 mL纳氏试剂中含有OH-4 mol,足以中和掉多余的硫酸并且不影响比色所需的碱度。本文使用0.005 mol/L的硫酸溶液作为蒸馏吸收液开展了初步的方法确认研究,进行了3组实际样品的基体加标回收率的6次平行测定、3组标准样品的6次平行测定,以及使用硼酸吸收液和硫酸吸收液3组实际样品的比对测定,结果表明实际样品的加标回收率均在95%至105%之间,标准样品的测定值均在保证值内,6组样品的相对标准偏差均在5%以内,比对试验的样品相对标准偏差在5%以内,准确度和精密度满足质量控制要求。
4 结语
本研究表明使用低浓度硫酸溶液作为氨氮的蒸馏吸收液,既可以省去硼酸馏出液pH值的调整过程,也可保证样品准确度和精密度的要求,数据可靠,在实际工作中可以应用。
