血浆与血清标本腺苷脱氨酶检测结果的一致性评估及血清参考区间的适宜性评估
2022-03-06熊刚曹丹刘艳婷赵思涵肖光军通信作者
熊刚,曹丹 ,刘艳婷,赵思涵,肖光军 (通信作者)
1 三台县妇幼保健院检验科 (四川绵阳 621100);2 遂宁市中心医院检验科(四川遂宁 629000)
腺苷脱氨酶(adenosine deaminase,ADA)是一种与机体嘌呤代谢和免疫功能密切相关的蛋白质[1],其在淋巴细胞的发育及成熟过程中起重要作用,并在免疫细胞的增殖、分化、功能等方面发挥着重要的调节作用[1]。相关研究表明,多种感染、肿瘤、代谢性疾病及免疫相关性疾病患者的血清ADA 水平增高,且ADA 水平与患者病情严重程度及预后密切相关,故ADA 被大量应用于临床诊疗及预后评估中[1-8]。目前,临床实验室常用紫外速率法和酶偶联显色法检测机体外周血中的ADA水平,但因我国未发布基于多中心的中国人群ADA 参考区间,故临床实验室常使用试剂盒说明书提供的血清参考区间[9-11]。相关研究显示,血浆与血清中的ADA 水平存在一定差异,且不同文献报道的研究结果也存在一定差异[12-13],但均推荐使用血清标本进行外周血ADA 水平的检测,以便于使用血清参考区间来解释检测结果。然而,大部分国产试剂盒说明书均注明可使用血清或血浆标本进行外周血ADA 水平的检测,故本研究对肝素钠抗凝血浆标本与血清标本ADA 检测结果的一致性进行了评估,并对ADA 检测试剂盒的血清参考区间在肝素钠抗凝血浆标本中的适宜性进行了评估,从而为临床实验室ADA 的检测及参考区间的引用提供指导。
1 资料与方法
1.1 一般资料
以遂宁市中心医院住院患者同时送检的肝素钠抗凝血浆标本和血清标本检测后剩余样本为研究对象,每天收集8份,连续5 d,共收集40份,用于血浆样本与血清样本ADA 检测结果的一致性评估;同时,参照卫生行业标准WS/T 402-2012《临床实验室检验项目参考区间的制定》及相关文献的要求[9-11],通过问卷调查、体格检查、B 超检查、影像检查及实验室筛查排除等方法[9-11],从2019年1—12月体检科20~79岁健康体检成人中筛选表观健康成人组成参考人群,以验证血清参考区间的适宜性。本研究共纳入参考个体1 483名,剔除离群值后剩余1479名,其中男731例,年龄为42(31,53)岁;女748例,年龄为39(30,50)岁。本研究经医院医学伦理委员会批准,所有研究对象均签署知情同意。
1.2 仪器与试剂
日立7600全自动生化分析仪;四川迈克生物股份有限公司提供的ADA 检测试剂盒(过氧化物酶法)、配套校准品和质控品,严格按照试剂盒说明书的要求设置生化分析仪的检测参数;血浆标本使用肝素钠抗凝真空采血管采集,血清标本使用不含任何添加剂的红色真空采血管采集,真空采血管及其配套采血针均由成都瑞琦医疗科技有限公司提供。需注意检测前检查仪器状态良好并对其进行定期校准和常规维护保养,且室内质控正常水平和病理水平均在控。
1.3 方法
1.3.1 标本采集与处理
40例住院患者的空腹血浆和血清标本均由住院部护士使用相应真空采血管规范采集,每管各3 ml;所有参考个体的标本均由检验科工作人员在体检科使用肝素钠抗凝真空采血管规范采集,每管3 ml。标本采集后,充分混匀,然后垂直放置于泡沫板上,及时送检,运输中避免剧烈震荡。实验室收到样本后,以4 000 r/min、5 min 的参数离心,然后使用1.5 ml 的离心管盛装分离后的血浆和血清,并于采样后2 h 内完成所有标本的检测。
1.3.2 血浆标本与血清标本ADA 检测结果的一致性评估
参照美国临床实验室标准化协会EP9-A2文件的要求,以同一患者的血清标本为参考标本(X),肝素钠抗凝血浆标本为待评价标本(Y)进行检测结果的对比[14-15],并绘制两标本间检测结果的偏倚图,采用配对t检验对两标本检测结果的均值进行分析。线性回归分析显示相关系数r≥0.975时,表示X取值范围合适,可通过线性回归方程来评估两标本间检测结果的斜率(b)和截距(a),然后计算4 、10、22 U/L(其中4、22 U/L 分别为血清参考区间的下限和上限)水平处血浆标本的预期偏倚(SE%)[15],并以2021年国家卫生健康委临床检验中心室间质量评价标准中ADA 总允许误差(TEa)的1/2为临床可接受标准,评估两标本间ADA 检测结果的一致性。SE%={(b-1)×X+a}×100/X,不同水平处的SE%均≤1/2TEa则表示两标本间检测结果具有一致性。ADA 的TEa为靶值±25%。
1.3.3 参考区间的验证与建立
采用Dixon法对参考人群血浆ADA 的检测结果进行离群值检验[9-11],然后通过1.3.2的一致性评估结果来判断是否需要自建参考区间。当肝素钠抗凝血浆标本与血清标本ADA 检测结果具有一致性时,则使用参考人群血浆ADA 检测结果来验证血清参考区间的适宜性,验证通过则表示可直接引用试剂盒说明书提供的血清参考区间,验证未通过则根据参考人群血浆ADA 水平采用非参数法自建参考区间(P2.5~P97.5)[9-11];而两标本间检测结果不具有一致性时,则根据参考人群血浆ADA 水平采用非参数法自建参考区间(P2.5~P97.5)[12-13,15]。各组血浆检测结果落在血清参考区间内的比例≥90%,则参考区间验证通过;反之,则验证未通过[9-11]。
1.4 统计学处理
采用SPSS 19.0统计软件及Excel 2007软件进行数据分析,计量资料正态性检验采用Kolmogorov-Smirnov检验,P<0.05表示呈非正态分布,呈正态分布的数据以±s表示,而呈非正态分布的数据则使用中位数(M)[四分位数(P25,P75)]表示,组间比较采用配对t检验,P<0.05为差异有统计学意义。
2 结果
2.1 血浆标本与血清标本ADA 检测结果的一致性
经离群值检验,组内和组间均未见离群值;同一患者肝素钠抗凝血浆标本与血清标本ADA 的检测结果分别为(12.01±5.78)U/L 和(12.35±5.95)U/L,差异有统计学意义(t=3.602,P<0.05);但经线性回归分析,回归方程为Y=0.9663X+0.0752,相关系数r为0.9952,说明可使用线性回归方程来计算血浆标本的SE%,从表1可见不同水平处两标本间的SE%均满足临床可接受标准,检测结果具有一致性。血浆标本与血清标本ADA 检测结果的散点图和偏倚图见图1、图2,不同水平处肝素钠抗凝血浆标本的SE%见表1。

图1 血清与血浆标本ADA 检测结果的散点图
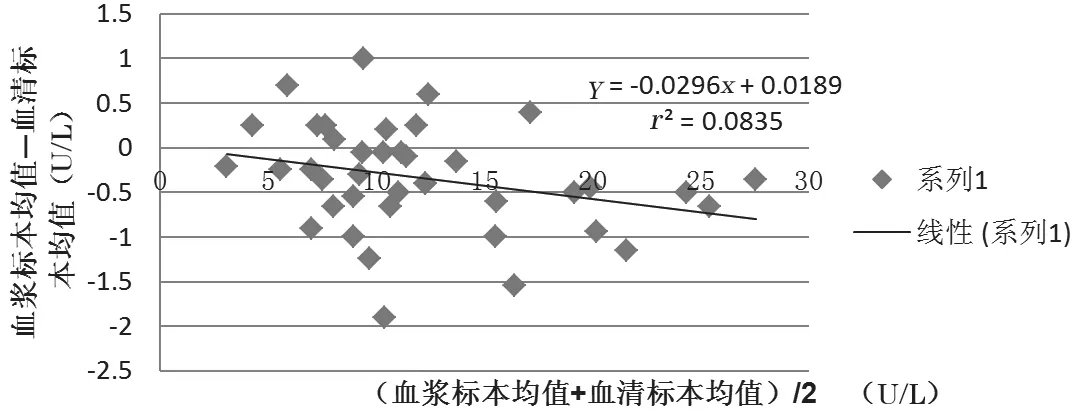
图 2 血浆与血清标本ADA 检测结果的偏倚图

表1 不同水平处肝素钠抗凝血浆标本的SE%
2.2 血清参考区间的适宜性验证
经Dixon检验剔除离群值后剩余1 479名参考个体,其性别和年龄分布见表2。根据年龄和性别将参考人群分为12个亚组,各组血浆检测结果落在血清参考区间内的符合率均≥90%,故各组参考区间验证均通过,见表2。

表2 血清参考区间在遂宁地区表观健康成人肝素钠抗凝血浆标本中的适宜性验证
3 讨论
由于我国ADA 检测试剂盒的生产厂家较多,检测原理及性能指标均存在一定差异,与不同厂家或不同型号的生化分析仪组成不同的检测系统后,导致各实验室间的检测结果存在较大差异;同时,由于ADA 检测缺少统一的质量标准,导致在试剂盒性能验证、实验室内仪器间对比、实验室间对比等活动中,各临床实验室所使用的可接受标准也存在一定的差异,从而导致相关文献的研究结论也存在一定差异[12-13]。本研究在进行肝素钠抗凝血浆标本与血清标本ADA 检测结果一致性评估时也受此因素的影响,因缺少统一的质量标准而选择募集本地区20~79岁表观健康成人来自建参考区间,但因国家卫生健康委临床检验中心在2020年新增了ADA 检测的室间质量评价活动,并发布了质量评价标准,故对血浆标本与血清标本ADA 检测结果一致性评估的数据重新进行了分析,并根据分析结果评估了血清参考区间在血浆标本中的适宜性。
本研究结果显示,肝素钠抗凝血浆标本与血清标本ADA 检测结果的差异有统计学意义(P<0.05),但线性回归分析结果显示两标本的检测结果具有良好的相关性(r=0.9952),其回归方程为Y=0.9663X+0.0752。在研究初期,因ADA 检测无质量评价标准,故采用谭延国等[13]的检验结果一致性评估方案来评估其一致性,其初步研究结果显示血浆标本与血清标本ADA 检测结果缺乏一致性,故推荐使用血清标本检测血液中ADA 的水平,若使用血浆标本则需自建血浆参考区间或进行血清参考区间的转换验证[13]。随着2020 年国家卫生健康委员会临床检验中心ADA 检测质量评价标准的发布,我们通过线性回归方程计算血浆标本在不同水平处的SE%,从表1可见其SE%均<1/2TEa,说明血浆标本与血清标本的ADA 检测结果具有一致性,可使用血浆标本代替血清标本来检测机体外周血的ADA 水平,并可使用血清参考区间来解释血浆标本的检测结果。但因参考区间受检测系统、服务人群、饮食结构、地理环境等多种因素的影响,相关文件均要求各临床实验室开展新项目或引用新的参考区间时需对其适宜性进行评估,故本研究通过前期准备自建血浆参考区间而收集的遂宁地区1 479名20~79岁表观健康成人血浆ADA的检测结果,来验证血清参考区间在血浆标本中的适宜性,从表2可见,男性和女性各年龄段的符合率均≥90%,说明参考区间验证通过,该血清参考区间可用于该地区20~79岁成人血浆ADA 检测结果的解释。同时,从表2可发现,该地区男性和女性外周血ADA 的水平均随年龄的增长缓慢上升,且同年龄段女性的ADA 水平高于男性,其原因需进一步研究,但临床结果解释时需考虑性别、年龄等因素对检测结果的影响。相关研究表明,部分检测项目在老年人、孕妇、儿童血液中的水平及其变化情况与成年人存在一定差异,临床实验室应重视其参考区间的调查与制定,但本研究纳入的研究对象为20~79岁的健康成人,未能对ADA 血清参考区间在孕妇、儿童等特殊人群中的适宜性进行评估,仍需进一步研究,必要时可采用直接法或间接法自建参考区间[16-20]。
综上所述,我国卫生行业标准或试剂盒说明书常规生化检测项目的参考区间均为血清参考区间,故大部分临床实验室使用血清标本进行常规生化项目的检测,若拟使用血浆标本代替血清标本进行检测时,即使试剂盒说明书注明两种标本均可使用,临床实验室也应对两标本检测结果的一致性及血清参考区间的适宜性进行评估;同时,随着科学技术的不断发展,检测技术、试剂盒质量及临床实验室质量水平均不断提高,为进一步满足临床诊疗需求,检验质量评价标准也可能会不断提高,当发生改变时,临床实验室应重新进行评估。
