人工智能辅助分析CTA影像诊断颅内动脉瘤的临床研究
2022-03-05曹长健邱晓明
叶 宇,王 珍,曹长健,邱晓明
(鄂东医疗集团市中心医院/湖北理工学院附属医院放射影像科,湖北 黄石 435000)
颅内动脉瘤合并蛛网膜下腔出血的发病率和病死率较高[1]。CT血管造影(CT angiography,CTA)作为临床颅内动脉瘤首选的检查方法,可清楚显示动脉瘤的基底部及颈部[2],对动脉瘤性蛛网膜下腔出血的诊断和手术方案制订具有重要意义[3],但头部CTA后处理耗时耗力,且随着检查人数的增加,给影像医生带来了极大压力;而人工智能(artificial intelligence,AI)根据序列收集数据并做出决策,可辅助临床医生,减少工作量[4],但其临床准确性尚不明确。因此,本研究以数字减影血管造影术(digital subtraction angiography,DSA)为金标准,将疑似颅内动脉瘤患者头部CTA图像的传统人工诊断结果与AI诊断结果进行对比分析,探讨两者单独或传统人工联合AI对颅内动脉瘤的检测效能。
1 资料与方法
1.1 临床资料
纳入我院2018年8月至2021年3月疑似颅内动脉瘤的患者359例,其中男177例,女182例,年龄14~77岁,平均(43.48±15.56)岁,所有患者均行CTA及DSA检查。本研究已获得我院医学伦理委员会批准(2021-FSK-K009)。
纳入标准:①有颅内动脉瘤类似症状,如一过性意识障碍、反复发作性头痛、蛛网膜下腔出血等;②有相关检查适应证;③CTA、DSA检查时间间隔短于1周。排除标准:①影像学资料或临床数据不完整;②CTA图像扫描质量较差导致AI无法识别。
1.2 CTA检查
患者取仰卧位,采用GE(Light Speed)64排CT采集原始数据,扫描基线设定为平行于听眦线,扫描范围为颅底至颅顶,扫描参数:管电压120 kV、管电流350 mA、螺距1、层厚0.625 mm。使用自动双筒高压注射器注射对比剂碘克沙醇注射液(含碘320 mg/mL)和生理盐水,对比剂注射剂量(mL)=患者体质量(kg)×0.9 (mL/kg),注射流率为4.5 mL/s,再以4.5 mL/s的流率注入40 mL生理盐水。所得图像以DICOM格式上传至GEAW4.7工作站及数坤AI软件(CerebralDoc2.1 2021版)。
1.3 方法
传统人工组:所有CTA图像上传至GEAW4.7工作站后,由2名经验丰富的高年资放射科医师对其行最大密度投影(maximal intensity projection,MIP)、多平面重建(multiplanar reconstruction,MPR)和容积重建(volume rendering,VR),重建层厚为0.625 mm。若发现脑血管瘤样突起则判定为动脉瘤,并记录动脉瘤个数、部位、形态、瘤颈及瘤高。若2名医师意见不一致,则与另1名资深神经放射科医师(具有15年神经影像经验)协商解决。
AI组:使用AI软件对所有CTA原始图像进行分析,使用级联的ResU-net算法在CTA原始轴位图像上分割动脉瘤,包括ResU-net1和ResU-net2两个模块。ResU-net1网络进行动脉瘤检测,编码器采用5层下采样,解码器通过5层上采样,输入通道数为1,输入原始CTA轴位图像,输出通道数为2;若输出结果的尺寸与输入尺寸相同,通道数则变为2。其中通道1的每个体素点表示动脉瘤的概率,当概率值大于0.5,则认为当前体素点是动脉瘤,以此作为AI诊断动脉瘤的标准;通道2的每个体素点表示当前体素点是动脉瘤中心点时该动脉瘤的长、宽、高信息,将检测到的动脉瘤切割出48×48×48像素的数据小体并输入ResU-net2网络,以进行动脉瘤分割。ResU-net2网络编码器采用3层下采样,解码器通过3层上采样,输出动脉瘤的分割结果。再通过后处理将生成的动脉瘤分割结果还原到原图对应位置。
人工联合AI组:由2名诊断医师使用AI软件对MIP、MPR、VR图像进行处理,再结合AI自动生成报告判断是否为动脉瘤,意见不一致时由资深神经放射科医师决定。
以DSA为金标准,分析传统人工组、AI组及人工联合AI组诊断颅内动脉瘤的效能,计算3种方法诊断颅内动脉瘤的灵敏度、特异度、假阳性率、假阴性率及准确度,并对传统人工组、AI组动脉瘤漏诊及误诊的原因进行分析。
1.4 统计学分析
采用SPSS 20.0统计软件对数据进行分析。计数资料以率(%)表示,3组间比较采用χ2检验。同时对传统人工组及AI组动脉瘤漏诊原因行行×列表χ2检验,当单元格期望频数小于5,则使用Fisher确切概率法。P<0.05为差异具有统计学意义。
2 结果
2.1 各组对颅内动脉瘤的检出效能比较
DSA诊断出颅内动脉瘤患者293例,共计368个动脉瘤,其中79例患者为多发动脉瘤。传统人工组、AI组、人工联合AI组对颅内动脉瘤的检出率分别为92.12%、92.12%、95.92%,组间比较差异无统计学意义(P>0.05)。但人工联合AI组识别颅内动脉瘤的灵敏度(95.92%)、特异度(92.42%)、准确度(95.39%)均高于单一诊断,假阳性率(7.58%)、假阴性率(4.08%)均低于单一诊断(表1、2)。
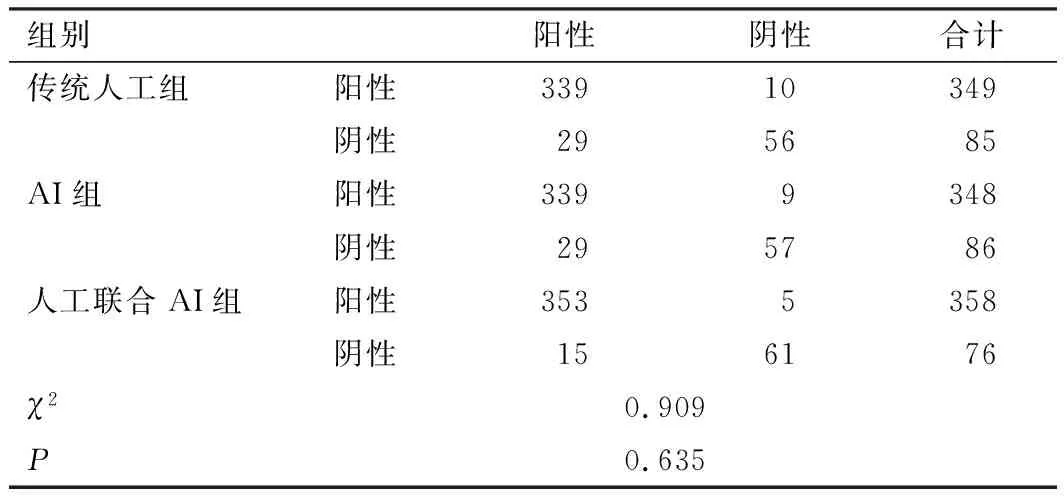
表1 3组诊断颅内动脉瘤的效能比较(n=368,个)
2.2 传统人工组及AI组颅内动脉瘤漏诊的原因分析
传统人工组及AI组均有29个动脉瘤漏诊,将2组动脉瘤直径、毗邻骨质、非常见部位、形态失常、合并动静脉畸形/烟雾病/夹闭术后复发、非责任动脉瘤等6个漏诊原因进行分析,结果显示,2组在毗邻骨质、合并动静脉畸形/烟雾病/夹闭术后复发、非责任动脉瘤方面比较,差异有统计学意义(P<0.05),见表3、图1。
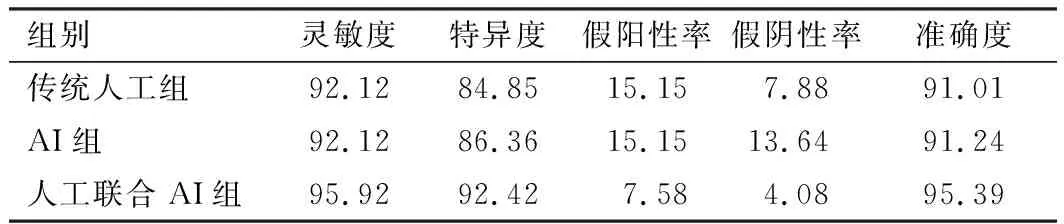
表2 3组识别颅内动脉瘤的真实性比较(%)
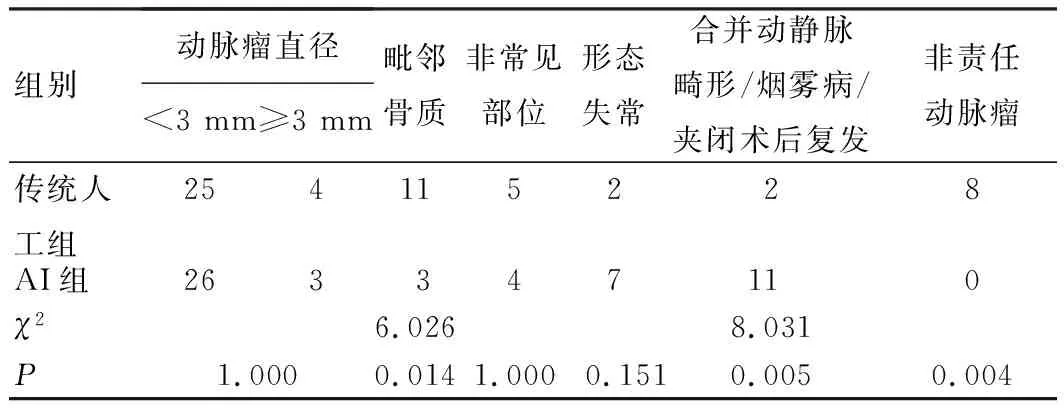
表3 动脉瘤漏诊原因比较(n=29,个)
注:灵敏度=真阳性个数/(真阳性个数+假阴性个数)×100%;特异度=真阴性个数/(真阴性个数+假阳性个数)×100%;假阳性率=假阳性个数/(真阴性个数+假阳性个数)×100%;假阴性率=假阴性个数/(真阳性个数+假阴性个数)×100%;准确度=(真阳性个数+真阴性个数)/总个数×100%
2.3 传统人工组及AI组颅内动脉瘤误诊情况
传统人工组及AI组均将8个脉络膜前动脉起始端动脉瘤误诊为颈内动脉交通段动脉瘤;AI组将4个小脑后下动脉瘤误诊为椎动脉动脉瘤,但传统人工组对椎动脉瘤无误诊;传统人工组将1个颈内动脉眼段、1个颈内动脉交通段及2个大脑中动脉经DSA确认为动脉圆锥处误诊为动脉瘤,但AI组均准确识别。
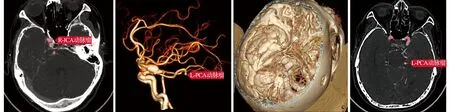
a:传统人工漏诊右侧颈内动脉眼段小动脉瘤,AI自动识别并标注;b:前交通动脉瘤夹闭术后动脉瘤局部复发,AI未能识别;c:传统人工因左侧大脑后动脉P3段小动脉瘤为非责任动脉瘤而漏诊;d:AI自动识别传统人工漏诊动脉瘤并标注
3 讨论
3.1 漏诊原因分析
本研究中,对于直径<3 mm的微小动脉瘤,传统人工漏诊25个,AI漏诊26个。既往文献表明,CTA漏诊的动脉瘤多为直径<3 mm的微小动脉瘤[5],其对微小动脉瘤的诊断敏感度仅为81.8%[6],对该类动脉瘤的检出具有局限性[7]。
本研究中传统人工组在诊断毗邻骨质、非责任动脉瘤方面漏诊率较AI组高,这是由于人为手动去除骨质时易过度去除周围动脉及动脉瘤结构,进而导致漏诊,且可能存在骨质残留或过度去除;而AI使用3D卷积神经网络实现头颈血管CTA重建,并可同步自动去除骨质[8],有效避免了人工去除骨质存在的问题。在颅内多发动脉瘤患者中,传统人工更多关注破裂动脉瘤,尤其当非责任动脉瘤较小或位置较隐蔽时易漏诊[9],而AI对于颅内动脉瘤的诊断基于算法分割,能避免非责任动脉瘤的漏诊。Dai等[10]对208例患者颅脑CTA图像的去骨相行全卷积神经网络训练,在103例验证集中得出其对动脉瘤的检测灵敏度为91.8%,本研究中AI对动脉瘤的检测灵敏度为92.12%,与该研究基本一致。目前,AI算法在分割颅内血管基础上还能检测相应脑血管区域血管直径,然后根据检查特征值诊断动脉瘤,易诊断出大的囊状、梭形动脉瘤,但对于部分形态失常、垂直于血管长轴或血管转弯处的动脉瘤无法识别,因此存在假阳性可能[11-12],这与传统计算机辅助设计算法有关。本研究中,AI对合并动静脉畸形/烟雾病/夹闭术后复发动脉瘤的漏诊率高于传统人工,这是由于AI深度学习模型对于动静脉畸形血管及烟雾病异常血管无法识别[13],而动脉瘤夹闭术后局部金属物放射伪影会产生遮盖干扰,因此AI对于这3类特殊类型的动脉瘤识别效能较差,而传统人工在这类动脉瘤的识别方面经验较为丰富,所以漏诊率较低。
3.2 误诊原因对比分析
本研究结果显示,传统人工及AI多将脉络膜前动脉起始端动脉瘤、小脑后下动脉瘤误诊为颈内动脉交通段动脉瘤及椎动脉动脉瘤。脉络膜前动脉起源于颈内动脉,其动脉瘤发生率占颅内动脉瘤的2%~5%,小脑后下动脉为椎动脉最大分支,其动脉瘤发生率占颅内动脉瘤的0.5%~3%[14-15],这两处血管的解剖特异性决定了其治疗的特殊性[16],故术前明确诊断对患者治疗方案的选择有重大意义。CTA对脉络膜前动脉显示欠佳,易将脉络膜前动脉起始端动脉瘤误诊为后交通动脉瘤,同时由于诊断医生的经验欠缺以及AI对这两种血管分割显示不足而易导致误诊。
本研究中传统人工组将1个颈内动脉眼段、1个颈内动脉交通段及2个大脑中动脉诊断为动脉瘤,经DSA确诊为动脉圆锥,而AI组无此类误诊。这是由于动脉圆锥顶端发出的细小血管不易被传统人工识别[17],但AI能识别远端小血管。因此,使用AI处理图像,再由诊断医师在工作站上多方位旋转图像、调节窗宽窗位,观察其远端发出的小血管影,可避免该类误诊的发生。
3.3 传统人工联合AI能有效提高颅内动脉瘤检出率
颅内动脉瘤漏诊常由多因素共同作用导致,并以某一个因素介导为主。本研究中传统人工组对于毗邻骨质的动脉瘤和非责任动脉瘤的漏诊率相对较高,而AI强大的自动去骨算法正好弥补了这一缺陷;但AI对合并动静脉畸形/烟雾病/夹闭术后复发动脉瘤的漏诊率较高,这是由于AI算法排除了合并动静脉畸形/烟雾病/夹闭术后复发导致的动脉瘤,因此AI对这类动脉瘤的识别存在缺陷,而传统人工的临床工作经验又正好填补这类空白区。本研究中传统人工及AI对于直径<3 mm、非常见部位、形态失常的动脉瘤均易漏诊,而人工联合AI能有效避免单一诊断方法导致的漏诊问题,对颅内动脉瘤诊断的灵敏度、特异度及准确度均较高。本研究通过对比DSA结果,弥补了传统人工及AI识别脉络膜前动脉起始端动脉瘤及小脑后下动脉瘤的不足,加深了临床对这两个部位动脉瘤的认识。
本研究纳入的病例为单中心数据,传统人工组可能存在临床经验局限性,如对小脑后下动脉瘤及脉络膜前动脉起始端动脉瘤认识不足;此外,AI颅内动脉瘤识别的神经网络分割模型排除了合并动静脉畸形/烟雾病/夹闭术后复发的动脉瘤,因而AI对于颅内动脉瘤的真实判断也存在局限性。
综上,传统人工及AI优势互补,两者联合能提高对颅内动脉瘤诊断的灵敏度、特异度及准确度,并降低假阳性率和假阴性率。
