猪肉粉中亚硝酸钠标准物质的研制
2022-02-26李梦怡王宏伟董喆曹进
李梦怡,王宏伟,董喆,曹进
(中国食品药品检定研究院,北京 100050)
亚硝酸盐是含有亚硝酸根阴离子的盐,较常见的形式是亚硝酸钠,它广泛存在于人类生活环境中。食用亚硝酸盐含量较高的腌制肉制品、泡菜及变质的蔬菜可引起中毒。参考世界卫生组织国际癌症研究机构公布的“致癌物清单初步整理”,在导致内源性亚硝化条件下摄入的硝酸盐或亚硝酸盐在2A 类致癌物清单中[1]。
食品基质标准物质在分析质量控制领域起到了举足轻重的作用[2]。在食品安全国家抽检工作中,承检机构被要求每一次检验均随行检测相应基质的标准物质作为内部质量控制,以保证检测结果的可靠性。通过国家标准物质资源共享平台查询,我国暂无肉粉中亚硝酸盐食品基质标准物质出售。目前市场上出售食品基质标准物质的种类远无法满足检验质量控制的需求,当产品售罄后,补货需要重新制备、定值、评估、申报,且供货周期不稳定。食品基质标准物质市场长期处于供不应求的状态。
为监控亚硝酸盐的检测能力,保证检测结果有效、可靠,并且具有溯源性、可比性和准确性,结合相关标准和类似基质标物研制方法[3-9],笔者研制了猪肉冻干粉中亚硝酸钠成分分析标准物质。该标准物质可用于相关检测实验进行亚硝酸钠分析方法的确认和过程质量控制,保证测试分析量值溯源链的有效性和不间断性,并为研制食品基质标准物质提供了可操作的流程实例。
1 实验部分
1.1 主要仪器与试剂
分光光度计:U 3900 型,单色光学系统,日立科学仪器(北京)有限公司。
电子分析天平:(1)AL 204 型,感量为0.1 mg;(2)XP 205 型,感量为0.01 mg,梅特勒-托利多国际贸易(上海)有限公司。
超纯水系统:H2Opro-DI-B 型,德国赛多利斯公司。
离心机:HC 型,转速大于5 000 r/min,安徽中科中佳科学仪器有限公司。
亚硝酸钠标准物质:质量分数为99.7%,北京曼哈格生物科技有限公司。
亚铁氰化钾、乙酸锌、冰乙酸、硼酸钠、盐酸、对氨基苯磺酸、盐酸萘乙二胺:均为分析纯,国药集团化学试剂有限公司。
实验用水为超纯水。
原料:新鲜市售猪肉。
1.2 溶液配制
精密称取亚硝酸钠10 mg(精确至0.1 mg),用水溶解并定容至10 mL,配制成亚硝酸钠质量浓度为1 000 μg/mL 的标准储备液,再用水稀释成亚硝酸钠质量浓度为5.0 μg/mL 的标准工作溶液。
1.3 样品制备
亚硝酸钠对湿度较为敏感,而猪肉的含水率很高,在储存过程中,为了保证基质不变质且目标物含量的稳定,最终采用冷冻干燥方式将猪肉制备成冻干粉。选择市售新鲜猪肉作为对照物质的基体加工原料,满足标准物质制备具有代表性、消除基体效应、均匀性、稳定性保证等相关要求。对市售猪肉进行加标浸泡、粉碎、混匀、冻干、均匀性初检。制成约含亚硝酸钠10 mg/kg 的粉末样品,分装为5 g/瓶,于塑料瓶密闭冷冻保存。
1.4 样品处理
1.4.1 样品复原
精密称取1 g 样品(精确至0.01 mg),置于150 mL 具塞锥形瓶中,以称样量4 倍质量的比例加入超纯水使其复原为肉糜,振摇使其充分混匀,浸泡30 min 以上。
1.4.2 提取与净化
(1)提取。向1.4.1 复原液中加入12.5 mL 的50 g/L 的饱和硼砂溶液,再加入150 mL 温度约为70 ℃的水,混匀,于沸水浴中加热15 min,取出,置于冷水浴中,冷却至室温。
(2)净化。定量转移上述提取液,置于200 mL容量瓶中,加入5 mL 106 g/L 亚铁氰化钾溶液,摇匀,再加入5 mL 220 g/L 乙酸锌溶液以沉淀蛋白质,用水稀释并定容至标线,摇匀,放置30 min,除去上层脂肪,上清液用滤纸过滤,弃去初滤液30 mL,滤液备用。
1.4.3 样品测定
吸取1.4.2 中滤液40.0 mL,置于50 mL 带塞比色管(试样管)中;另分别吸取0.00、0.20、0.40、0.80、1.50、2.00 mL 亚硝酸钠标准工作溶液,分别置于50 mL 带塞比色管(标准管)中。分别于标准管与试样管中加入2 mL 4 g/L 对氨基苯磺酸溶液,混匀,静置3~5 min 后,再各加入1 mL 2 g/L 盐酸萘乙二胺溶液,加水定容至标线,混匀,静置15 min,用1 cm 比色杯,以零管调节零点,于波长538 nm 处测定吸光度,绘制标准工作曲线[10-12]。
1.5 样品均匀性和稳定性考察
分别参照CNAS-GL03: 2006 《能力验证样品均匀性和稳定性评价指南》、CNAS-GL017: 2018 《标准物质/标准样品定值的一般原则和统计方法》、JJF 1343—2012 《标准物质定值的通用原则及统计学原理》中关于均匀性、稳定性检验的要求进行统计[13-15]。
1.5.1 均匀性检验
当实验样品总数小于500 时,随机抽取15 个样品进行均匀性检验,每个样品平行测定2 次。采用单因素方差分析,计算测定结果的F值,在95%置信区间内,当F值小于查表值Fα时,可认为样品是均匀的。
1.5.2 稳定性检验
(1)短期稳定性。样品采用棕色塑料瓶包装,属于避光密封状态,因此短期稳定性主要考察在运输过程中,高温、高湿条件对猪肉粉中亚硝酸钠含量的影响。按照目前的物流运输速度,运输时间一般不超过7 天。模拟在40 ℃、湿度为80%的极端条件下存放7 天后,对标准物质进行短期稳定性研究。以均匀性检测结果为短期稳定性0 点,分别在第1、3、7 天取样,每次取3 份样品,每份样品检测2 次,采用t检验法评定样品的短期稳定性。
(2)长期稳定性。按照先密后疏的考察原则设置不同的采样时间点,采用同步稳定性评估方法进行稳定性分析。以均匀性检测结果为长期稳定性0点,按推荐方式储存样品。分别在第1、2、4、6 月取样,每次取3 份样品,每份样品检测2 次,采用t检验法评定样品的长期稳定性。
1.6 定值方法
分别参照JJF 1343—2012 《标准物质定值的通用原则及统计学原理》、ISO GUIDE 35: 2017 《均匀性和稳定性表征和评估用标准物质指南》,采用同一种方法多家实验室联合定值的方式对标准物质进行定值。选择7 家在行业领域中经验丰富且经国家认证的检测实验室或检测中心,分别向每个定值实验室提供肉粉空白样品和阳性样品各不少于4 份,每个样品分别平行测定2 组数据。各定值机构向中国食品药品检定研究院提供不少于8 组测量数据。同时,定值过程中,标准物质研制单位制定了明确的定值方案,并要求随行做加标回收试验,以确保各实验室定值结果可靠、稳定。


剔除离群值后,计算出各实验室检测结果中位值的中位值,该总体中位值即样品的定值结果。
1.7 不确定度的评定
1.7.1 指定值的不确定度计算
计算各协作定值单位结果的中位值,记为Ni。以这些中位值的中位值作为指定值,记为X。计算N1、N2…Ni与X之差的绝对值,记为Q1、Q2…Qi,其中位值记为Qm。协作定值引入的不确定度按照公式(1)计算:

1.7.2 均匀性的不确定度计算
均匀性的不确定度及相对不确定度分别按公式(3)、(4)计算,结果见表6。

1.7.3 长期稳定性的不确定度计算
将稳定性检验结果按时间-浓度做线性拟合,计算拟合直线残差为斜率不确定度,如公式(5)。按公式(6)、(7)分别计算长期稳定性的不确定度和相对不确定度。


1.7.4 合成不确定度计算
以定值、均匀性、稳定性引入的不确定度计算标准物质的合成相对不确定度,按公式(8)计算。按照公式(9)计算标准物质合成不确定度。在95%的置信区间,取包含因子k=2,按照公式(10)计算标准物质的扩展不确定度。

2 结果与分析
2.1 均匀性检验结果
按1.5 方法进行样品均匀性检验,采用单因素方差分析方法对样品测定结果进行数据统计,肉糜样品中亚硝酸钠含量测定结果如表1 所示,F检验分析结果如表2 所示。

表1 肉糜样品中亚硝酸钠含量测定结果 mg/kg

表2 肉糜样品中亚硝酸钠含量测定方差分析结果
查表得F0.05(14,15)=2.42,猪肉粉中亚硝酸钠标准物质的F计算值为1.95,F<F0.05(14,15),表明在95%置信区间内,研制的猪肉粉中亚硝酸钠标准物质样品均匀性良好。
2.2 稳定性检验结果
2.2.1 短期稳定性
按1.5.2 方法进行样品短期稳定性检验,检测结果见表3。

表3 亚硝酸钠短期稳定性检测结果
以均匀性检测结果为稳定性0 天,采用t检验法评定样品的短期稳定性。由表3 可知,短期稳定性的t值均小于查表值,表明在40 ℃、湿度为80%的极端条件下,研制的猪肉粉中亚硝酸钠标准物质在7 天内是稳定的。
2.2.2 长期稳定性
按照1.5.2 方法进行样品长期稳定性检验,检测结果见表4。以均匀性检测结果为稳定性0 天,与稳定性3 个月次的检测结果(表4)以时间-浓度做线性拟合,并做回归方差分析(表5)。

表4 长期稳定性检测结果 mg/kg

表5 长期稳定性检测回归方差分析(95%置信水平)
由表5 可知,在95%的置信水平,斜率的P值大于0.05,说明研制的猪肉粉中亚硝酸钠标准物质在6 个月内稳定性良好[15]。
2.3 协作定值结果及离群值检验
发放协作定值样品,按照1.6 方法进行定值,回收各协作单位定值检测结果,其中单位A~F 与样品制备方H 均返回8 个检测数据,单位G 返回10 个检测数据,协作定值结果见表6。

表6 协作定值结果 mg/kg
采用格拉布斯(Grubb’s)检验,对8 家协作定值单位的实验室内检测结果进行离群值检验,检验结果见表7。由表7 可知,格拉布斯法组内可疑值检验νi/S均小于查表值λ(0.05,8)=2.126,未观测到组内离群值。

表7 格拉布斯法组内可疑值检验结果
采用狄克森检验对对8 家定值单位(7 家协作定值单位和样品制备方H)的实验室间检验结果的一致性进行评价,检验结果见表8。由表8 可知,狄克森检验对组间数据进行离群值检验,r1及rn值均小于查表值f(0.05,8)=0.608,未观测到组间离群值。

表8 狄克逊法组间显著性差异检验
采用科克伦检验对组间数据做等精度检验,检验结果见表9。由表9 可知,单位测定数据C值小于临界值C(0.05,8,8)=0.318 5,各组数据等精度,可保留所有数据。
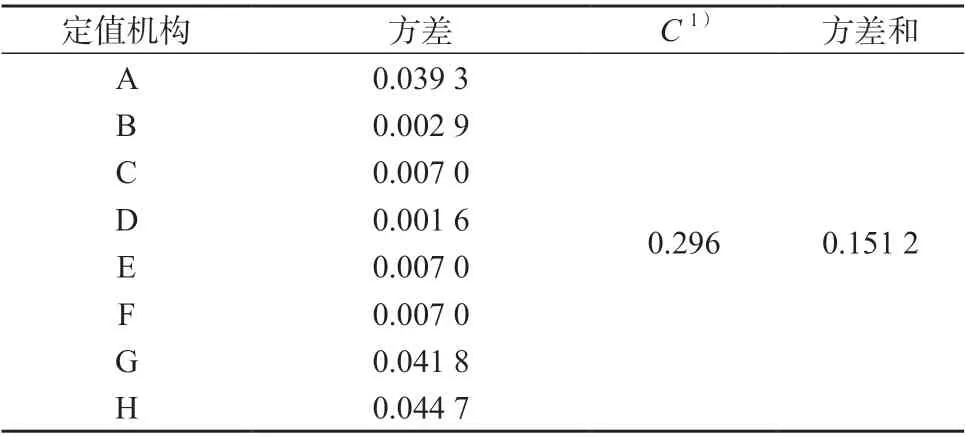
表9 科克伦法组间等精度检验
2.4 定值不确定度的计算
按照1.7 方法进行猪肉粉中亚硝酸钠标准物质定值不确定度计算。定值过程引入的不确定度计算结果见表10。

表10 猪肉粉中亚硝酸钠协作定值计算结果
猪肉粉中亚硝酸钠标准物质协作定值、均匀性、稳定性引入的不确定度计算结果见表11。

表11 不确定度计算结果
按95%的置信区间,取包含因子k=2,按照公式(10)计算猪肉粉中亚硝酸钠标准物质的扩展不确定度为1.01 mg/kg。
2.5 猪肉粉标准物质的定值结果
分别经过均匀性检验、稳定性检验以及8 家实验室协作定值,最终确定猪肉粉标准物质中亚硝酸钠的定值结果(以肉糜计)为(10.35±1.01) mg/kg(k=2)。
3 结语
制备了猪肉粉中亚硝酸钠标准物质。采用盐酸萘乙二胺法对样品中亚硝酸钠含量进行测定。样品均匀性和稳定性满足标准物质制备要求,经8 家实验室协作定值,并对定值结果的不确定度进行评估,最终确定该样品中亚硝酸钠的定值结果(以肉糜计)为(10.35±1.01) mg/kg(k=2)。研制的猪肉粉标准物质具备做猪肉粉中亚硝酸钠检测基体参考物质的使用条件[16]。
