木醋液改性羟基磷灰石对溶液中Cd2+的吸附特性
2022-02-22杨晨琛万亚珍梅丹丹张文辉张爽爽
杨晨琛,万亚珍,梅丹丹,张文辉,张爽爽,周 灿
(1.郑州大学化工学院,郑州 450000;2.河南力浮科技有限公司,郑州 450000)
0 引 言
水是人类赖以生存和发展的物质基础,也是经济社会发展不可或缺的宝贵自然资源。然而一些自然活动,如火山活动、岩石风化等,以及一些人类活动,如矿山开采、肥料和杀虫剂的滥用等,给地表水、地下水等水资源带来了重金属污染[1]。其中,Cd2+具有毒性强、迁移率高的特点,易在食物链中富集[2]。人体中积累过量的Cd2+会对肾脏、骨骼等造成损害,导致骨软化和骨萎缩[3],严重危害人类健康。
去除溶液中Cd2+的方法有很多,如:化学沉淀、电化学处理、膜过滤、吸附等[4]。其中,吸附法具有成本低、效率高、操作简便等优势[5],是常用的Cd2+污染水处理方法。羟基磷灰石(hydroxyapatite, HAP)具有特殊的结构,Ca2+容易与金属阳离子发生离子交换而被取代[6],在溶液中有较好的水不溶性,已经被研究用于溶液中Cd2+的去除。然而,HAP对Cd2+的吸附容量是有限的,需要对HAP进行处理或改性以增强吸附能力。目前对HAP吸附Cd2+的研究主要从两方面展开,一种是寻找新的廉价的材料为磷源或钙源制备HAP,另一种是对HAP进行改性以增加其去除Cd2+的能力。本研究结合了这两个方面,使用廉价的材料改性HAP,探究改性后的HAP对溶液中Cd2+的吸附特性。
木醋液(wood vinegar, WV)是木材等生物质缓慢热解产生的烟雾粗冷凝物,来源广泛、成本低,现已作为植物生长调节剂、食品保鲜剂、抗菌消炎剂等应用于农林生产、食品加工、医疗卫生等领域[7]。WV对环境无污染,已被研究作为污染物去除的添加剂[8-9]。本研究使用WV为改性剂来制备木醋液改性羟基磷灰石(wood vinegar modified hydroxyapatite, WV-HAP),并对其结构和形貌进行了表征。同时,探究了WV-HAP对Cd2+的吸附特性和机理,以期为WV-HAP处理含Cd2+污染水提供一定的理论依据。
1 实 验
1.1 试 剂
硝酸镉,分析纯,上海麦克林生化科技有限公司;羟基磷灰石,分析纯,南京都莱生物技术有限公司;木醋液,石家庄宏森活性炭有限公司;硝酸,分析纯,南京化学试剂股份有限公司;氢氧化钠,分析纯,天津市风船化学试剂科技有限公司。
1.2 WV-HAP的制备
HAP与稀释500倍的WV按照固液比1 g ∶10 mL的比例混合,在80 ℃下搅拌6 h,产品通过离心从溶液中分离出来,用蒸馏水洗涤,在60 ℃下干燥至恒重,即得到WV-HAP。
1.3 吸附试验
在一定温度和pH值下,将吸附剂与一定浓度Cd2+溶液按照2 g/L的比例混合置于聚乙烯管中,通过搅拌一定的时间进行吸附试验,溶液的pH值用0.1 mol/L的硝酸和0.1 mol/L的氢氧化钠调节。在以上的操作条件下,通过改变溶液初始pH值为2~8、初始Cd2+浓度为50~1 050 mg/L、接触时间1~480 min和温度298~318 K来探讨这些操作参数对WV-HAP对Cd2+吸附特性的影响。所有吸附试验重复三次,用TAS-990原子吸收分光光度计测定溶液中Cd2+和Ca2+的浓度。Cd2+的去除效率(R,%)、Cd2+在吸附剂上的吸附容量(qe,mg/g)由公式(1)、公式(2)计算[10]:
(1)
(2)
式中:C0为溶液的初始Cd2+浓度,mg/L;Ce为溶液的平衡Cd2+浓度,mg/L;V为溶液的体积,L;m为吸附剂的质量,g。
1.4 表 征
用D8 ADVANCE X射线衍射(XRD)仪分析物相,加速电压40 kV,扫描范围10°~90°;用Nicolet IR200傅里叶变换红外光谱(FT-IR)仪分析基团,收集4 000~400 cm-1范围内的光谱;用ASPS 2460比表面积和孔径分析仪分析比表面积和孔径,测定样品在77 K下的N2吸附-解吸等温曲线;用AURIGA-BU扫描电镜(SEM)观察表面形貌,用其能谱仪的部分分析样品成分。
2 结果与讨论
2.1 WV-HAP的表征分析
HAP和WV-HAP的XRD谱如图1所示。由图1可以看出,出现在2θ=25.77°、31.75°、34.02°、39.78°、46.69°、49.36°的衍射峰分别对应于HAP(PDF#09-0432)的(002)、(211)、(202)、(130)、(222)、(213)晶面。WV-HAP的衍射峰位置和HAP一致,且没有明显的新衍射峰形成,表明WV改性并未改变HAP的物相结构。与HAP相比,WV-HAP的衍射峰强度增大,表明WV改性后结晶度提高了。


图1 HAP和WV-HAP的XRD谱Fig.1 XRD patterns of HAP and WV-HAP

图2 HAP和WV-HAP的FT-IR谱Fig.2 FT-IR spectra of HAP and WV-HAP
HAP和WV-HAP的SEM照片如图3所示,图3(a)~(c)分别为HAP放大30 000倍、6 000倍、500倍的SEM照片,图3(d)~(f)分别为WV-HAP放大30 000倍、6 000倍、500倍的SEM照片。从图3(a)、(b)、(d)、(e)可以看出,HAP表面存在致密的光滑结构,经WV改性后,WV-HAP表面变得粗糙且表面的孔道增加。从图3(c)、(f)可知,HAP主要为球形颗粒,与HAP相比,WV-HAP完整的球状颗粒很少,这是酸性的WV对HAP的酸蚀作用所致。
表1为HAP和WV-HAP的比表面积、孔体积和孔隙大小的数据。从表1看出,与HAP相比,WV-HAP的比表面积和孔体积增大、孔径减小,这归因于改性过程酸性WV对HAP的成孔作用。比表面积和孔体积越大,对重金属离子的吸附能力越强[12]。


图3 HAP和WV-HAP的SEM照片Fig.3 SEM images of HAP and WV-HAP

表1 HAP和WV-HAP的表面特性Table 1 Surface features of HAP and WV-HAP
2.2 WV-HAP对Cd2+的吸附特性
2.2.1 溶液初始pH值对吸附效率的影响
溶液的初始pH值是影响吸附过程的重要因素,因为它会影响重金属在溶液中的存在状态和吸附剂的表面电荷[13]。当溶液pH值达到8.5时,Cd2+形成氢氧化镉沉淀而去除[14]。因此,为了减弱沉淀对吸附Cd2+的影响,在pH 值为2~8范围内进行吸附试验。
图4为初始pH值对HAP和WV-HAP对Cd2+去除效率及对吸附Cd2+后释放Ca2+的影响。从图4(a)可以看出,WV-HAP在广泛的pH值范围内对Cd2+都有较高的去除效率(74.62%~97.54%),且均高于HAP。溶液pH值为5时,WV-HAP对Cd2+的去除效率最高,为97.54%,此时吸附容量也最大,为46.43 mg/g。在较低的pH值下,溶液中存在较多的H+与Cd2+竞争,导致WV-HAP对Cd2+的去除效率较低。随着溶液初始pH值的增大,H+与Cd2+的竞争减弱,WV-HAP对Cd2+的去除效率增加。

图4 初始pH值对HAP和WV-HAP对Cd2+去除效率的影响及对吸附Cd2+后释放Ca2+的影响 (Cd2+100 mg/L,添加量2 g/L,298 K,4 h)Fig.4 Effect of initial pH on Cd2+ removal efficiency by HAP and WV-HAP and release of Ca2+ after adsorption of Cd2+ (Cd2+100 mg/L, adsorbent dosage 2 g/L, 298 K, 4 h)
为了探究WV-HAP吸附Cd2+的机理,测定了吸附Cd2+后溶液中Ca2+的浓度。从图4(b)可以看出,在较低的pH值下,溶液中Ca2+浓度较高,这是较强的酸性导致了WV-HAP的溶解。在pH值为2时,溶液中Ca2+浓度最高,然而对Cd2+的去除效率并不高,这说明溶解-沉淀机制并不是WV-HAP去除Cd2+的主要机制。在pH值为4~8时,WV-HAP具有较高的水不溶性,然而溶液中仍有Ca2+,且此时对Cd2+的去除效率较高,这表明离子交换是WV-HAP去除Cd2+的主要机制。在pH 值为2~8内,WV-HAP吸附Cd2+后溶液中Ca2+的浓度均高于HAP,这归因于WV改性后,WV-HAP的比表面积和孔体积增大使得离子交换变得容易。
在广泛pH值下WV-HAP对Cd2+的去除效率都较高,可以减少在实际污染水处理过程中调节pH值的成本,具有一定的经济效益。在溶液pH值为5时,WV-HAP对Cd2+的去除效率最高,因此,以下的吸附试验均在pH值为5时进行。
2.2.2 初始离子浓度对吸附容量的影响及吸附等温线分析
一定量的吸附剂含有的吸附位点和吸附容量是有限的,当吸附位点完全被重金属离子占据时,即达到最大吸附容量。因此,探究初始离子浓度变化对吸附的影响有利于确定吸附剂的最大吸附容量。
图5为初始离子浓度对HAP和WV-HAP吸附Cd2+的影响及WV-HAP吸附Cd2+的等温吸附模型拟合。从图5(a)可以看出,随着初始Cd2+浓度的增加,HAP和WV-HAP对Cd2+的吸附容量均呈现先增后稳定的趋势,WV-HAP显示出比HAP更高的对Cd2+的吸附容量。表2为298 K时HAP、WV-HAP吸附Cd2+的等温吸附模型拟合参数,从表2中可以看出,298 K时,WV-HAP对Cd2+的最大吸附容量为125.31 mg/g,高于HAP的最大吸附容量104.28 mg/g。这是因为WV改性后,WV-HAP表面变得粗糙,比表面积和孔体积增大,使得更多的吸附位点暴露出来,Ca2+与Cd2+的离子交换作用增强,有利于对Cd2+的吸附。
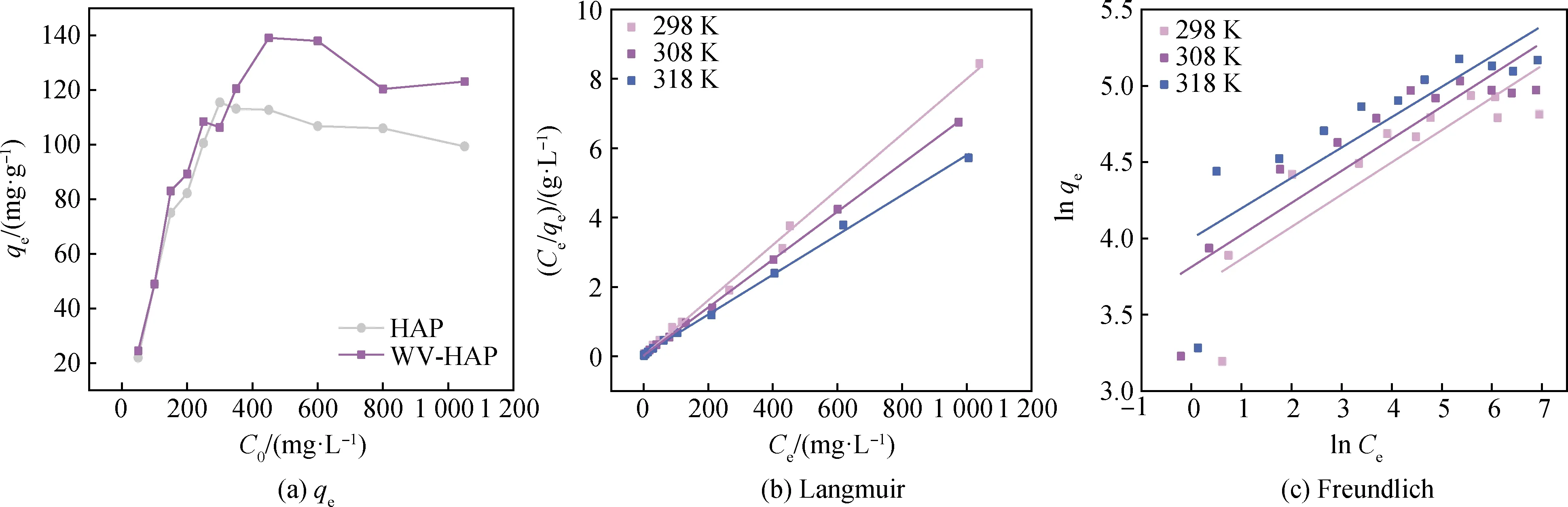
图5 初始离子浓度对HAP和WV-HAP吸附Cd2+的影响(a)(pH 5,添加量2 g/L,298 K,4 h)及WV-HAP吸附 Cd2+的等温吸附模型拟合(b,c)(pH 5,添加量2 g/L,4 h)Fig.5 Effect of initial ion concentration on Cd2+ adsorption by HAP and WV-HAP (a) (pH 5, adsorbent dosage 2 g/L, 298 K, 4 h) and fitting of isothermal adsorption model for Cd2+ adsorption by WV-HAP (b, c) (pH 5, adsorbent dosage 2 g/L, 4 h)

表2 298 K时HAP、WV-HAP吸附Cd2+的等温吸附模型拟合参数Table 2 Fitting parameters of the isothermal adsorption model for HAP and WV-HAP adsorption of Cd2+ at 298 K
在不同的溶液初始pH值和初始离子浓度下,WV-HAP都表现出优于HAP的对Cd2+的吸附能力,这表明WV改性的有效性。因此,在以下的研究中主要探讨WV-HAP对Cd2+的吸附特性。
对WV-HAP在不同初始浓度下吸附Cd2+的数据进行等温吸附模型的拟合,拟合的参数如表3所示。结合图5(b)和(c)可以看出,WV-HAP对溶液中Cd2+的吸附过程与Langmuir模型有较高的拟合,根据拟合计算出的最大吸附量可达173.91 mg/g(318 K),表现出对Cd2+较强的吸附能力。WV-HAP上的吸附位点是有限数的均质位点,吸附过程为单分子层吸附。Freundlich模型中的n表示吸附驱动力或表面不均匀性的大小,n的值在0~10范围内表示有利于吸附[15]。从表3可以看出,WV-HAP的n值均在0~10范围内,表明在目前的试验条件下对吸附是有利的。

表3 WV-HAP吸附Cd2+的等温吸附模型拟合参数Table 3 Fitting parameters of isothermal adsorption model of Cd2+ adsorbed by WV-HAP
2.2.3 接触时间对吸附容量的影响及动力学分析
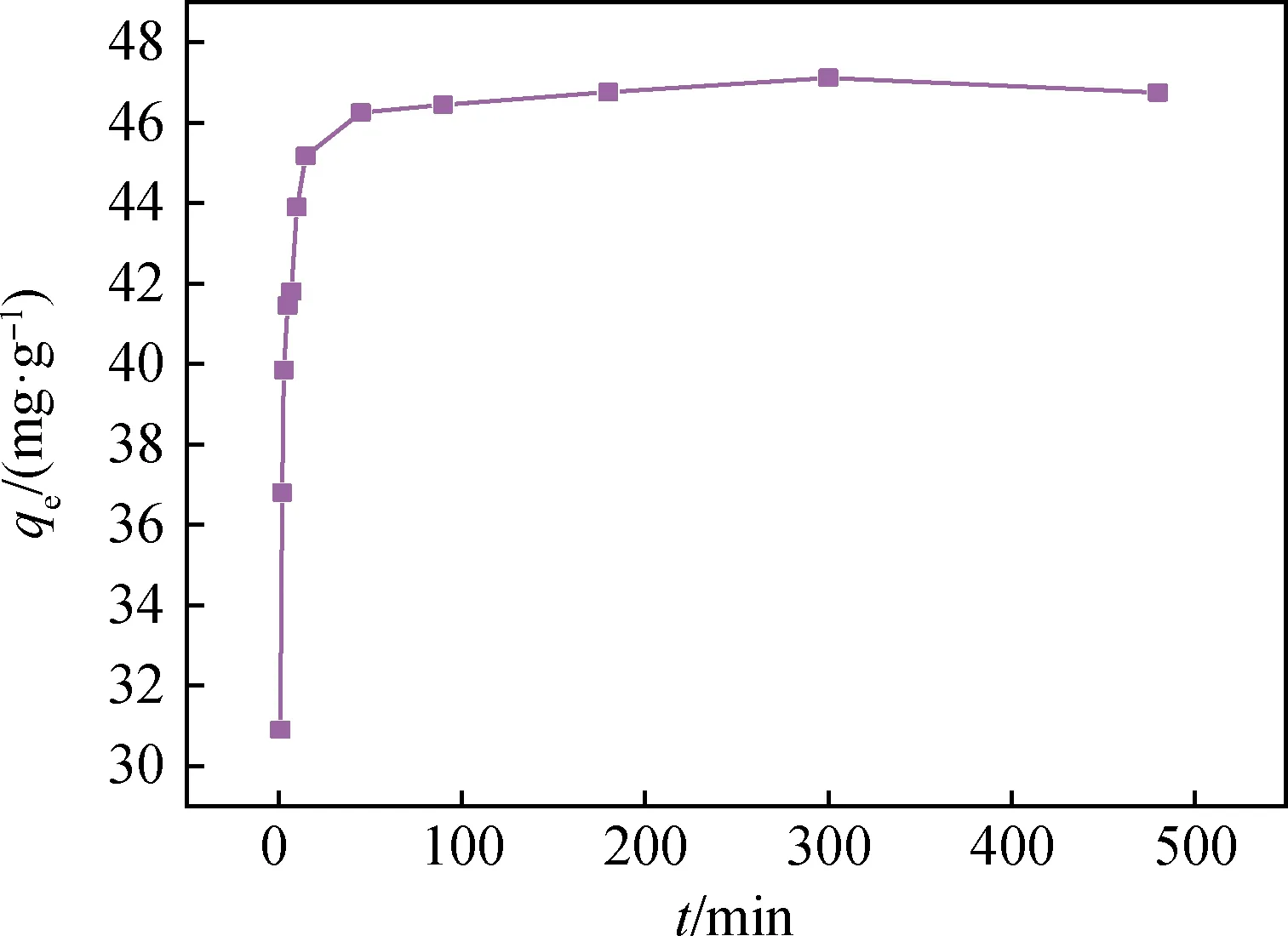
图6 接触时间对WV-HAP吸附Cd2+的影响 (Cd2+100 mg/L,添加量2 g/L,298 K,pH 5)Fig.6 Effect of contact time on Cd2+ adsorption by WV-HAP (Cd2+100 mg/L, adsorbent dosage 2 g/L, 298 K, pH 5)
图6为接触时间对WV-HAP吸附Cd2+的影响。从图6中可以看出,WV-HAP对Cd2+的快速吸附发生在前15 min,然后吸附容量缓慢增加,并在90 min达到吸附平衡,达平衡后对Cd2+的吸附容量趋于稳定(46.45~47.12 mg/g)。
对WV-HAP在不同接触时间下吸附Cd2+的数据进行动力学模型的拟合,来探究吸附特性。图7为WV-HAP吸附Cd2+的动力学模型拟合。拟合的参数如表4所示,结合图7(a)和(b)可以看出,WV-HAP对Cd2+的吸附过程与准二级动力学模型有较高的拟合,相关性达0.999 98。根据拟合计算出的平衡吸附容量为46.90 mg/g,与试验值46.75 mg/g非常接近。WV-HAP吸附Cd2+的主要速率控制步骤是化学反应或化学吸附。因此可以使用颗粒内扩散模型来找到特定的速率控制步骤。
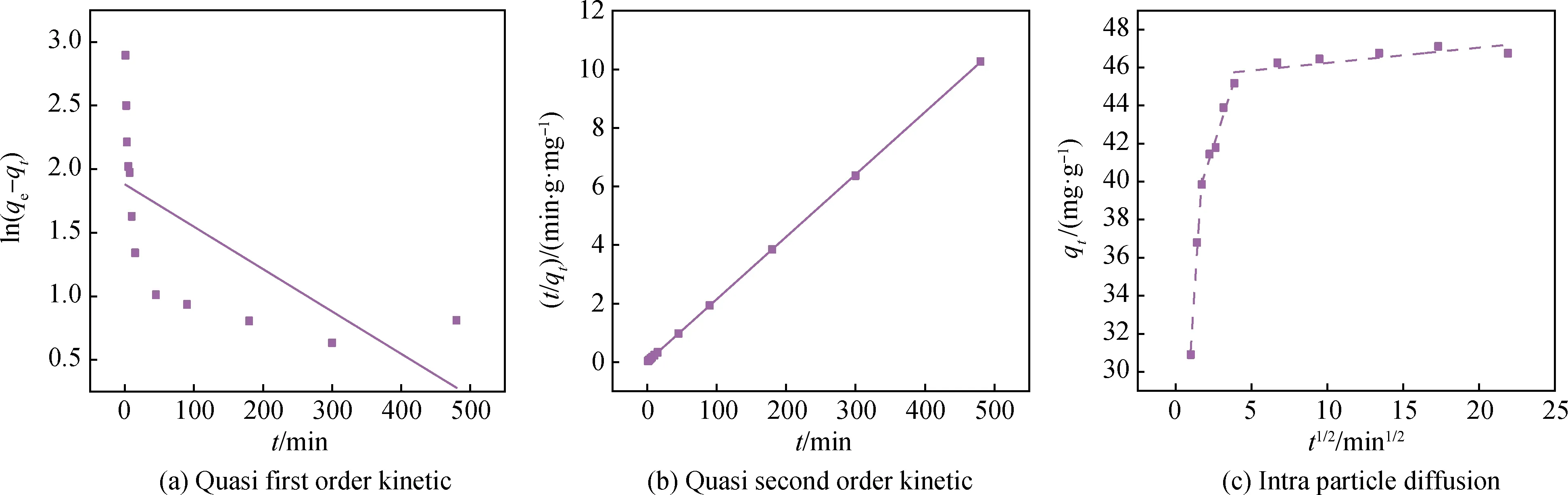
图7 WV-HAP吸附Cd2+的动力学模型拟合(Cd2+100 mg/L,WV-HAP 2 g/L,298 K,pH 5)Fig.7 Adsorption kinetics fitting models of Cd2+ on WV-HAP (Cd2+100 mg/L, WV-HAP 2 g/L, 298 K, pH 5)

表4 WV-HAP吸附Cd2+的准一级、准二级动力学参数Table 4 Quasi first and quasi second order kinetic parameters of Cd2+ adsorbed by WV-HAP


表5 WV-HAP对Cd2+的颗粒内扩散模型参数Table 5 Intra particle diffusion model parameters of Cd2+ by WV-HAP
2.2.4 温度对吸附容量的影响及热力学分析

图8 温度对WV-HAP吸附Cd2+的影响 (Cd2+50~1 050 mg/L,添加量2 g/L,4 h,pH 5)Fig.8 Effect of temperature on Cd2+ adsorption by WV-HAP (Cd2+50~1 050 mg/L, adsorbent dosage 2 g/L, 4 h, pH 5)
进行了不同温度(298 K、308 K、318 K)下的批量吸附试验来探究温度对WV-HAP对Cd2+吸附容量的影响。如图8所示,随着温度的升高,WV-HAP对Cd2+的吸附容量升高,这说明吸附过程是吸热的。
热力学研究是预测吸附机制不可或缺的组成部分。WV-HAP吸附Cd2+的热力学参数如表6所示。焓变(ΔH)>0,表明WV-HAP对Cd2+的吸附过程是吸热的,温度升高有利于对Cd2+的吸附;熵变(ΔS)>0,表明吸附过程中固液界面的无序度增加;吉布斯自由能(ΔG)<0,且随着温度升高,ΔG的值越来越小,表明WV-HAP吸附Cd2+的过程是自发的,温度越高,对吸附越有利。
2.3 吸附机理分析
对WV-HAP吸附Cd2+前后的样品进行XRD、FT-IR、SEM-EDS分析,探究吸附机理。

表6 WV-HAP吸附Cd2+的热力学参数Table 6 Thermodynamic parameters of Cd2+ adsorbed by WV-HAP
图9为WV-HAP吸附Cd2+前后的XRD谱,分析发现衍射峰稍微向更高的角度偏移,即主峰(211)从2θ=31.89°移动到31.94°,(002)晶面特征峰从2θ=25.85°移动到25.90°,这表明吸附Cd2+后WV-HAP中的Ca2+(0.99)通过离子交换被更小的Cd2+(0.97)取代,导致晶胞尺寸减小[17]。没有发现Ca10(PO4)6(OH)2、Cd3(PO4)2等Cd2+的磷酸盐沉淀的相,表明WV-HAP吸附Cd2+的过程主要为离子交换。

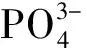
选择WV-HAP中完整的球状结构进行扫描电镜分析,以观察吸附Cd2+前后形貌的改变。图11(a)、(b)分别为WV-HAP放大10 000倍、5 000倍的SEM照片,图11(c)、(d)分别为WV-HAP-Cd放大10 000倍、5 000倍的SEM照片。WV-HAP中的孔道和凹槽可以吸附Cd2+,从图11(c)、(d)可以看出,吸附Cd2+后材料表面的孔道被覆盖和阻塞,表面存在大量的小颗粒,经过EDS分析(见图12)发现这是吸附在WV-HAP表面的Cd2+。吸附试验后的WV-HAP表面均匀的分布着Cd2+。

图9 WV-HAP吸附Cd2+前后的XRD谱Fig.9 XRD patterns of WV-HAP before and after adsorption of Cd2+

图10 WV-HAP吸附Cd2+前后的FT-IR谱Fig.10 FT-IR spectra of WV-HAP before and after adsorption of Cd2+

图11 WV-HAP吸附Cd2+前后的SEM照片Fig.11 SEM images of WV-HAP before and after adsorption of Cd2+
将不同初始pH值下HAP和WV-HAP吸附Cd2+后去除的Cd2+浓度和溶液中游离的Ca2+浓度列于表7,对离子交换这一机理进行定量的分析。从表7中可以看出,HAP在初始pH值为2~8、WV-HAP在初始pH值为3~8时,Cd2+的去除浓度均高于游离的Ca2+浓度,这证实了表面吸附和孔道吸附机理的存在。由于试验只对初始pH值为5时吸附Cd2+后的WV-HAP进行了XRD的表征,发现并没有生成Ca10(PO4)6(OH)2,即此条件下没有溶解-沉淀机理的存在,可以得出初始pH值为5时WV-HAP吸附Cd2+的机理中离子交换占45.67%。Li等[20]的研究表明离子交换机制约占磁性羟基磷灰石负载氧化石墨烯对Pb2+总吸附量的62.15%,由于HAP材料对Pb2+的吸附能力优于对Cd2+的吸附能力[11],这一数据对本试验离子交换的比例也具有一定的参考意义。

图12 WV-HAP吸附Cd2+前后的EDS谱Fig.12 EDS spectra of WV-HAP before and after adsorption of Cd2+

表7 不同初始pH值下HAP、WV-HAP吸附Cd2+后去除的Cd2+浓度和溶液中游离的Ca2+浓度Table 7 Concentration of Cd2+ removed and the concentration of free Ca2+ in solution after Cd2+ adsorption by HAP and WV-HAP at different initial pH value


(3)

(4)
Ca10(PO4)6(OH)2+xCd2+→Ca10-xCdx(PO4)6(OH)2+xCa2+
(5)
3 结 论
(2)吸附条件相同时,WV-HAP在pH值为2~8和初始Cd2+浓度50~1 050 mg/L时表现出对Cd2+的吸附能力都优于HAP。298 K时,根据Langumuir等温吸附模型计算的WV-HAP的最大吸附量为125.31 mg/g,大于HAP的最大吸附量104.28 mg/g。经过WV改性后,增加了WV-HAP对Cd2+的吸附能力,表明改性是有意义的,既提高了材料对Cd2+的吸附能力,又增加了WV的利用价值。
(3)WV-HAP对Cd2+的吸附过程遵循Langmuir等温吸附模型和准二级动力学模型。热力学研究表明,吸附过程是自发的和吸热的。吸附机理主要是表面吸附、孔道吸附和离子交换,在溶液初始pH值为5时,离子交换机制占WV-HAP对Cd2+总吸附量的45.67%。WV-HAP在较广泛的pH值范围内对Cd2+都有较高的去除效率和吸附容量,表现出其作为Cd2+吸附剂的优良性能,为溶液中Cd2+的去除提供了一定的思路。
