牛血清蛋白纳米金团簇基于荧光共振能量转移法灵敏检测尿酸
2022-02-17丛剑涵罗云敬齐小花邹明强孔陈晨
丛剑涵, 罗云敬*, 齐小花, 邹明强, 孔陈晨
1. 北京工业大学环境与生命学部, 环境与病毒肿瘤学北京市重点实验室, 北京 100124
2. 中国检验检疫科学研究院, 北京 100123
引 言
尿酸(uric acid, UA)是人类系统中嘌呤核苷酸代谢的最终产物, 通常存在于生物液体如血清和尿液中, 并且由于尿酸的溶解性极低, 使其易于在人体内累积[1]。 尿酸过多积累会形成固体尿酸盐, 导致诸如高尿酸血症, 痛风性急性关节炎, 肾结石和高血压等疾病, 而血清中尿酸异常低可能会引发帕金森病或多发性硬化[2-3]。 此外, 尿酸作为一种替代性抗氧化剂, 能够清除细胞中氧自由基, 从而使其在许多生理病理和损害发生中起到潜在的神经保护作用[4]。 人体在健康的生理状态下体内尿酸的含量相对稳定, 男性150~420 μmol·L-1, 女性90~357 μmol·L-1, 但在病理状态下, 其含量会发生明显波动。 因此, 血清中尿酸的测定是临床检测中最重要的生化指标之一, 开发一种具有高度选择性, 高灵敏, 高效的尿酸检测方法具有重要意义。
目前, 尿酸的测定方法主要包括高效液相色谱, 质谱, 紫外分光光度, 电化学, 化学发光和毛细管电泳法[5-10]。 Ma等[10]开发了一种毛细管电泳法测定体液中尿酸。 Liu等[11]通过高效液相色谱-质谱联用技术同时测定人唾液中尿酸和肌酐。 陆娟等[12]采用静电纺丝法制备了碳量子点@纳米Co3O4生物传感器检测人血清中的尿酸。 然而上述方法普遍存在繁琐的衍生、 修饰和复杂的前处理等问题, 且仪器价格昂贵、 成本高和特异性低, 限制了其在临床试验中尿酸检测的潜在应用。 作为一种新型的纳米材料, AuNCs荧光探针具有操作简单、 快速、 灵敏度高的优点。 由于其良好的光学性能, 光稳定性和生物相容性, 以及其简单且无毒的制备方法[13], 在临床样品检测中具有广阔的应用前景。
本文以BSA为模板分子成功制备了BSA-AuNCs荧光探针, 并基于尿酸酶促反应产物H2O2对BSA-AuNCs荧光探针的猝灭效应, 开发了一种基于荧光共振能量转移(FRET)的超灵敏生物传感器检测尿酸。 由于强荧光的BSA-AuNCs和氧化态的ox-TMB之间有效的FRET, 使得该方法简便快速, 灵敏度高。
1 实验部分
1.1 试剂和仪器
四水合氯金酸(HAuCl4·4H2O, 国药控股有限公司); BSA(纯度>98%, 美国Amresco公司); H2O2(30%分析纯, 北京化工厂); TMB, UA, Urate Oxidase(纯度>98%, 上海麦克林生化科技有限公司); NaOH, Na2HPO4, NaH2PO4, Citric acid(分析纯, 国药控股有限公司); 实验用水为超纯水(电导率>18 MΩ·cm)。
SH-3恒温磁力搅拌器(北京金科发展公司); PHS-25数字pH计(上海精密科学仪器公司); JEM-2100 透射电子显微镜(日本); U-3010紫外-可见分光光度计(UV, HITACHI日立); F-4500 荧光分光光度计(FL, HITACHI日立); Labofuge 400R离心机(美国Thermo公司)。
1.2 基于BSA-AuNCs荧光探针的合成方法
由BSA合成的AuNCs作为生物学模板参考以前的方法[14], 将125 mg BSA加入到2.5 mL超纯水中, 于37 ℃水浴中搅拌至溶解, 在剧烈搅拌下迅速向BSA溶液中加入HAuCl4水溶液(10 mmol·L-1, 2.5 mL)混匀5 min后, 加入NaOH溶液(1 mol·L-1, 0.25 mL), 在37 ℃下温和搅拌24 h。 所得BSA-AuNCs溶液的颜色从浅黄色变为浅棕色, 最后变为深棕色。 然后, 将获得的溶液在黑暗中静置24 h, 之后倒入20 000 MWCO透析袋中透析24 h(每8 h更换一次水), 以除去未反应的小分子HAuCl4和NaOH。 将透析后的混合溶液用注射器经过0.22 μm的微孔滤膜过滤除去多余的大粒径的杂质。 最终将获得的溶液在黑暗中于4 ℃下保存。
1.3 BSA-AuNCs荧光探针的表征
荧光探针的形貌通过高分辨场发射透射电镜(TEM)进行测试。 然后分别测试探针的紫外-可见光谱和荧光光谱, 并分别确定所有测试条件在5和10 nm下的激发和发射狭缝宽度。 实验的pH值采用20 mmol·L-1柠檬酸-磷酸盐缓冲溶液控制。 经37 ℃温水浴中适当温育后, 在UV和FL上分别记录紫外吸收光谱和荧光光谱以定性。
1.4 基于FRET生物传感器的建立
依次将100 μL稀释后的BSA-AuNCs溶液、 700 μL 20 mmol·L-1柠檬酸-磷酸盐缓冲溶液(pH 6.0)、 100 μL 5 mmol·L-1TMB溶液和100 μL 2 mmol·L-1H2O2溶液于1.5 mL离心管中混匀, 将混合溶液在37℃温水浴中温育15 min后, 在UV上测量ox-TMB吸收光谱, 在FL上测量荧光光谱。
1.5 H2O2的荧光猝灭检测
1.6 荧光猝灭检测UA
配制20 mmol·L-1UA储备液, 用柠檬酸-磷酸盐缓冲溶液稀释UA储备液至不同浓度, 将700 μL柠檬酸-磷酸盐缓冲液(pH 6.0, 20 mmol·L-1)、 100 μL稀释后的BSA-AuNCs溶液、 100 μL 5 mmol·L-1TMB溶液、 15 μL尿酸酶(10 mg·mL-1)和不同浓度的UA在37 ℃黑暗中温育15 min。 然后用FL以500 nm激发波长记录荧光光谱。
1.7 用该方法对血液样本进行分析
首先将血样(来自3名健康志愿者), 以3 500 r·min-1离心5 min, 去除部分沉淀物, 以消除蛋白质可能对人血清的干扰, 获得浅黄色血清。 随后, 将一定体积的上层血清样品与10 mg·mL-1的尿酸酶在37 ℃下温育10 min, 然后取100 μL上述氧化后的溶液与700 μL柠檬酸-磷酸盐缓冲液(pH 6.0, 20 mmol·L-1), 100 μL稀释后的BSA-AuNCs溶液、 100 μL 5 mmol·L-1TMB溶液混合摇匀, 在37 ℃黑暗中温育15 min。 最后, 在FL上进行血清中UA的分析。
2 结果与讨论
2.1 BSA-AuNCs荧光探针的表征
BSA-AuNCs的TEM图像如图1所示, BSA-AuNCs是单分散的, 呈圆球形且分布均匀, 最小粒径0.86 nm, 最大粒径3.00 nm, 粒径平均直径为1.86 nm。 图2显示了BSA-AuNCs的UV-Vis吸收光谱、 荧光激发和发射光谱以及HAuCl4和BSA的UV-Vis吸收光谱。 曲线1显示BSA-AuNCs在275 nm附近具有强吸收峰, 曲线2和曲线3分别是HAuCl4和BSA的UV-Vis吸收曲线, 由图2可知, 三者UV-Vis吸收光谱明显不同。 当在500 nm激发时, BSA-AuNCs发射峰出现在617 nm。 插图显示在紫外灯365 nm的激发下, 深棕色的BSA-AuNCs溶液发出强烈的红色荧光。 上述结果与文献[14-15]相似, 表明成功地制备了BSA-AuNCs荧光探针。
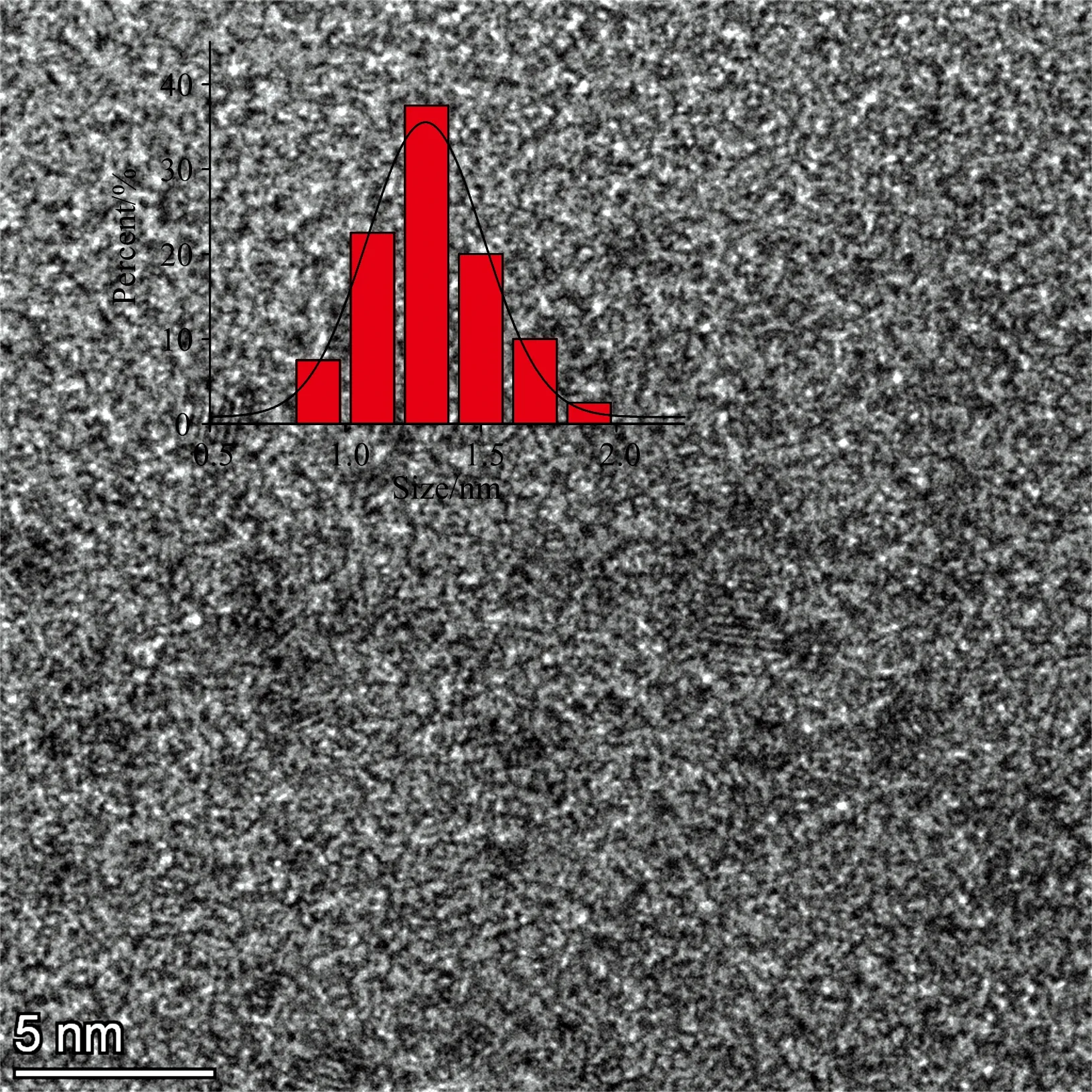
图1 BSA-AuNCs的TEM; 插图为BSA-AuNCs粒径分布图

图2 BSA-AuNCs(1); HAuCl4(2); BSA(3)的紫外吸收光谱; BSA-AuNCs的荧光激发光谱(4)和发射光谱(5); 插图为BSA-AuNCs在日光和365 nm紫外灯下的照片
2.2 FRET生物传感器增强荧光猝灭
BSA-AuNCs的良好稳定性归因于被模板分子完全包裹的金核的化学惰性。 从而使其在FRET中的应用成为可能, 如图3(a)所示, 在BSA-AuNCs和TMB存在下加入H2O2, 此时BSA-AuNCs显示出固有的过氧化物酶活性, 在没有BSA-AuNCs的情况下, H2O2几乎不能氧化TMB。 在654 nm处显示为无色溶液且无明显吸收[图3(a), 1], 在BSA-AuNCs-TMB[图3(a), 2]和BSA-AuNCs-H2O2[图3(a), 3]中发现了相同的结果, 然而, 当将BSA-AuNCs引入H2O2和TMB溶液中时, 它可以催化H2O2将TMB氧化为ox-TMB。 ox-TMB在654 nm处出现最大吸收光谱并且获得明显的蓝色溶液[图3(a), 4]。 如图3(b)由于BSA-AuNCs的发射光谱和ox-TMB的最大吸收光谱重叠, 证明他们之间存在FRET的可能, 插图显示, 可见光下, 在BSA-AuNCs催化下TMB被氧化前后, 颜色从无色变为蓝色。 因此, 该传感系统产生了双光信号的变化。

图3 不同组分溶液的紫外-可见吸收光谱 (1) TMB+H2O2; (2) BSA-AuNCs+TMB; (3) BSA-AuNCs+H2O2; (4) BSA-AuNCs+TMB+H2O2; 插图显示相应组分溶液的照片(a); BSA-AuNCs的发射光谱和ox-TMB的紫外吸收光谱; 插图为BSA-AuNCs催化H2O2氧化TMB前后颜色变化对比照片(b)
引入TMB进行荧光检测, 当BSA-AuNCs中仅存在TMB时, 不会改变其荧光强度和吸收[图4(2)], 加入一定量H2O2时, 测量荧光值略有降低, 并能保持荧光值数小时无明显波动[图4(3)]。 然而将TMB与H2O2和BSA-AuNCs共同作用时, 其荧光强度迅速降低, 且较单独加入H2O2时显示出荧光猝灭明显增强, 这比不含TMB的H2O2样品直接检测要明显得多[图4(4)]。 这是由于BSA-AuNCs和ox-TMB之间的内部过滤作用, BSA-AuNCs和ox-TMB分别作为FRET的供体和受体, 在能量转移过程中, 受体ox-TMB在BSA-AuNCs发射区域表现出较强的吸收, 使得供体BSA-AuNCs的荧光强度被显著猝灭。 因此, 基于FRET的分析方法具有灵敏度高, 可视化等优点, 证明了这是一种超灵敏荧光传感器。

图4 不同BSA-AuNCs样品的荧光光谱
2.3 FRET生物传感器辅助荧光猝灭系统的优化
为了获得更高的H2O2和UA的检测灵敏度, 我们考虑了各种可能的影响因素, 包括溶液酸度、 离子强度、 培养温度和时间, 对实验条件进行了优化。
2.3.1 pH的影响
为做好政府与群众的联系纽带,该中心积极回应百姓需求,自2011年7月27日成立以来,共受理各类食品药品安全问题咨询和投诉举报达36余万件,受理量年均增长30%,举报查实率近70%,平均办结时间19天,群众诉求100%得到回复。2014年,中心开通语音留言功能,落实专人回听,并在非高峰时段进行受理,全年“额外”受理市民投诉举报6936件,占全年电话受理总量的10.6%。2015年初,中心接到大量求购“苯巴比妥片”的电话后及时上报,同年4月,该药品恢复生产供应。中心逐一告知来电人恢复供药的信息及就近购药地点,得到市民广泛好评。
考察了不同pH的柠檬酸-磷酸盐缓冲溶液对BSA-AuNCs在检测中荧光强度的影响, 如图5(a), 结果表明: 当BSA-AuNCs溶液在pH(6.0~8.0)范围内对H2O2的相对强度(F0/F)略有变化, 其中F0和F分别是在不存在和存在H2O2和TMB的情况下BSA-AuNCs的荧光强度, 考虑到进一步的生物学应用和最佳的检测效果, 我们选择了pH6.0作为最佳酸度。
2.3.2 离子强度的影响
离子强度是光谱检测方法中的一个重要影响因素, 在这项工作中, 我们使用NaCl来控制离子强度, 以研究荧光猝灭的效果, 如图5(b), 随NaCl浓度(0, 2.0, 5.0, 10.0, 20.0, 50.0, 80.0, 100.0, 120.0, 150.0, 153.8 mmol·L-1)的增加, BSA-AuNCs对H2O2的荧光响应没有明显变化, 表明我们的方法可以在正常生理盐浓度中进行。
2.3.3 温度的影响
如图5(c)所示, 实验测试了温度对FRET辅助荧光猝灭系统的影响, 当温度从25 ℃上升到60 ℃时, 在25~37 ℃时,F0/F逐渐升高, 当温度到达37 ℃时, 达到最佳状态, 温度由37 ℃变化到60 ℃时,F0/F略有降低, 因此, 这里我们采用37 ℃的生理温度作为最佳检测条件。
2.3.4 反应时间的影响
在动力学研究中, 为了检测BSA-AuNCs对H2O2相对荧光强度随时间的变化, 对反应时间进行了动态检测, 如图5(d)所示, 显示在BSA-AuNCs溶液中加入TMB和H2O2后, 反应时间5~80 min呈动态猝灭, 发现荧光强度在开始的15 min内几乎呈线性且显著下降, 然后保持恒定。 因此, 采用15 min作为最佳反应时间, 与不加入TMB应用BSA-AuNCs荧光探针直接检测H2O2需70 min时相比, 大大缩短了反应时间。
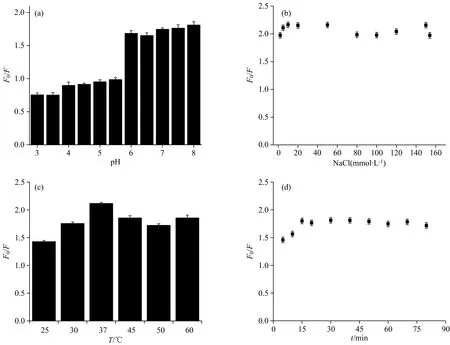
图5 pH(a), 离子强度(b), 温度(c), 反应时间(d)对荧光的影响, 含50 μmol·L-1 H2O2, 5 mmol·L-1 TMB的BSA-AuNCs
在最佳条件下, 不同H2O2浓度下BSA-AuNCs的荧光强度, 如图6(a)所示, 随H2O2浓度(0, 0.02, 0.5, 2.5, 7, 9, 12, 15, 20, 25, 50, 80 μmol·L-1)的变化, BSA-AuNCs的荧光强度逐渐被猝灭, 如图6(b)所示, H2O2对BSA-AuNCs在0.5~20 μmol·L-1范围内的猝灭程度(F0-F)/F0线性相关, 线性回归方程为(F0-F)/F0=0.025 83cH2O2+0.095 12, 线性相关系数为0.994 5。 H2O2的检出限为0.07 μmol·L-1, 表明H2O2具有较低的检测限。 比不用FRET生物传感器辅助荧光猝灭系统检测H2O2样品(检出限6.6 μmol·L-1)低近两个数量级[16]。 因此, 基于FRET的传感器具有灵敏度高, 检测限低, 可视化的优点, 大大提高了其检测性能, 为进一步灵敏地检测UA提供了基础。
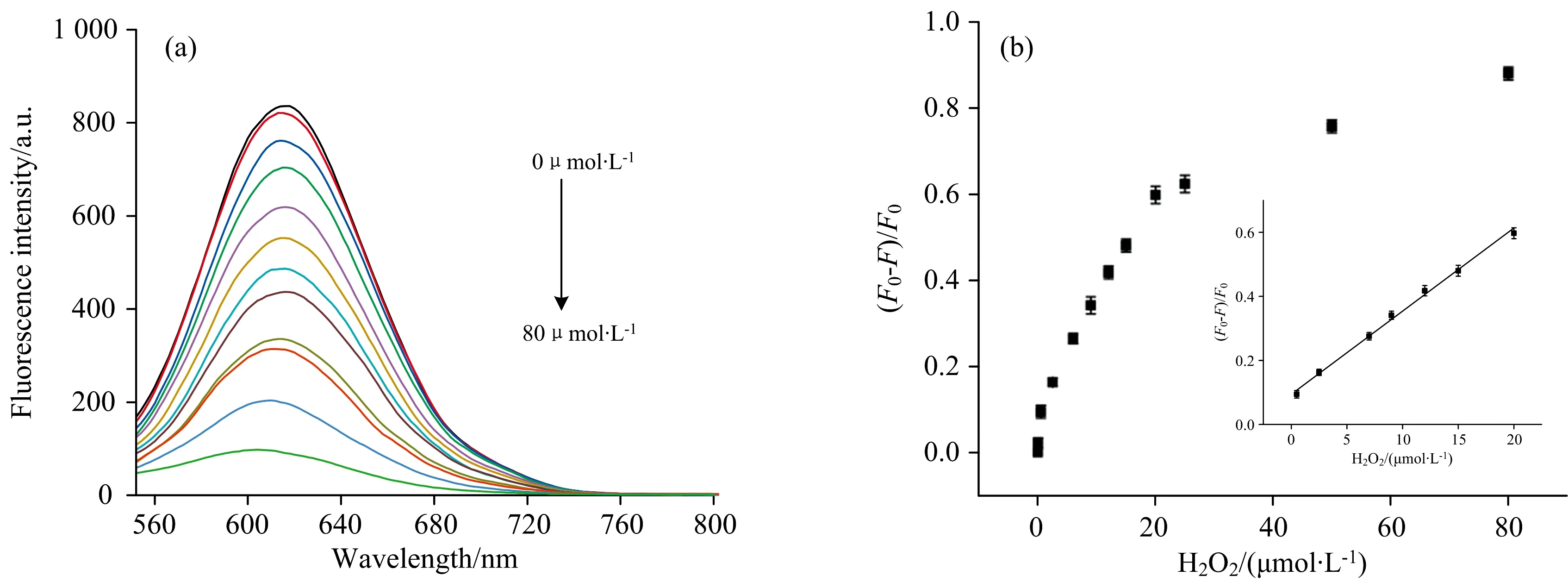
图6 BSA-AuNCs对不同量的H2O2和TMB共存的荧光光谱图(a); 线性关系Stern-Volmer图(b)
2.4 UA的检测
基于以上的检测结果, 我们已经建立了一种对H2O2的灵敏、 可视化的检测方法。 由于H2O2是一系列特定底物氧化酶的酶促反应产物, 因此H2O2的灵敏检测可以扩展到生物催化过程的应用中。 尿酸氧化酶在UA的存在下催化和氧化UA生成H2O2, 尿囊素(Allantoin)和二氧化碳(CO2)。 基于FRET法灵敏检测UA如示意图1所示。

示意图1 BSA-AuNCs荧光探针基于FRET检测H2O2和UA的示意图
结果显示, 当添加TMB后, 在检测UA的酶促反应产物时, 显示出荧光猝灭较UA单独存在时增强, 如图7(a)所示, 随UA浓度(0, 0.7, 2.0, 15, 40, 65, 70, 80, 100, 150, 200 μmol·L-1)的增加, BSA-AuNCs的荧光强度持续降低, 并且研究了仅向BSA-AuNCs中添加UA或尿酸氧化酶不会引起其荧光强度的变化。 而当UA和尿酸氧化酶同时存在时, BSA-AuNCs的荧光发生猝灭, 这表明BSA-AuNCs的荧光强度降低是由于尿酸氧化酶催化尿酸产生H2O2引起的。 在尿酸氧化酶存在下, 不同浓度的UA与BSA-AuNCs反应的相对强度(F0-F)/F0, 如图7(b)所示, 其中F0和F分别是不存在UA和存在UA的荧光强度, 结果发现, 在2.0~100 μmol·L-1范围内, 猝灭程度呈良好线性关系, 表示为(F0-F)/F0=0.005 85cUA+0.103 64, 线性相关系数为0.995 4, 检出限为0.26 μmol·L-1。 远低于人体正常尿酸含量的最低值(90 μmol·L-1)。 因此, 设计的FRET, 灵敏传感器在检测UA方面优于以前的报道[16-17], 显示了高灵敏度和低检测限的优势。 为其进一步应用于临床血样的检测提供了基础。

图7 BSA-AuNCs对不同量的UA和TMB共存的荧光光谱图(a); 线性关系Stern-Volmer图(b)
2.5 BSA-AuNCs的选择性评估
为了证明我们设计的灵敏传感器的选择性, 还研究了一些其他潜在干扰物对BSA-AuNCs的响应, 实验是在最佳检测条件和10 mg·mL-1尿酸氧化酶存在下进行的, UA的浓度为50 μmol·L-1, 干扰物质BSA, 谷胱苷肽(GSH), 抗坏血酸(Vc), 柠檬酸(CA), 尿素(Urea), 葡萄糖(Glu), 甘氨酸(Gly), 酪氨酸(Tyr), 氯化钠(NaCl)和氯化钾(KCl)的浓度为5 mmol·L-1, 结果如图8, 上述干扰物质中仅Vc提供了较小的荧光增强, 除此之外其他物质存在下BSA-AuNCs的荧光强度几乎保持恒定, 仅当存在UA时, 荧光才显著猝灭。 这归因于尿酸氧化酶的高催化活性和对UA的高特异性, 结果表明, 所提出的灵敏UA检测方法具有高选择性。

图8 UA的潜在干扰物对BSA-AuNCs荧光探针的影响
2.6 临床血液样本的分析
由于该方法具有的高灵敏度、 高度选择性和高特异性, 因此将本方法应用于实际临床血样中UA的测定, 结果如表1, 采用标准加样回收的方法检测血样中的UA, 加标回收率为97.3%~104.7%, 相对标准偏差RSD为2.4%~3.2%, 表明此方法可以应用于临床血液样本中UA的灵敏检测。

表1 血液样本UA回收率结果
3 结 论
以BSA作为模板分子, 以简单、 绿色的方法合成了BSA-AuNCs荧光探针, 基于超灵敏的FRET多功能生物传感系统检测H2O2和UA, BSA-AuNCs在这里显示出特征性的过氧化物酶活性, 在检测中催化H2O2氧化TMB, 从而生成ox-TMB。 强荧光的BSA-AuNCs和ox-TMB之间有效的FRET使得对H2O2和UA的检测限极低, 分别为0.07和0.26 μmol·L-1, BSA-AuNCs催化的过氧化物酶底物TMB生成ox-TMB的颜色变化可以更直观的观察到实际样品中的UA。 与之前的方法相比, 本方法操作简单, 快速, 具有较高的灵敏度和选择性且可视化, 此方法用于测定临床实际血样中UA的浓度, 获得了较为满意的结果, 有望应用于临床实际样品中UA的快速、 灵敏和高特异的检测。 本研究设计的FRET传感器在这里显示出灵敏度高, 检测限低等优点, 大大提高了UA酶促反应产物H2O2的检测性能, 使得该方法有助于实现其他特定酶促反应产物的快速筛查分析。
