石墨@TiO2纳米复合材料的溶剂热合成及其性能
2022-01-01谈尚华闫共芹武桐
谈尚华 闫共芹 武桐





摘 要:为获得一种具有理论容量高、循环性能佳、光催化性能优异的新型多功能材料,在石墨存在下,以钛酸四丁酯为钛源,利用简单的一步溶剂热法制备不同石墨含量的石墨@TiO2复合材料并对其进行表征。将石墨@TiO2复合材料作为锂离子电池负极材料测试了其电化学性能,并将其用作降解甲基橙溶液的光催化剂测试了其光催化性能。结果表明:锐钛矿型TiO2纳米线呈三维相互交织状包覆在石墨片表面,使复合材料具有较高的比表面积;复合材料中TiO2含量越高,其初始放电比容量越大,在100 mA/g电流密度下的初始放电比容量最高可达到464.9 mA·h/g,在2 A/g电流密度下的初始放电比容量最高可达到120.3 mA·h/g;而复合材料中TiO2含量越低,其可逆循环性能越好,在100 mA/g电流密度下循环100次后放电比容量为310.8 mA·h/g;石墨@TiO2复合材料光催化性能随着TiO2含量的增加而增强,在紫外光照射60 min后,甲基橙溶液的降解率最高可达98.72%。研究表明,石墨@TiO2复合材料具有优异的电化学性能和光催化性能,有望替代传统的负极材料和光催化剂材料,具有广阔的应用前景。
关键词:石墨@ TiO2纳米复合材料;溶剂热法;电化学性能;光催化性能
中图分类号:TB334 DOI:10.16375/j.cnki.cn45-1395/t.2022.01.016
0 引言
TiO2作为一种传统的半导体材料,具有来源广泛、价格低廉、低毒无污染以及优异的光催化性能[1-3]等优点,被广泛用作光催化材料。已有研究表明,将TiO2与碳类材料进行复合后能进一步有效提升复合材料的光催化性能。如Yao等[4]采用无机/有机骨架复合双模板法,制备出了N掺杂的TiO2/C纳米复合材料,结果表明复合材料具有较大的比表面积,用作光催化材料时对亚甲基蓝(MB)溶液的降解率为基准P25材料(商业基准二氧化钛光催化剂材料)降解率的48倍。Yu等[5]将制备出的石墨@N-TiO2纳米复合材料与纯TiO2材料进行对比,结果表明复合材料在可见光照射20 min后,对MB溶液的降解率高达98%,远高于单一TiO2材料对MB溶液的降解率,且复合材料在经过4次光催化降解实验后,其光催化性能仅降低了17%,这表明该复合材料具有优良的光催化性能和较好的催化稳定性。然而,该复合材料的制备过程较为复杂且成本较高,因此,急需一种低成本和操作简单的方法以制备出具有优良光催化性能的石墨@TiO2复合材料。
TiO2纳米材料具有良好的循环稳定性[6-8],可用作锂离子电池负极材料。但TiO2材料的理论比容量较低(168 mA·h/g),导电性较差,随着锂离子电池对负极材料的要求逐渐提升,单一TiO2纳米材料无法满足锂离子电池对负极材料性能的要求。因此,人们尝试将TiO2纳米材料与碳类材料进行复合以制备出具有较高循环容量、循环稳定性能优异、导电性能较佳的复合材料。如Zhang等[9]利用导电空心多孔花粉碳微球作为骨架,通过简单的一步溶剂热法制备出了具有中空多孔结构的石墨@TiO2复合材料,并将其在N2气氛中以700 ℃煅烧。研究发现,煅烧后的复合材料具有优异的电化学性能,在1C的电流密度下循环100次后仍具有203.1 mA·h/g的可逆比容量;在5C的高电流密度下循环1 000次后,仍具有148 mA·h/g的可逆比容量,表明复合材料具有优异的循环稳定性。Fu等[10]通过水热法制备了还原氧化石墨烯负载TiO2纳米棒的复合材料,结果表明复合材料具有较大的比表面积(149.5 m2/g),在1C的电流密度下循环100次后其可逆比容量为 267 mA·h/g;在10C電流密度下循环500次后可逆比容量为151 mA·h/g,证明了复合材料具有优异的循环稳定性和一定的可逆比容量。通过TiO2与碳类材料的复合获得了具有优异的循环稳定性和较高可逆比容量的负极材料,但相对目前人们对高比容量锂离子电池的需求来说,仍需要进一步开展研究以提高其可逆比容量。
本文通过简单的一步溶剂热法制备了不同石墨含量的石墨@TiO2复合材料,并测试了复合材料中不同石墨含量对复合材料电化学性能和光催化性能的影响。结果表明:TiO2含量较高的复合材料具有最高的初始充放电比容量和最佳的光催化性能,TiO2含量最低的复合材料在100 mA/g电流密度下循环100次后具有最高的可逆比容量,表明复合材料具有较高的充放电比容量和较好的循环稳定性,以及优异的光催化性能,有望成为一种高性能锂离子电池负极材料和光催化剂材料。
1 实验部分
1.1 实验材料
石墨粉,上海华谊集团华原化工有限公司胶体化工厂;钛酸丁酯,甲基橙,AR,天津市科密欧化学试剂有限公司;丙三醇,AR,广东光华科技股份有限公司;无水乙醇,AR,成都市科隆化学品有限公司。
1.2 实验设备
X射线衍射仪(DX-2700,丹东浩元仪器有限公司);显微共焦拉曼光谱仪(XploRA,HORIBA Jobin Yvon);场发射扫描电子显微镜(SEM,蔡司SIGMA);X射线能谱仪(EDS,布鲁克QUANTAX)。
1.3 石墨@TiO2复合材料的制备
将一定质量的石墨加入15 mL无水乙醇中,超声分散1 h后加入1 mL钛酸四丁酯(TBOT)并搅拌5 min,然后再加入5 mL丙三醇并继续搅拌30 min。将混合溶液移入体积为50 mL的聚四氟乙烯内衬不锈钢高压反应釜中,加热至200 ℃并保温14 h。自然冷却至室温后,用离心机分离得到固体产物,并用无水乙醇和去离子水混合溶液(体积比为1∶2)多次清洗,直至离心后的沉淀表面没有白色层。将剩余的黑色沉淀置于60 ℃烘箱内干燥12 h,将干燥后的产物置于气氛炉内,在空气中450 ℃煅烧2 h,升(降)温速度为10 ℃/min,即可制得石墨@TiO2复合材料。实验过程中加入石墨的质量分别为0.5 g、1.0 g、2.0 g,样品分别编号为TG-1、TG-2、TG-3。
1.4 光催化性能测试
通过测量石墨@TiO2复合材料对甲基橙的降解率来表征其光催化性能[11]。具体操作过程如下:首先,将0.03 g石墨@TiO2纳米复合材料加入100 mL配置好的甲基橙水溶液中,其中甲基橙水溶液的浓度为15 mg/L,超声20 min使之混合均匀;然后,将混合均匀的溶液置于暗箱中磁力搅拌30 min,使染料和催化剂达到吸附平衡;最后,采用165 W的汞灯进行光催化分解实验,每隔20 min取7 mL悬浮液,将悬浮液离心分离后取上清液,用双光束紫外/可见分光光度计(UV-1900PC,上海美析仪器有限公司)测溶液最大吸收波长处的吸光度值,并按式(1)计算甲基橙的降解率[12]:
[D%=(A0-At)/A0×100] , (1)
式中:[D]表示甲基橙的降解率,[A0]表示甲基橙溶液吸附平衡的初始吸光度,[At]表示t时刻甲基橙溶液的吸光度。
1.5 电化学性能测试
将石墨@TiO2纳米复合材料、导电碳黑、聚偏二氟乙烯(PVDF)按8∶1∶1的质量比溶于 N-甲基-2-吡咯烷酮(NMP)中,其中PVDF与NMP的配比为m(PVDF)∶V(NMP)=0.025∶1,搅拌4 h使其混合均匀。将上述混合浆液均匀涂敷于铜箔表面,在65 ℃下干燥12 h后,采用精密圆盘切割机(深圳科晶MSK-T10)将其裁剪为圆形极片,将极片称重并在80 ℃真空干燥箱内干燥12 h后得到锂电池极片。以金属锂片作为对电极,Celgard-2400聚丙烯微孔膜为隔膜,浓度为1 mol/L的LiPF6/EC(碳酸乙烯酯)+DMC(碳酸二甲酯)(V(EC)∶ V(DMC)=1∶1)溶液为电解液,在充满N2的手套箱内组装成CR2016型纽扣电池[13]。静止24 h后采用电化学工作站(AUTOLAB-M204,瑞士万通中国有限公司)进行电化学阻抗测试和循环伏安测试。电化学阻抗测试参数设定为10 mV的电压幅值,0.01~105 Hz的频率范围;循环伏安测试参数设定为0.1 mV/s的扫描速率,0.01~3 V的电压范围。同时在LAND电池测试系统(CT3001A,武汉蓝电)进行充放电循环实验,电压范围为0.01~3 V,电流测试密度在100~2 000 mA/g。
2 结果与讨论
2.1 形貌和成分分析
图1为石墨@TiO2复合材料的扫描电子显微镜(SEM)图像和X射线能谱图谱(EDS)。其中, 图1(a)—图1(c)为石墨加入量为1.0 g所得复合材料(TG-2)不同放大倍数的SEM图像。从扫描电镜图像可知,复合材料仍保留了石墨的片状形貌(如图1(c)红色线包围的区域),在石墨片的表面均匀包覆了一层网状结构的TiO2(如图1(b)所示),网状TiO2层由细小的TiO2纳米颗粒组装且长度约为 150 nm的纳米线相互交织而成,如圖1(a)所示。图1(d)和图1(e)、图1(f)和图1(g)分别为石墨加入量为0.5 g和2.0 g制得的复合材料(TG-1和 TG-3)在不同放大倍数下的SEM图。从图可以看出,不同石墨加入量的复合材料形貌基本相似,均为由TiO2纳米线组成的网状结构包覆石墨片的复合材料。对不同石墨添加量的复合材料进行能谱(EDS)分析,结果如图1(h)所示,3个样品的能谱谱图中均存在Ti、C、O的元素峰,证明了复合材料中石墨和TiO2的存在。 <G:\202201\图片\谈尚华\图1(a).jpg>
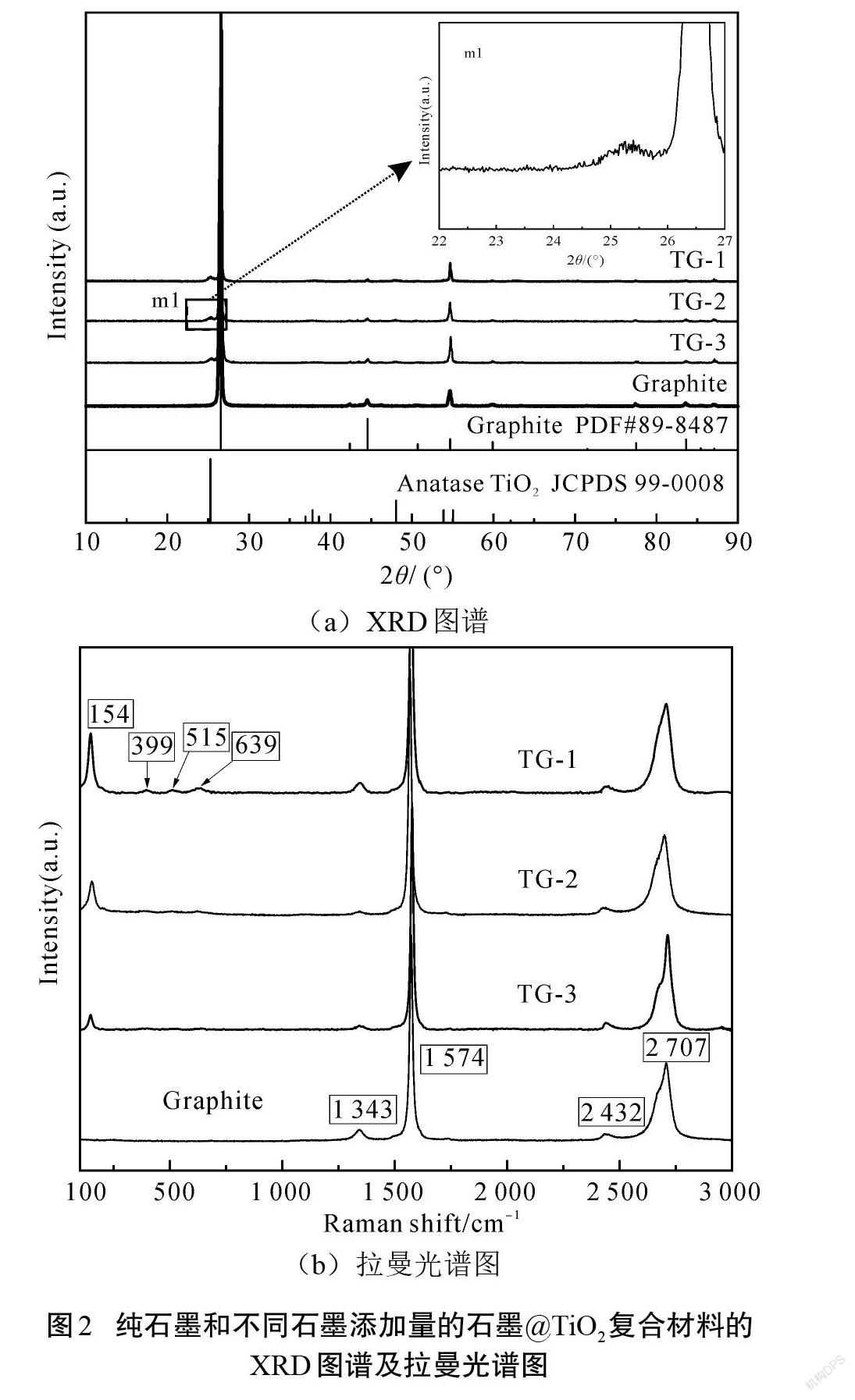
为了进一步验证复合材料的组成,对纯石墨和图1所示的不同石墨添加量的石墨@TiO2复合材料进行X射线衍射和拉曼光谱散射测试,如图2所示。图2(a)为X射线衍射图谱,由图谱可知,单一石墨和石墨@TiO2复合材料在26.5°、44.6°、54.7°、83.6°处存在明显的衍射峰,根据标准图谱可知,这些衍射峰对应于石墨(002)、(101)、(004)、(112)晶面的标准衍射峰(Graphite, PDF#89-8487)。由于复合材料中添加的商业石墨具有非常好的结晶度,其衍射峰强度高,从而使得复合材料在450 ℃煅烧2 h后的TiO2衍射峰不明显。但对衍射图谱部分区域进行放大可以发现复合材料在2θ为25.3°处有一个微弱的衍射峰(如图2(a)中的m1放大图所示),根据标准衍射图谱可知,该衍射峰对应为锐钛矿型二氧化钛的(101)晶面(Anatase,JCPDS 99-0008),表明复合材料中含有锐钛矿相TiO2。
图2(b)为石墨和石墨@TiO2复合材料的拉曼光谱图,测试采用的光栅为1 800/mm,测试波长为532 nm,测试范围在100~3 000 cm-1。从光谱图可以看出,不同石墨添加量的石墨@TiO2复合材料在1 343 cm-1、1 574 cm-1、2 432 cm-1、2 707 cm-1处出现的拉曼位移和纯石墨的拉曼位移一致。3种复合材料在154 cm-1处均出现了典型的锐钛矿型二氧化钛的拉曼峰,证明复合材料中存在锐钛矿型TiO2。由于TG-1复合材料中石墨添加量最少,TiO2含量占比最大,使得该材料在拉曼位移为 399 cm-1、515 cm-1、639 cm-1处显示出了锐钛矿型二氧化钛的其他典型拉曼峰。因此,结合复合材料的EDS图谱、X射线衍射和拉曼光谱散射图谱,证明了通过简单的一步溶剂热法成功合成了石墨@TiO2复合材料。
2.2 比表面积和孔径分析
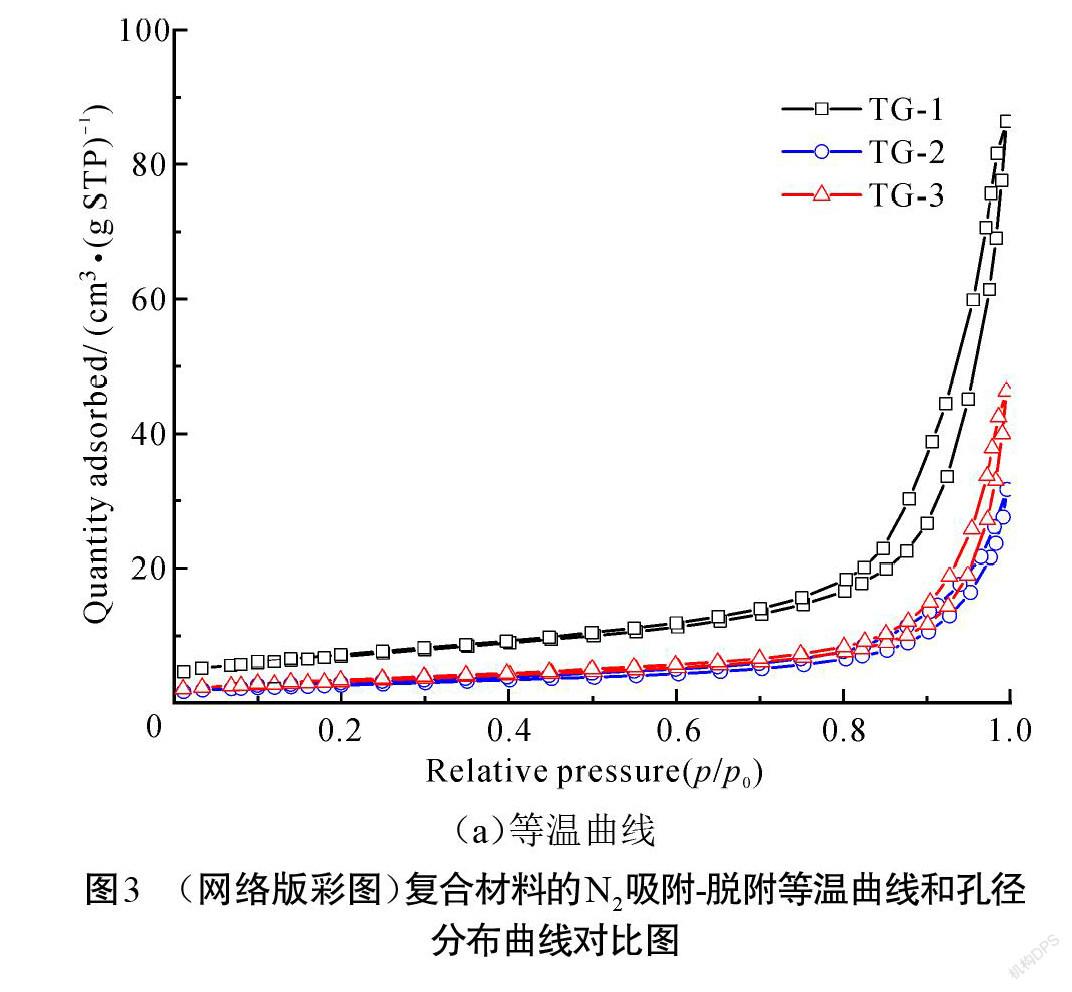
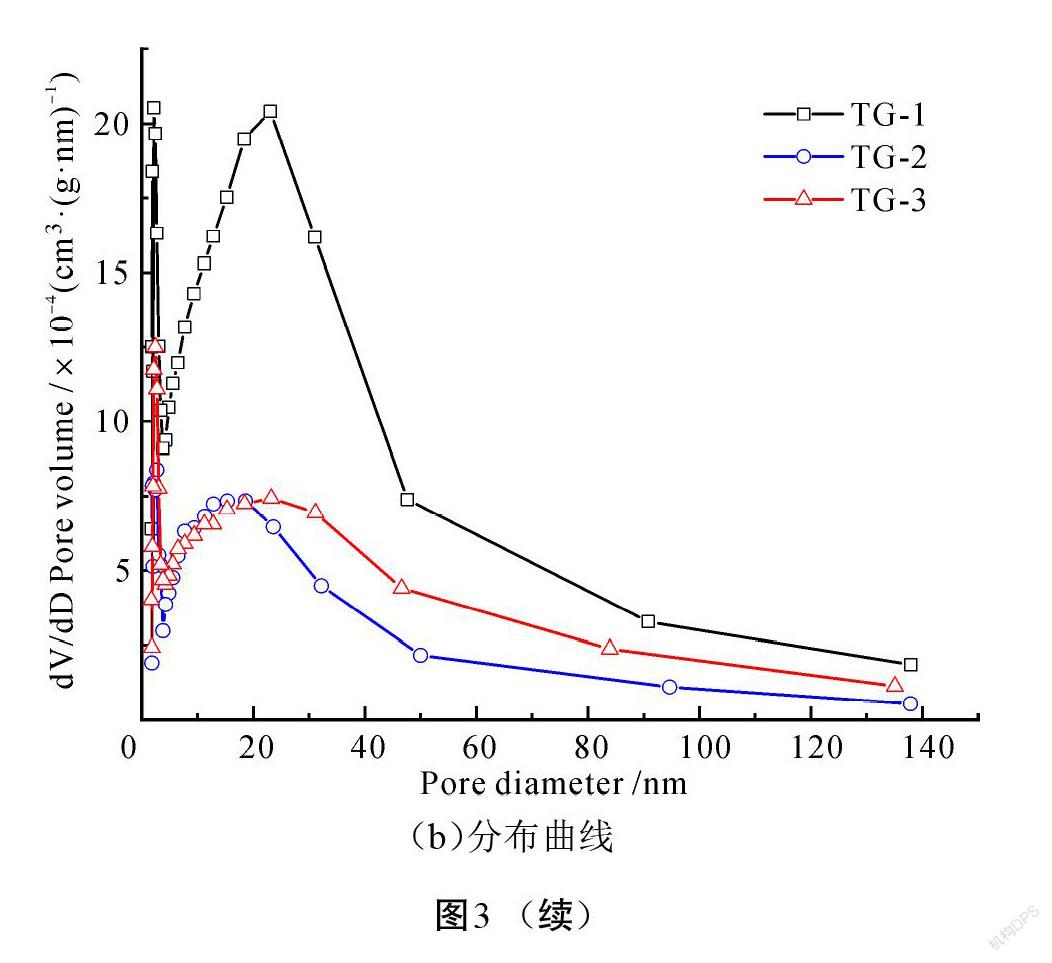
为研究复合材料的比表面积和孔径分布,对添加不同石墨量的石墨@TiO2复合材料进行N2吸附-脱附测试。图3为TG-1、TG-2、TG-3复合材料的N2吸附-脱附等温线和BJH孔径分布曲线对比图。通过图3(a)可以发现三者的吸附-脱附等温曲线均表现为IV型等温线,表明3种复合材料的孔隙均由中孔和大孔组成。根据Brunauer-Emmett-Teller(BET)模型[14],可以计算出TG-1、TG-2、TG-3的BET比表面积分别为24.754 9 m2/g、9.186 8 m2/g、11.138 5 m2/g。图3(b)是复合材料的BJH孔径分布曲线,通过BJH方法计算得出TG-1、TG-2、TG-3的平均孔径尺寸分别为20.801 7 nm、19.360 3 nm、22.732 6 nm,平均孔径大小基本相同。由于复合材料具有的纳米孔隙结构和较大比表面积的特性,使得复合材料在作为锂离子电池负极材料时,在充放电循环过程中能提供较多的锂离子接触活性位点,可以有效地提升材料的电化学性能;而在作为光催化剂时,能提供较多的吸光面积,从而有效改善材料的光催化性能。
2.3 电化学性能分析
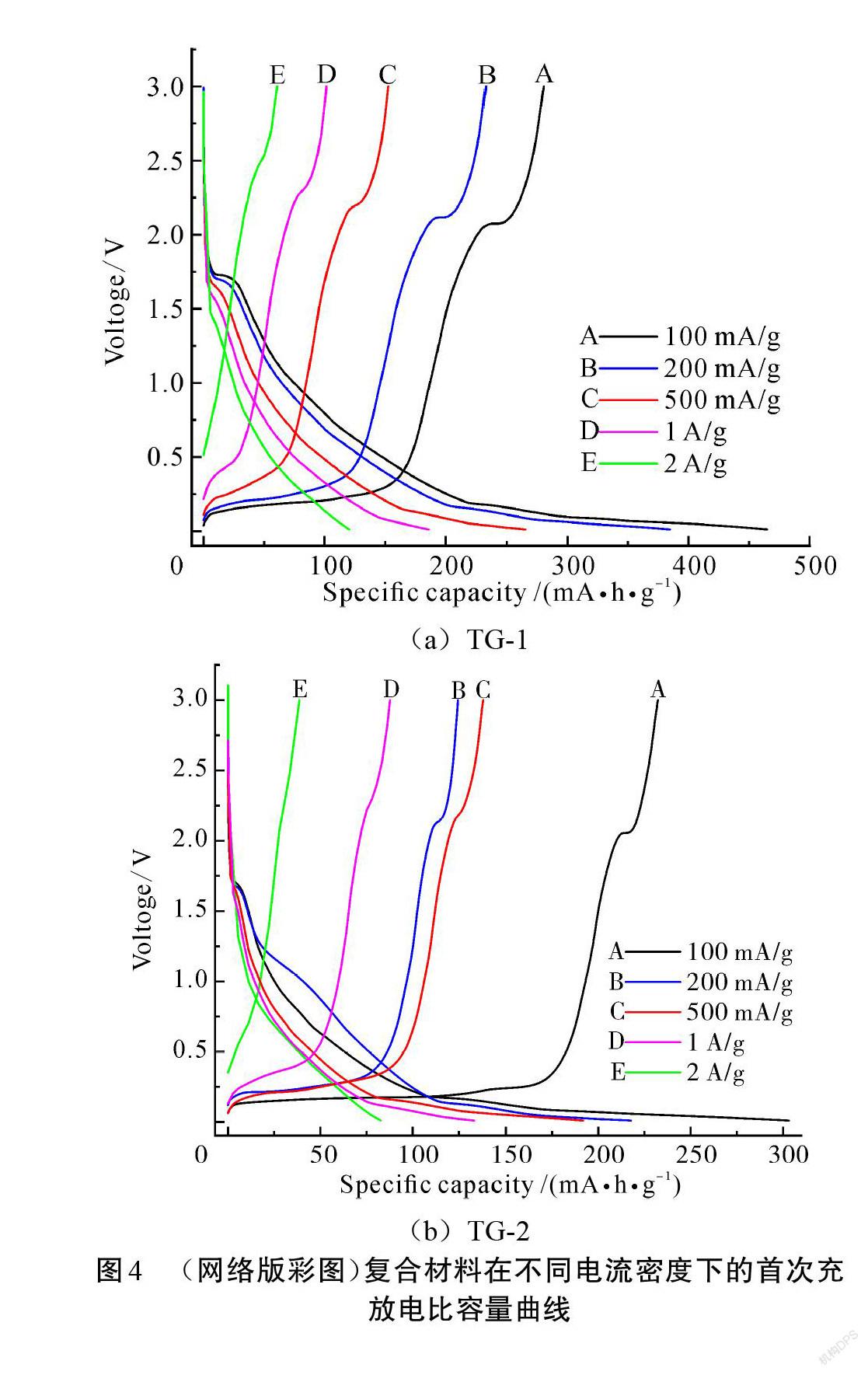
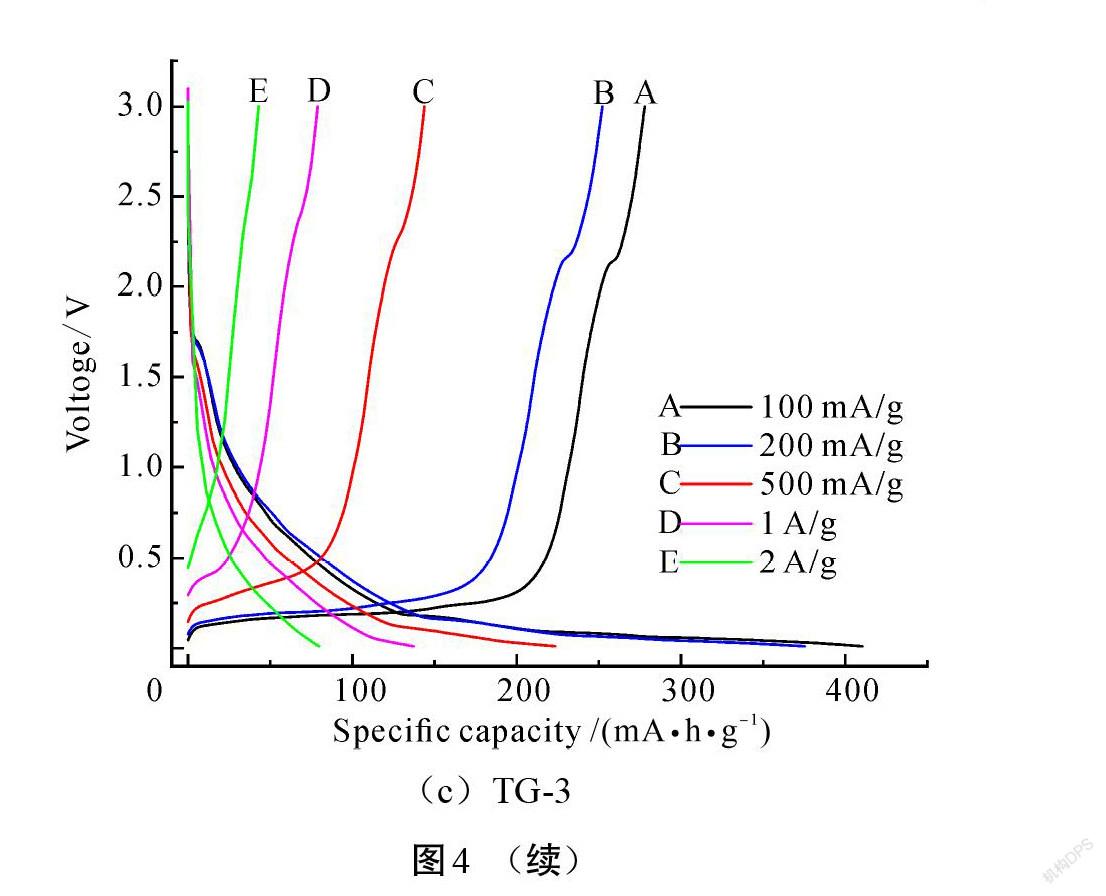
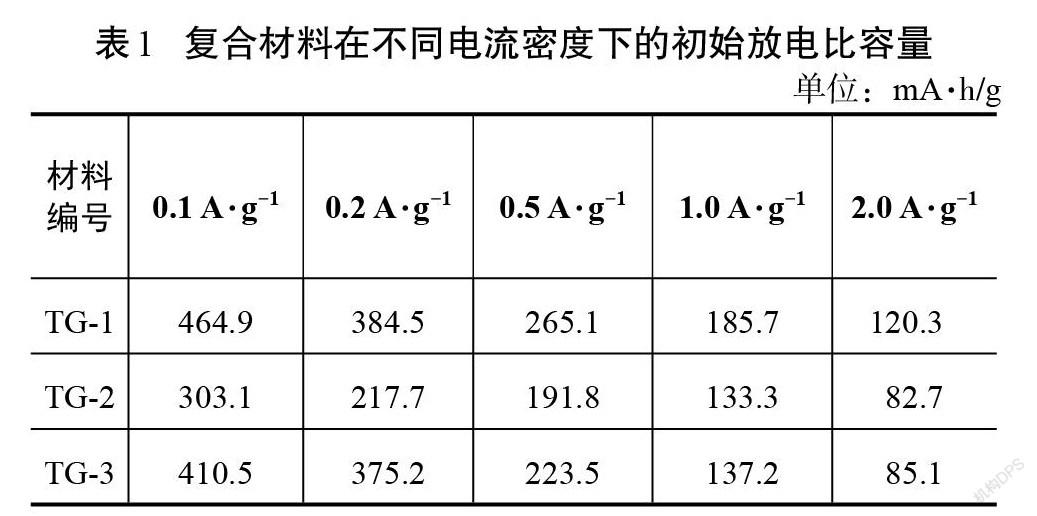
图4和表1分别为不同石墨添加量的石墨@TiO2复合材料在不同电流密度下的首次充放电曲线和初始充放电比容量数据表。由图4和表1可知,在电流密度为100 mA/g的条件下,TG-1、TG-2、TG-3复合材料首次放电比容量分别为464.9 mA·h/g、303.1 mA·h/g、410.5 mA·h/g。3种复合材料的初始放电比容量与单一TiO2或石墨相比,其大小关系为:TG-1>TG-3>石墨(350 mA·h/g)>TiO2(330 mA·h/g)>TG-2。可以发现,TG-2复合材料的初始放电比容量为3种复合材料中最小的,同时也小于单一TiO2或石墨的初始放电比容量,表明二元复合材料中以 TG-2的配比关系制备出的复合材料电化学性能最差。结合复合材料的比表面积大小数据可以发现,TG-2复合材料具有最小的比表面积,使得材料在充放电循环过程中具有最小的锂离子接触活性位点,从而导致该配比的复合材料具有最小的充放电比容量。而TG-1复合材料中,由于TiO2含量比例最高且具有最大的比表面积,因而使得TG-1
復合材料具有最大的初始放电比容量,说明复合材料的初始放电比容量与其比表面积有关。在材料的充放电曲线中,单一TiO2的放电平台电压值和充电平台电压值大概为1.7 V和2.1 V[15],单一石墨原材料的放电平台电压和充电平台电压值分别大概为0.16 V和 0.06 V、0.19 V和0.25 V(如图5(d)所示)。从图4可以看出,TG-1、TG-2、TG-3等3种复合材料在100 mA/g电流密度下的首次充放电曲线中均存在TiO2和石墨的充放电平台,由于3种复合材料中TiO2比例的不同,导致3种复合材料的TiO2充放电平台存在一定的差异,充放电平台大小关系为 TG-1>TG-2>TG-3。此外,由图4可以看出,随着电流密度的增大,TG-1、TG-2、TG-3的首次充放电比容量也随之减小,这可归因于TiO2在电流密度增加时其比容量的衰减[16],但3种复合材料在相同电流密度下的初始充放电比容量依旧保持着 TG-1>TG-3>TG-2的关系。进一步研究发现,复合材料具有较高初始放电比容量可归因于材料具有大比表面积和TiO2颗粒具有的纳米级尺寸,从而可以有效地促进锂离子的嵌入和脱出,在电极上还能缩短锂离子的扩散路径并提高电子的传导率。TiO2材料和石墨材料的嵌锂和脱锂反应可以表示为式(2)[17]和式(3)[18],其中[x]约为0.5。
[TiO2+xLi++xe-1⇔LixTiO2], (2)
[6C+yLi++ye-1⇔LiyC6]. (3)
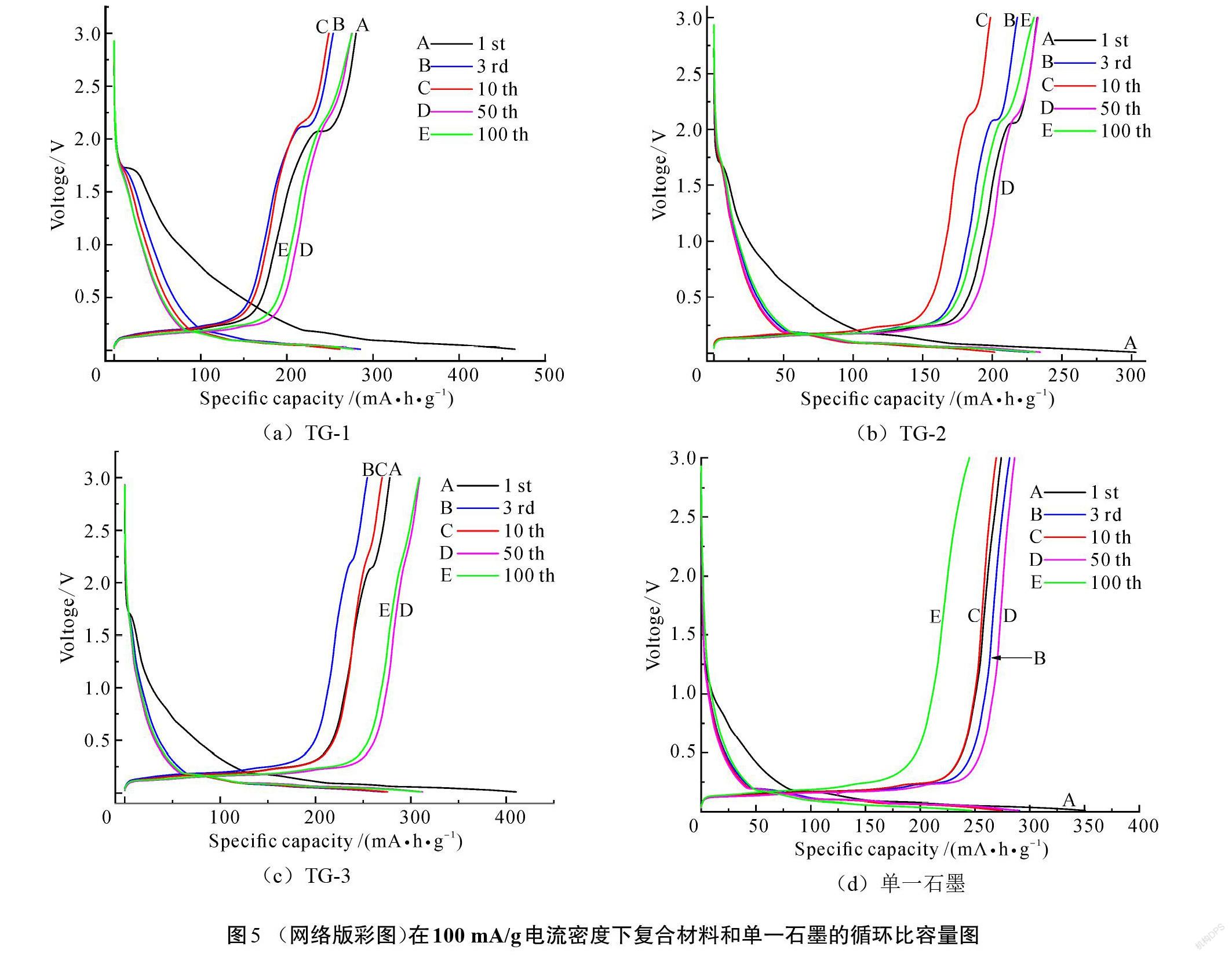
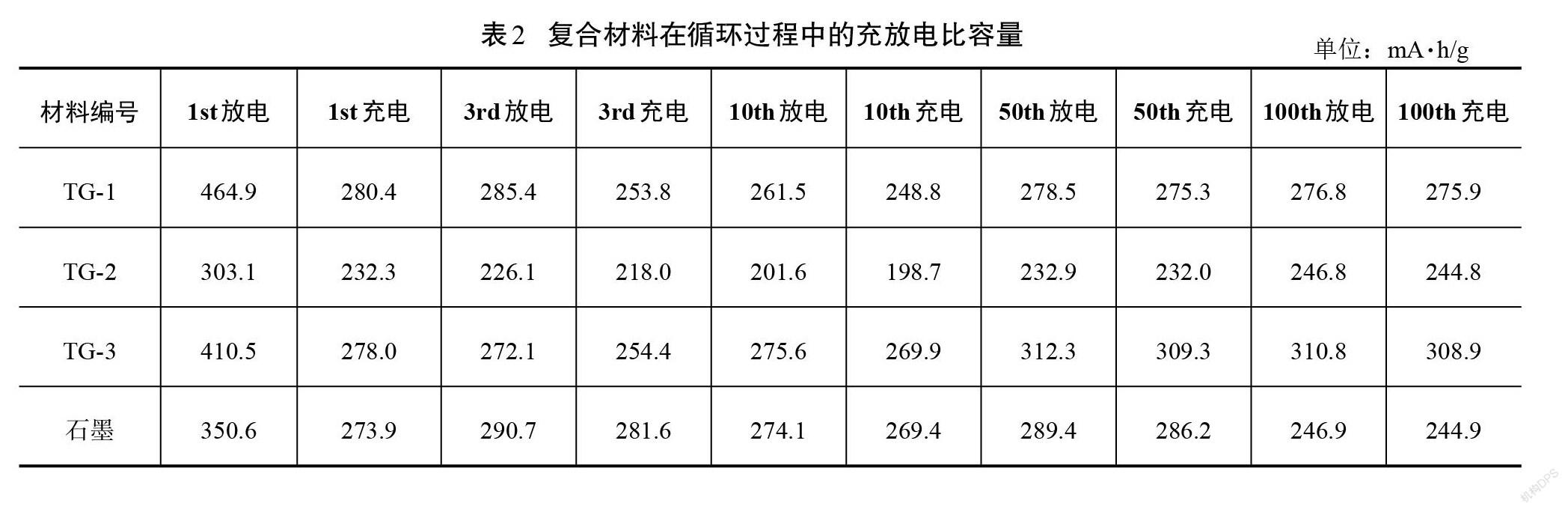
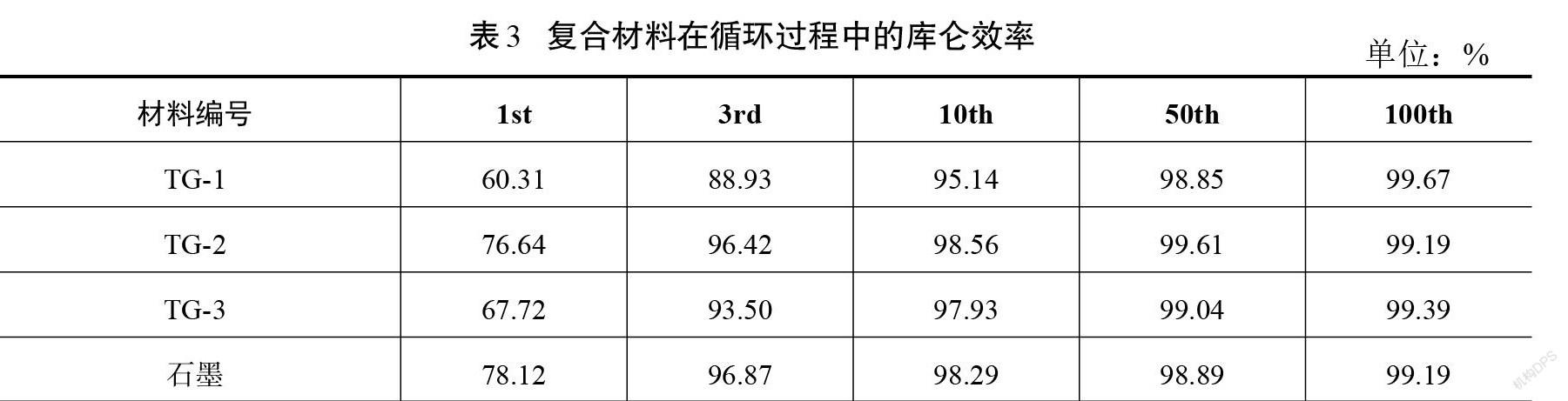
为了进一步研究复合材料作为锂离子电池负极材料时的电化学性能,对3种复合材料进行了充放电循环测试。图5为TG-1、TG-2、TG-3复合材料和单一石墨在100 mA/g电流密度下的循环比容量图,表2为TG-1、TG-2、TG-3复合材料和单一石墨材料在循环过程中的充放电比容量,表3为TG-1、 TG-2、TG-3复合材料和单一石墨材料在循环过程中的库仑效率。从图5和表2、表3可以看出,TG-1复合材料的初始放电比容量和充电比容量分别为464.9 mA·h/g和280.4 mA·h/g,对应的库仑效率为60.31%;TG-2复合材料的初始放电比容量和充电比容量分别为303.1 mA·h/g和232.3 mA·h/g,对应的库仑效率为76.64%;TG-3复合材料的初始放电比容量和充电比容量分别为410.5 mA·h/g和278.0 mA·h/g,对应的库仑效率为67.72%。3种复合材料在首次充放电循环中均具有较大的不可逆比容量损失,这可归因于首次充放电过程中电解质的不可逆分解以及电极中固态电解质界面膜(SEI)的形成[19]。随着循环次数的增加,库伦效率逐渐增加,在充放电循环10次以后,比容量的衰减基本为0,库仑效率接近100%,这是因为在材料表面已经形成了相对稳定的SEI膜,使得材料在循环10次之后表现出较好的循环稳定性。随着循环次数的进一步增加,电解质在电极材料中的渗透率逐渐增加,提高了电子和锂离子的传递速率[20],从而使3种复合材料在第50次循环时的放电比容量均大于第10次循环时的放电比容量,如表2所示。经过100次充放电循环后,3种复合材料TG-1、TG-2、TG-3放电比容量衰减值分别为188.1 mA·h/g、56.3 mA·h/g、99.7 mA·h/g。结合3种复合材料的比表面积数据可知,比表面积越大,材料的初始充放电比容量越高,但是循环100次后的比容量衰减值最大。这可归因于材料的比表面积越大,材料与锂离子接触活性位点越多,从而有效促进了复合材料在充放电循环过程中锂离子在电极和电解质界面之间的转移速率,使其具有高的初始充放电比容量;但大的比表面积使电极材料在循环过程中会与电解质接触面积增多,在充放电循环时材料表面形成更多的固态电解质界面膜,从而造成了更多的比容量损失。从表2可以看出,3种材料在充放电循环100次后的放电比容量大小关系为TG-3>TG-1>TG-2≈石墨。因此,对比3种材料可以发现,当复合材料中TiO2含量最多时(TG-1),材料在充放电循环时具有最大的首次充放电比容量,但其循环稳定后的充放电比容量较低;当复合材料中TiO2含量较小时(TG-3),材料在充放电循环时具有较低的首次充放电比容量,但其在循环稳定后的充放电比容量较高。
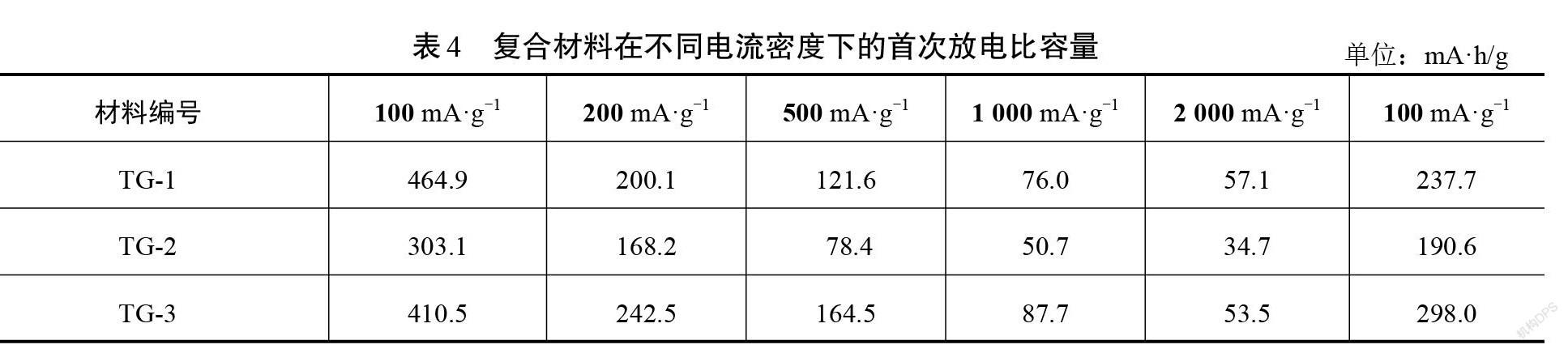
为了进一步研究复合材料在不同电流密度下的循环性能,研究了复合材料在不同电流密度下分别循环20次的放电比容量及库仑效率。图6为复合材料的循环特征图,图6(a)、图6(b)、图6(c)分别为TG-1、TG-2、TG-3复合材料的放电比容量及库仑效率图。表4为TG-1、TG-2、TG-3复合材料在不同电流密度下的首次放电比容量。从图6可以看出,3种复合材料在100 mA/g的前10次充放电循环过程中,材料的放电比容量逐渐降低,这可归因于充放电循环过程中负极材料表面不断形成新的SEI膜,从而导致比容量的损失。但是随着充放电循环次数的增加,复合材料的放电比容量损失逐渐减小,这是由于材料表面已逐步形成了稳定的SEI膜,使得材料的库仑效率逐渐提升并接近100%。因此,由于复合材料在100 mA/g电流密度下循环10次后已经形成了稳定的SEI膜,当电流密度改变为200 mA/g、500 mA/g、1 A/g、2 A/g后,3种复合材料基本都没有放电比容量的损失,在之后的每一个20次循环时,放电比容量曲线基本保持直线,但随着电流密度的增大,复合材料的放电比容量减小。当复合材料在2 A/g电流密度循环20次后电流密度再次恢复为100 mA/g时,循环稳定后材料的放电比容量大小与第一次100 mA/g电流密度下循环稳定后的放电比容量大小基本相等,这说明了该复合材料在经过较大电流密度循环后,当电流密度恢复时材料的放电比容量能回到首次低电流稳定后的数值,证明了所制备的石墨@TiO2复合材料具有出色的循环稳定性和容量保持性能。
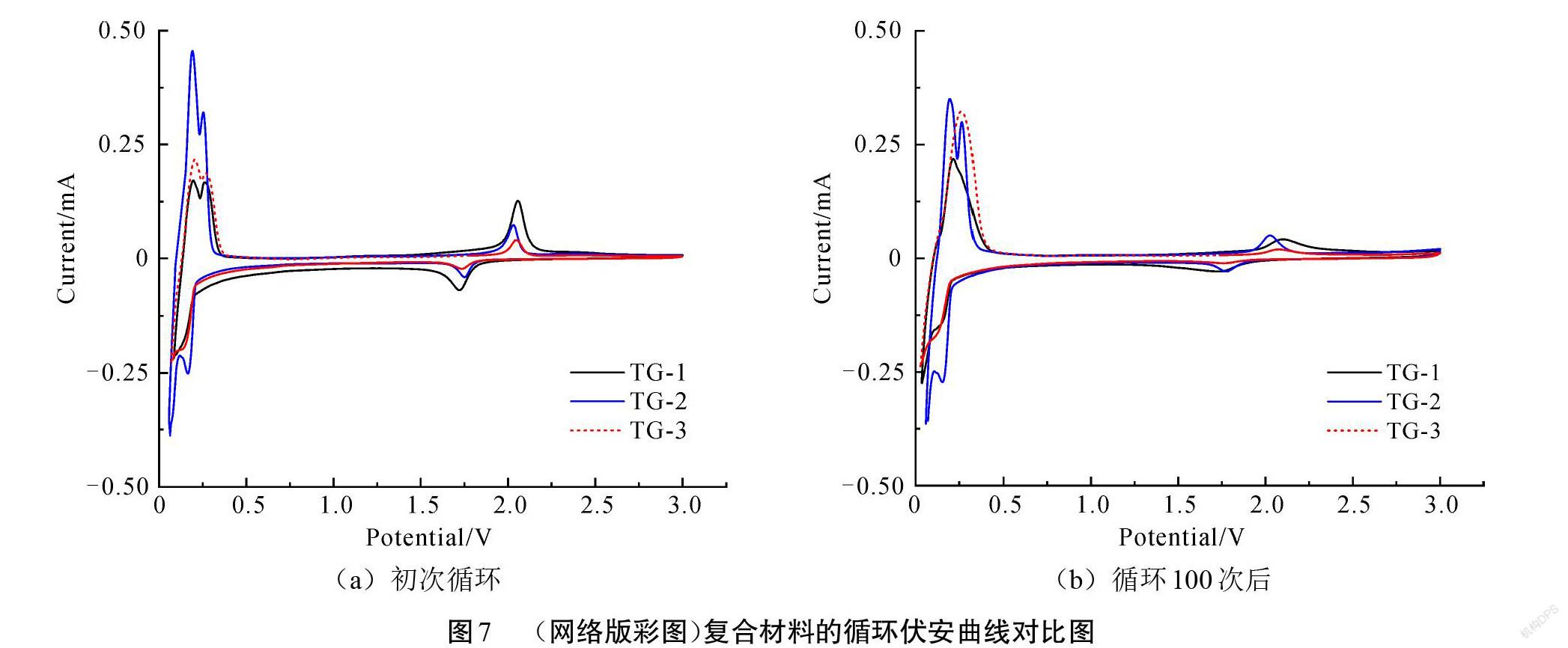
图7为3种石墨@TiO2复合材料的循环伏安曲线(CV)对比图。图7(a)为初次循环的CV曲线,可以看出,在TG-1复合材料的初次循环CV曲线上的1.7 V附近有一个较高的还原峰,表示在放电过程中锂离子的嵌入过程,该电压值能较好地对应于图4(a)充放电曲线中的初始放电平台电压值;在2.1 V附近有一个氧化峰,表示充电过程中锂离子的脱嵌过程,对应于图4(a)中的初始充电平台电压值。对比3种材料的初始CV曲线图,可以看出,由于TiO2材料含量的不同,从而使3种材料在1.7 V/2.1 V处的还原/氧化峰高度不一,峰高大小为TG-1>TG-2>TG-3,且峰值电压存在细微差异。3种复合材料的初始CV曲线上还存在电压为0.19 V和0.25 V的氧化峰,表示复合材料中石墨成分在充电过程中锂离子的脱嵌过程,对应于图5(d)单一石墨的初始充电平台电压值。TG-2复合材料在电压为0.06 V和0.16 V处出现了明显的还原峰,表示复合材料中石墨成分在放电过程中锂离子的嵌入过程,对应于图5(d)单一石墨的初始放电平台电压值。但TG-1和TG-3复合材料只在电压值为0.06 V处出现了一个还原峰,0.16 V处的还原峰不明显,这可能是由于3种复合材料的成分配比关系导致复合材料的峰值出现差异。图7(b)为3种复合材料循环100次之后的CV曲线,在充放电循环100次后,对应的TiO2材料的还原/氧化峰均出现了明显的降低,且TG-1复合材料的峰值变化最为明显,原因是在100次循环之后,复合材料表面的TiO2大部分已经变成了稳定的固态电解质界面膜,不再参与锂离子的嵌入和脱出反应,对应于图5中复合材料在循环100次后不再出现明显的TiO2充放电平台。可以发现3种复合材料在充放电循环100次后,石墨材料的还原/氧化峰变化均不明显,表明复合材料在100次循环过程中,只有部分的石墨材料转变成了SEI膜。
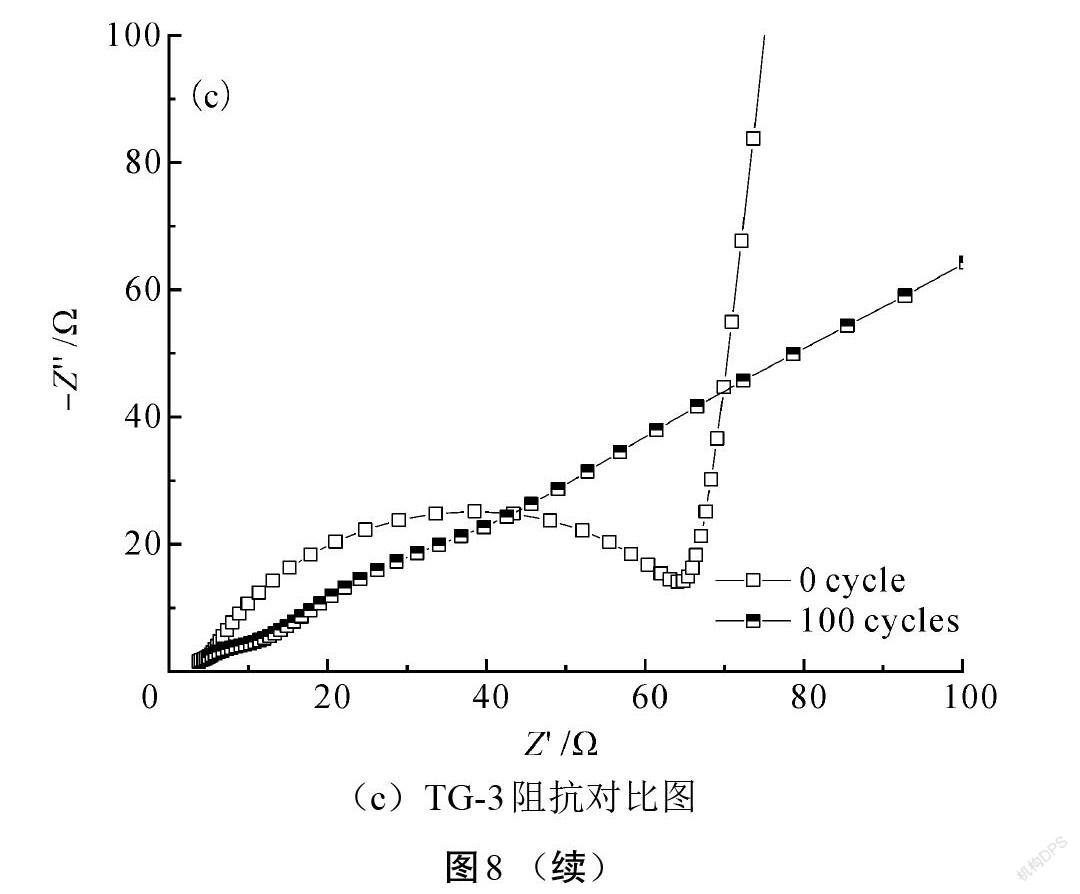
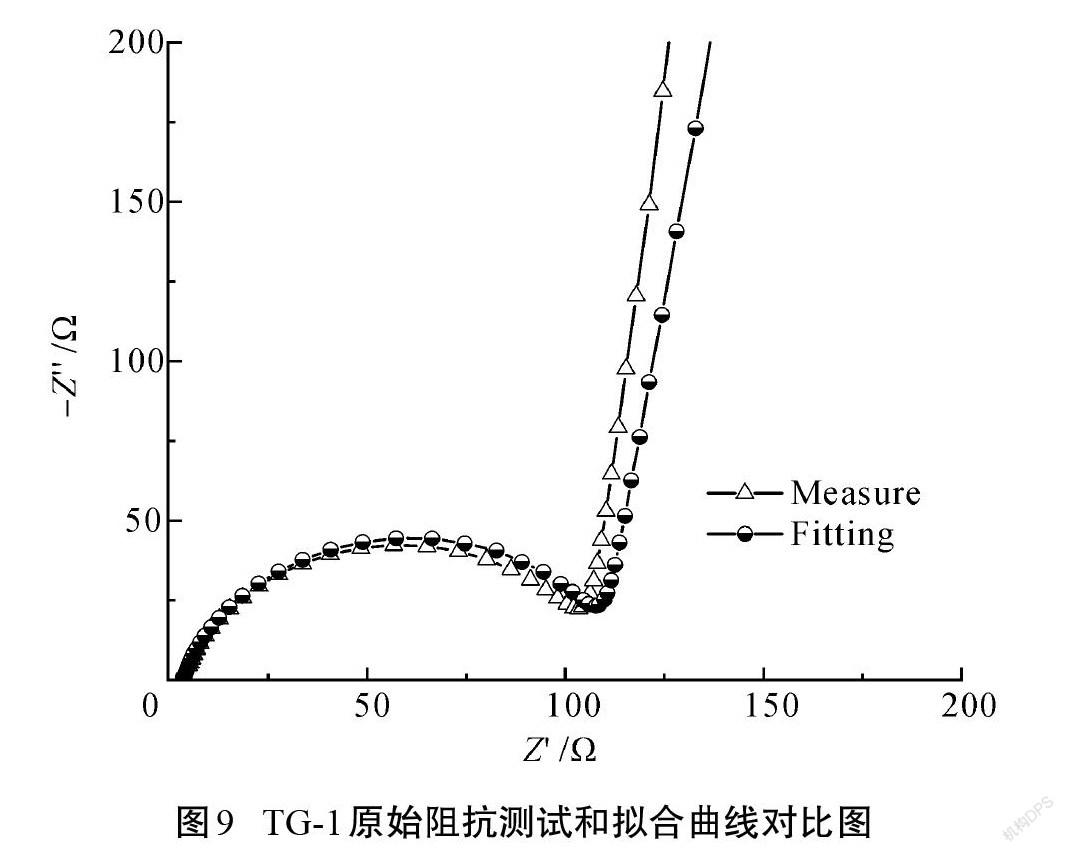
图8为复合材料的电化学阻抗谱曲线(EIS)。图8(a)、图8(b)、图8(c)分别为TG-1、TG-2和TG-3复合材料的初始阻抗和循环100次后的阻抗对比图,图9为TG-1复合材料的初始阻抗测试和拟合曲线对比图。由Kronig-Kramers模拟显示TG-1、TG-2和TG-3复合材料初始EIS的χ2值分别为 9.562 6[×]10-6、1.294 6[×]10-6、1.931 3[×]10-6,均远小于0.01,表明测量出的EIS曲线能很好地反应材料电极阻抗的真实数据[21]。从EIS曲线可知,3种复合材料初始阻抗曲线均由高频半圆曲线(代表电荷转移阻抗)和低频斜线(代表锂离子扩散产生的阻抗)组成[22]。由于TiO2材料為半导体材料,其导电性比石墨材料差;由于TG-1、TG-2、TG-3复合材料的TiO2含量不同,使得3种材料的初始阻抗不同。对比三者的初始EIS曲线的高频半圆部分,阻抗大小关系为TG-1>TG-2>TG-3,与3种复合材料中TiO2含量相对应。对比3种复合材料EIS曲线的低频斜线部分,TG-1和TG-3基本相同,归因于这2种复合材料表面均由结构相似的TiO2材料构成,因此,对应的锂离子扩散性能基本相同,但TG-2与其余两者不同,这是由于TG-2复合材料的电化学性能较差导致的。此外,通过EIS曲线还可以发现,经过100次循环后,阻抗谱线的高频半圆部分出现了较大的变化,其中TG-1的半圆直径减小,这是因为循环100次后,复合材料表面的TiO2材料大部分转变成了具有高离子电导率的SEI膜。而TG-2和TG-3复合材料在循环后的高频半圆部分基本消失不见,这可能是复合材料表面的TiO2层基本转变成了SEI膜造成的。对比3种复合材料在循环100次后的EIS曲线低频斜线部分,可以发现斜率均发生了变化,且三者的斜率基本相似,表明3种材料在循环100次后,材料的锂离子扩散性能发生了相似的变化。
2.4 光催化性能分析
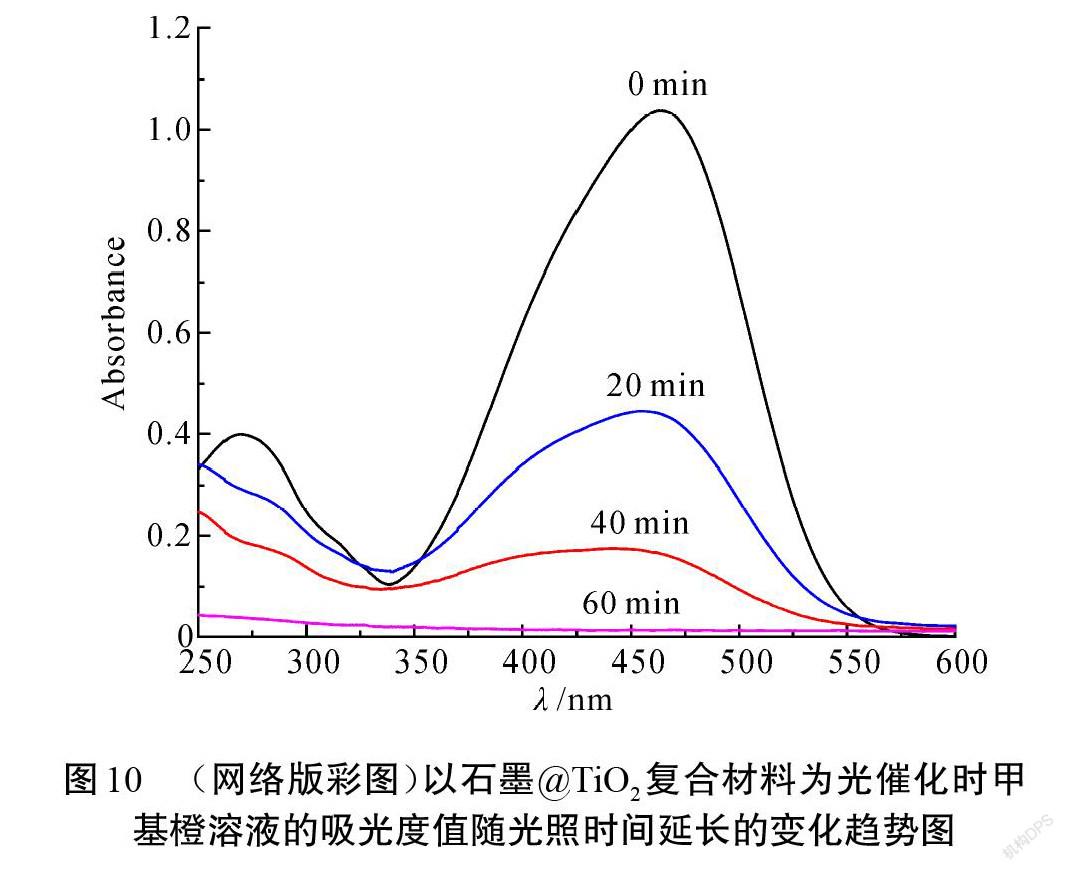
为研究复合材料的光催化性能,测试了其对甲基橙溶液的光催化降解速率。图10为TG-2复合材料作为光催化剂时,甲基橙溶液随着紫外光(UV)照射时间的延长而发生的吸光度变化曲线。研究发现,随着紫外光照射时间的延长,甲基橙溶液在波长为464 nm处的吸光度值逐渐降低;在紫外光照射60 min后,溶液的吸光度曲线趋于直线,表明紫外光照射60 min后甲基橙溶液已被完全降解,这说明制备的石墨@TiO2复合材料具有优异的光催化 性能。
圖11为在不同催化反应条件和时间下甲基橙溶液的降解速率对比图。由图可以看出,在催化反应60 min后,以TG-2为光催化剂且没有紫外光照射的条件下甲基橙溶液的降解率仅为4.67%,而有紫外光照射但没有光催化剂时甲基橙溶液降解率为8.12%,有紫外光照射且以单一石墨为光催化剂时甲基橙溶液降解率为11.84%;然而,以TG-2为光催化剂且有紫外光照射的甲基橙溶液的降解率高达98.85%,这表明石墨@TiO2复合材料光催化剂和紫外光照射对于甲基橙溶液的降解起到关键性的作用,石墨@TiO2复合材料在紫外光照射下具有优异的光催化性能。同时,也通过测试TG-1和TG-3光催化性能,发现在紫外光照射下,以TG-1、TG-3复合材料为光催化剂的甲基橙溶液在60 min后的降解率分别为98.72%、83.38%,表明这2种复合材料同样具有优异的光催化性能。以TG-1、TG-2、TG-3复合材料为光催化剂的甲基橙溶液在紫外光照射40 min后的降解率分别为90.48%、84.13%、68.51%。复合材料的光催化降解性能与复合材料中TiO2的含量成正比,催化性能优异程度排序为: TG-1>TG-2>TG-3,说明石墨@TiO2复合材料具有优异的光催化性能,是由于复合材料表面存在较大比表面积的TiO2,从而使得催化剂与降解物之间具有较高的接触面积,在光催化过程中增加了催化剂对光的吸收,因此,甲基橙溶液的降解率较高,使复合材料表现出优异的光催化性能。
3 总结
本文采用简单的一步溶剂热法制备出了具有锐钛矿相和大比表面积的石墨@TiO2复合材料,且通过改变前驱体中石墨的添加量制备出了不同配比的复合材料。当作为锂离子电池负极材料时,复合材料均具有较高的初始充放电比容量以及优异的循环稳定性。研究表明,复合材料中不同的TiO2含量对其复合材料的电化学性能影响明显,如初始充放电比容量和循环容量,复合材料中TiO2材料含量最多时复合材料的初始充放电比容量最大,在100 mA/g电流密度下可获得最大的初始放电比容量为464.9 mA·h/g,在2 A/g电流密度下最大的初始放电比容量为120.3 mA·h/g。而复合材料中TiO2材料含量最小时,复合材料具有最大的循环容量,在100 mA/g
电流密度下循环100次后的放电比容量为310.8 mA·h/g。当作为光催化剂时,石墨@TiO2复合材料均表现出优异的光催化性能,且随着复合材料中TiO2含量的增加,复合材料的光催化性能逐渐增强,在UV照射60 min后,甲基橙溶液的最高降解率为98.72%。
参考文献
[1] CHAUHAN A,SHARMA M,KUMAR S,et al.TiO2@C core@shell nanocomposites: a single precursor synthesis of photocatalyst for efficient solar water treatment[J].Journal of Hazardous Materials,2020,381:120883.
[2] HUANG H S,SONG Y,LI N J,et al.One-step in-situ preparation of N-doped TiO2@C derived from Ti3C2 MXene for enhanced visible-light driven photodegradation[J].Applied Catalysis B:Environmental,2019, 251:154-161.
[3] ZHANG G,GAO M,TIAN M,et al.In situ hydrothermal preparation and photocatalytic desulfurization performance of graphene wrapped TiO2 composites[J].Journal of Solid State Chemistry,2019,279:120953.
[4] YAO L J,WANG H,ZHANG Y Q,et al.Fabrication of N doped TiO2/C nanocomposites with hierarchical porous structure and high photocatalytic activity[J].Microporous and Mesoporous Materials,2019,288:109604.
[5] YU Y M,XIA J X,CHEN C,et al.One-step synthesis of a visible-light driven C@N-TiO2 porous nanocomposite:enhanced absorption,photocatalytic and photoelectrochemical performance[J].Journal of Physics and Chemistry of Solids,2020,136:109169.
[6] YUAN Y F,CHEN F,CAI G C,et al.Ultrafine TiO2 nanocrystalline anchored on nitrogen-doped amorphous mesoporous hollow carbon nanospheres as advanced anode for lithium ion batteries[J].Electrochimica Acta,2019, 296:669-675.
[7] CHEN J,LI Y,MU J C,et al.C@TiO2 nanocomposites with impressive electrochemical performances as anode material for lithium-ion batteries[J].Journal of Alloys and Compounds,2018,742:828-834.
[8] DEVINA W,NAM D,HWANG J,et al.Carbon-coated,hierarchically mesoporous TiO2 microparticles as an anode material for lithium and sodium ion batteries[J].Electrochimica Acta,2019,321:134639.
[9] ZHANG Y F,ZHANG N,CHEN J,et al.Preparation and lithium storage properties of C@TiO2/3D carbon hollow sphere skeleton composites[J]. Journal of Alloys and Compounds,2020,815:152511.
[10] FU Y X,DAI Y,PEI X Y,et al.TiO2 nanorods anchor on reduced graphene oxide (R-TiO2/rGO) composite as anode for high performance lithium-ion batteries[J]. Applied Surface Science,2019,497:143553.
[11] 张文康,梁燕艺,刘瑶,等.CdS/g-C3N4复合材料的制备及其光催化性能研究[J].广西科技大学学报,2018,29(4):66-73.
[12] BADVI K,JAVANBAKHT V.Enhanced photocatalytic degradation of dye contaminants with TiO2 immobilized on ZSM-5 zeolite modified with nickel nanoparticles[J].Journal of Cleaner Production,2021,280:124518.
[13] 闫共芹,蒋安邦,何强.Zn掺杂In2O3的水热法制备及其光催化与电化学性能研究[J].广西科技大学学报,2017,28(1):6-11.
[14] SING K S W.Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity[J].Pure and Applied Chemistry,1985,57(4):603-619.
[15] OH S I,KIM J C,DAR M A,et al.Synthesis and characterization of uniform hollow TiO2 nanofibers using electrospun fibrous cellulosic templates for lithium-ion battery electrodes[J].Journal of Alloys and Compounds,2019,800:483-489.
[16] FASAKIN O,OYEDOTUN K O,KEBEDE M,et al.Preparation and physico-chemical investigation of anatase TiO2 nanotubes for a stable anode of lithium-ion battery[J].Energy Reports,2020,6(S7):92-101.
[17] ZU G N,LI H Y,LIU S J,et al.Highly efficient mass determination of TiO2 nanotube arrays and its application in lithium-ion batteries[J].Sustainable Materials and Technologies,2018,18:e00079.
[18] 伊廷鋒,谢颖.锂离子电池电极材料[M].北京:化学工业出版社,2019.
[19] LIAO W M,SHAN Z Q,TIAN J H.Facile fabrication of Fe3O4@TiO2@C yolk-shell spheres as anode material for lithium ion batteries[J].Transactions of Tianjin University,2020,26(1):3-12.
[20] LIU S Z,ZHU K L,TIAN J H,et al.Submicron-sized mesoporous anatase TiO2 beads with trapped SnO2 for long-term,high-rate lithium storage[J].Journal of Alloys and Compounds,2015,639(15):60-67.
[21] REN P,PEI P C,LI Y H,et al.Diagnosis of water failures in proton exchange membrane fuel cell with zero-phase ohmic resistance and fixed-low-frequency impedance[J].Applied Energy,2019,239:785-792.
[22] LIU Q,HOU J G,XU C X,et al.TiO2 particles wrapped onto macroporous germanium skeleton as high performance anode for lithium-ion batteries[J].Chemical Engineering Journal,2020,381:122649.
Solvothermal synthesis and performance of C @ TiO2
nanocomposites
TAN Shanghua1, YAN Gongqin*1, WU Tong2
(1. School of Mechanical and Automotive Engineering, Guangxi University of Science and Technology,
Liuzhou 545616, China; 2. Shanghai Jingruiyang Industrial Co., Ltd, Shanghai 201314, China)
Abstract: C@TiO2 composite materials with different graphite contents were prepared by a simple
one-step solvothermal method in the presence of graphite using tetrabutyl titanate as the titanium source to obtain a new multifunctional material with high theoretical capacity, good cycle performance and excellent photocatalytic performance. The C@TiO2 composite material was used as lithium-ion
battery anode material and photocatalyst for the degradation of methyl orange solution to test its
electrochemical performance and photocatalytic performance. The results show that the anatase TiO2 nanowires are three-dimensionally interwoven and coated on the surface of the graphite sheet, so that the sample has a higher specific surface area. The higher the content of TiO2 in the sample, the greater the initial discharge specific capacity; the initial discharge specific capacity can be the highest (464.9 mA·h/g) at a current density of 100 mA/g. The initial discharge specific capacity at a current density of 2 A/g can reach up to 120.3 mA·h/g. The lower the content of TiO2 in the sample, the higher its initial discharge specific capacity, the discharge specific capacity after 100 charge/discharge cycles at a current density of 100 mA/g is 310.8 mA·h/g. Photocatalytic test results show that the C@TiO2 has excellent photocatalytic performance, and the photocatalytic performance increases with the increase of TiO2 content. After 60 minutes, the degradation rate of methyl orange solution can reach as high as 98.72%. The research shows that the obtained C@TiO2 composite has excellent electrochemical and photocatalytic properties, which is expected to replace the traditional anode materials and
photocatalyst materials, and has broad application prospects.
Key words: C@TiO2 nanocomposites; solvothermal synthesis; electrochemical property; photocatalytic property
(責任编辑:黎 娅)
