酸性溶液除氯技术研究现状及进展
2021-11-08张阳史丙丁马保中王猛王成彦
张阳,史丙丁,马保中,王猛,王成彦
(1.北京科技大学冶金与生态工程学院,北京 100083;2.稀贵金属绿色回收与提取北京市重点实验室,北京 100083)
近年来,由于矿产资源的过度开采,矿石品位下降,即使是经过浮选后的精矿,氯元素含量也呈现上升趋势,导致冶炼系统中氯含量升高。有色金属冶炼中,冶炼工艺不同,冶炼系统中氯的走向也不同。火法冶炼中大部分氯以氯化物的形式进入含硫烟气中,在烟气净化系统中进入污酸,形成含氯的硫酸溶液;湿法冶炼以锌冶炼为例,锌精矿经过焙烧和浸出,其中的一部分氯随焙砂进入锌浸出液中,而后续净化工艺对氯离子的净化作用较小,因此得到的电解液经多次循环使用后,会形成氯离子含量较高的硫酸锌电解液。此外,为缓解矿石资源短缺而开发的烟尘的综合回收利用,因氧化锌烟尘中氟氯含量较高,进一步导致电解液中氟氯含量上升。冶炼过程中,这些酸性溶液循环使用,使氯离子不断累积,酸液中的氯离子浓度越来越高。酸性溶液中的氯离子能增强酸液的腐蚀能力,甚至能腐蚀破坏合金、不锈钢和金属表面的钝化膜,对冶金设备和金属部件造成腐蚀,设备和部件更换频繁,增加生产成本,在湿法炼锌中还会加快电极腐蚀速度,使电解锌质量下降。因此,高含氯量的酸性溶液会使冶金生产效率下降,经济效益降低,引起车间安全隐患,严重危害工业生产,冶金工业酸性溶液氯离子去除研究具有重要意义。
1 含氯酸性溶液的产生及危害
1.1 含氯污酸的产生及其危害
许多有色金属在矿石中是以硫化物的形式存在的,如铜、镍、铅等,在以这些金属的硫化矿为原料进行火法冶炼时,会产生大量含硫烟气,这些烟气中还含有金属氧化物微尘、氯化物、氟化物、脉石粉粒、CO、水蒸气、砷化物等杂质。这类含硫烟气通常采取转化法制取硫酸。转化法烟气制酸的工艺过程为:烟气净化-气体干燥-二氧化硫转化—三氧化硫吸收。
烟气的洗涤净化通常在洗涤塔中进行,图1 所示为某镍铜冶炼厂烟气净化工序使用的四位一体湍冲洗涤塔[1]。高温烟气进入洗涤塔内被塔顶喷淋出的稀酸洗涤,经降温、除尘后送往填料塔。稀酸经过循环槽和沉降槽后重新用于喷淋,烟气中的氯化物很容易被水和稀酸吸收,因而进入循环酸中,多次循环后,酸液中的氯含量升高,氯离子浓度能达到2.0 g/L 以上[2-4]。

图1 某镍铜冶炼厂烟气净化系统[1]Fig.1 Flue gas purification system of a nickel copper smelter[1]
冶金中的设备多为金属合金,在生产过程中,酸性溶液在高速流动下不断冲刷设备表面,造成腐蚀,而酸性溶液中的氯离子对腐蚀过程起着催化作用,且氯离子能够促进酸液对金属表面钝化膜的溶解,甚至氯离子直接穿过钝化膜,与内部金属反应[4]。即使是具有耐腐蚀性能的不锈钢在受到含有氯离子的酸液冲刷时,也容易在其奥氏体的应力部位产生腐蚀裂纹,腐蚀又由裂纹进一步向内部发展,甚至导致穿孔或者断裂[5]。烟气净化系统中的含氯酸液对洗涤设备造成了严重腐蚀,洗涤塔、管道、喷嘴、酸泵等腐蚀尤其严重,造成了喷淋酸分布不均匀,酸泵喷嘴更换频繁等问题,增加生产成本,降低净化效率。因此,酸性溶液中的氯离子对烟气净化过程造成了十分严重的危害。
1.2 含氯硫酸锌电解液的产生及危害
近年来,我国锌冶炼产能不断扩大,锌需求量逐年增长,锌精矿供应远小于冶炼需要。为缓解矿石资源的短缺问题,开发了氧化锌烟尘的综合回收利用,而氧化锌烟尘中氟氯含量较高,几乎全部进入浸出液中,导致电解液中氟氯含量上升[6-7]。在常规湿法炼锌中,锌精矿中70%的氯在焙烧中随烟气以低熔点氯化物的形式进入烟气处理系统,最后进入污酸中,其余则随锌焙砂和烟尘通过浸出进入锌浸出液[8],这一部分约占浸出液中氯总量的65%,除此之外,湿法系统中氯的来源还有铟萃余液和生产用水[8-9]。
浸出液经过三段净化后进入电解槽,在电解过程中,含氯离子的电解液会腐蚀电极极板。锌电解过程使用铝板作为阴极极板,在铝板的表面有一层耐腐蚀的氧化薄膜,也称为钝化膜,这层钝化膜的主要成分是Al2O3和Al(OH)3。铝表面的钝化膜形成速度快,厚度大,且非常致密完整,与金属主体结合牢固,因而可以在酸性溶液中做极板。电解时,金属锌就沉积在这层钝化膜上,由于这层钝化膜的结构与电积锌的晶体结构差别很大,因而两者之间的结合并不牢固,易于剥离。
当酸性的硫酸锌电解液中有氯离子存在时,由于氯离子对O2-、OH-的排斥和置换作用,与铝板表面的钝化膜反应生成了AlCl3和[AlCl6]3-离子进入溶液,钝化膜受到腐蚀,发生的反应为:

钝化膜被破坏,电解液与铝板接触造成铝板腐蚀,沉积在极板上的锌也不易剥离,为此需要频繁更换极板,生产成本提高,生产效率降低。
当溶液中氯的含量较高时,不仅仅是阴极铝板,阳极铅板(Pb-Ag 合金)的腐蚀速度也将增大。铅板在用于电解前先进行镀膜,在极板表面形成一层PbO2膜,它不如铝钝化膜那样致密,膜上仍存在一些细小的孔隙,水化程度不大的氯离子半径很小,能轻易从这些的孔隙中渗入到保护膜内,与铅反应,反应方程式为:

所生成的PbCl2溶解度比PbSO4高得多,在25 ℃时,PbCl2溶解度为10.786 g/L,PbSO4溶解度为0.045 2 g/L。因此,PbCl2将转化为PbSO4,以固相形式析出,同时释放出氯离子,又能重新与铅阳极作用,不断腐蚀阳极极板。生成的固体PbSO4颗粒掺杂进电积锌中,使锌产品的质量降低[6]。
因此,硫酸锌电解液中的氯会加速电极腐蚀,使电极寿命缩短,电积锌剥离困难,产品中铅含量增加,使生产成本提高,产品质量降低,生产效率降低。当电解液中的氯离子含量超过0.5 g/L 时,电极极板腐蚀速度加快,锌产品品质受到严重影响。降低电解液中的氯含量,能够减少电极极板的消耗,提高产品质量,减少设备和管道的腐蚀,提高生产效率。
2 国内外除氯研究现状
去除酸性溶液中氯离子的方法主要有化学沉淀法、离子交换法、萃取法、针铁矿法、电化学法等,其中主要方法是沉淀法,包括AgCl 沉淀、BiOCl 沉淀、CuCl 沉淀等。
2.1 氯化银法除氯
氯化银沉淀法除氯的原理是将硫酸银加入到含氯酸液中,反应生成溶解度比硫酸银(溶解度8.3 g/L)更小的氯化银沉淀(溶解度0.001 95 g/L)来去除溶液中的氯离子,发生的化学反应为:

这种除氯方法操作简单,除氯效果极好,在常温下脱除率就可以达到99%以上。但是该方法存在银盐价格高且难回收的缺点。
对于AgCl 沉淀的处理方式有2 种,一是将其还原为Ag 单质;二是将其转化为Ag2SO4重新利用。氯化银的还原精炼方法主要有2 大类:液相还原法和高温熔融还原法,前者为使用水合肼、甲醛、硼氢化钠、双氧水、甲酸等还原剂还原,或锌粉、铁粉、铜粉等金属置换;后者为利用碳酸钠、硼砂、碳、氢气等还原剂高温熔融还原[10]。下面介绍几种常用的还原方法:
1)水合肼还原法。用水合肼,即联氨水溶液还原氯化银制取纯银粉,向氯化银浆料中加入水合肼还原氯化银的反应方程式为:

向体系中加入氨水或通入氨气可以使部分AgCl 形成银氨络离子,加快还原反应。有实验对影响还原过程的因素进行了研究,表明pH和搅拌对还原影响显著,在pH 为10~11,联氨用量为2 倍理论量的条件下,充分反应30 min,银的还原率可达99%以上[11]。
这种方法流程短,操作简单,制取的银粉粒度细,纯度高,但水合肼毒性极强,不适宜工业生产。
2)甲醛还原法。向氯化银悬料加入10% NaOH溶液调整pH 至11,再缓慢加入甲醛,发生还原反应,反应方程式为:

该反应为放热反应,且反应速度快。得到的海绵银需要多次洗涤去除其中的甲醛,最终银锭纯度大于99%。王宪忠等采用亚硫酸钠浸出-甲醛还原方法处理氯化银渣,银综合回收率达98%以上[12]。
3)硼氢化钠还原法。向氯化银中加入浓NaOH调pH 至12.5,在60~80 ℃条件下加入3%NaBH4溶液还原氯化银,还原得到的海绵银纯度大于99.9%,还原反应为[10]:
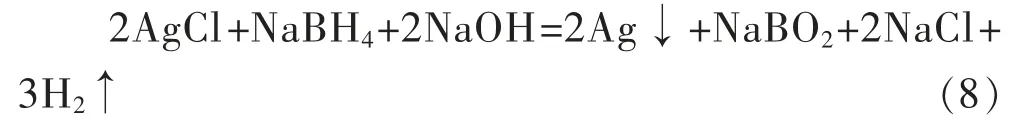
由于硼氢化钠有较强的毒性,并未应用于生产。目前,硼氢化钠常作为还原剂用于制备纳米银粉,已有较多研究报道了这种还原方法。
4)置换法。利用活泼性较强的金属将溶液中活泼性较弱的银置换出来,通常使用锌粉、铁粉、铜粉等金属进行置换[13]。由于置换反应需要在酸性条件下进行,以锌粉为还原剂时,有较多的锌粉与酸反应,增加锌粉消耗,同时释放大量热,不适宜工业生产。铁粉和铜粉都能较好地置换银,但铁粉还原反应速度更快,且铁价格低于铜,更适于实际生产。
2.2 氯化亚铜法除氯
以使用铜渣作除氯剂为例,氯化亚铜法除氯的原理是使铜渣中的铜溶解到酸液中,溶液中的铜离子与铜发生反歧化反应生成亚铜离子进行除氯。反应方程式为:
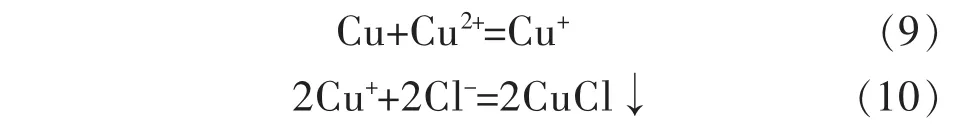
生成的氯化亚铜沉淀可以通过碱洗法脱氯产生Cu2O,Cu2O 再返回除氯。碱洗法化学反应为:

这种方法的优点是使用湿法炼锌净化工序产生的铜镉渣为原料进行除氯,适用于锌浸出液除氯,CuCl 经过处理后再生可返回使用。缺点是除氯时间长,除氯效果受铜渣铜含量限制,适用于氯含量低的溶液。根据溶液中Cu+的来源将该法分为3 种:①湿法炼锌净化工段产生的铜镉渣;②锌粉还原硫酸铜产生的活性铜;③氧化亚铜除氯剂。
申永强等进行正交实验探究氯化亚铜法除氯的各种因素对脱除率的影响。结果显示影响因素的主次排列顺序为:无水硫酸铜与Cl-的物质的量之比>温度>铜与Cl-的物质的量之比>反应时间[14]。
Li 等对氯化亚铜沉淀除氯过程进行了热力学分析,得到如下结论:①CuCl 形成与pH,[Cu]T、[Cl-]有关。②在Cu-Cl--H2O 系中,Cu2+和Cu+将分别与氯离子形成一系列络合物CuCl-、CuCl2-、CuCl32-、CuCl3-等,通过计算得到氯化亚铜净化脱氯极限为0.04 g/L。使用含氯0.150 g/L 的锌浸出液进行了小型实验,锌粉加入量为3 g/L,五水硫酸铜加入量为28 g/L,pH=1.0,在40 ℃下,反应1 h,脱除率为60 %左右[15]。
某冶炼厂研究了铜渣法除氯中各因素对除氯效果的影响。该厂冶炼系统的锌浸出液氯含量为1.08 g/L,向其中加入含铜40%~50%的铜渣和二氧化锰,在50~70 ℃下反应100 min,氯脱除率达85%以上[6]。
某锌冶炼厂利用湿法炼锌净化工段自产的铜渣去除废电解液中氯,通过实验确定较优工艺条件:20 ℃下,铜渣加入量6 g/L,反应10 min,可将电解液中氯含量降低到0.1 g/L 以下。该厂自2010 年采用该工艺以来,每年处理废电解液近20 万m3[16]。
Yang 等对氯化亚铜法除氯进行条件实验确定了较优条件,之后通过把浸出液上清液运输到镉工序段,使用镉工序段产出的高品位铜镉渣除氯,实现了低成本运作的产业化试验。此次试验由于成本、设备和设施等原因,反应条件未达到理想,氯脱除率平均为47.02%,相比于较优实验条件下的60.3%脱除率有所下降[17]。
叶标等提出用红色粉末除氯剂Cu2O,与溶液中的氯离子结合生成白色CuCl 沉淀,过滤后,得除氯合格液与除氯渣,将除氯渣与碱作用又还原生成红色粉末沉淀物Cu2O 与氯化钠溶液,将除氯渣与碱反应生成的溶液进行过滤,得到固相含水再生红色Cu2O,作为除氯剂再循环除氯,液相氯化钠溶液蒸发结晶生产氯化钠晶体[18]。
氯化亚铜法除氯是一种应用规模较大的除氯技术,常应用于锌湿法冶炼工艺用于降低硫酸锌电解液中的氯含量,也可应用于含氯废水的处理。由于铜离子残留的问题,该方法并不适用于污酸除氯。在锌湿法冶炼中,可将除氯放在除铜镉过程之前来保证电解液中没有铜离子残留,若使用此方法对污酸进行除氯,常规的锌粉除铜法会导致锌离子残留在溶液中和溶液酸度的降低。因此该方法更适用于锌湿法炼锌工艺锌电解液中氯的脱除。
2.3 氯氧铋法除氯
氯氧铋法除氯的原理是利用氧化铋溶解在酸溶液中产生的铋离子,在氯离子作用下,转化为难溶的氯氧铋沉淀,从而实现氯的脱除。反应方程式如下:
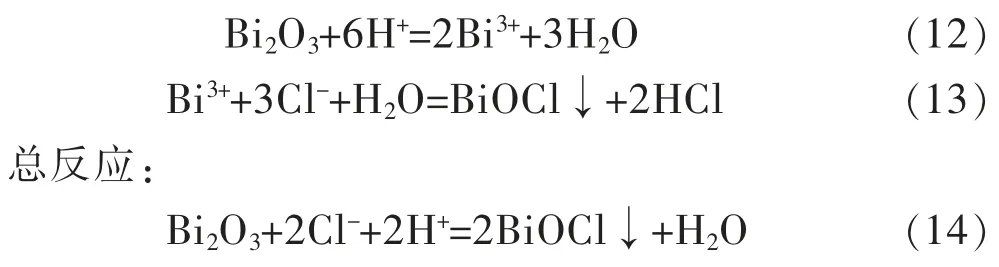
氯氧铋在高温条件下经高碱性溶液能再生为氧化铋,重新用于除氯。若温度较低或溶液低碱性则会生成氢氧化铋,而氢氧化铋不能用于除氯[19]。反应如下:
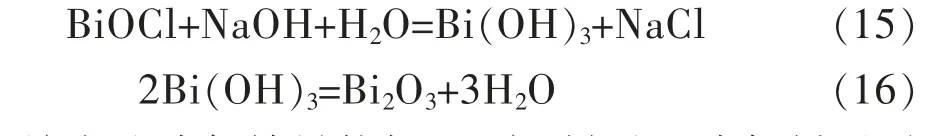
该方法除氯效果较好,反应时间短,除氯剂可再生重复使用,但氧化铋价格较贵。
Wen 进行实验得到以下结论:氧化铋除氯在15~20 min 即可达到最大脱除率;温度对脱除效果影响不大,在10~90 ℃温度范围内脱除率均为70%~80%;再生得到的氧化铋与初始氧化铋除氯效果相差不大,均在70%以上[20]。
罗玉德提出一种使用氧化铋去除含氯硫酸锌溶液中氯离子的方法。该方法除氯流程图如图2 所示。先将氧化铋加入到40~80 g/L 的稀硫酸溶液中进行酸化,使用酸化得到的一水合碱式硫酸铋进行除氯,得到氯氧铋沉淀物;将沉淀分离出置于含有氧化铋晶种浓度为35~70 g/L 的碱溶液中,得到氧化铋和氯化物溶液,氧化铋返回除氯,氯化物溶液蒸发结晶为固体氯化物。经过实验,含氯2.2 g/L 的硫酸锌溶液的氯脱除率达到90%以上,再生实验除氯率为98%~99%[21]。

图2 氧化铋除氯流程[21]Fig.2 Flow chart of bismuth oxide method for chlorine removal[21]
刘洪嶂等对氧化铋除氯过程进行了实验并将其实现产业化应用。实验发现:①pH 在3.0 以下时铋损失量达到0.3 g/L,在3.0 以上时,铋损失较少,为0.004 g/L,pH 调节剂宜选择碱式碳酸锌;②氧化铋加入量对脱除率有明显影响,5~30 倍之间,加入量越大,脱除率越高;③碱洗过程的温度控制在90 ℃,碱含60 g/L,氯氧铋可基本转换为氧化铋。产业化应用使用的氧化铋由铅冶炼系统中贵金属工序的铋渣制备,冶炼系统中硫酸锌溶液中含氯约为1.5 g/L 左右,氧化铋加入量为理论除氯用量的15~20 倍,可将氯含量降低至0.3 g/L 左右,氯脱除率为80%左右,同时还能去除约30%~40%的氟。氧化铋可再生重复使用,长期使用因杂质过多影响除氯效果时,除杂后可再次循环使用[22]。
吴文伟进行以氯氧铋为原料制备纳米级氧化铋的研究。采用碳酸氢铵-氨水溶液作脱氯剂进行2 次脱氯,同时氯氧铋转型为氧化铋前驱体碳酸氧铋(BiO)2CO3,将碳酸氧铋热解即可得到纳米氧化铋产品,氯含量为0.62%,平均粒径约40 nm[23]。
通过控制条件,该方法可以获得较高的氯脱除率,但除氯过程需严格控制pH 以减少Bi3+在溶液中的溶解,不适用于处理酸度较大的溶液。
2.4 离子交换法
离子交换法是使用离子交换树脂进行除氯,用于除氯的树脂多为强碱性阴离子交换树脂,这种树脂能在水中离解出阴离子,然后带有正电基团的树脂会吸附并与溶液中的氯离子结合,从而脱除氯离子。
离子交换法具有树脂再生容易、流程短、操作简单、运营成本低等优点,但除氯效果低,树脂再生率不高,再生后液处理难度较大[24]。
树脂在使用过程中会由于氧化或其他环境因素导致结构被破坏,即树脂变质,失去离子交换能力。如Fe3+、二氧化硅、溶液氧含量等[25]。
以717 强碱型阴离子交换树脂为例,出厂为氯型的离子交换树脂(RCL)经稀硫酸转型成硫酸型(R2-SO4),在硫酸锌溶液中与Cl-发生如下可逆反应:

硫酸型树脂转化为氯型,溶液中氯离子转移到树脂中,将氯型树脂与溶液分离,用稀硫酸淋洗可重新转型为硫酸型继续除氯。
王晓丹等研究201×7 型阴离子交换树脂对硫酸锌电解液除氯的效果。使用氯离子含量为1.36 g/L 的硫酸锌电解液进行动态交换试验,一级离子交换的脱除率为31.74%。失效树脂可用硫酸溶液再生,再生率为83.4%[26]。
邹晓勇等使用大孔阴离子树脂对硫酸锌电解液进行氯的脱除实验。吸附解吸实验发现在pH 为5.4,温度为50 ℃条件下,树脂对氯离子的吸附效果较好,氯的交换容量为27.2 mg/g 湿树脂,用0.5 mol/L 硫酸溶液解吸,解吸率可达到96.6%。实验发现该型树脂对F-也有一定的脱除效果。在扩大试验中树脂平均交换容量为18.2 mg/g 湿树脂,吸附后氯离子含量为0.24 g/L[27]。
宋志红提出一种硫酸锌电解液离子交换法除氟氯技术。使用阴离子交换树脂D201,在pH=2.5~5.5,温度5~85 ℃条件下,吸附时间为5~15 h,氯脱除率基本大于80%,氟脱除率大于50%,锌损失量小于0.5%,使用10%硫酸溶液解吸,解吸时间为3~6 h[28]。
离子交换法因其具有操作简单,成本低,流程短等优点而获得了较多的应用,通过已有的研究和应用表明,该方法能有效脱除溶液中的氯离子,但处理周期长,树脂的变质会对脱除效果产生较大影响。
2.5 针铁矿法
针铁矿(FeOOH)具有羟基结构,在酸性溶液中,针铁矿沉淀表面的羟基质子化,增加了表面的正电荷,造成晶体表面离子电荷不完全平衡,吸附溶液中的氯离子和氟离子,从而达到脱除氯离子的目的。另外,由于F-、Cl-半径(0.136 nm和0.181 nm)接近氢氧根的半径(0.140 nm),所以它们能够在针铁矿的形成时进入晶格,伴随针铁矿沉淀脱除[29-30]。相关化学反应方程式为:
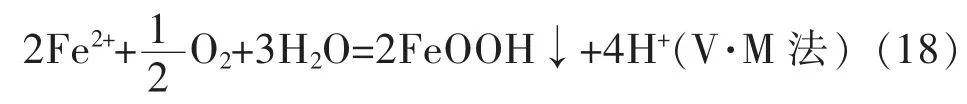
针铁矿法[31]能有效脱除氟、氯的同时还可以脱除大部分的砷、锑,优点是能耗低、成本低,但渣中锌夹杂量较多,锌损失率较大。
张元福等进行了针铁矿法脱除锌浸出液中氟氯的研究。进行了小型试验考察铁用量、酸度和温度对氟氯脱除的影响,并分别使用V·M 法和E·Z 法进行扩大试验。浸出液中总铁含量为8~10 g/L、pH 为3~4.5,在85~90 ℃下,氯和氟脱除率均在75%以上,砷、锑脱除率大于95%,能够将氯脱除到0.05 g/L 以下,且E·Z 法脱除氯效果优于V·M 法[32]。
针铁矿法是湿法炼锌中锌浸出液除铁的一种常用方法,因针铁矿的特殊结构,该过程对氯和氟也有一定的脱除效果,但脱除率不高,依赖于溶液的总铁含量和pH,适用于氯离子浓度不高的锌浸出液中氯的脱除。
2.6 萃取法
萃取法既可以除氯也可以除氟,对此方法的研究多以锌浸出液为研究对象,根据萃取物质的不同,可分为2 种方式,一种是萃取锌,氟、氯留在萃残液中[33];另一种是萃取氟、氯,锌留在萃残液中。
萃取法脱除效率高、成本低、操作简单,但存在萃取和反萃时分相时间长,有机相乳化和萃取剂、稀释剂等有机物易被夹带进入电解液等问题[24]。
罗远辉等采用P204 溶剂萃取含氟氯的锌浸出液。通过先将锌萃取到溶剂中,再控制条件将锌反萃回电解液中来除氯。调整锌浸出液pH 为4.0,相比(有机相与水相的体积比)为2.0,在40 ℃下萃取5 min,氯和氟的浓度分别降低到0.079 g/L和0.042 g/L,氯和氟的脱除率均高于99%。反萃过程相比为0.5,在40 ℃下反萃5 min,锌回收率大于95%[34]。
楚立军等采用N235 萃取含氟、氯的锌浸出液,将氯和氟萃取到有机相中,锌留存于萃余液,锌损失率低于5%,氯脱除率高于94%,氟脱除率高于80%。通过在有机相中添加异辛醇,控制萃取、水洗、反萃温度为40~45 ℃,可避免出现分相时间长和有机相乳化。萃余液中氯和氟浓度分别为0.082 g/L和0.011 g/L[35]。
萃取法因存在机相乳化和分相时间长的问题而未应用于生产,但诸多实验表明该方法脱除率较高,脱除效果好,也有一些的研究通过控制条件解决了分相时间长和有机相乳化问题的方法,但仍需进一步研究和实践。
2.7 电化学法
电化学法除氯已应用于钢筋混凝土除氯,通过电化学反应将钢筋混凝土中的氯离子转化为氯气排出,图3 所示为电化学法去除钢筋混凝土中氯离子的原理图[36]。电化学法除氟也有研究证明其可行性[37-38]。目前已有的酸性溶液电化学法除氯的研究是通过控制电化学体系的条件,使溶液中的氯离子以沉淀的形式去除,从而脱除氯离子。

图3 电化学法除氯原理[36]Fig.3 Schematic diagram of electrochemical dechlorination[36]
Wu 等以铜板为工作电极,研究了硫酸锌水溶液中氯离子的电化学去除,氯脱除率为54.5%。研究表明脱氯效果受阳极电位、搅拌强度和反应时间影响。电化学反应机理为:阳极铜被氧化产生Cu+和Cu2+与溶液中的Cl-反应生成CuCl、CuCl2-和CuCl32-等,CuCl 沉积在阳极表面,使氯从溶液中脱除[39]。
2.8 氧化法
氧化法主要是使用的氧化剂将溶液中的氯离子氧化为氯气从溶液中脱除的方法,脱除工艺由氧化剂的种类决定。这种方法多处于研究阶段,应用较少。
Bolton 等发明一种用臭氧从含有锰离子和氯离子的酸性硫酸锌溶液中去除锰离子而不失去大量锌离子的工艺,发现当锰离子浓度降至较低水平时臭氧与氯离子发生反应,氯离子被氧化为氯气从溶液中排出。对含3.74 g/L 锰离子和0.107 g/L 氯离子的硫酸锌溶液,通过如图4 所示的装置将锰离子和氯离子脱除到0.03 g/L和0.003 g/L[40]。

图4 臭氧去除锰和氯的装置[40]Fig.4 Removal of manganese and chlorine by ozone[40]
郭亚丹等采用自制的电催化氧化装置对高含氯硫酸废水进行除氯实验,装置如图5 所示,使用石墨板作阳极,钛板作阴极,溶液中的氯离子在阳极被氧化,生成氯气以及次氯酸、次氯酸根和高氯酸根等活性中间产物,氯气从溶液中排从而除去除废水中的氯离子。处理实际含氯硫酸废水时,Cl-去除率达到了82.36%[41]。

图5 电催化氧化装置[41]Fig.5 Electrocatalytic oxidation apparatus[41]
2.9 浓缩吹脱法
浓缩吹脱法脱氯是基于HCl 易挥发的性质,通过控制条件进行减压、蒸发、浓缩等操作促进HCl 挥发从溶液中脱除。王恒全研究了减压蒸发法去除硫酸锌电解液中的氯的试验。浓缩比为6∶1 进行减压蒸发,蒸发过程中,约有8%的酸以三氧化硫烟雾的形式损失,硫酸锌盐析结晶但可回收,氯的脱除率为90%[42]。之后进行了半工业化试验,获得较好的脱除效果和经济效益。该方法也可同时除氟,脱除率达到86%[43]。有部分工厂采用此方法进行氟氯的脱除,但产生的HCl,HF 等有毒有害气体难以处理。
3 结语与展望
由于人类对矿石的大量开采,品质高的矿石越来越少,想要从源头上控制冶炼工序中氯的含量是无法实现的,所以只能在含氯酸液对冶炼造成危害之前脱除。本文总结了目前已应用或研究较多的酸性溶液除氯的方法,其中沉淀法、针铁矿法、离子交换法和浓缩吹脱法均有应用。酸性溶液中,与氯离子性质相似的氟离子也是一种危害很大的粒子,能腐蚀玻璃陶瓷部件,危害锌电解过程。因此,酸性溶液氟氯的脱除是湿法冶金中一个重要的研究课题。
在以上除氯方法中,沉淀法应用最为广泛,脱除效果较好,但是对氟几乎没有脱除效果;离子交换法可以通过使用不同的树脂脱除氟氯,但是脱除效果一般,且树脂长期使用脱除效果逐渐变差;针铁矿法是湿法炼锌工序除氯的有效方法,控制合适条件可将氟氯脱除到满足锌冶炼的条件;电化学法和氧化法仍处在研究阶段;浓缩吹脱法可同时去除氟氯,工业上已有应用,但产生的HCl和HF 气体严重污染车间环境。总的来说每种方法都有不同的特点和优缺点,且酸液成分也因原料和工艺的不同而不同,选择合适的除氯方法十分重要。
今后,酸性溶液中氟氯的脱除研究应以提高脱除效率、低成本、节能环保为主要方向,氟氯离子的有效脱除和合理处置对改善冶炼工艺和环境保护都具有重要意义。
