SiC/C纤维热力学生长机理研究
2021-09-13杨凡凡李晋宇刘玉浩郝桓民范丽君黄小萧温广武
杨凡凡,张 瑜,张 涛,王 健,赵 伟,李晋宇,王 坤,刘玉浩,郝桓民,范丽君,黄小萧,温广武
(1.哈尔滨工业大学(威海)材料科学与工程学院,威海 264200;2.哈尔滨工业大学材料科学与工程学院,哈尔滨 150001;3.烟台鲁航炭材料科技有限公司,烟台 262006;4.山东理工大学材料科学与工程学院,淄博 255049)
0 引 言
碳纤维(CFs) 是一种优异的碳材料,比强度是钢的16倍以上,但密度仅为钢的1/5左右[1]。碳纤维的弹性模量通常高于230 GPa,是钢的弹性模量的1.8~2.6倍[2-4],此外还具有低电阻率[5-6]、耐酸[7]、耐腐蚀、耐油、耐辐射[8]和良好的抗热震性能[9]。自从20世纪60年代作为商品首次亮相以来,碳纤维作为一种受到广泛关注的新材料,已迅速用于航空航天和民用工业等高科技领域[10-11]。然而,碳纤维高温抗氧化性能弱[12-14]:当在温度超过550 ℃的大气气氛下,碳纤维本身将迅速开始氧化[15-17],失去其强化作用[18-19]。而SiC具有低的热膨胀和耐高温氧化性能[20-21],能弥补碳纤维抗氧化性能的不足。此外SiC具有高机械强度、抗蠕变性能以及与陶瓷基体的相容性好等优异性能[22-24],是理想的高温耐烧蚀材料。
SiC纤维制备工艺较长,且成本较高。如果采用商品化的碳纤维作为核,通过涂敷硅溶胶,制备表面SiC涂层[25-27],能够满足一些耐高温烧蚀的应用环境。而硅溶胶与碳纤维的反应过程尚不明确,因此本文从热力学角度对硅溶胶与碳纤维的反应阶段、反应吉布斯自由能进行了计算,归纳了SiC涂层的生长模型,对制备壳核结构SiC/C纤维提供理论依据。
1 实 验
1.1 原材料及设备
主要化学原料及试剂的各项相关信息如表1所示。

表1 原料和试剂Table 1 Raw materials and reagents
主要仪器设备的各项相关信息如表2所示。

表2 主要仪器设备Table 2 Main apparatus
1.2 SiC纤维的制备
试验流程为:首先对碳纤维进行表面处理,将碳纤维用NaOH溶液浸泡,除去表面油污,然后经硝酸酸化,超声处理,增大其表面粗糙度,并在表面形成羟基、羧基等含氧极性官能团[28]。使用乙二醇作为稀释溶液将硅溶胶稀释,得到包含不同浓度的硅溶胶的涂料溶液。将处理过的碳纤维布剪成2 cm×1 cm的小片用于涂层测试,将每片浸涂在硅溶胶涂料溶液中,随后取出,并在Ar气氛中于1 600 ℃保温30 min,硅溶胶与碳纤维发生碳热还原反应形成SiC覆盖层。对制得的产物进行SEM、拉曼等表征。
具体方法如下:在500 mL烧杯中放入少量5%(质量分数)NaOH溶液,将碳纤维试样浸入溶液5 min,然后在另一个500 mL烧杯中放入100 mL的浓硝酸(65%(质量分数)),搅拌后将碳纤维试样加入烧杯中,60 ℃超声处理1 h。之后取100 mL硅溶胶放入烧杯中,分别加入100 mL、200 mL、300 mL乙二醇稀释,用该溶液浸渍5 min处理后的碳纤维,然后在45 ℃的空气中干燥24 h。然后将干燥的样品在Ar气氛保护下以2.5 ℃/min的升温速度加热至1 600 ℃,保温30 min。
1.3 分析和测试
以集成的热力学数据库软件HSC Chemistry用于研究反应系统中可能发生的化学反应。采用德国Zeiss公司生产的场发射扫描电子显微镜对样品进行形貌分析和元素分析,仪器型号为MERLIN Compact,操作电压为20 kV。在对试样进行表面形貌观察分析前,先将样品研磨成粉末,再通过导电胶带将粉末样品粘附在MX2600FE扫描电镜所使用的铜板上,并对其进行喷金处理。另外使用该设备配备的能量色散X射线光谱仪 (EDS) 对样品进行取点在深度1 μm、X-射线作用小于300 nm的范围内表征元素组成。采用英国Renishaw in Via的Renishaw RM-1000激光显微拉曼光谱仪对材料进行分子结构的表征。将样品粉末置于显微镜载物台上,在稳定条件下进行扫描,波长为532 nm,扫描3次,光强度为10%。
2 结果与讨论
2.1 SiC生长热力学模拟计算
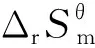
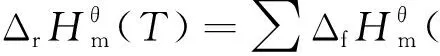
(1)
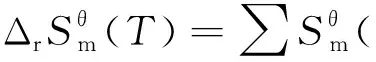
(2)
(3)
(4)
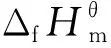
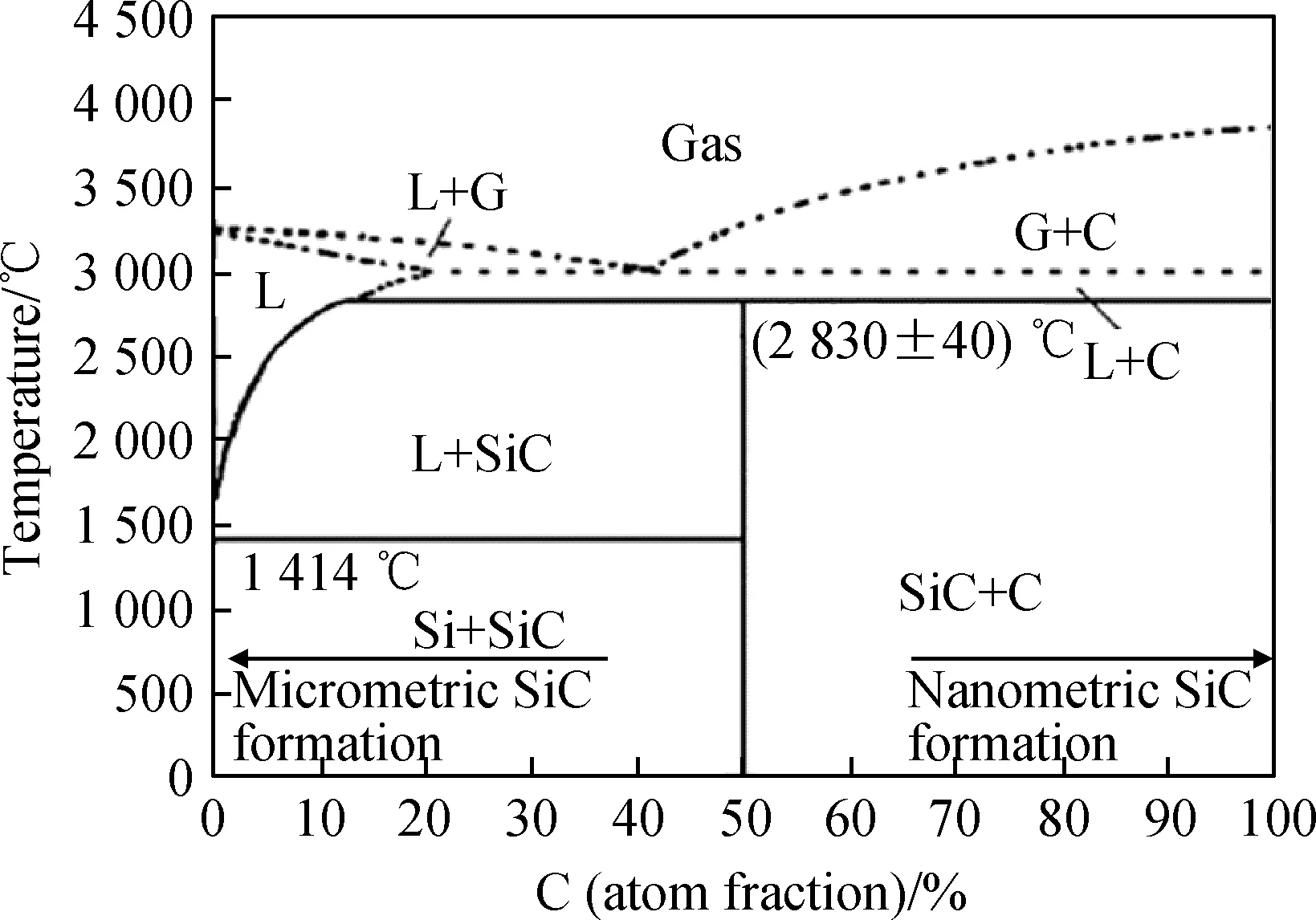
图1 Si-C相图[29]Fig.1 Si-C phase diagram[29]
对于气体摩尔数变化值∑νB(g)≠0的封闭体系产生的化学反应,反应系统压力的变化将导致化学平衡发生变化。根据热力学等温方程[30]:
(5)

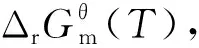
对由硅溶胶和碳纤维组成的Si-C-O反应体系进行了热力学分析。在Si-C-O系统中,通过碳热还原生成SiC包覆层的化学反应主要为C(s)和SiO2(s)形成SiC(s)并释放CO(g)的过程。在整个反应过程中不同原料之间可能发生的反应可分为产生SiO(g)的反应、产生CO(g)的反应和产生SiC(s)的反应。
表3为在Si-C-O系统中可能形成中间反应物SiO(g)的反应。

表3 生成中间反应物SiO(g)的反应Table 3 Reaction to form the intermediate reactant SiO(g)
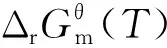
在Si-C-O系统中,反应中有可能产生中间反应产物CO(g)的部分如表4所示。

表4 生成中间反应物CO(g)的反应Table 4 Reaction to form the intermediate reactant CO(g)
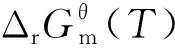
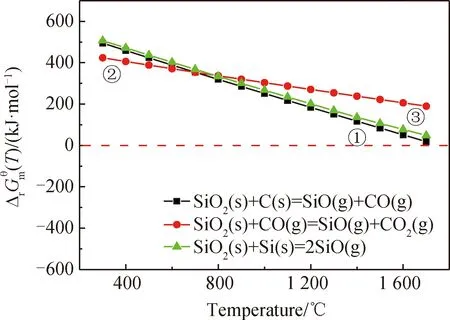
图2 标准大气压下产生SiO(g)的反应中与温度T关系Fig.2 Produced under standard atmospheric pressurethe SiO(g) of the reaction relationship with temperature T

图3 标准大气压下产生CO(g)的反应中与温度T关系Fig.3 Produced under standard atmospheric pressurethe CO(g) of the reaction relationship with temperature T
在Si-C-O系统中,可能产生SiC的反应如表5所示。

表5 可能生成SiC(s)的反应Table 5 Reactions that may produce SiC(s)
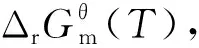
图4 标准状态下各个生成 SiC(s)反应与温度T关系图Fig.4 Standard state of each generated SiC(s) reaction and temperature T diagram
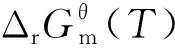
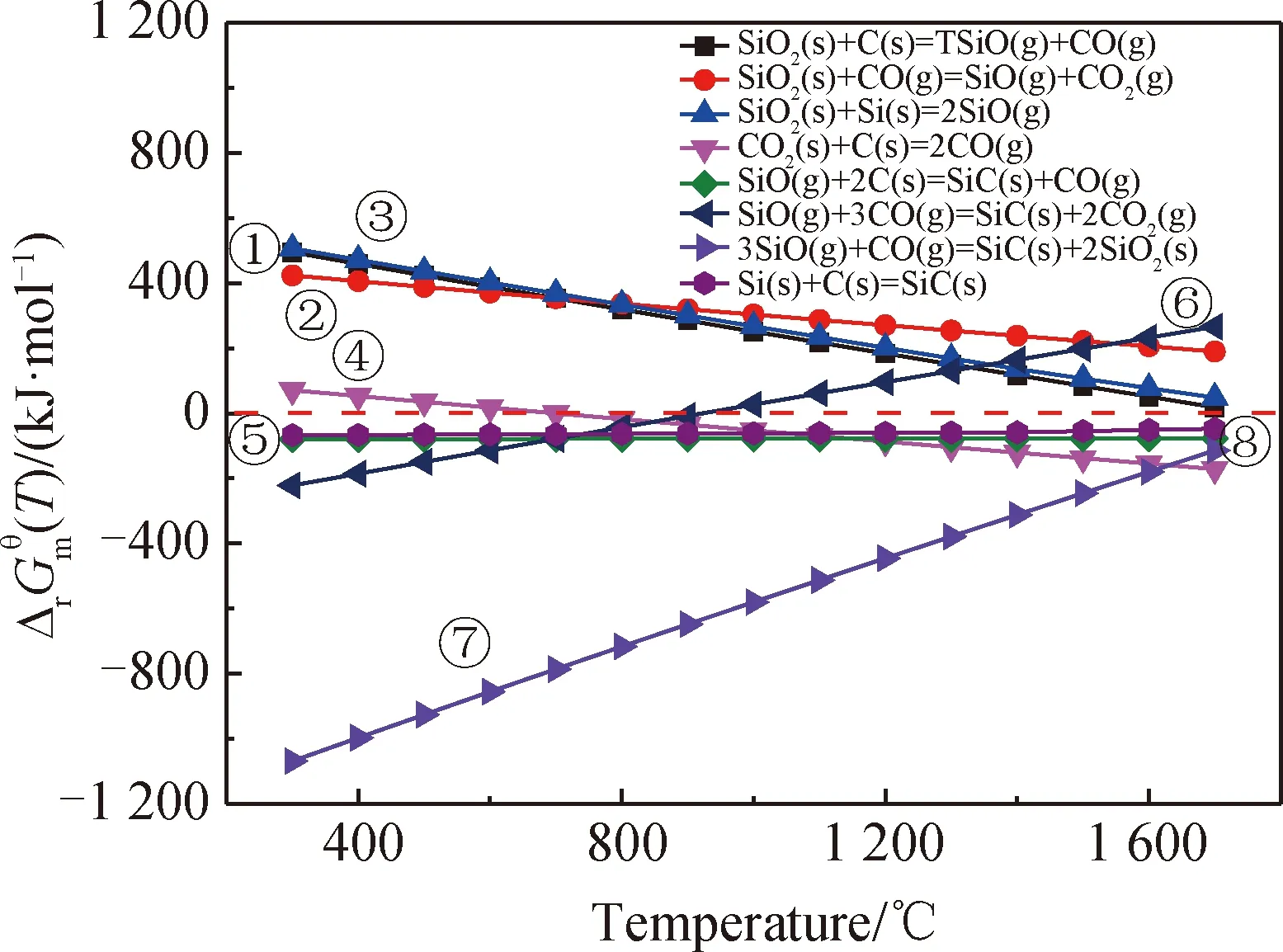
图5 标准大气压下Si-C-O体系中每个反应与温度T关系Fig.5 Si-C-O system under normal atmospheric pressure ineach reaction relationship with temperature T
根据Si-C-O反应体系中SiC包覆层生长的热力学分析,可以初步建立SiC涂层生长过程中的气-固反应生长机理。首先,产生中间反应物SiO(g)和CO(g),并产生SiC粒子,之后中间反应产物SiO(g)和CO(g)反应以实现SiC包覆层的生长。
Si-C-O反应系统的特定中间反应和生长过程可以表示为:
SiO(g)及CO(g)生成反应:
SiO2(s)+C(s)=SiO(g)+CO(g)
SiO2(s)+Si(s)=2SiO(g)
C(s)+CO2(g)=2CO(g)
SiC晶核生成反应:
SiO(g)+2C(s)=SiC(s)+CO(g)
Si(s)+C(s)=SiC(s)
SiC包覆层生长反应:
SiO(g)+3CO(g)=SiC(s)+2CO2(g)
3SiO(g)+CO(g)=SiC(s)+2SiO2(g)
根据集成的热力学数据库软件HSC Chemistry分析可能的SiC生成途径,并计算在不同温度(T)下不同反应系统中可能发生的中间反应。根据吉布斯自由能判据,计算每个反应的可能性,结论如下:
在Si-C-O反应体系中,从反应体系中的每个反应都需要相对容易发生的角度来看,中间反应物SiO(g)主要是由SiO2(s)和C(s)发生反应,而CO(g)主要形成的原因是CO(g)与C(s)的反应以及SiO(g)与C(s)的反应,同时,高温系统将朝着积极的方向促进这些反应。之后,SiO(g)与C(s)反应形成SiC核,同时继续释放CO(g),Si(s)与C(s)反应形成SiC(s)核,然后中间反应物SiO(g)与CO(g)反应产生SiC(s)以实现SiC包覆层的生长,这三个反应也都是高温系统下的正向反应。其中C(s)和CO2(g),SiO(g)和CO(g)在1 500~1 650 ℃的环境下,反应可以自发地向正反应方向进行。
2.2 结构与形貌分析
按照方案进行了m(硅溶胶) ∶m(乙二醇)=1 ∶1和1 ∶2的两组试验,并进行了SEM表征如图6所示。对1 600 ℃保温0.5 h的样品进行观察,m(硅溶胶) ∶m(乙二醇)=1 ∶1的样品均有微纳结构涂层生成。通过(图6(e)、(f))可以观察到碳纤维表面包覆一层粗糙的壳层,厚度约为2 μm,纤维直径6 μm。通过(图6(a)、(b))在坩埚边沿采集的样品明显更加杂乱,在碳纤维表面产生很多纳米线,而通过(图6(c)、(d))可以看出坩埚中心样品包覆更加均匀,由此可知,碳热还原法制备的SiC纤维包覆完整,可观察到明显分层结构,但会产生游离Si。

图6 m(硅溶胶) ∶m(乙二醇)=1 ∶1制备条件下所得SiC/C纤维的SEM形貌(a)、(b)坩埚边沿样品;(c)、(d)坩埚中心样品;(e)、(f)坩埚中心样品低倍率Fig.6 SEM morphology of SiC/C fiber obtained under the preparation condition of m(silica sol) ∶m(ethylene glycol)=1 ∶1(a), (b) crucible edge sample; (c), (d) crucible center sample; (e), (f) low multiplication rate crucible center sample
对1 600 ℃保温0.5 h的样品进行观察,m(硅溶胶) ∶m(乙二醇)=1 ∶2的样品SEM形貌如图7所示。通过(图7(a)、(b))可以观察到不管是在坩埚中心或在坩埚边沿,碳纤维表面都会包覆SiC壳层,厚度约为2 μm,并且通过(图7(c))可以看出若乙二醇过量,可能由于反应不充分产生粘结。可以看出随着硅溶胶浓度降低,仅被SiC纤维包覆的碳纤维数量明显增多,可以推测硅溶胶浓度降低可以改善包覆质量。

图7 m(硅溶胶) ∶m(乙二醇)=1 ∶2制备条件下所得SiC/C纤维的SEM形貌(a)坩埚中心所得样品;(b)、(c)坩埚边沿所得样品;(d)坩埚中心样品高倍率Fig.7 SEM morphology of SiC/C fiber obtained under the preparation condition of m(silica sol) ∶m(ethylene glycol)=1 ∶2(a) crucible edge sample; (b), (c) crucible center sample; (d) high multiplication rate crucible center sample
图8和图9分别展示了m(硅溶胶) ∶m(乙二醇)=1 ∶1与m(硅溶胶) ∶m(乙二醇)=1 ∶2烧结形成的两组SiC/C纤维的拉曼图谱。其中图8为m(硅溶胶) ∶m(乙二醇)=1 ∶1组,图9为m(硅溶胶) ∶m(乙二醇)=1 ∶2组。这两组拉曼光谱都在约1 360 cm-1和1 600 cm-1处表现出D和G特征峰[31],并且都在大约2 700 cm-1处出现2D特征峰。碳类的材料中的D特征峰源于与sp3缺陷位点相关的晶格畸变,而G特征峰则与所有sp2杂化的拉伸相关。2D特征峰可以被用来根据其相对于G特征峰的相对强度及其位置来指示(002)晶面的质量和层数。这同时也表明了SiC/C纤维确实是多层结构。从图8(a)和图9中可以看到,随着m(硅溶胶) ∶m(乙二醇)比值的增加,ID/IG峰值比变化并不大,即存在被SiC涂层包覆的碳纤维,同时2D峰一直很明显,可以看出包覆效果良好,有明显分层现象。而图8(b)显示m(硅溶胶) ∶m(乙二醇)=1 ∶1制得样品在795 cm-1左右出现特殊的峰,与碳类材料特征峰不符,推测这是由m(硅溶胶) ∶m(乙二醇)比例较高时,反应不完全,因此出现新的特征峰,出现了SiC 横向光学声子模[32]。
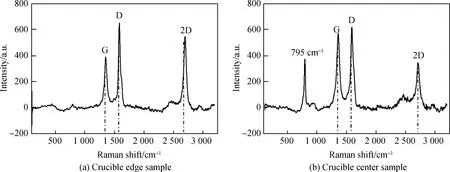
图8 m(硅溶胶) ∶m(乙二醇)=1 ∶1制得样品的拉曼图谱Fig.8 Raman spectra of m(silica sol) ∶m(ethylene glycol)=1 ∶1
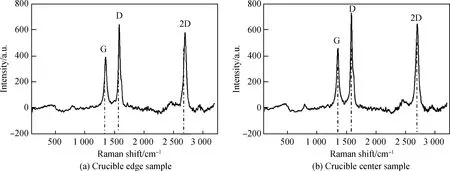
图9 m(硅溶胶) ∶m(乙二醇)=1 ∶2制得样品的拉曼图谱Fig.9 Raman spectra of m(silica sol) ∶m(ethylene glycol)=1 ∶2
2.3 SiC合成动力学理论研究及反应机理
通常认为,SiC的合成是固相反应,固相反应的驱动力来自颗粒的自扩散。对于纯固相反应,由于固体颗粒原子迁移受晶格周围原子的作用力较大,大多数固相反应都很慢。本试验中由于生成气态Si—O原子团簇,对快速生成SiC包覆层发挥着重要作用,因此SiC的生成不是纯固相反应。
就整个合成系统而言,以下反应给出了SiC包覆层生长的可能过程:
(1)反应整体是吸热反应,管式炉的热量激活Si—O蒸气的形成;
(2)C和SiO2的紧密结合控制初始反应速率;
(3)SiO、CO和Si的扩散导致SiC生长;
(4)Si(g)、SiO(g)等的形成加速了SiC包覆层的生长;
(5)SiO、C和Si反应形成SiC的共同交互作用,进一步促进SiC包覆层生长;
(6)CO逸出一定程度抑制SiC包覆层的生长。
对于在低温条件下合成β-SiC,上述步骤中CO的扩散,硅溶胶中SiO2和碳纤维的紧密结合,热能的传递以及较高温度下SiO2(g)和SiO(g)的扩散起着决定性的作用,并可以控制反应速度。在这种条件下,具有扩散的传质过程相对简单。
对于高温条件下的SiC合成,特别是在箱式炉中,尽管上述步骤中的任何环节都很重要,但材料扩散仍在整个过程中起着重要作用。在反应过程中,整个炉子受两个扩散机制控制。
在坩埚周围产生的SiO2蒸气在碳纤维表面上进行还原反应而生成SiO(g)。这两种气体在其自身的蒸气压力下径向向外扩散,并被碳纤维吸附形成SiC。在该过程中,反应产生大量的CO(g),其中一部分通过扩散逸出坩埚,然后另一部分扩散到SiO2的表面以继续还原SiO2,从而继续产生SiO。因为SiO(g)、SiO2(g)和CO(g)的扩散路径包括通过粒子间隙的扩散和通过SiC涂层的扩散。可以清晰的分析出,通过粒子间隙的扩散要比较容易。
在温度低于1 500 ℃的区域中,SiO2与碳纤维固相接触,在接触面上发生碳热反应而生成SiC。此时,主要是SiO2物质扩散到碳纤维中,在形成SiC界面层之后,扩散需要继续通过界面层。
当在坩埚内部产生大量的SiC时,炉中的扩散情况变得更加复杂。扩散功率的大小和材料的传递不仅受温度的影响,而且还受空气动力特性的影响。当坩埚内部的温度稳定在1 600 ℃左右时,伴随SiC(s)的分解和不同SiC物质(如SiC2、Si2C等)的形成。大量的硅蒸气,以及坩埚中各种气体的分压增加,从而增加了坩埚中的总气体压力。大量的各种气相扩散到外层,这提高了坩埚中的反应能力,加快了外层空间中SiC形成的反应速率,也加快了坩埚内部SiC涂层的生长速率。在保持坩埚内压力大的条件下,材料的快速扩散决定了反应速度,并在坩埚内部产生了包覆较均匀的SiC涂层,这意味着整个系统的反应和扩散机理可以表示为:SiC分解产生C+Si,硅蒸气扩散到外层。SiC晶体长大→大晶体SiC、SiC2,Si2C形成在结晶圆柱的内部,并迅速扩散到外层。在一定的温度和压力条件下,SiO(g)扩散到C颗粒的表面形成SiC涂层。无论使用哪种表面处理方法,反应产物的转移都是通过扩散穿过反应产物SiC层的厚度x来完成的。在某些条件下,SiO(g)扩散到碳纤维的表面形成SiC层。如果SiC层的厚度为x,则扩散面积为S,并且SiO在SiC层中的扩散系数为DSiO,SiC层的生长速率:
(6)
式中:k为常数,将该式积分,之后设t=0,则得:
x2=kDSiOt
(7)
即随着时间的延长, SiC涂层的生成速度越来越慢。
SiC涂层的生成作为一个十分复杂的反应过程,其反应机理的研究是十分必要的,根据SiC/C纤维SiC涂层生长的动力学机制及炉内扩散机制和热力学研究,可以基本确定,在以Ar为保护气1 600 ℃下SiC涂层的生长机理,其在碳纤维表面反应的生长机理如图10所示:
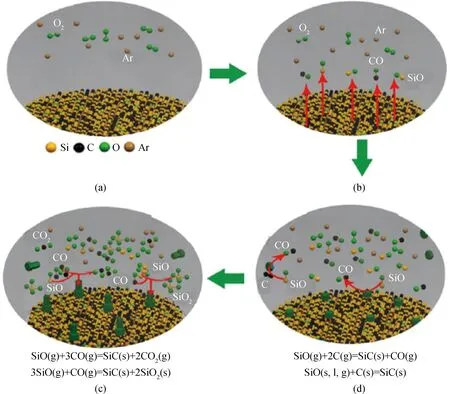
图10 碳纤维表面反应模型示意图[33]Fig.10 Diagram of surface reaction model of carbon fiber[33]
3 结 论
通过HSC Chemistry热力学软件对硅溶胶和碳纤维构成的Si-O-C系统进行了热力学分析,根据热力学数据对可能的反应过程进行了热力学数据计算。通过热力学第二定律的吉布斯自由能判据,对可能反应倾向进行了计算。结果表明,SiC包覆层的生成是由扩散控制的吸热反应,气固反应和气气反应促进了SiC包覆层的生成。通过试验发现,SiC包覆层厚度受温度影响(验证了吸热反应),最大包覆层厚度为2 μm,当硅溶胶过量时,会有自由Si出现。该理论计算对可控制备SiC/C纤维提供参考依据。
