电场辅助活性炭吸附法去除水中的Cu2+
2021-03-17高新源李爱民刘佩春宋海鸥刘玉斌战树岩南京大学环境学院江苏南京003天津万峰环保科技有限公司天津300308
高新源,李爱民,刘佩春,李 阳,宋海鸥,刘玉斌,战树岩 (.南京大学环境学院,江苏 南京 003;.天津万峰环保科技有限公司,天津 300308)
随着经济快速发展,大量工业废水产生,据统计2017 年全国废水排放量约771 亿t,其中工业废水排放量约为181.6 亿t.工业废水中尤其是电镀废水及线路板废水,包含大量重金属离子,其中的Cu2+危害极大, Cu2+不仅会影响动植物的生长发育及生理代谢[1-2],而且会毒害人类身体健康[3].国际卫生组织规定,饮用水中的Cu2+浓度需低于1.5mg/L[4].
许多先进技术应用到重金属废水处理中,如吸附法、沉淀法、还原法、膜分离法及生物处理法等[5-8].活性炭吸附法作为一种低成本高效的处理方法越来越引起研究者的重视[9-10],并被广泛应用到重金属离子处理中.Gao 等[11]采用松木锯末活性炭吸附Cu2+,得到主要以化学吸附为主,其吸附能力达到19mg/g. Wu 等[12]采用等离子体改性的活性炭吸附Cu2+,吸附能力值为22.8mg/g. Demirbas 等[13]采用榛子壳活性炭吸附 Cu2+,得到最大吸附能力为58.27mg/g,采用盐酸脱附,循环四次后,脱附率为74%~79%. Wu 等[14]采用核桃壳活性炭吸附Cu2+,最大吸附能力为32.3mg/L,循环4 次后,脱附率为80%.
综上可知,活性炭吸附重金属Cu2+过程中存在吸附效率低、脱附困难、脱附率低及活性炭再生困难等问题,限制了活性炭吸附重金属离子的应用和发展.
本文通过采用电场辅助活性炭吸附法去除水中Cu2+,改善吸附效率及脱附率,并探讨电场辅助活性炭吸附法去除Cu2+的机理以及电极的再生性,以期优化活性炭吸附重金属Cu2+过程吸附-脱附循环,并为电场辅助活性炭吸附Cu2+技术应用提供理论参考.
1 材料与方法
1.1 实验材料
本实验中选用的吸附材料为商业活性炭,粒径为0.075mm,其特征参数如表1 所示,将活性炭用去离子水清洗后在恒温烘箱内烘干,清除活性炭空隙及表面杂质.将烘干后的活性炭、聚四氟乙烯悬浮液及石墨粉按质量比8.5:1:0.5 混合,搅拌均匀,将浆体混合物涂覆在泡沫镍基体上,然后在100℃恒温烘箱内加热24h,制成活性炭电极板.其中,电极板涂覆面积为80mm×100mm,两块电极板中投加的活性炭质量为2g.

表1 活性炭的参数特征Table 1 Parameter characteristics of activated carbon
1.2 活性炭表面分析
活性炭的表面基团分别采用傅里叶变换红外光谱仪(FTIR, iS50-Thermo-fisher)和X 射线光电子能谱(XPS, PHI 5300ESCAsystem, Perkin-Elmer,美国)分析测定.
1.3 实验流程

图1 实验装置示意Fig.1 Schematic diagram of the experimental apparatus
实验装置示意图如图1 所示,两块制备的电极由聚丙烯网间隔,间隔距离为1mm,直流电源通过泡沫镍集流体为两电极提供电压.配置溶液由蠕动泵泵入两极板间,在电场牵引作用下,阴离子向正极偏转,阳离子向负极偏转,最终吸附在电极板中的活性炭材料上,从而净化出水溶液.
1.4 实验方法
本实验采用蒸馏水和CuSO4·5H2O配置Cu2+溶液,其中溶液pH 值采用0.1mol/L 的HCl 和0.1mol/L 的NaOH 调节.实验中溶液流速由蠕动泵调节控制,本实验中溶液流速选取20mL/min,CuSO4溶液取100mL,实验温度为25℃.实验过程中,每隔一定时间,记录烧杯中硫酸铜溶液的电导率.一定范围内,溶液质量浓度与电导率成正比,可以通过测定溶液电导率的变化来反映其离子质量浓度的变化,从而计算离子去除率[15].
溶液中Cu2+浓度变化采用SevenCompact S220(梅特勒-托利多)设备检测,在给定时间t 内,Cu2+吸附量qt(mg/g)计算公式如下:

式中: C0为初始Cu2+浓度, mg/L; Ct为t 时间时Cu2+浓度,mg/L;V 为溶液体积,L;W 为投加的活性炭的量,g.
2 结果与讨论
2.1 活性炭表面性质分析
图2 分别采用FTIR 及XPS 分析活性炭的表面基团,由图2(a)可知,在波数1415,1635 及3440cm-1处有明显的峰,分别对应的官能团为羧基(—COOH),羰基(—C=O)及羟基(—OH)[16-17].将活性炭中C1s和O1s 的XPS 谱图采用XPSPeak V4.1 进行分峰处理[11,18-19],如图2(b)和(c)所示,吸附材料活性炭表面的官能团同样主要以羧基,羰基及羟基为主,而羧基,羰基及羟基官能团易参与重金属的吸附过程[18-20].


图2 活性炭的红外谱图和XPS 谱图Fig.2 FTIR spectra and XPS spectra of the activated carbon
2.2 电场辅助对Cu2+去除率的影响

图3 电压对Cu2+吸附的影响Fig.3 Effect of the voltage on the adsorption of copper ions
用CuSO4·5H2O 和蒸馏水配置电导率为(1200±10)μS/cm 的溶液100mL,确定极板间距为1mm,溶液流速为20mL/min.电压分别选取0, 0.5, 1.0 和1.5V,循环吸附60min,测试溶液电导率变化.由图3 可知,随着电压升高,Cu2+去除率明显增加.电极间未施加电压时,循环吸附60min,溶液的电导率仅仅下降11.5%.当电压增加到1.0V 时,溶液的电导率下降37.2%,比未加电压组分提高了223.5%.同理,电压为1.5V时,循环吸附60min后溶液的电导率下降43.8%.电场的辅助会极大增加活性炭电极吸附Cu2+能力.
当电压增加到1.5V 时,电极表面出现小气泡,电极发生电解反应(电解水所需要的理论最小电压为1.23V),这不仅会消耗电极材料,产生二次污染物,而且增加了处理成本,同时会有Cu(OH)2产生污染活性炭电极[6].因此,辅助电压不宜过高,本研究选用的电压为1.0V.
2.3 电场作用下活性炭吸附Cu2+机理分析
活性炭吸附Cu2+中主要以化学吸附为主[12,14],之前研究[11-12]表明主要是以活性炭官能团羧基(—COOH),羰基(—C=O)等参与Cu2+吸附,具体吸附反应如下所示:

图4 为添加电压下活性炭吸附Cu2+后的FTIR分析,当活性炭吸附Cu2+后,吸附的官能团峰值会发生偏转[11-12,14].由图4 可知,在波数1415cm-1的峰,在吸附Cu2+后转移至1385cm-1附近,产生明显的偏差,证实该处对应的官能团—COOH 参与了Cu2+吸附反应,同理可知,在波数1635cm-1附近的官能团—C=O 也参与了Cu2+的吸附反应.而在0V 电压下,峰值均发生偏移,且几乎一致.因此,电场引入后,活性炭表面官能团吸附Cu2+仍存在,电场对表面基团化学吸附影响较小.

图4 添加电压后活性炭吸附Cu2+后的FTIR 分析Fig.4 FTIR Spectra of activated carbon after adsording copper ions under the voltage
电场作用下离子的迁移速率增加,定向移动增强,对电极吸附铜离子能力增强,对电极吸附Cu2+能力增强.但由图3 所示,电场作用下活性炭对Cu2+的吸附效率极大提高,当活性炭电极间施加1.0V 电压时,Cu2+的去除率提高了223.5%,已不仅仅是离子迁移速率可决定的.
采用Langmuir 和Freundlich 吸附模型来分析电场作用下活性炭吸附Cu2+过程.其模型表达式分别如下所示[21-22]:

式中: Ce为平衡浓度, mg/L; qe为平衡吸附量, mg/g;Qm最大吸附能力, mg/g; b 为吸附能.

式中: Ce为平衡浓度, mg/L; qe为平衡吸附量, mg/g; Kf为表征吸附剂吸附能力的常数; 1/n 为吸附强度常数.
分别配置Cu2+初始浓度为75,150,300, 600mg/L溶液各100mL,在电压1.0V,溶液流速为20mL/min条件下循环吸附80min,测试其平衡吸附量qe(mg/g)及平衡浓度Ce(mg/L).
图5 和表2 是采用Langmuir 和Freundlich 等温线模型对1.0V 电场辅助活性炭吸附Cu2+过程的分析.由表2 和图5 可知,Freundlich 等温线模型拟合效果优于Langmuir模型,Freundlich吸附等温线中相关系数R2达到0.997.Freundlich 等温线模型的假设是一种多层吸附,而Langmuir 等温线模型表述的材料表面吸附点位上的单层吸附模式.因此,电场辅助下活性炭对Cu2+的吸附不仅仅是单层吸附,更多的是一种多层吸附形式.
其中,活性炭表面官能团吸附反应是材料表面特定吸附点位上的单层吸附.当活性炭电极上施加电压后,处在溶液中的带电固体表面,由于静电吸引力作用,必然要吸引等电量的、与固体表面上带有相反电荷的离子环绕在固体离子的周围,便在固液两相之间形成双电层,束缚溶液中的离子[23].活性炭电极会以双电层形式吸附大量离子,双电层吸附存在紧密层和扩散层[24-25],属于多层吸附.因此,在电场辅助活性炭吸附Cu2+过程中,电场在活性炭表面产生的双电层吸附占主导作用,而一定范围内随着电压升高,双电层厚度增加[6],电吸附的Cu2+增加,如图3 所示.

图5 电场辅助活性炭吸附Cu2+的Langmuir 和Freundlich分析Fig.5 Analysis of Langmuir and Freundlich for the adsorption of copper ions on activated carbon adsorbents under an assisted electrical field
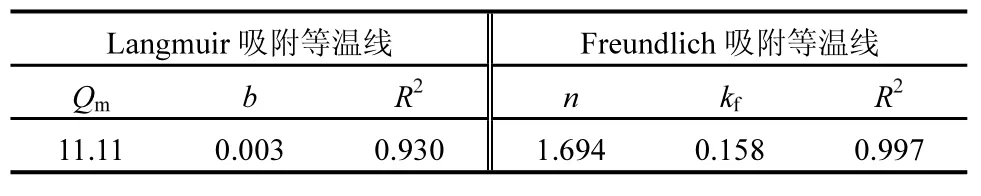
表2 电场辅助活性炭吸附Cu2+过程的Langmuir 和Freundlich 等温线模型参数及相关系数Table 2 Langmuir and Freundlich isotherm parameters and correlation coefficients for the adsorption of copper ions on activated carbon adsorbents under an assisted electrical field
2.4 pH 值对电场辅助活性炭吸附Cu2+的影响
分别在不同pH 值下(2、3、4、5、6),分析电场辅助活性炭吸附Cu2+能力,当pH 值超过6 时会出现Cu(OH)2沉淀[26],因此,溶液的pH 值最大选取为6.
如图6 所示,无论是否添加电场辅助,随着pH 值的减小,Cu2+吸附能力明显减小.电极间不施加电压时,活性炭主要以化学吸附的形式吸附Cu2+,而当pH值降低时,溶液中H+浓度升高,H+会与Cu2+竞争活性炭上的吸附点位[12],故活性炭在低pH 值下的Cu2+吸附量较小.

图6 不同pH 值下活性炭吸附Cu2+能力Fig.6 Adsorption capacity of copper ions on activated carbon at different pH values
当两电极板间施加1.0V 电压时,随着溶液中H+浓度升高,H+同样会与Cu2+竞争双电层吸附点位,H+比Cu2+在电场作用下迁移速率更快,会优先吸附到电极表面的双电层,从而降低活性炭电极对Cu2+的吸附能力.
2.5 电场辅助活性炭吸附Cu2+的脱附及电极再生分析
本文中分别采用断电脱附、短接脱附、反接脱附3 种方式进行脱附测试,如图7 所示, 断电脱附是在电吸附结束后切断电源,双电层中吸附的离子会脱落,随原水流出而形成浓水;短接脱附过程中将两电极联通,吸附在双电层离子会迅速脱落;反接脱附过程中添加1.0V 的相反电压, 吸附到双电层离子同样会迅速脱落,随原水流出而形成浓水.

图7 脱附方式示意Fig.7 Schematic Diagram of desorption modes

图8 不同脱附方式下Cu2+脱附率分析Fig.8 Analysis of desorption rate of copper ions under different desorption modes
由图8 可知,短接脱附方式比断电的脱附速率更快且脱附率更高,脱附 60min 后,脱附率达到79.1%,而断电方式的脱附率仅为55.3%.
反接脱附方式比短接的脱附速率更快,但由图8可知,脱附20min 后溶液中的电导率出现降低,反接脱附时,离子会反向再吸附到对面电极,脱附和反向再吸附同时进行,反向再吸附现象影响了活性炭的脱附效率以及活性炭电极板的再生性.因此,短接脱附方式不仅脱附率高,脱附速率快,而且运行成本低,是一种电场辅助活性炭吸附Cu2+过程中适宜的脱附方式.
由图 9 可知,活性炭吸附 Cu2+后,在波数1415cm-1的峰(—COOH, 如图2(a)所示),经过短接脱附后,对应的峰值是1389cm-1,与初始值1415cm-1的仍有较大偏差,说明短接脱附难以将表面官能团吸附的Cu2+脱附出来,同理可知,羰基(—C=O)官能团吸附的Cu2+同样未有效脱附,进而导致电场辅助活性炭吸附Cu2+的脱附率偏低.
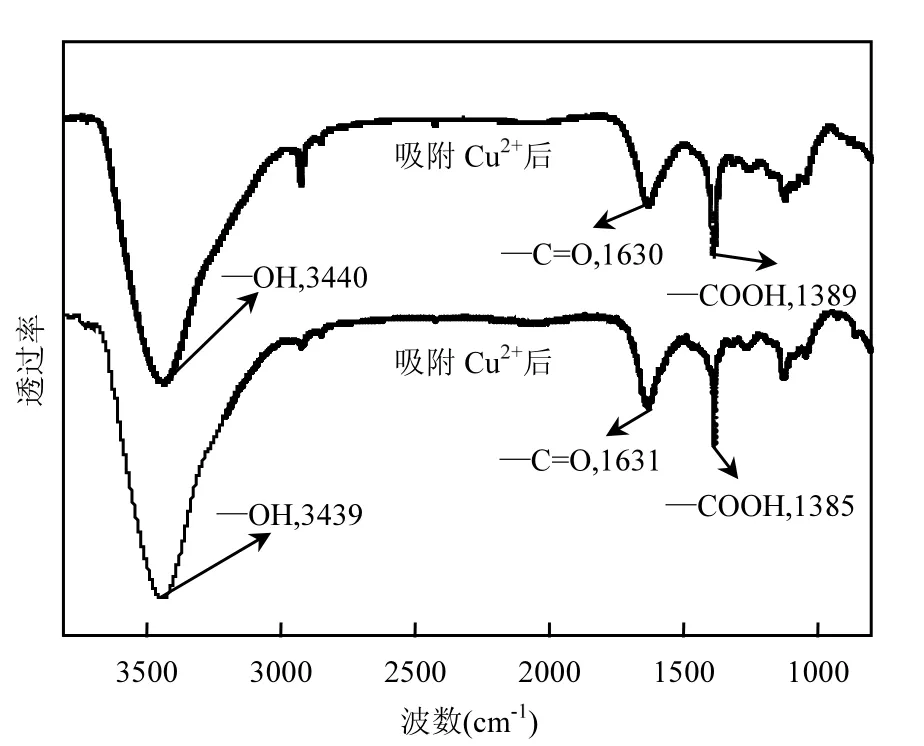
图9 活性炭吸附Cu2+和短接脱附后的FTIR 图谱Fig.9 FTIR spectra of activated carbon after adsorption of copper ions and desorption by short circuit

图10 脱附率及电极再生分析Fig.10 Analysis of the desorption rate and the electrode regeneration
采用短接脱附方式,电场辅助活性炭循环进行Cu2+的吸附-脱附过程,如图10 所示.由于表面官能团吸附的Cu2+未能有效脱附,第一次活性炭电极的脱附率仅有79.1%,进而导致第二次吸附时的Cu2+去除率仅有29.8%,明显低于第一次的吸附能力.活性炭表面化学吸附的Cu2+,其脱附再生困难,通常需要添加酸或碱辅助脱附[11-13].短接脱附方式很难将活性炭表面官能团吸附的离子有效脱附,进而导致活性炭表面吸附点位减少,Cu2+吸附能力降低.但是,第二次循环的脱附率明显高于第一次.由于活性炭表面官能团吸附Cu2+未脱附,第二次吸附主要以双电层静电吸附为主,脱附效率增高.同样,得益于表面官能团化学吸附Cu2+的减少,电场辅助活性炭吸附Cu2+,循环吸附-脱附3~4 次时,脱附率均高于第一次,电极的再生性良好.
3 结论
3.1 本文采用电场辅助活性炭吸附水中重金属Cu2+,电场辅助可以明显提高Cu2+的去除率.当电极板施加1.0V 电压时,Cu2+去除率提高了223.5%.
3.2 当添加电场辅助后,活性炭电极表面形成的双电层对Cu2+吸附占主导作用,其次是活性炭表面的官能团点位吸附.当溶液中H+浓度过高时会与Cu2+竞争吸附点位,从而降低Cu2+吸附量.
3.3 电极短接脱附方式进行Cu2+脱附,脱附率达到79.1%,但经FTIR 图谱显示,表面官能团吸附的Cu2+难以脱附出来.
3.4 由于短接脱附过程中表面官能团吸附的Cu2+极难脱附出来,循环2-4 次时Cu2+吸附主要以电吸附为主,脱附率明显提高,电极再生性改善.
