河南裕丹参中活性成分含量的测定及分析
2021-02-24杨文杰韦一言
杨文杰,韦一言,汪 雨
(成都锦欣中医医院药剂科,四川 成都 610066)
中药丹参是唇形科植物丹参(Salvia miltiorrhiza Bge.)的干燥根和根茎[1]。丹参具有活血祛瘀、通经止痛、清心除烦、凉血消痈之功效,常被临床上用于治疗心脑血管疾病[2]。目前,国内外的学者已从丹参中发现了100 多种化学成分, 且其中尚有部分有待于进一步分离、鉴定的化学成分[3]。丹参中的主要活性成分可分为两大类,一是脂溶性的丹参酮类化合物,二是水溶性的丹参酚酸类化合物(多为邻苯二羟基类化合物)[4-5]。现代医学研究表明,丹参酚酸B 具有扩张冠状动脉、改善血液循环等作用。Xu 等[6]研究表明,丹参酮Ⅰ对转基因小鼠体内肺腺肿瘤的形成具有明显的抑制作用,而隐丹参酮能抑制肿瘤细胞的增殖、转移及侵袭,进而可发挥抗肿瘤的作用[7-8]。河南裕丹参的品质优良,是“中国名牌产品”之一。研究发现,裕丹参中丹参酮类成分和丹参酚酸B 的含量远高于药典中规定的丹参中此类成分的含量[9]。本文主要是测定并分析裕丹参中活性成分的含量。
1 仪器和试剂
1.1 实验仪器
UV-2550 紫外- 可见分光光度计(由岛津企业管理有限公司制造),JBIT5374-1991 电子分析天平(由上海奥豪斯仪器有限公司制造),DJ-500J 亚太电子天平(由亚太计量仪器有限公司制造),0.22 μm 和0.45 μm 的微孔滤膜(由津腾实验设备有限公司生产),RE-52A 型旋转蒸发仪(由上海亚荣仪器厂制造),KQ-250DE 型数控超声清洗器(由昆山市超声仪器有限公司制造),JHBE-50 闪式提取器(由北京金刚科技发展有限公司制造),电热恒温水浴锅(由北京永明医疗仪器有限公司制造),200 μl 和1000μl 的移液器〔由芬兰百得实验室仪器(中国)有限公司制造〕。
1.2 实验试剂
甲醇(由天津风船化学试剂科技有限公司生产),乙醇(由新乡三伟消毒制剂有限公司生产),丹参酮ⅡA。
2 方法与结果
2.1 裕丹参总浸膏的制备
称取粉碎后的裕丹参300 g,加入10 倍量浓度为75%的乙醇浸泡1 h。采用闪式提取(简称闪提)法对药材进行提取,第一次闪提3 min,静置15 min 后进行第二次闪提(共3 min),之后用10 倍量浓度为75%的乙醇对药材进行第三次闪提(共3 min)。将三次闪提得到的滤液合在一起。用旋转蒸发仪在65℃下对滤液进行旋干浓缩,将浓缩物转移至坩埚中,在水浴锅上(温度为55℃)蒸干,得到裕丹参总膏138.4 g,得膏率为46.1%。
2.2 裕丹参中总丹参酮含量的测定
2.2.1 对照品溶液的制备 称取2 mg 的丹参酮ⅡA,用甲醇进行溶解,然后在25 ml 的容量瓶中定容至刻度线,将其摇匀后密闭、遮光保存,作为丹参酮ⅡA 对照品溶液。
2.2.2 测定波长的选择 吸取2.5 ml 的丹参酮ⅡA 对照品溶液,采用紫外- 可见分光光度法在200 ~800 nm 的波段对丹参酮ⅡA 对照品溶液进行紫外光扫描。扫描的结果见图1。通过对图1 进行分析可知,270 nm 的波长为最大吸收波长,即为检测波长。
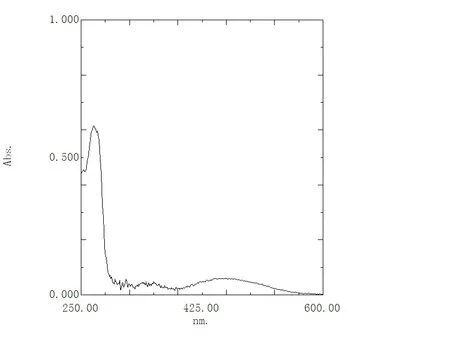
图1 丹参酮ⅡA 对照品溶液的紫外吸收光谱图
2.2.3 样品溶液的制备 称取丹参总浸膏5 mg,以甲醇为溶剂在25 ml 的容量瓶中定容至刻度线,将其摇匀后密闭、遮光保存,作为样品溶液。
2.2.4 线性关系考察 分别用25 倍、21 倍、17 倍、13 倍、9 倍和5 倍的甲醇对对照品溶液进行稀释,将其浓度稀释为1.63 μg/ml、1.94 μg/ml、2.40 μg/ml、3.14 μg/ml、4.53 μg/ml 和8.16 μg/ml。然后采用紫外- 可见分光光度法依次在270 nm 的波长下测定各对照品溶液的吸光度值。测定的结果显示,浓度为1.63 μg/ml、1.94 μg/ml、2.40 μg/ml、3.14 μg/ml、4.53 μg/ml 和8.16 μg/ml 对照品溶液对应的吸光度值分别为0.272、0.31、0.388、0.502、0.669和1.18。以丹参酮ⅡA 的浓度(C)为自变量,以吸光度值(A)为因变量绘制标准曲线,得到以下线性回归方程:A=0.1384C+0.05167,r=0.9993。
2.2.5 精密度实验 取2.4 μg/ml 的丹参酮ⅡA 对照品溶液,采用紫外- 可见分光光度法在270 nm 的波长下测定其吸光度值,共重复检测5 次。检测的结果显示,丹参酮ⅡA 对照品溶液的相对标准偏差(RSD)为0.5%。这一结果表明该检测方法的精密度良好。
2.2.6 重复性实验 按2.2.3 项下的方法将5 份裕丹参总浸膏制备成样品溶液。对样品溶液进行适当稀释,然后采用紫外-可见分光光度法在270 nm 的波长下依次测定各样品溶液的吸光度值。检测的结果显示,5 份样品溶液的吸光度值分别为0.726、0.724、0.727、0.726 和0.728,样品溶液的RSD为0.21%。这一结果表明该检测方法的重复性良好。
2.2.7 稳定性实验 取2.4 μg/ml 的样品溶液,每隔15 min采用紫外- 可见分光光度法在270 nm 的波长下检测一次样品溶液的吸光度值,共检测6 次。对样品溶液进行6 次检测的结果显示,其吸光度值分别为0.387、0.385、0.388、0.389、0.382 和0.387,样品溶液的RSD 为0.49%。这一结果表明样品溶液在90 min 内的性质稳定。
2.2.8 不同年份裕丹参中总丹参酮含量的测定结果 分别称取3 份不同年份(2018 年和2016 年)的裕丹参制备成裕丹参总浸膏,再按照2.2.3 项下的方法制备成样品溶液。对样品溶液进行适当稀释,然后采用紫外- 可见分光光度法在270 nm 的波长下依次检测各样品溶液的吸光度值。检测的结果显示,2018 年3 份裕丹参中总丹参酮的平均含量为4.79%,2016 年3 份裕丹参中总丹参酮的平均含量为4.26%。详见表1。
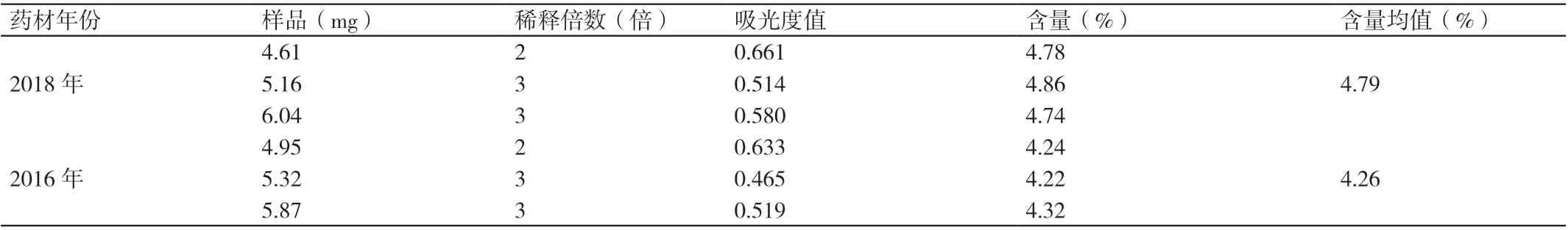
表1 不同年份裕丹参中总丹参酮含量的测定结果
2.3 裕丹参中丹参总酚酸含量的测定
2.3.1 对照品溶液的制备 称取5 mg 的丹参酚酸B 标准品,在25 ml 的容量瓶中用60% 的甲醇定容至刻度线,将其摇匀后密闭、遮光保存,作为丹参酚酸B 对照品溶液。
2.3.2 测定波长的选择 吸取2.5 ml 的丹参酚酸B 对照品溶液,对其进行适当稀释,然后采用紫外- 可见分光光度法在200 ~800 nm 的波段对丹参酚酸B 对照品溶液进行紫外光扫描。扫描的结果见图2。通过对图2 进行分析可知,286 nm 波长为最大吸收波长,即为检测波长。
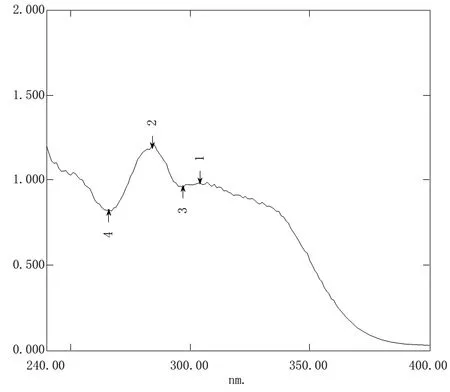
图2 丹参酚酸B 对照品溶液的紫外吸收光谱图
2.3.3 样品溶液的制备 称取丹参总浸膏5 mg,以60%的甲醇为溶剂在25 ml 的容量瓶中定容至刻度线,将其摇匀后密闭、遮光保存,作为样品溶液。
2.3.4 线性关系考察 精密量取0.1 ml、0.2 ml、0.4 ml、0.8 ml、1.6 ml 和3.2 ml 的丹参酚酸B 对照品溶液,将其分别置于10 ml 的容量瓶中,并以60% 的甲醇为溶剂分别定容至刻度线,然后采用紫外- 可见分光光度法依次在286 nm的波长下测定各丹参酚酸B 对照品溶液的吸光度值。检测的结果显示,0.1 ml、0.2 ml、0.4 ml、0.8 ml、1.6 ml 和3.2 ml 的丹参酚酸B 对照品溶液对应的吸光度值分别为0.036、0.065、0.123、0.237、0.477 和0.93。以丹参酚酸B 浓度(C)为自变量,以吸光度值(A)为因变量绘制标准曲线,得到以下线性回归方程:A=0.01445C+0.00787,r=0.9998。
2.3.5 精密度实验 取16 μg/ml 的丹参酚酸B 对照品溶液,采用紫外- 可见分光光度法在286 nm 的波长下检测其吸光度值,共重复检测5 次。检测的结果显示,丹参酚酸B 对照品溶液的RSD 为0.81%。这一结果表明该检测方法的精密度良好。
2.3.6 重复性实验 按2.2.3 项下的方法制备5 份样品溶液,对样品溶液进行适当稀释,然后采用紫外- 可见分光光度法在286 nm 的波长下依次检测各样品溶液的吸光度值。测得的结果是,5 份样品溶液的吸光度值分别为0.434、0.436、0.437、0.433、0.431 和0.550,样品溶液的RSD 为0.55%。这一结果表明该检测方法的重复性良好。
2.3.7 稳定性实验 取32 μg/ml 的样品溶液,每隔15 min采用紫外- 可见分光光度法在286 nm 的波长下检测一次样品溶液的吸光度值,共检测6 次。对样品溶液进行6 次检测的结果显示,其吸光度值分别为0.477、0.479、0.475、0.476、0.474 和0.471,样品溶液的RSD 为0.42%。这一结果表明样品溶液在90 min 内的性质稳定。
2.3.8 不同年份裕丹参中丹参总酚酸含量的测定结果 分别称取3 份不同年份(2018 年和2016 年)的裕丹参制备成裕丹参总浸膏,再按照2.2.3 项下的方法制备成样品溶液。对样品溶液进行适当稀释,然后采用紫外- 可见分光光度法在286 nm 的波长下依次检测各样品溶液的吸光度值。检测的结果显示,2018 年3 份裕丹参中丹参总酚酸的平均含量为37.9%,2016 年3 份裕丹参中丹参总酚酸的平均含量为34.7%。详见表2。

表2 不同年份裕丹参中丹参总酚酸含量的测定结果
3 讨论
2015 版《中国药典》中规定丹参中丹参酮类的总量不得低于0.25%。本研究的结果显示,2018 年3 份裕丹参中总丹参酮的平均含量为4.79%,2016 年3 份裕丹参中总丹参酮的平均含量为4.26%;2018 年3 份裕丹参中丹参总酚酸的平均含量为37.9%,2016 年3 份裕丹参中丹参总酚酸的平均含量为34.7%。由此可见,河南裕丹参中丹参酮类成分的含量远高于《中国药典》中规定的丹参中丹参酮类成分的含量。翟宏宇等[10-11]对产自河南、山东、四川、安徽、甘肃、江苏、河北、山西等地的丹参中活性成分的含量进行检测,结果显示,河南所产丹参中活性成分的含量最高。
综上所述,河南裕丹参中总丹参酮和丹参总酚酸的含量较高,其品质优良。河南裕丹参中总丹参酮和丹参总酚酸的含量会随着贮存时间的延长而减少。
