缺氧外泌体传递miR-199a-5p 对胃癌细胞SGC-7901迁移和侵袭的影响
2021-01-21沈伟锋邵平扬
周 辉,沈伟锋,邵平扬
(嘉兴市第一医院检验科,浙江 嘉兴 314001)
微小RNA(microRNA,miRNA)是一类长度为19~25 个核苷酸的单链非编码RNA,能够通过与靶基因的3′端非翻译区(3′-UTR)特异结合,促进目标mRNA 降解或抑制其翻译。miRNA 能够调节细胞中约30%的mRNA 的表达,在细胞分化、增值和凋亡等各种生物学过程中发挥重要作用[1]。研究发现[2],许多miRNA 与癌症的发生发展密切相关,在细胞内发挥了促癌或者抑癌的作用。外泌体是由细胞内吞泡膜向内凹陷形成的多泡小体与细胞膜融合后释放到细胞外的小囊泡,直径为30~150 nm,广泛存在于各种体液中[3,4]。在肿瘤微环境中,通过外泌体传递蛋白质、脂质、mRNA 和miRNA 等物质是除了分泌细胞因子、趋化因子和生长因子等可溶性介质外细胞间通讯的重要方式[5,6]。胃癌是消化系统最常见的恶性肿瘤之一,根据世界卫生组织报告[7],胃癌是全球发病率第5 高、致死率第3 高的癌症,2018 年全球新发胃癌病例超过100 万例,同时因胃癌致死病例超过78.3 万例。中国是胃癌高发国家,其发病率和致死率均仅次于肺癌[8]。淋巴结转移是胃癌最常见的转移形式,其发生率随肿瘤浸润深度的增加而提高[9]。淋巴结转移阳性胃癌患者5 年无复发生存率仅为53%[10,11]。缺氧是包括胃癌在内所有实体瘤一种普遍和持续存在的共同特征,对肿瘤的发生发展起着至关重要的作用[12]。缺氧不但能够促进胃癌细胞的增殖、侵袭和迁移能力,还会促进胃癌细胞上皮间质转化(epithelial-mesenchymal transitions,EMT)和对化疗药物耐受[13-15]。本研究通过分析缺氧诱导的SGC-7901 胃癌细胞系来源的外泌体传递miRNA 对常氧胃癌细胞的作用,揭示外泌体在缺氧微环境中对胃癌侵袭和转移的作用,现报道如下。
1 材料与方法
1.1 主要试剂和仪器 人胃腺癌细胞系SGC-7901(中国科学院上海细胞库);RPMI-1640 培养基(Hyclone);胎 牛 血 清(fetal bovineserum,FBS)(Hyclone);无外泌体培养基Exo-clearTM Complete Growth Medium(SBI);外泌体提取试剂ExoQuick-TCTM Exosome Precipitation Solution(SBI);Celltracker CM-DiI 活细胞示踪剂(上海翊圣);miR-199a-5p 类似物(miR-199a-5p mimics) 和miR-199a-5p 类似物阴性对照(miR-199a-5p mimicsNC)(委托上海吉玛生物公司合成);lipofectamine 2000(Thermo Fisher Scientific);JEM-1230 透射电子显微镜(JEOL);3311 型CO2细胞培养箱(Thermo Fisher);CKX41 光学倒置显微镜(Olympus)、NanoDrop超微量分光光度仪(Thermo Fisher)、StepOne Plus 荧光定量PCR 仪(ABI);G:BOX 系列智能荧光、化学发光成像系统(Syngene)、垂直电泳仪(BIO-Rad)。
1.2 方法
1.2.1 细胞培养和缺氧诱导 SGC-7901 细胞置于含10% FBS、100 U/ml 青霉素和100 μg/ml 链霉素的RPMI-1640 培养基中,在37℃、5%CO2的培养箱中传代培养。取对数生长期的细胞使用无外泌体培养基培养24 h 后用于后续实验。使用含200 μmol/L CoCl2的无外泌体培养基培养细胞模拟细胞缺氧,以不含CoCl2的无外泌体培养基为对照。
1.2.2 外泌体的提取 SGC-7901 细胞分别在常氧(Normoxia)和缺氧(Hypoxia)条件下培养24 h,收集细胞培养液。细胞培养液3000 g 离心15 min 去除细胞及细胞碎片。转移上清液至无菌离心管,加入上清液1/5 体积的外泌体提取液,混匀后4 ℃静置过夜。1500 g 离心30 min,弃上清;1500 g 离心5 min去除残余液体。使用PBS 缓冲液重悬外泌体,BCA法测定蛋白浓度,置于-80 ℃冰箱保存。
1.2.3 透射电子显微术分析 取10 μl 外泌体样品于蜡盘上。取铜网使有支持膜的表面与样品液表面接触,静置5 min 取出铜网,用滤纸条吸除多余的液滴,稍晾干。取3%磷钨酸溶液,滴于腊盘上。吸附有样品的铜网放置于染液表面(样品与染液接触),静置5 min。取出铜网,用滤纸条吸除多余的液滴,白炽灯下晾干。使用透射电子显微镜观察外泌体形态并拍照。
1.2.4 Western 免疫印记 使用RIPA 裂解液提取外泌体总蛋白,BCA 法测定蛋白浓度。取30 μg 提取的总蛋白,经15%十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate -polyacrylamide gel electrophoresis,SDS-PAGE)至溴酚蓝迁移至分离胶下缘后转膜。用5%脱脂牛奶室温封闭1 h,加入1∶1000 稀释的兔抗人CD9、CD63 单克隆抗体,4℃摇床上孵育过夜,加入辣根过氧化物酶标记的羊抗兔二抗(1∶10000)室温孵育1 h,ECL 化学发光试剂显色,凝胶成像分析仪中化学光敏模式曝光显影。
1.2.5 划痕实验 通过体外划痕实验检测细胞的迁移能力[16]。细胞消化后接种至6 孔板,培养24 h 至细胞铺满板底后,用200 μl 枪头垂直于孔板制造细胞划痕。吸去细胞培养液,用PBS 冲洗孔板3 次以洗去划痕产生的细胞碎片。加入无血清培养基,拍照记录。将培养板放入培养箱培养,24 h 后取出拍照,根据收集图片数据分析实验结果。划痕闭合率(%)=细胞迁移后的表面积/总表面积×100。
1.2.6 侵袭实验 使用Matrigel 包被Transwell 小室,细胞消化后使用含0.5% FBS 的RPMI-1640 培养基稀释细胞并接种于上室,下室加入400 μl 含10%FBS 的RPMI-1640 培养基。16 h 后刮去上室细胞,使用甲醛水溶液固定30 min 后结晶紫染色20 min,显微镜下拍照,使用ImageJ 软件统计迁移到膜下的细胞数。
1.2.7 miRNA 测序和生物信息学分析 正常和缺氧外泌体miRNA 文库构建、序列测定和生物信息学分析由广州吉赛生物完成。使用STAR 对读取的数据绘制基因组,miRdeep 用于计算miRNA 的表达[17]。采用TMM(trimmed mean of M-values)方法对测序片段计数矩阵进行标准化处理。用edgeR 程序鉴定差异表达基因,表达差异超过1.5 倍且P<0.05 的miRNA 认为是差异表达。
1.2.8 实时荧光定量PCR 根据miRNA miRNeasy Micro Kit 操作说明分别提取缺氧和常氧细胞外泌体RNA,并使用实时荧光逆转录定量PCR(realtime quantitative reverse transcription -polymerase chain reaction,real-time qRT-PCR)测定miR-199a-5p 的表达量,使用GAPDH 作为内参。
1.2.9 miR-199a-5p 类似物转染 使用lipofectamine 2000 把miR-199a-5pmimics 或miR-199a-5p mimicsNC 导入SGC-7901 细胞中以提高细胞内miR-199a-5p 水平,转染浓度为50 nmol/L。
1.3 统计学方法 应用SPSS 26.0 统计软件进行数据分析。计量资料以()表示,采用t检验;以P<0.05表示差异有统计学意义。
2 结果
2.1 外泌体形态观察 透射电子显微镜下显示,常氧和缺氧SGC-7901 细胞分泌的外泌体均呈圆形或椭圆形的杯状结构,直径为50~150 nm,多个视野对比外泌体形态未见明显差异,见图1。
2.2 外泌体标志物检测 常氧和缺氧SGC-7901 细胞分泌外泌体进行Western 印记分析,结果显示两组外泌体均表达CD63 和Tsg101 蛋白标志物,见图2。
2.3 缺氧肿瘤细胞来源的外泌体对常氧肿瘤细胞的迁移和侵袭的影响 划痕实验显示,缺氧处理SGC-7901 细胞分泌的外泌体共培养的常氧SGC-7901细胞划痕闭合率高于常氧SGC-7901 细胞分泌的外泌体共培养的常氧SGC-7901 细胞(P<0.05),见图3A。侵袭实验显示,缺氧处理SGC-7901 细胞分泌的外泌体共培养的常氧SGC-7901 细胞移动到transwell 小室下方的数量高于常氧SGC-7901 细胞分泌的外泌体共培养的常氧SGC-7901 细胞数量(P<0.05),见图3B。
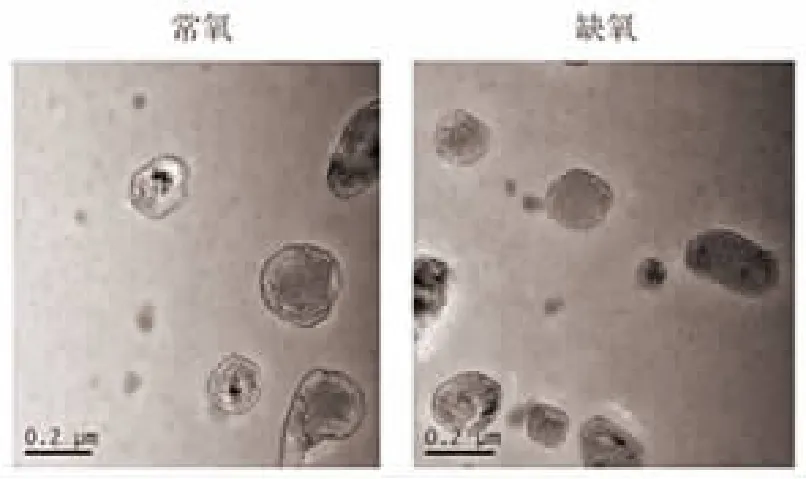
图1 常氧和缺氧条件下SGC-7901 细胞源性外泌体的电镜特点(×50000)
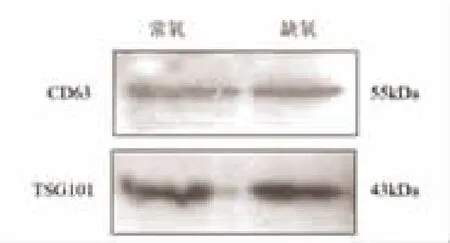
图2 常氧和缺氧SGC-7901 细胞分泌外泌体CD63和Tsg101 蛋白标志物表达情况
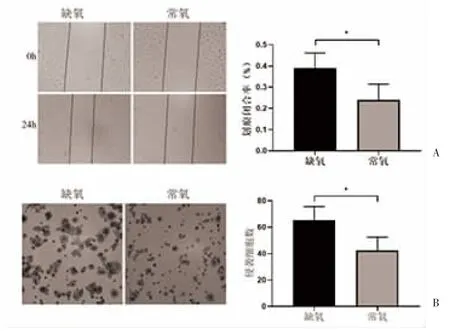
图3 缺氧肿瘤细胞来源外泌体对常氧肿瘤细胞迁移和侵袭的影响
2.4 缺氧外泌体miRNA 的表达情况 测序和RTPCR 研究显示,缺氧外泌体中miR-199a-5p 的表达高于常氧外泌体(P<0.05),见图4。
2.5 缺氧外泌体传递miR-199a-5p 对常氧胃癌细胞侵袭和转移的影响 为了分析缺氧SGC-7901 细胞源性外泌体是否通过传递miR-199a-5p 促进常氧SGC-7901 细胞侵袭和转移,将miR-199a-5p mimics 和miR-a99a-5p NC 分别导入缺氧培养的SGC-7901 细胞,提取外泌体与常氧SGC-7901 细胞共培养。划痕实验显示,导入miR-199a-5p mimics 细胞来源的外泌体共培养的常氧SGC-7901 细胞划痕闭合率高于导入miR-199a-5p mimicsNC 细胞来源的外泌体共培养的常氧SGC-7901 细胞(P<0.05),见图5A。侵袭实验显示,导入miR-199a-5p mimics 细胞来源的外泌体共培养的常氧SGC-7901 细胞移动到transwell 小室下方的数量高于导入miR-199a-5p mimicsNC 细胞来源的外泌体共培养的常氧SGC-7901 细胞(P<0.05),见图5B。
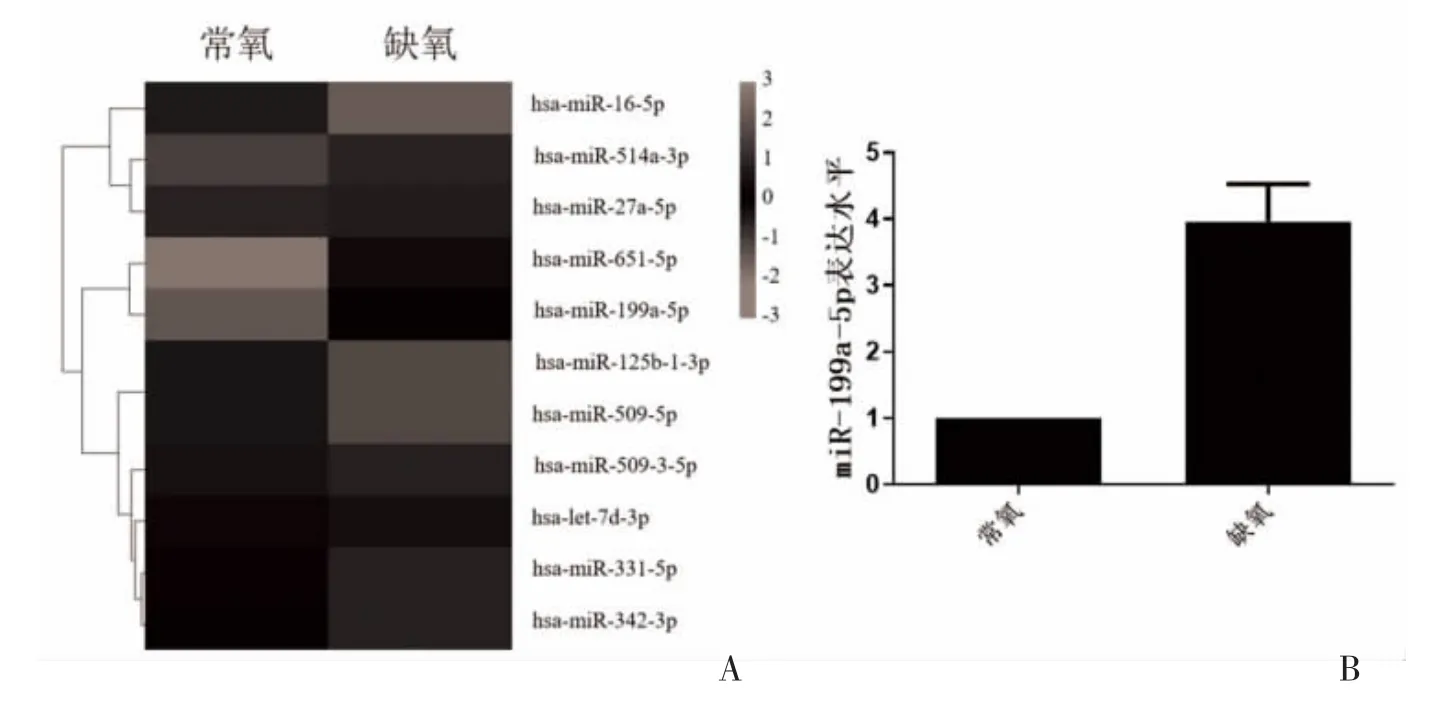
图4 缺氧外泌体miRNA 的表达情况
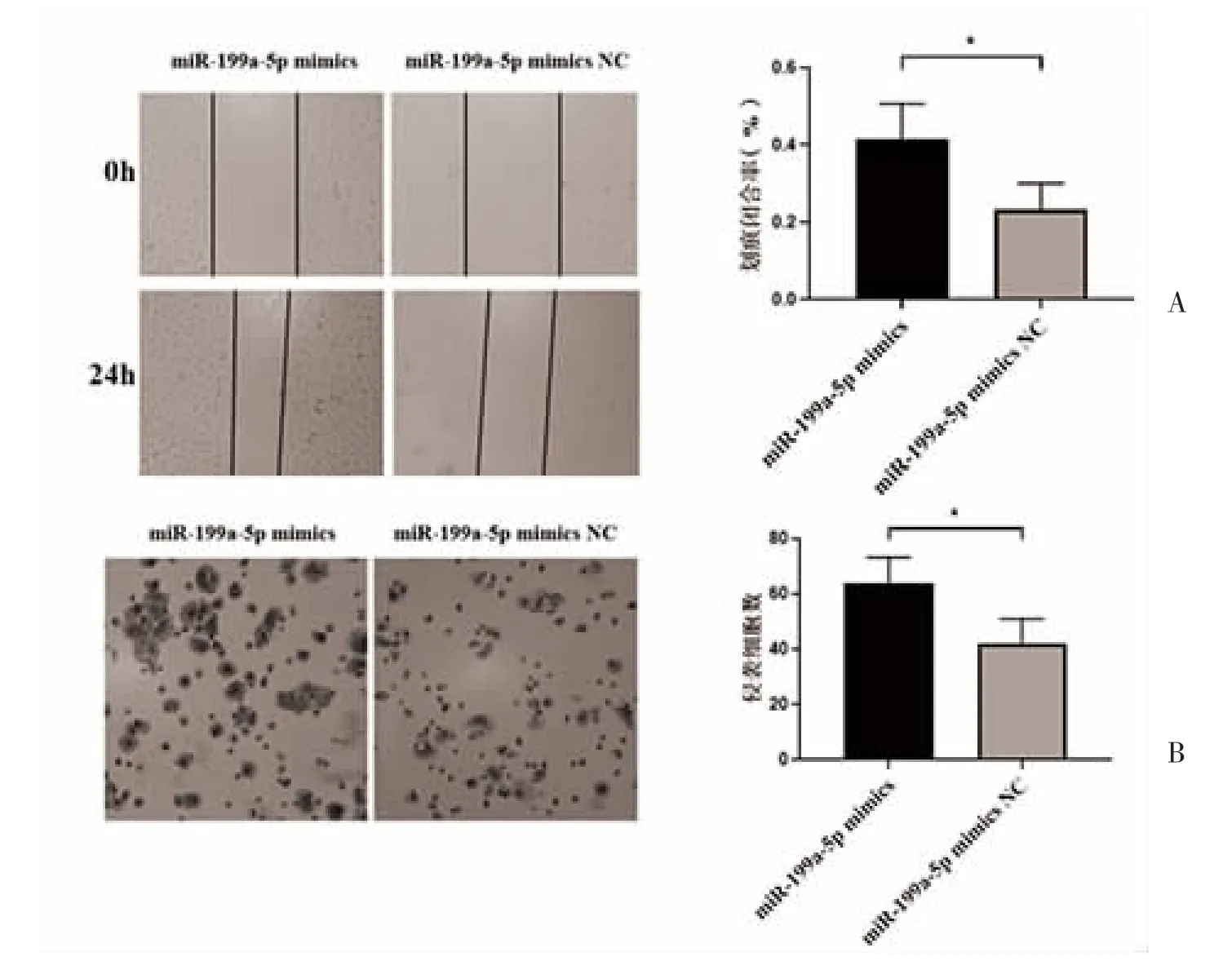
图5 缺氧肿瘤细胞来源外泌体传递miR-199a-5p 对常氧肿瘤细胞的迁移和侵袭的影响
3 讨论
外泌体由细胞分泌释放,在血液等循环系统内传播,最后可被其他细胞吞噬,是细胞间通讯的重要介质[18]。外泌体可以介导长距离细胞间通讯而无需细胞间接触,加上纳米大小的尺寸和生物相容性的特性使其成为潜在的药物载体受到临床广泛关注[19]。缺氧是由于肿瘤细胞快速增殖造成大量氧气被消耗,且肿瘤内部往往因血管生成异常等原因导致氧气供应不足,使得肿瘤细胞处于缺氧的微环境中[20,21]。多项研究发现[22-24],缺氧可通过多种方式影响肿瘤的生物学行为,如加速肿瘤的扩散和恶性进展,调控癌细胞的分化,选择性抵抗凋亡和促进化疗耐药等,特别是在肿瘤的转移过程中,从EMT 到器官亲和性转移,缺氧都起到了重要的调节作用[25]。在胃癌中,缺氧也发挥了重要的促癌作用,其不但能够促进胃癌细胞的增殖、侵袭和迁移能力,还会促进胃癌细胞EMT 和对化疗药物耐受[13-15]。
本研究使用外泌体提取试剂分别提取了常氧和缺氧SGC-7901 细胞分泌的外泌体,透射电镜结果发现,两种培养条件的细胞分泌的外泌体均呈直径为50~150 nm 圆形或椭圆形的杯状结构,表明缺氧环境没有改变SGC-7901 细胞分泌的外泌体的大小和形态。Western 印记验证了常氧和缺氧外泌体均表达已知的外泌体蛋白标志物CD63 和Tsg101。为了分析缺氧胃癌细胞分泌的外泌体在肿瘤微环境中的作用,本研究使用含CoCl2的无外泌体培养基培养SGC-7901 细胞模拟细胞缺氧,提取外泌体后与常氧SGC-7901 细胞共培养,划痕和侵袭实验显示,缺氧SGC-7901 细胞来源外泌体能够促进常氧SGC-7901 细胞迁移和侵袭。
近些年,外泌体介导miRNA 在细胞间通讯中的作用尤其受到关注,因miRNA 可以通过调控靶基因的表达调节一系列病理生理反应。研究发现[26],来自肿瘤细胞的外泌体中的miRNA 能够通过重塑肿瘤微环境来支持肿瘤的生长。Hsieh CH 等[27]研究发现,头颈部鳞状细胞癌细胞外泌体来源的miR-21 增加了肿瘤相关巨噬细胞的M2 样极化。另有研究发现[28],缺氧微环境与肿瘤细胞分泌的外泌体miRNA 变化密切相关。Wang X 等[29]研究发现,缺氧肿瘤源性miR-301a 通过调控PTEN/PI3Kγ 介导M2 巨噬细胞极化促进胰腺癌转移,且缺氧使肺癌细胞分泌外泌体中miR-103a 水平升高,从而增强肿瘤血管生成和血管通透性,最终导致肿瘤转移。然而,外泌体miRNA 改变与胃癌进展过程中缺氧之间关系的作用和机制尚未被详细揭示。本研究利用测序和RTPCR 发现,缺氧外泌体中miR-199a-5p 的表达高于常氧外泌体,为了进一步分析缺氧SGC-7901 细胞源性外泌体是否通过传递miR-199a-5p 促进常氧SGC-7901 细胞侵袭和转移,本研究将miR-199a-5p mimics 导入缺氧培养的SGC-7901 细胞,划痕和侵袭实验显示,缺氧SGC-7901 细胞来源外泌体能够传递miR-199a-5p 促进常氧SGC-7901 细胞迁移和侵袭。
综上所述,缺氧微环境可能会刺激胃癌细胞产生富含miR-199a-5p 的外泌体,并将其输送至周围常氧胃癌细胞以促进其迁移和侵袭。
