环状定点诱变技术在载体构建中的应用
2020-11-06王斌邢体坤宋路萍杨振苹荆新蕊王亚萍黄帅张静静
王斌 邢体坤 宋路萍 杨振苹 荆新蕊 王亚萍 黄帅 张静静


[摘要]目的 探讨环状定点诱变技术在目标质粒单碱基突变,酶切位点修改和片段删除中的应用。方法 设计包含目标突变,部分互补且5端含有5~8 bp突出的引物对,环状质粒作为模板进行扩增,甲基化酶DpnI酶消化去除模板质粒。转化DH5α感受态进行缺口修复,获得定点突变的目标质粒。结果 通过酶切和基因测序证明,环状定点诱变技术可高效用于单碱基突变、酶切位点修改和片段删除等突变。结论 环状定点诱变技术能够简便、高效、快捷地实现目标质粒的单碱基突变、酶切位点修改和片段删除,基本满足药物开发过程中载体构建的需求。
[关键词]环状定点诱变;片段删除;酶切位点;PCR扩增
[中图分类号] R450 [文献标识码] A [文章编号] 1674-4721(2020)9(b)-0032-04
Application of circular site-directed mutagenesis in vector construction
WANG Bin1 XING Ti-kun2 SONG Lu-ping2 YANG Zhen-ping2 JING Xin-rui2 WANG Ya-ping2 HUANG Shuai2 ZHANG Jing-jing2
1. Department of Quality Control, HUALAN Genetic Engineering Co., Ltd., He′nan Province, Xinxiang 453000, China; 2. Department of Recombinant Cell, HUALAN Genetic Engineering Co., Ltd., He′nan Province, Xinxiang 453000, China
[Abstract] Objective To explore the application of circular site-directed mutagenesis technology in single base mutation, restriction site modification and fragment deletion of the target plasmid. Methods The primer pairs were designed including target mutation, partial complementation, and 5 end contains 5-8 bp protruding. The circular plasmid was used as template for amplification and digested and removed by methylase enzyme DpnI. Transform DH5α for gap repair then site-directed mutation plasmid was obtained. Results Through the validation by enzyme cutting and gene sequencing, circular site-directed mutagenesis technology could be efficiently used in single base mutation, modification of enzyme site and deletion of fragment. Conclusion The circular site-directed mutagenesis technology is simple, efficient and quick to realize single base mutation, restriction site modification and fragment deletion of the target plasmid, which can basically meet the needs of molecular construction in the process of drug development.
[Key words] Circular site-directed mutagenesis technology; Fragment deletion; Restriction enzyme cutting site; PCR amplification
定點诱变是体外特异性地取代、插入或缺失DNA序列任何一个特定碱基的技术[1]。近几年来定点诱变技术发展迅速,不仅用于基因和蛋白功能的基础研究,还用于反向遗传学改造,主要方法包括重叠PCR法、长引物PCR法、环状定点诱变技术和酶介导的诱变等技术[2-7]。重叠PCR法、长引物PCR法和酶介导的诱变技术操作复杂,费事费力;环状定点诱变技术操作简单,诱变效率高,倍受广大研究者青睐[5-7]。该技术利用PCR扩增引入目标突变,经甲基化酶DpnI消化原始质粒,宿主内进行修复和环化,高效产生目标质粒[6-7]。药物开发为提高药物的生物学活性、半衰期、特异性和安全性,对药物分子进行定向改造不可避免[8-10]。环状定点诱变技术在单碱基突变中的应用广泛,本研究探讨该技术在酶切位点插入、替换和删除基因片段等突变类型中的应用,为生物药物研发过程中的载体构建提供方法学基础。近几年来,随着基因编辑和基因疗法的兴起[11-12],环状定点诱变技术在前期核酸改造中也发挥着不可或缺的作用。本研究旨在探讨环状定点诱变技术在目标质粒单碱基突变,酶切位点修改和片段删除中的应用,现报道如下。
1材料与方法
1.1供试品
pUC57-7NB2AA质粒(金斯瑞生物科技有限公司;订单编号:C8100EI120);pET26b-7NB2AA(华兰生物自我构建保存原核表达质粒)。
1.2材料
B528413型DH5α大肠感受态和A505255型琼脂粉(生工生物工程股份有限公司);LP0042型蛋白胨(赛默飞世尔科技公司);212750型酵母粉(Becton Dickinson公司);1161B型NdeI、1010B型BamHI、1160B型NcoI、1094A型Xho I和1235A型DpnI内切酶(宝日医生物技术有限公司);AP211型EasyPfu DNA Polymerase(北京全式金生物技术有限公司);K0502型Gene JET Plasmid Miniprep Kit(赛默飞世尔科技公司)。
1.3仪器设备
HYG-A型全恒温摇瓶柜(太仓实验设备厂);1-15PK型台式离心机(赛多利斯公司);SW-CJ-2FD型洁净工作台(苏州安泰空气技术有限公司);S100型PCR反应扩增仪(BIO-RAD公司);WD-9403C型紫外仪、DYY-10C型电泳仪和DYCP-31DN型电泳槽(北京六一生物科技有限公司);Alpha Imager HP型凝胶成像系统(Protein Simple公司);Nano Drop ONE型微量分光光度计(赛默飞世尔科技公司)。
1.4定点诱变实验流程
1.4.1引物设计原则
引物包含预期突变序列且位于互补区域中间,突变两侧至少10 bp,引物5端含有5~8 bp突出碱基(图1)。
1.4.2定点诱变
以环状质粒作为模板PCR扩增,甲基化酶DpnI酶消化1 h,取消化产物5 μl转化DH5α感受态,涂板过夜培养,挑单克隆培养、提取质粒、鉴定目标克隆。
1.4.2.1 PCR扩增 按照拟突变质粒1 μl,引物F(10 μM)1 μl,引物R(10 μM)1 μl,dNTP(2.5 mM)4 μl,Easypfu Buffer 5 μl,Easypfu Buffer 1 μl,补水至50 μl的反应体系;94℃预变性4 min,94℃变性30 s,(Tm-5)℃退火30 s,72℃延伸(扩增长度/500)10 min,4℃最后保温反应条件进行PCR扩增30个循环。扩增产物经DpnI消化后即可用于转化。
1.4.2.2 DpnI消化原始质粒 扩增PCR产物需要经过DpnI甲基化酶去除拟突变质粒,反应体系为DpnI 1 μl,T Buffer 5 μl,PCR反应产物5 μl,补水至50 μl;反应条件为37℃孵育1 h。甲基化酶消化原始质粒后,取5 μl反应体系,转化DH5α即可完成克隆构建,待鉴定。
1.5酶切鑒定
按照Gene JET Plasmid Miniprep Kit试剂盒说明书提取质粒。内切酶A 0.25 μl,内切酶B 0.25 μl,双酶切缓冲液1 μl,待鉴定质粒1 μl定反应体系,37℃酶切1 h进行酶切鉴定。点样5 μl酶切反应体系进行核酸电泳鉴定,判断克隆是否为阳性。阳性克隆送样测序验证定点诱变实验结果。
2结果
2.1单碱基突变
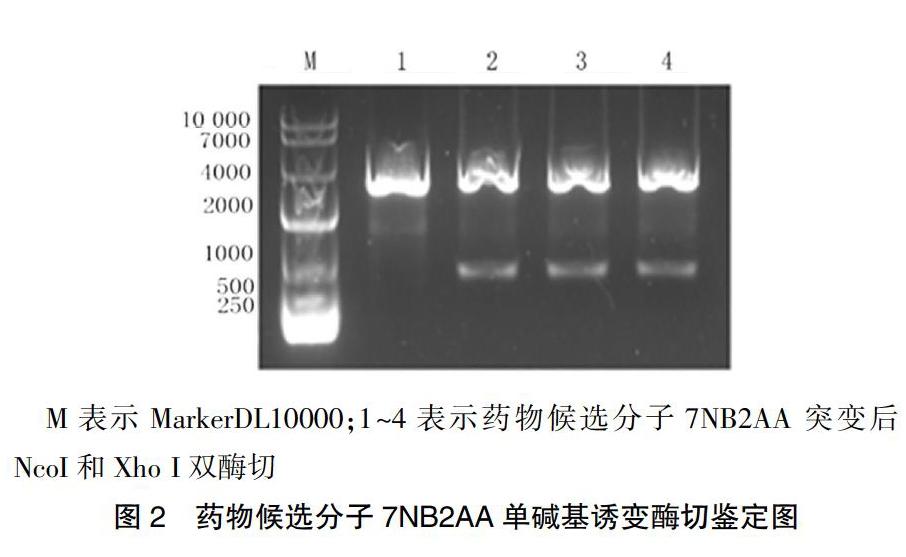
为了提高7NB2AA药物候选分子与其配体之间的亲和力,利用分子模拟软件Discovery Studio建模分析。模型显示7NB2AA分子A102为关键位点,需要进行A102V(GCT→GTT)单氨基酸突变。设计引物7NB2AA-F:AAACAGGCAAGATTGTTGACTAC AACT,7NB2AA-R:GTTTGTAGTTGTAGTCAACAATC TTG(方框标记代表拟突变位点)。金斯瑞合成pUC57-7NB2AA质粒为模板扩增目的序列,DpnI消化去除原始质粒,转化DH5α,提取质粒,酶切鉴定、测序分析。结果显示,酶切鉴定4个克隆中,其中3个为阳性克隆,送样测序鉴定,序列和预期结果一致(图2、图3,封四)。环状定点诱变技术进行基因单碱基定点突变高效可行。
M表示MarkerDL10000;1~4表示药物候选分子7NB2AA 突变后NcoI和Xho I双酶切
2.2酶切位点修改
信号肽后前6个氨基酸决定信号肽酶切割效率,对周质空间分泌表达至关重要[13]。为了优化药物候选分子7NB2AA周质空间表达,对信号肽后酶切位点进行改造。原始载体pUC57-7NB2AA的PelB信号肽后为NcoI酶切位点,编码MG两个冗余氨基酸残基,+1蛋氨酸侧链较大,不利于周质空间表达。利用环状定点诱变技术对其进行改造,删除NcoI酶切位点和修改为BamHI小侧链氨基酸(GS)。使用表1引物,pUC57-7NB2AA质粒为模板扩增目的序列,DpnI消化去除原始质粒,转化DH5α,提取质粒,酶切鉴定、测序。结果显示,挑选克隆均为阳性,测序序列与预期一致,环状定点诱变技术高效可行(图4、图5,封四)。酶切位点修改在载体改造和表达量优化中使用频繁。本研究通过环状定点诱变技术可以高效、快速实现酶切位点删除和替换。
2.3片段删除
载体构建中片段删除是分子生物学的常规操作。以7NB2AA蛋白表达质粒为例,环状定点诱变技术将其PleB信号肽去除,改为胞内表达质粒。设计引物7NB2AA-sig-F:AAGAAGGAGATATACATATGCAGGT GCAACTGCAG,7NB2AA-sig-R:CTTTCCTGCAGTTG CACCTGCATATGTATATCTCC。pET26b-7NB2AA质粒为模板扩增目的序列,DpnI消化切除原始质粒,转化DH5α,提取质粒,酶切鉴定、测序鉴定。结果显示,酶切鉴定有阳性克隆,送样测序鉴定显示PelB信号肽成功删除(图6、图7,封四)。本研究证明环状定点诱变技术删除基因片段可行。
3讨论
环状定点突变技术多用于单碱基突变,酶切位点修改和片段删除报道较少。本研究扩展了该技术在生物医药领域的应用范围:①抗体药物Fc结构N297A,L235E和 M428L/N434S等突变改善抗体依赖细胞介导的细胞毒作用(ADCC)[14];②去除药物研发筛选技术(单B细胞筛选技术[15])的冗余酶切位点,加快药物研发进程;③去除药物开发早期目标蛋白携带的His6、HA或GFP等标签[16],促进药物研发早期活性评价。本研究环状定点诱变技术删除的PelB信号肽长度仅为63 bp,理论可以实现更长片段的删除(笔者在XTEN融合蛋白技术研究中成功删除1728 bp的片段);此外,技术可以实现连续1~6个碱基的任意突变,理论可以实现更长碱基对发突变(限制因素为引物合成长度),下一步研究拟证明该技術的最长突变极限。
本研究验证了环状定点突变技术在单碱基突变中应用的可行性。此外,本研究证明该技术可进行质粒的酶切位点删除、替换和基因片段删除等突变。环状定点突变技术高效改造蛋白药物关键氨基酸,去除的冗余酶切位点和蛋白药物的冗余标签,在生物药研发中备受青睐。
[参考文献]
[1]王秋颖.基因体外定点诱变技术[J].山西农业大学学报,2007,27(6):124-126.
[2]Dong M,Wang F,Li Q,et al.A single digestion,single-stranded oligonucleotide mediated PCR-independent site-directed mutagenesis method[J].Appl Microbiol Biotechnol,2020,104(9):3993-4003.
[3]Forloni M,Liu A,Wajapeyee N.Altered beta-Lactamase Selection Approach for Site-Directed Mutagenesis[J].Cold Spring Harb Protoc,2018,2018(8):670-676.
[4]Xia Y,Li K,Li J,et al.T5 exonuclease-dependent assembly offers a low-cost method for efficient cloning and site-directed mutagenesis[J].Nucleic Acids Res,2019,47(3):1-11.
[5]曹阳,李冬田,尹冰楠,等.重叠延伸PCR方法的建立与应用[J].河北医药,2005,27(11):803-804.
[6]刘玉冰,李晓霞,王宝利,等.一步PCR法在单碱基定点诱变中的应用[J].天津医科大学学报,2007,13(1):98-99.
[7]周亚芹,张洪梅,董艳,等.环状定点诱变技术在单碱基定点诱变中的应用[J].现代医学,2009,37(5):321-324.
[8]Crisci S,Amitrano F,Saggese M,et al.Overview of Current Targeted Anti-Cancer Drugs for Therapy in Onco-Hematology[J].Medicina(Kaunas),2019,55(8):414.
[9]Qu G,Li A,Acevedo-Rocha CG,et al.The Crucial Role of Methodology Development in Directed Evolution of Selective Enzymes[J].Angew Chem Int Ed Engl,2020,59(32):13 204-13 231.
[10]Sayous V,Lubrano P,Li Y,et al.Unbiased libraries in protein directed evolution[J].Biochim Biophys Acta Proteins Proteom,2020,1868(2):140 321.
[11]She W,Ni J,Shui K,et al.Rapid and Error-Free Site-Directed Mutagenesis by a PCR-Free In Vitro CRISPR/Cas9-Mediated Mutagenic System[J].ACS Synth Biol,2018,7(9):2236-2244.
[12]Kanazashi Y,Hirose A,Takahashi I,et al.Simultaneous site-directed mutagenesis of duplicated loci in soybean using a single guide RNA[J].Plant Cell Rep,2018,37(3):553-563.
[13]Watanabe K,Tsuchida Y,Okibe N,et al.Scanning the Corynebacterium glutamicum R genome for high-efficiency secretion signal sequences[J].Microbiology,2009,155(Pt 3):741-750.
[14]Wang X,Mathieu M,Brezski RJ.IgG Fc engineering to modulate antibody effector functions[J].Protein Cell,2018,9(1):63-73.
[15]Wardemann H,Busse CE.Expression Cloning of Antibodies from Single Human B Cells[J].Methods Mol Biol,2019,1956:105-125.
[16]Strain-Damerell C,Burgess-Brown N.High-Throughput Site-Directed Mutagenesis[J].Methods Mol Biol,2019,2025:281-296.
(收稿日期:2020-05-19)
