结直肠癌根治术后并发静脉血栓栓塞的相关危险因素分析*
2020-10-28李舸宋博李杰王久惠肖红英
李舸,宋博,李杰,王久惠,肖红英
610041 成都,四川省肿瘤医院·研究所,四川省癌症防治中心,电子科技大学医学院 急诊综合科(李舸、王久惠、肖红英),胃肠外科中心(宋博、李杰)
静脉血栓栓塞(venous thromboembolism,VTE)主要包括深静脉血栓(deep vein thrombosis,DVT)形成和肺血栓栓塞(pulmonary thromboembolism,PTE),是临床常见病之一。VTE易引起心源性休克等严重并发症导致患者死亡,故临床上该疾病的一级预防极其重要。研究显示,外科手术是VTE发生的独立危险因素,与其他腹部外科手术相比,结直肠手术因特殊体位、手术时间长等原因使患者术后更容易发生VTE,尤其以结直肠癌(colorectal cancer,CRC)根治术后更为多见[1-4],曾报道其发生率高达37%~46%[5]。CRC根治术后患者并发VTE不仅降低了手术疗效、加重了术后痛苦、延长了住院时间、增加了治疗费用,同时可能严重威胁患者的生命[6],故临床上应重点加强对CRC根治术后并发VTE的预防。随着外科技术的更新发展和医疗器械的成熟应用,目前国内外多依靠腹腔镜技术行根治性CRC切除手术,故本文选取四川省肿瘤医院2017年1月至2018年12月期间进行腹腔镜下CRC根治术的患者为研究对象,分析术后并发VTE的相关危险因素,以期为腹腔镜下CRC术后VTE的预防和诊治提供参考依据。
1 资料与方法
1.1 研究设计
选取2017年1月至2018年12月在四川省肿瘤医院胃肠外科一病区行腹腔镜下CRC根治术治疗的214例患者为研究对象,收集患者静脉血栓的相关临床资料进行回顾性分析。所有手术均由同一位医师主刀,且所有资料均根据患者住院病历电脑记录所得。入组患者术后均未预防性抗凝治疗,术后第2 d指导患者翻身、下床活动、锻炼肺功能,术后不常规进行凝血功能检测及血管超声检查。
1.2 纳入和排除标准
1.2.1纳入标准 1)术前病理诊断为结肠癌或直肠癌,并行腹腔镜下CRC根治术的患者;2)术前凝血功能及肝功能正常;3)术前未预防性抗凝治疗;4)临床资料保存完善。
1.2.2排除标准 1)术前病理为结直肠良性肿瘤患者;2)长期使用影响凝血功能药物患者;3)合并其他恶性肿瘤患者;4)术前证实已存在DVT患者;5)临床资料欠缺者。
1.3 VTE诊断方法
除临床可见VTE相关的症状和体征(DVT出现疼痛、肢体肿胀、皮温增高、活动受限等;PTE出现原因不明的气促、胸痛、心动过速、情绪不安、呼吸急促甚至晕厥、血氧饱和度下降等)外,患者实验室检查(全血细胞计数、血小板计数、凝血酶原时间、活化部分凝血活酶时间、血肌酐等)可能出现异常,所有患者需经彩色多普勒超声或深静脉造影提示血管存在局部充盈缺损或完全堵塞。PTE需靠CT或肺泡灌注扫描明确诊断。
1.4 观察指标
查阅患者的病例资料,根据患者术后2周内是否发生VTE,分为VTE组16例和非VTE组198例,回顾性分析患者的临床资料,主要收集指标有:年龄(≥60岁或<60岁)、性别、是否吸烟、是否嗜酒、BMI≥25 kg/m2或<25 kg/m2、既往VTE病史(有或无)、伴随疾病(有或无)、是否术前化疗、是否术前放疗;手术时间(≥3 h或<3 h)、术中出血(≥100 mL或<100 mL)、输血(是或否)、肿瘤部位(直肠或结肠)、术后美国癌症联合会(American Joint Committee on Cancer,AJCC)分期(0~II期或III~IV期);感染(是或否)、术后制动时间(≥2 d或<2 d)、静脉穿刺次数(≥5次或<5次)。
1.5 统计学方法
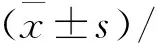
2 结 果
2.1 CRC患者术后并发VTE的单因素分析
两组患者男性114例,女性100例;年龄27~86岁,平均(55.38±12.07)岁。经单因素分析,非VTE组和VTE组患者在年龄、既往VTE病史、2型糖尿病、心血管疾病、高脂血症、手术时间、感染、术后制动时间、静脉穿刺次数上差异有统计学意义(P<0.05);而两组患者在性别、是否吸烟、是否嗜酒、BMI、是否合并呼吸系统疾病、术前化疗、术前放疗、AJCC分期、肿瘤部位、术中出血、是否输血上差异无统计学意义(表1、2)。
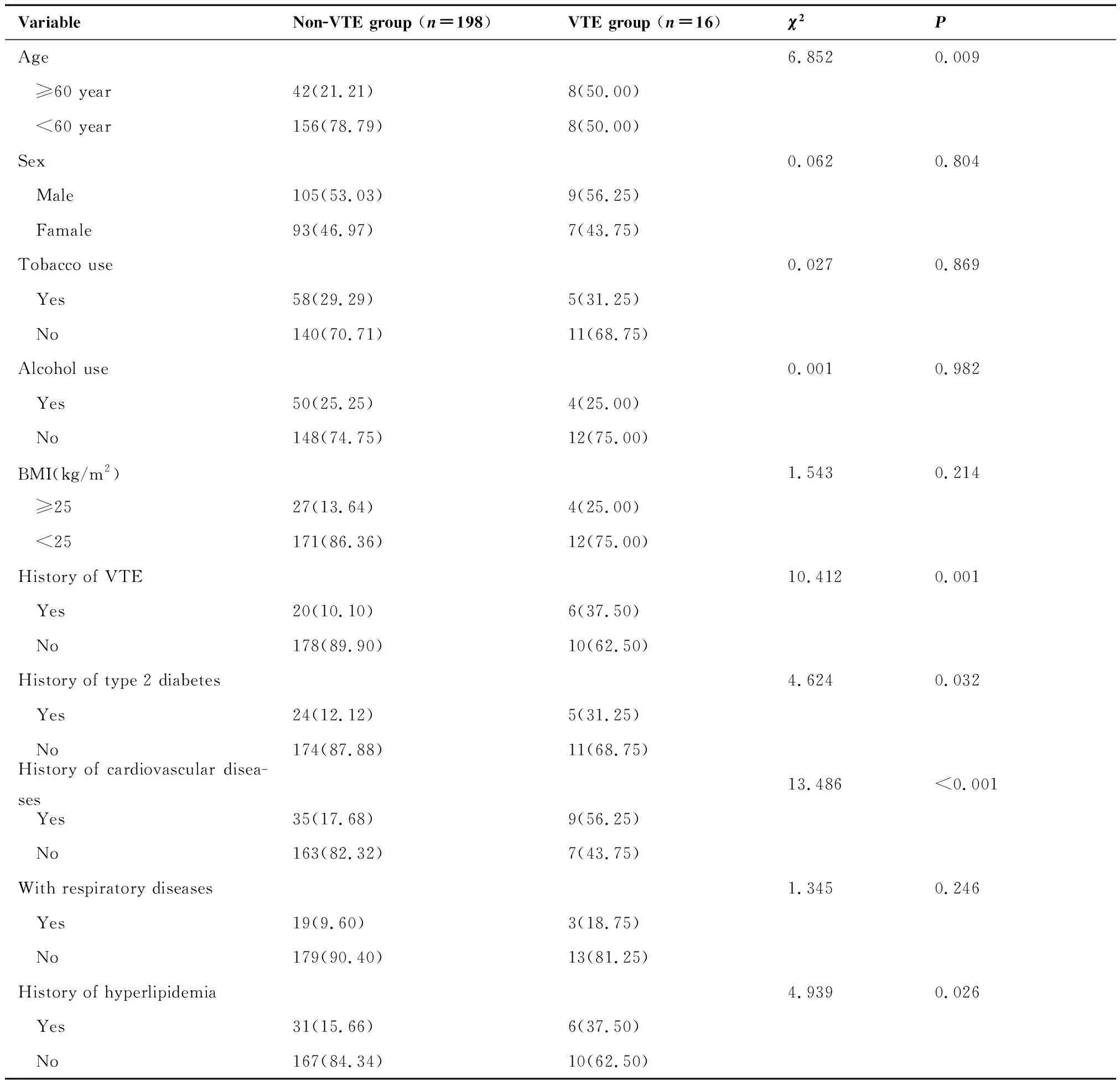
表1 非VTE组和VTE组患者临床特点对比
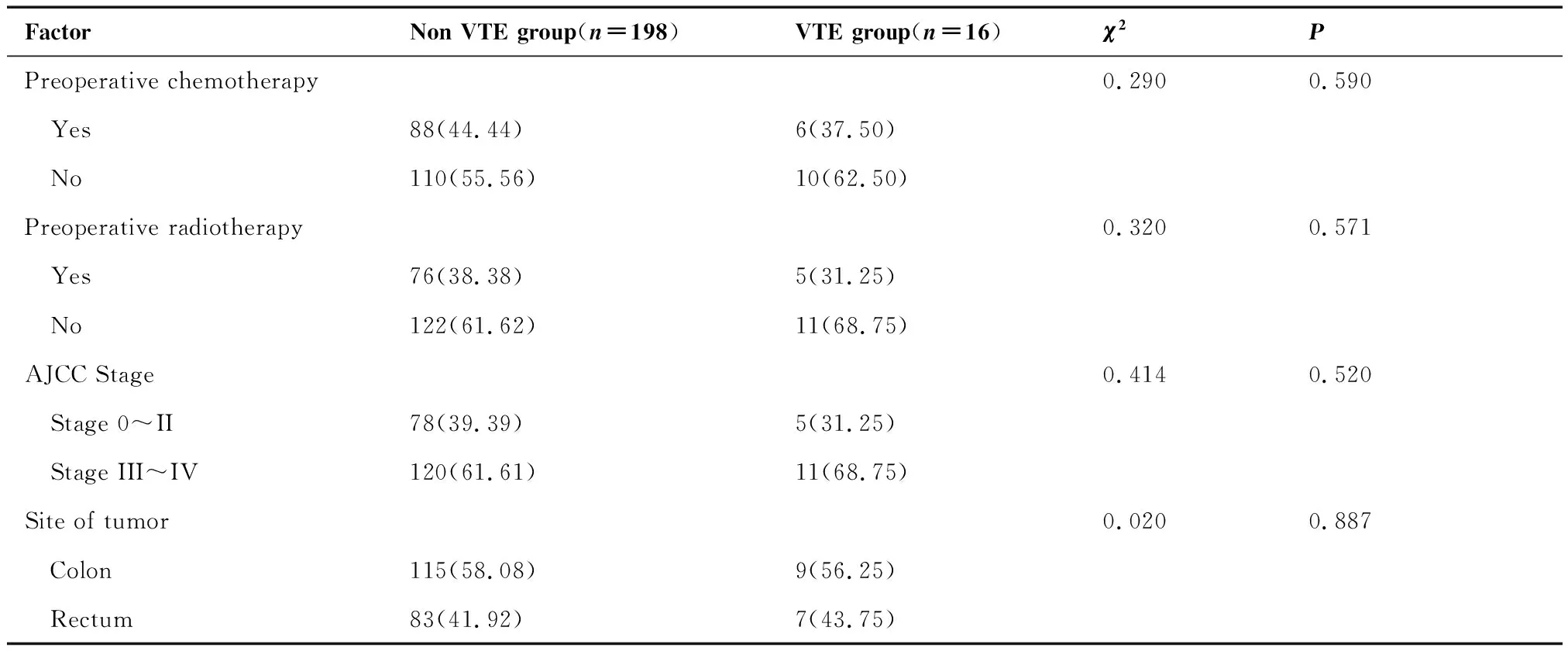
FactorNon VTE group(n=198)VTE group(n=16)χ2PPreoperative chemotherapy0.2900.590 Yes88(44.44)6(37.50) No110(55.56)10(62.50)Preoperative radiotherapy0.3200.571 Yes76(38.38)5(31.25) No122(61.62) 11(68.75)AJCC Stage0.4140.520 Stage 0~II78(39.39)5(31.25) Stage III~IV120(61.61) 11(68.75)Site of tumor0.0200.887 Colon115(58.08)9(56.25) Rectum83(41.92)7(43.75)
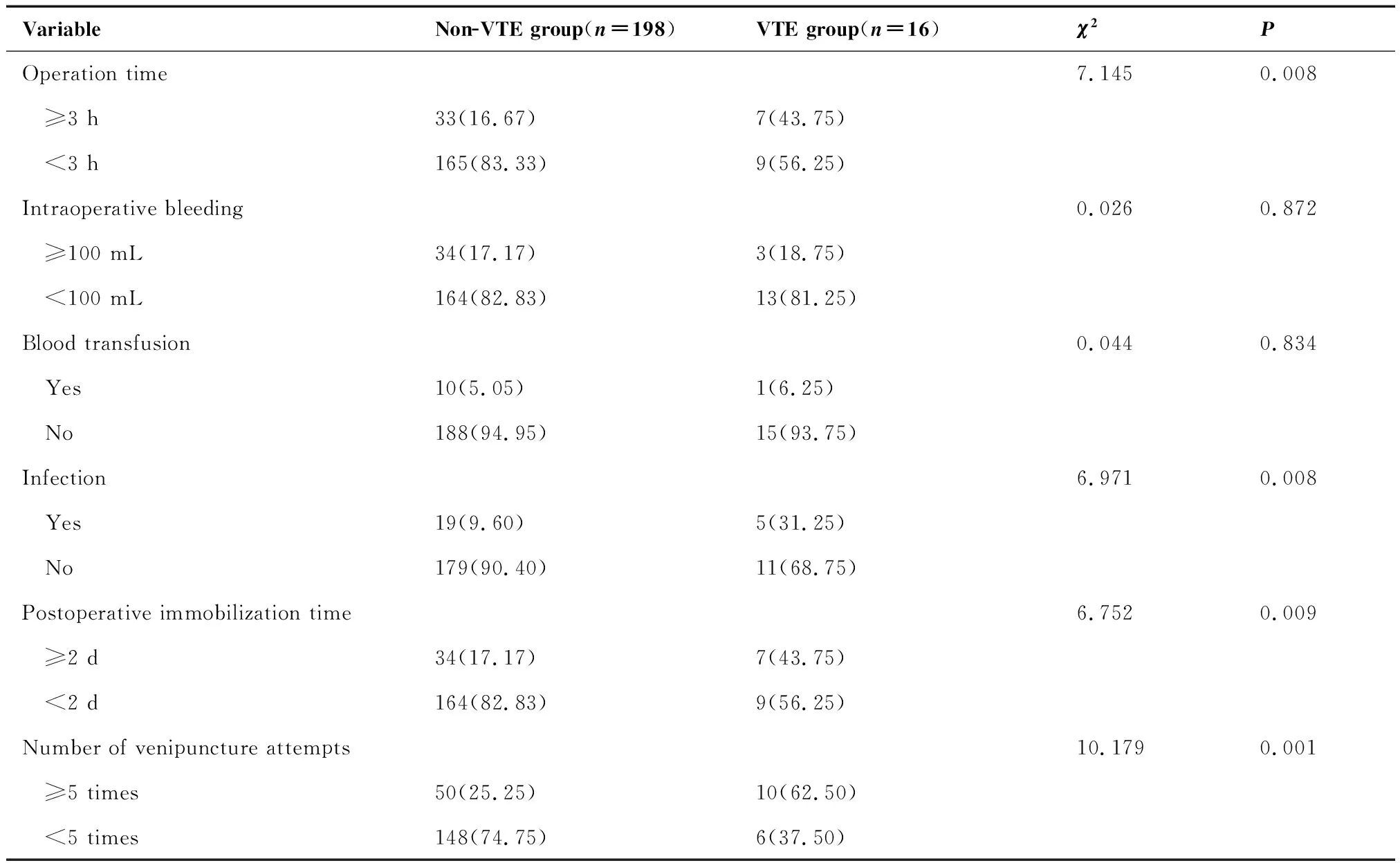
表2 非VTE组和VTE组患者治疗情况对比
2.2 CRC患者术后并发VTE的多因素分析
将年龄、既往VTE病史、2型糖尿病、心血管疾病、高脂血症、手术时间、感染、术后制动时间、静脉穿刺次数等单因素整理出的相关危险因素进行赋值(各变量赋值结果见表3),赋值后进行多因素Logistic回归分析。经多因素回归分析得出,年龄(P=0.033)、既往VTE病史(P=0.010)、2型糖尿病(P=0.030)、心血管疾病(P=0.019)、高脂血症(P=0.041)、手术时间(P=0.024)、感染(P=0.002)、术后制动时间(P=0.010)、静脉穿刺次数(P=0.023)与CRC患者术后并发VTE有回归关系(表4)。

表3 结直肠癌患者术后并发VTE相关危险因素的赋值
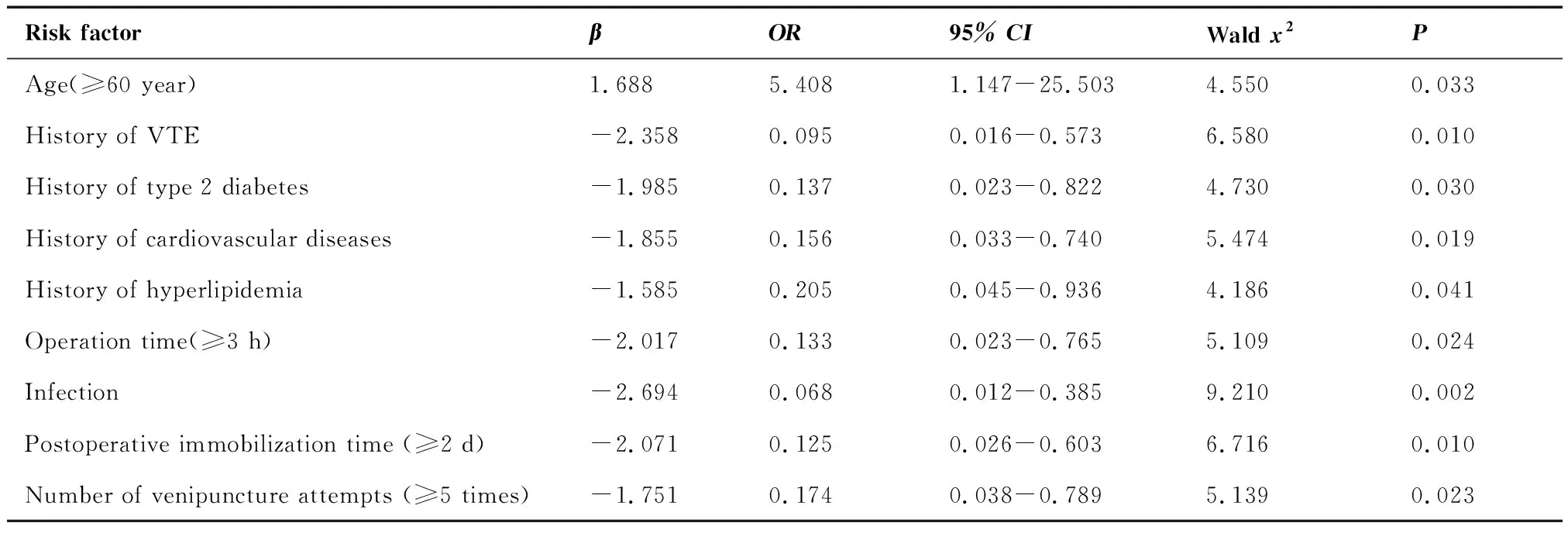
表4 结直肠癌患者术后并发VTE多因素Logistic回归分析
3 讨 论
VTE是指静脉血液在多种危险因素的作用下,体内全身或局部凝血系统的凝血或抗凝平衡失调,导致血液在静脉腔内异常凝结,阻塞静脉管腔,进而静脉回流障碍,其中下肢DVT最为常见[7]。VTE通过阻塞一处或多处的血液流动,引起心源性休克,是目前导致死亡率和复发率较高的疾病之一,严重威胁人们的生命[8],给社会带来了巨大的经济损失和医疗负担。近年来越来越多的报道提示目前我国VTE的发病率持续升高,严重降低了患者的生活质量,影响了患者的生存时间。
19世纪中期Virchow概述了静脉血栓形成的三大因素:静脉血流瘀滞、静脉壁损伤和血液高凝状态。近年来通过大量临床研究与实验观察提示VTE的发生是多种因素组合导致,尤其是血流缓慢和高凝状态。外科手术是VTE的独立危险因素,而CRC手术具有更高的VTE发生率[2,9],CRC术后患者发生VTE同样也是多种因素共同作用的结果。明确CRC术后发生VTE的相关危险因素为预防其发生提供了重要依据[10-11]。
3.1 CRC术后并发VTE的一般临床危险因素
据流行病学统计CRC多发生在高龄患者,同时常合并高血压、心脏病、高脂血症等内科疾病。患者的血管不同程度的趋于老化、部分血管内膜损伤、血管弹性差、血流速度减慢,使得血液中的红细胞、血小板和纤维蛋白在血管内异常聚集,阻碍血液回流并形成高凝状态,诱发静脉血栓。本研究通过多因素分析表明高龄、合并心脏疾病、血脂异常偏高是导致静脉血栓形成的重要危险因素。另外,临床上也有术前合并低蛋白血症增加VTE发生概率的报道[12-13]。血清中的白蛋白减少导致其抑制血小板聚集能力、结合凝血酶发挥的抗凝能力下降,同时减弱了凝血因子的中和作用,增加了VTE的发生风险。同时患者长期服用影响凝血功能的药物、改变生活及行为方式,也会促成静脉血栓的形成[14]。
本研究提示术后并发感染也是VTE形成的独立危险因素,感染时体内释放大量炎性物质激活单核细胞和瘤体细胞,改变血流状态,导致静脉血栓形成,同SHORR的随机试验结果[15]。另外有研究表明,既往VTE病史是再次发生VTE的影响因素。有VTE既往史的患者发生新的VTE的可能性是没有VTE既往史患者的8倍,5年内VTE的复发率为26.1%[16]。本文通过多因素回归分析也发现非VTE组患者和VTE组患者在既往病史上有统计学差异。
3.2 CRC术后并发VTE的特有临床危险因素
目前大量研究表明恶性肿瘤本身与VTE的形成密切相关。恶性肿瘤侵袭性强、肿瘤组织生长迅速,导致正常血管内皮遭受破坏,机体丧失血栓防御功能。另外肿瘤细胞、内皮细胞和血小板之间存在复杂的相互作用,使得肿瘤细胞对血管内皮黏附、肿瘤对血管压迫导致血液瘀滞[17]。同时瘤体释放肿瘤因子,比如分泌激活凝血酶样物质,刺激机体产生更多的血小板,改变自身血液的凝固性,进而导致静脉血栓的形成。有报道指出恶性肿瘤并发血栓的发生率为10%~15%[18],甚至高达25%[19],也有资料显示特发性VTE症患者中有约10%数年内查出癌症[20]。另外,存在大量临床资料提示CRC的AJCC分期与VTE的发生相关,高级别肿瘤患者发生VTE的风险比低级别患者更大[21-22]。而本研究结果提示0~II期与III~IV期患者在发生VTE上无统计学差异,分析原因可能是本研究纳入患者数量较少,尚待大样本的数据进一步验证这一结果。
随着医疗技术的进步和器械的应用,目前临床上CRC外科手术大多采用腹腔镜技术。腹腔镜下CRC手术与开腹手术相比手术时间更长、术中麻醉时间更久,对患者心肺功能的恢复影响更大,且手术多采用头低脚高的特殊体位,使手术过程中全身血液循环减慢;同时手术需要完整切除肿瘤及部分肠管,对患者创伤大,体内易产生应激性刺激因子,使凝血与抗凝平衡失调,最终导致静脉血栓。术后腹部伤口疼痛、留置尿管引流管等导致患者不便翻身,长时间卧床休息;短时间禁食水,使患者体液减少、血液浓缩并形成血液高凝状态,继而大量营养支持、静脉多次穿刺补液,加重血管内壁的损伤,加速了静脉血栓的形成。除此之外,也有研究提示手术过程中的气腹压力会影响静脉血栓的形成[10]。持续的高压气腹压迫下腔静脉和髂静脉,阻碍下肢静脉回流,血液淤积逐渐形成高凝状态;长时间的下肢静脉高压导致管腔扩张,损伤甚至撕裂血管内皮,暴露胶原纤维、释放凝血因子,最终增加了VTE发生风险。
化疗药物存在较强的血管毒性,除直接损伤血管内皮细胞影响血液流动性外,也会改变血液的凝固性;同时化疗常需PICC置管,导管长期留置在患者体内,直接导致静脉血栓发生;若化疗期输液时间大于3天,可能进一步增加了VTE的发生风险[23-24]。电离辐射是导致肿瘤患者血管损伤的另一个重要原因,血管内皮细胞和平滑肌细胞是辐射敏感细胞,放射线不仅会引起血管炎症反应,同时也会对血管细胞增殖产生影响,故放疗可能会导致VTE的发生[25]。但本研究结果提示CRC患者术前放化疗对术后VTE的发生没有显著影响,分析原因可能是病例数量较少导致统计学差异不明显,仍待大量本数据进一步分析和验证。
综上所述,我们认为CRC患者术后发生VTE与患者年龄大、合并内科疾病、既往存在VTE病史、手术时间长、术后长期制动、术后感染、静脉穿刺次数多有关,所以临床上应该针对性的对CRC术后存在VTE相关风险的患者加以管理和干预,以起到良好的预防作用。当然,本研究病例少、局限且为回顾性研究,期待有多中心、前瞻性、大病例的临床研究进一步阐明CRC术后VTE的相关危险因素,以期指导预防和治疗VTE。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。
