TiO2纳米管阵列电合成的扩散-反应耦合强化机制研究
2020-10-27周黄常禹范兴张楠楠陶长元
周黄,常禹,范兴,张楠楠,陶长元
(重庆大学化学化工学院,重庆401331)
引 言
TiO2因具有安全稳定、氧化能力强以及高催化活性等优点,在解决环境污染和缓解能源危机方面具有优势,被寄予厚望[1−9]。其中高度有序的TiO2纳米管阵列具有高比表面积、传输通道高效、物理化学性能稳定等特点,在光催化、传感器、太阳能电池以及生物等方面应用广泛[10−16]。Grätzel 等[17]通过简单的电化学阳极氧化钛金属板法制备出高度有序排列的TiO2纳米管。随后众多研究人员对TiO2纳米结构的生长、修饰、性质和应用进行了大量的深入工作。TiO2纳米管阵列的制备方法有水热法、模板法、溶胶−凝胶法以及阳极氧化法[18−20]。模板法、溶胶凝胶法、水热合成法制备的TiO2纳米管管长、管径有限,且不易通过实验条件控制。而阳极氧化法因其制备的TiO2纳米管阵列高度有序、分布均匀且结构多变易控而被广泛采用。此外,相对于水热法和模板法制备TiO2纳米管,阳极氧化法还有一个不可忽略的优势,即TiO2纳米管与Ti 基底直接相连,用作电极时,无需黏结剂,Ti 基底可直接作为集流体[21]。近年来的研究结果表明,通过阳极氧化法制备TiO2纳米管过程中影响TiO2纳米管形貌、管径及孔径的因素有很多,如电解液中氟离子浓度、水含量、施加电压或电流、阳极氧化时间和电解液的温度等[22−24]。
尽管阳极氧化法制备TiO2纳米管已经研究了十几年,但形成机理方面的报道仍相对较少,尤其是TiO2纳米管阵列生长过程的动力学机制方面的基础研究极为匮乏[25−26], 这极大限制了TiO2纳米管阵列的规模化可控制备以及反应器设计。已有研究认为在电氧化制备TiO2纳米管过程中,金属先溶解成离子,然后水解在电极表面形成凝胶膜。同时,H2O被氧化生成O2和H+。在阴离子配体的作用下,氧化凝胶表面局部过量的H+使其发生点蚀,从而形成纳米管/孔。然后离子在孔中积累,加速腐蚀,导致纳米管的生长。气泡的渗出加速了气孔的扩大[27]。上述点蚀机理简单易行。然而很难解释纳米结构的高度周期性分布和沿纳米管深度方向的均匀性。高价离子的水解和凝胶化,如Ti4+和Al3+通常是多个步骤的过程,涉及大量中间体,比如TiOHx4−x低聚羟基钛中间体。电氧化过程中的扩散步骤将与电氧化步骤耦合,使动力学更加复杂。有报道称,在钛和铝电氧化过程中,存在电化学振荡和其他非线性动力学行为[28−29]。Tao等[30]详细解释了TiO2纳米管阵列的自组织形成机制,提出溶解−击穿模型,他们指出由于氧化物的膨胀效应以及反应热的原因,使机体内部能量增大。为使内部能量和表面能平衡,表面能必须增大,此时氧化物层表面产生裂隙缝,再通过裂隙出的击穿−溶解反应形成纳米管。以上所做的研究都是从电流的动态变化来研究TiO2纳米管阵列的化学形成过程,并提出相应的模型,解释了纳米管形貌的变化。但是此模型中所涉及的反应机制难以解释此过程中出现的电流振荡现象,更无法解析纳米管两端通透等现象。近代非平衡非线性物理化学理论研究表明:在远离平衡的反应扩散耦合体系中,如果存在中间体自催化活化等非线性动力学机制,将可能导致产生空间有序的斑图结构以及周期性电化学振荡等非线性现象[31]。相关理论已广泛应用于解释生物周期律等宏观时空自组织现象。然而在解释纳米/微米系统中的非线性自组织机制方面文献报道甚少[32−33]。非线性动力学机制的研究将有助于合成更先进的氧化物纳米阵列。
本文系统考察了阳极氧化法制备TiO2纳米管阵列过程的生长机制。探索了温度、电压、氟含量及水含量等对TiO2纳米管生长速率以及不同生长阶段电化学行为的影响,制备了结构规整的TiO2纳米管阵列。研究还利用电化学阻抗等方法测试TiO2纳米管生长初期界面电化学的演变,并分析了等效电路的变化,基于非线性动力学理论的视角探讨了TiO2纳米管阵列生长过程中非线性动力学机制。
1 实验材料和方法
1.1 材料
乙二醇、氟化铵、无水乙醇、丙酮和氢氟酸,分析纯,重庆川东化工(集团)有限公司化学试剂厂;钛片电极(99.9%):2 mm×2 cm×2 cm,宝鸡市利泰有色金属有限公司;不锈钢片电极:2 mm×2 cm×2 cm,重庆助研科技有限公司;银/氯化银参比电极,重庆助研科技有限公司;试验用去离子水经New Human Power Ⅱ制备。
1.2 实验方法
1.2.1 样品前处理 将尺寸为2 mm×2 cm×2 cm 的钛片以及尺寸为2 mm×2 cm×2 cm 的不锈钢片用砂纸(600#、800#、1600#)打磨抛光,然后分别以乙醇,丙酮为清洗液超声清洗10 min 去除表面油污,再经去离子水以及乙醇清洗后自然干燥,待用。
1.2.2 阳极氧化 没有特别说明,烧杯中电解质均含去离子水[2%(体积)]、乙二醇[98%(体积)]、氟化铵[0.3%(质量)]。将不锈钢片和和钛片分别插于对应的孔中,固定后保持间距为2 cm,然后将整个装置放入集热式恒温加热磁力搅拌器,恒温的温度设定为30℃。将不锈钢电极与直流稳压电源(Honbao Experimental Instrumental Factory,China)的 负 极 相连,钛片与直流稳压电源的正极相连,设置直流稳压电源的输出电压为(55、65、85、100 V)。最后打开直流稳压电源,根据反应特定的时间进行电解反应。反应初始可以观察到钛片表面由因抛光得到的灰白色转变为蓝色,然后又转变为淡黄色,而不锈钢电极上产生了许多气泡。电解结束后,阳极钛片在室温下自然风干24 h 并于马弗炉中煅烧2 h(450℃)。升温速率为10℃/min。
1.3 样品表征与分析测试
退火后TiO2纳米管的形貌经场发射扫描电镜进行形貌表征(FE−SEM,Hitachi S−4800,Japan)。电解电流随时间的变化通过CHI660D 电化学工作站(Shanghai Chenhua, China)采集采样电阻分压测定。交流阻抗分析,采用银/氯化银电极作为参比电极在原电解体系中进行测试。
2 实验结果与讨论
2.1 二氧化钛纳米管结构随电解时间的演变
阳极氧化过程中的电流−时间(I-t)曲线能够较直接地反映TiO2纳米管的形成及变化情况,根据图1(a)可知,随着电解时间的延长,电解电流经历了快速下降阶段(1)、小幅上升阶段(2)、逐渐下降阶段(3)~(4)等几个阶段。为探究纳米有序结构随电解时间的变化规律,图1(b)~(d)呈现了在去离子水[2%(体积)]、乙二醇[98%(体积)]、氟化铵[0.3%(质量)]的体系中,65 V 恒压电解过程中不同阶段阳极TiO2结构形貌的变化。
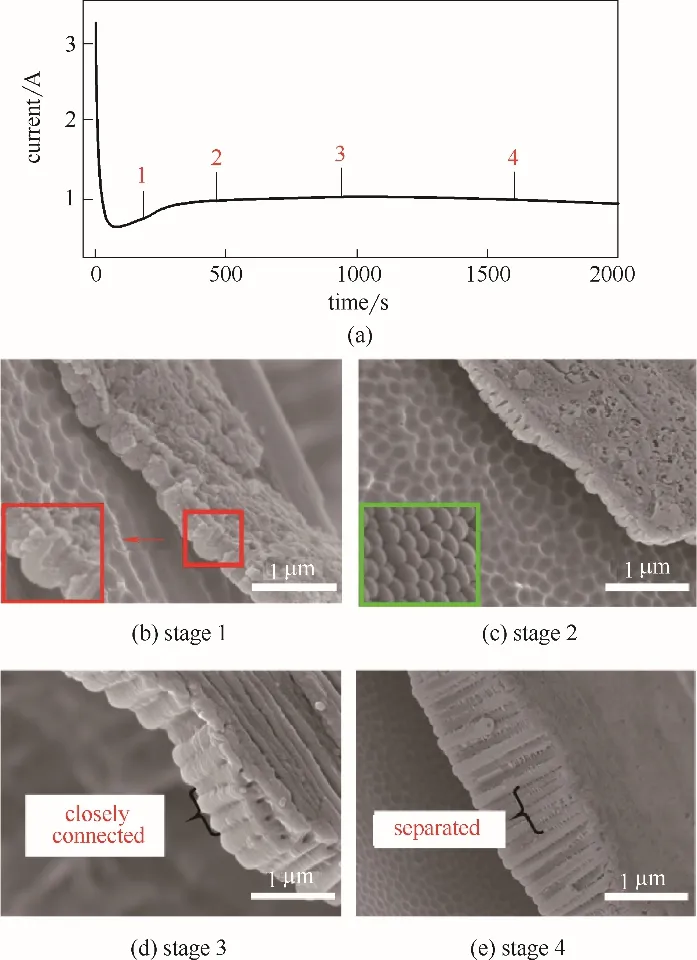
图1 钛电极表面TiO2纳米管生成过程中电流时间曲线(a)以及(a)图中TiO2纳米管生成过程中阶段(1)~(4)的SEM图[(b)~(e)]Fig.1 Plot of current vs time in growth process of TiO2nanotubes by anodization on surface of Ti electrode(a)and SEM images[(b)—(e)]of TiO2 nanotube arrays at stage(1)—(4)in Fig.1(a),respectively
在氧化的最初阶段(1),电极表面形成了致密的氧化膜且膜厚约为80~100 nm,表面形貌如图1(b)所示,为多孔状;在氧化阶段(2),氧化膜被F−化学溶解,随后溶解的同时又发生生成反应,电流密度增加,氧化物薄膜上开始出现不规则的纳米管阵列且这些纳米管与钛基底相连,表面形貌如图1(c)所示;在氧化阶段(3),随着电解时间延长纳米管阵列趋于规整并不断生长,如图1(d)~(e)。先前的研究认为在电解初期,在钛基底表面形成一层氧化膜后,氧化膜层承受的电场强度急剧增大,在含氟溶液和电场的共同作用下,TiO2阻挡层发生随机击穿溶解形成孔核,随着氧化时间的增加,随机分布的孔核发展成为小孔,孔的密度也不断增加,最后均匀分布在表面。然而,TiO2纳米管形成的过程中出现的许多现象是目前这个理论无法解释的,例如纳米结构的高度周期性分布和沿纳米管深度方向的均匀性、反应中间体扩散反应耦合导致的自组织形成的纳米半球,如图1(c)中纳米管底部半球形形貌,所以TiO2纳米管的形成机理至今仍不明确。
本研究中提出阳极电解Ti 形成Ti4+,进一步水解成含水低聚羟基钛中间体,低聚羟基钛中间体在电场作用下有序排列成纳米管阵列结构,后在某些条件下失去水生成二氧化钛的电解过程。此电解过程中电极反应与电解液中离子扩散耦合形成了纳米管生长过程中的非线性特征。首先,阳极电解初期,表面电解生成钛离子并水解产生钛氢氧化物覆盖在阳极表面,甚至形成致密的氢氧化物层,如图1(b),电导率剧降使体系电流也随之快速降低;而后此层氢氧化物层部分逐渐溶解,且低聚羟基钛中间体在电场作用下自组织形成纳米管雏形,如图1(c),随阳极氧化时间延长,纳米管不断生长且趋于规整,纳米管上部的氢氧化物层因溶解而变薄且致密,如图1(d)和(e)。
2.2 电解电压对纳米管生长的影响
为研究阳极氧化制备TiO2纳米管阵列过程中,氧化电压对纳米管生长速率的影响,在0.3%(质量)NH4F,去离子水[2%(体积)]、乙二醇[98%(体积)]的体系中制备TiO2纳米管阵列,氧化时间为2 h,其中图2(a)是在不同电压(55、65、85、100 V)下制备TiO2纳米管阵列以及对应生长过程中记录的电流−时间曲线。
电解电压为TiO2纳米管特征形貌,纳米管生长速率的重要影响因素,如图2(a),体系电流密度随电压的增加而升高,表明纳米管生长随电压的增大而加快。图2(b)~(c)表明,随着电压增大,逐渐得到较为规整TiO2纳米管,随着电压进一步增大,部分TiO2纳米管断裂,如图2(d)。实验中电压增加到100 V时,已经不成管状结构,为类似絮状结构,如图2(e)。一方面,电压升高加快了纳米管管底电场辅助氧化反应和氧化物溶解反应,即电化学刻蚀速率随电压的增大而变快;另一方面加速了电解液中离子的迁移。有机体系中,电场作用下的离子迁移作用远大于由于离子浓度差而引起的离子扩散作用。乙二醇体系中,含H+极少,H+从纳米管管底产生,H+在电场作用向纳米管管口方向迁移,完成管口成型的TiO2纳米管的溶解反应。所以随电压的增大,迁移速率增快,因而管口成型纳米管的溶解反应也变快,但增加的幅度不如电化学刻蚀速率。因此,电压增大带来的结果使纳米管生长速率加快,纳米管增长,随着电压的进一步升高,反应过程中低聚羟基钛中间体扩散−反应耦合失稳,从而导致空间有序结构消失。
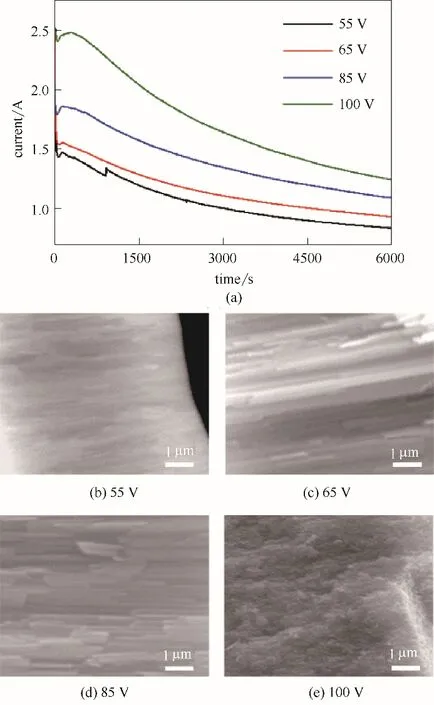
图2 不同电解电压下阳极氧化法制备TiO2纳米管生长过程中的电流时间曲线(a)以及对应TiO2纳米管的SEM图[(b)~(e)]Fig.2 Plot of current vs time(a)and the SEM images[(b)—(e)]in the growth process of TiO2 nanotubes by anodization under different voltage
本实验中提出,纳米管阵列是低聚羟基钛中间体在电场作用下自组织形成的,电压过大或过低都会影响钛低聚羟基钛中间体的自组织生长情况,以及其中间体扩散−反应耦合,所以电解电压过大或过小都会对纳米管阵列的有序性产生影响。
2.3 氟含量对纳米管生长的影响
当其他条件确定时,增加氟离子的量不仅会改变电解液的pH,同时将促进TiO2的溶解,所以氟含量必须控制在较低水平以减小溶解,但同时又需要达到保证纳米管生长的水平。在图3(a)中,随着氟离子量的增加,阳极氧化电流也逐渐增加,在该氟离子的量的区间内,表明纳米管生长随氟离子的量增大而加快。NH4F 浓度为0.3%(质量)电解液中,随阳极氧化时间的增加,各阶段的Nyquist 图为圆弧段,为简单反应的特征谱图,如图3(b)。NH4F 浓度为0.7%(质量)电解液中,阳极氧化初期,谱图中曲线在高频时向第四象限弯曲,体系均表现一定的感抗行为;阳极氧化时间为200 s 时,Nyquist 图低频段弧趋近为45°的直线,等效电路中将出现Walburg 阻抗(n=0.5),此时电极反应受扩散步骤控制,体系浓差极化明显。根据特征阻抗谱图的变化,得出随氟含量变化体系等效电路的演化图,如图3(d)。随氟含量的增加,体系表现出一定的感抗行为(L)[图3(d)中Cdl为双电容]。
从得到的电分析测试结果可以看出,当氟含量较低时,等效电路为一简单反应电路,表明此时电极反应由电荷转移步骤(阳极钛的氧化反应)控制;氟含量增加后,等效电路中增加等效电阻R0和电感L,且与反应电阻Rf并联,表明此时体系中除有钛的氧化反应外,还有电阻为R0的反应发生,且此反应有感抗(L)性质。在本研究提出的反应机理中为水合钛氢氧化物之间的相互转化反应,而此系列反应与扩散的耦合为引起纳米管生长过程中出现非线性规律的根本来源。因此在氟含量较高时,体系表现了非线性机制,结合图3(d)与图1 表明,体系非线性存在于钛氢氧化物溶解伴随有初期纳米管生长阶段[阶段(1)]。
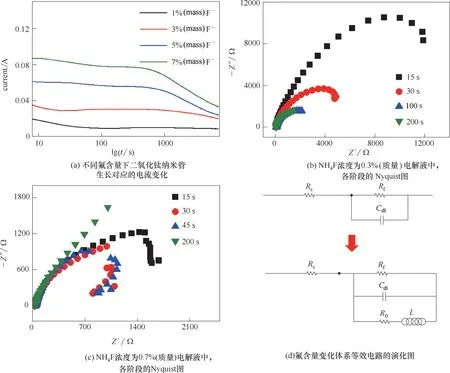
图3 氟含量对TiO2纳米管生长的影响Fig.3 Effect of F−concentration on the growth of TiO2 nanotubes
2.4 电解质水含量对纳米管生长的影响
为了探究纳米管生长初期界面电化学机制的演变,图4 总结了电解质含水量分别为2%~8%(体积)的体系在不同电解时间的Nyquist 图。当电解液中水含量增加时,电解回路的电流初始值,以及稳定状态时的电流值都减小;水含量为2%(体积)时,电流初始值最大,随时间延长,平衡电流减小,减小到与水含量为6%(体积)时相当时,曲线没有第三阶段氧化物部分溶解部分,电流逐渐减小,同上文中讨论的氟含量曲线一致。所以,水含量越少电解回路电流越大,纳米管的生长速率越快;但增加到一定值时,反而会减小纳米管的生长速率。
图5(a)为电解Ti 片10 s 后对应的测试结果,结果显示为反向的容抗弧。随电解时间延长,测得的容抗弧为正。而图5(c)中显示10 s对应的Nyquist图形近似45°的直线。这表明此时存在Walburg 阻抗(n=0.5)[34]。电解时间超过30 s 后,Nyquist 图形变严重。分析认为这一现象是电极表面弥散效应引起的。
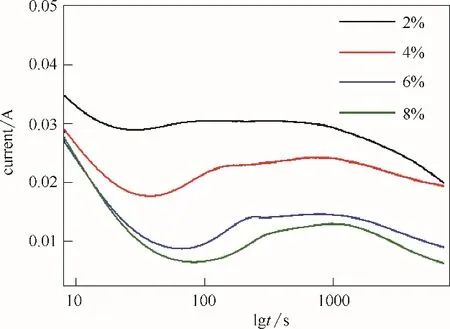
图4 不同电解质含水量对应的阳极氧化电流变化Fig.4 Plot of current vs.time during growth of TiO2 nanotube arrays for varying water concentration
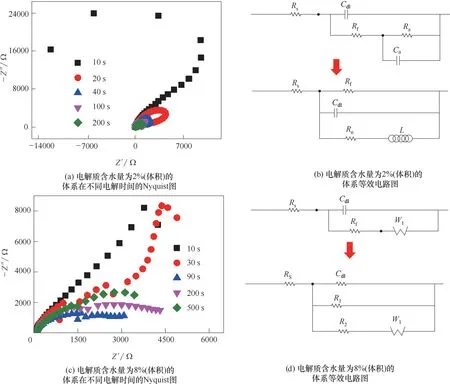
图5 水含量对TiO2纳米管生长的影响Fig.5 The effects of H2O content on the growth of TiO2 nanotubes
在此基础上,研究建立了不同含水量电解体系中的等效电路图。图5(b)为含水量2%(体积)的电解体系等效电路随时间的演化图。阳极氧化时间为10 s时,等效电路中等效电阻Ra<0,等效电容Ca>0。随着阳极氧化时间的延长,体系表现出一定的感抗行为(L)。此时,体系可能形成能够反馈机制导致电流出现振荡。图5(d)为水含量8%(体积)的电解体系等效电路随时间的演化图。可知刚开始电解时体系存在半无限扩散电阻。此时电解反应主要由半无限扩散控制。随着电解时间延长,Nyquist 图变为加宽的容抗弧。通过对比可知含水量的变化将导致体系的反应动力学机制发生重大改变。水含量较低时,反应体系的等效电路与氟含量为2%(质量)时相同,体系电化学性质也应相似,体系反应中包括钛的阳极氧化反应以及钛氢氧化物之间的相互转化反应等,此时体系可能形成反馈机制导致电流出现振荡;而水含量增加时,阻抗谱图为加宽的容抗弧(加宽的容抗弧为两阻抗大小相似的电极反应耦合产生)。另一方面,阳极氧化钛产生Ti4+的同时,阳极表面电解液中水也发生氧化反应产生O2,水含量大时,水的氧化反应加强,钛的氧化和水的氧化反应耦合形成了阻抗谱图中加宽的容抗弧。
综合以上实验结果,在氟含量较高或水含量较低时,电化学测试的阻抗谱中出现感抗弧,建立的等效电路中出现等效电感元件,而此元件的产生表明体系的系列反应中存在有非线性的反馈机制。此现象均出现在纳米管生长初期阶段,如图1中的阶段(1)。
2.5 反应动力学机制分析
根据非平衡态理论[35],如果反应体系中存在两种类型的中间体,则扩散反应耦合体系中可能形成有序结构。一种中间体可以加速反应,这就是所谓的活化子,而另一种中间体可以减缓反应,这就是所谓的抑制子[36]。当活化子的扩散系数小于抑制子时,可通过自组织过程形成周期性的空间结构。低聚羟基钛反应中间体的非线性反应行为,为有序纳米结构的自组织提供了周期空间结构和周期电流振荡的联系[37]。上述试验结果表明,电解中间产物的反应行为受反应时间以及含水量影响很大。分析认为,电解过程中,阳极Ti 电氧化产生Ti4+和H+,其在电场驱动下迁移远离电极表面,并在远离电极表面的过程中发生水解反应,形成氢氧化钛等小分子[38]。它们可进一步缩合,形成Ti(OH)4(H2O)2、Ti2(OH)8(H2O)2、Ti2O(OH)4(H2O)22+、Ti(OH)3(H2O)+等缩合离子[39]。缩合离子不仅可作为成核中心引发胶团生长,还可以水解产生新的成核中心加速形成更多的胶团。缩合离子等水解中间体有助于加速钛凝胶的形成,而H2O 与H+却可以通过促进水解来抑制胶团的生长。此外,H2O 与H+扩散系数比缩合离子等水解中间体大,这符合形成有序斑图结构的必要条件。分析认为,电极表面[H2O]以及凝胶浓度随电解时间的变化为体系扩散−反应动力学机制演化提供了可能。
阳极电解过程中,Ti4+和H+产生于电极表面,反应式如式(1)~式(2)
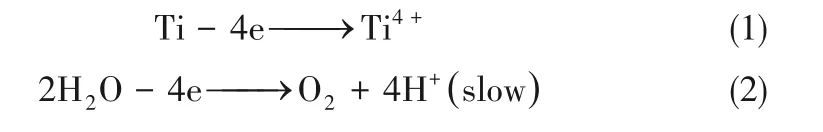
反应初期,阳极表面[H2O]相对较大,水氧化导致pH下降;随后氢氧化物凝胶形成,电极表面[H2O]逐渐减小,H+的生成速率减慢,而H+的扩散系数较大。
H+和Ti4+与胶体反应形成带电胶体离子,聚合后形成致密胶体层,形成高价胶体离子
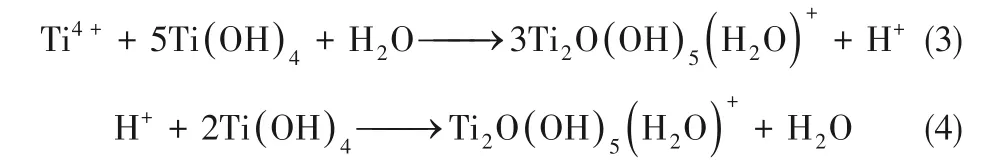
TiO2纳米管阵列形成过程主要是由羟基钛化合物水解及缩聚过程的中间体反应扩散耦合机制决定。但是该过程也会受其他离子的影响,尤其是F−等卤素离子。其中,F−离子不仅是作为支撑电解质的阴离子,同样也会与Ti离子反应结合,形成氟化物。
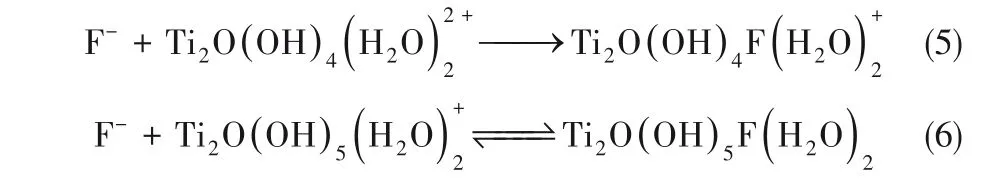
当胶团体系中H+扩散与生成达到平衡时,可认为体系电极表面附近主要存在如式(7)~式(13)七个反应
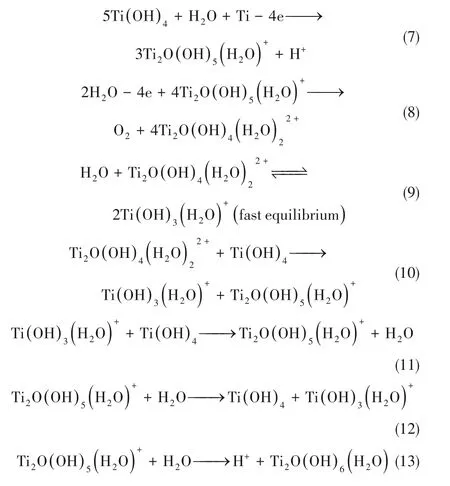
式(1)、式(3)综合可得式(7),H+活性强,会快速与低价胶体离子反应生成高价胶体离子
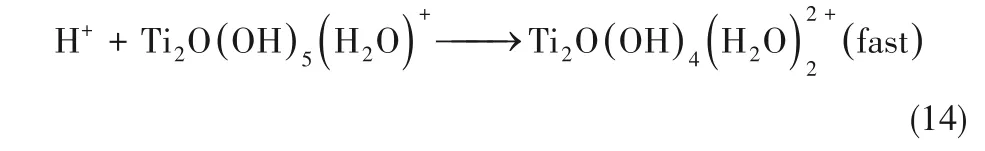
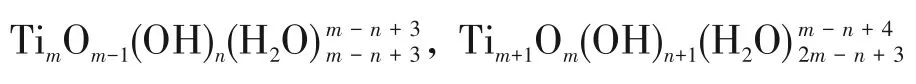
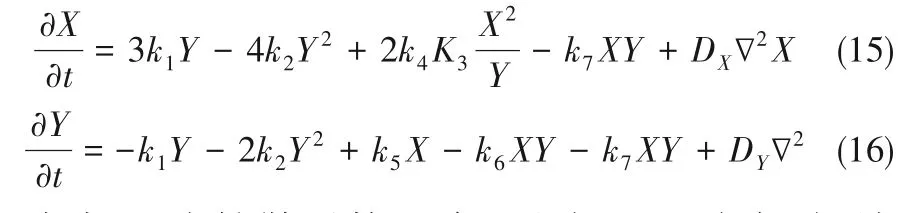
式中,D 为扩散系数矩阵。电解过程稳定时,纳米管中远离电极表面的地方,无电子转移,形成致密胶体层后,Ti4+和H+在胶体层中的扩散极慢,因此式(3)、式(4)的反应速率很慢,可以忽略,此时体系的二变量动力学方程组为
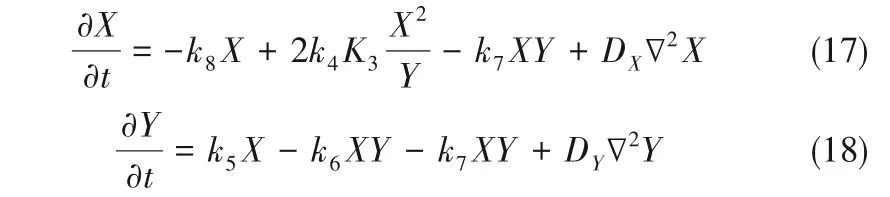
对式(17)、式(18)做微扰,令

式中,X0,Y0分别为δX/δt=0且δY/δt=0时方程组的稳态解。对式(17)、式(18)进行线性稳定性分析,近似忽略高阶项,可导出Jacob行列式J
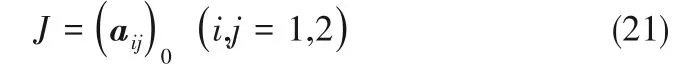
其中得到a11、a12、a21、a22如下
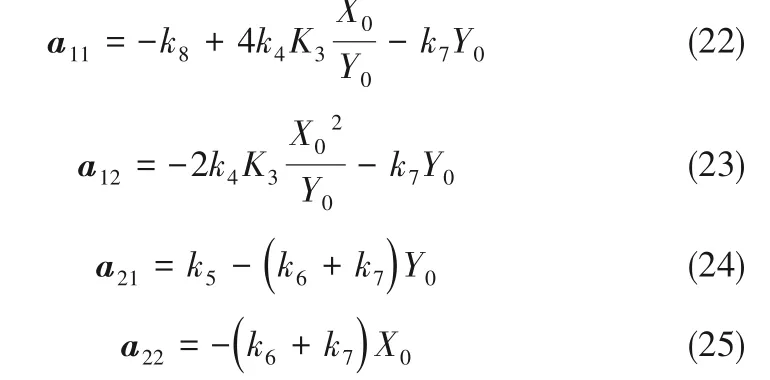
取模数为k时,
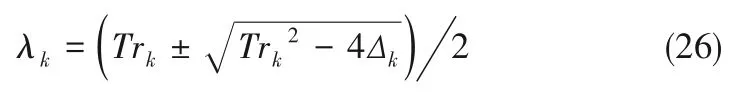
式中,Trk为Jacob 矩阵的秩,Δk为Jacob 行列式的值
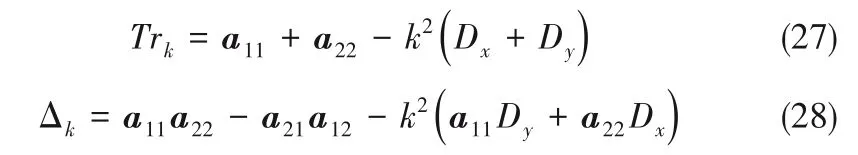
式中,下角标x,y分别为X0,Y0的微扰变量。则系统对微扰的最危险模数kc
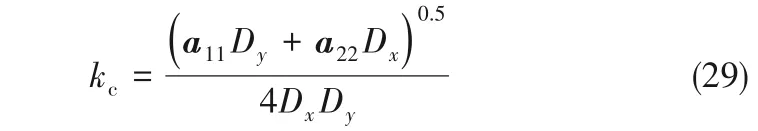
此时Δkc有最小值,
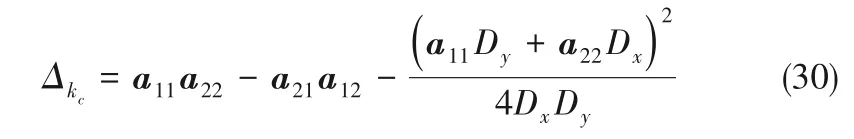
随着电解进行,缩合离子粒径逐渐增加,当所形成的离子粒径较大时,有Dy>>Dx,Δkc近似值如下
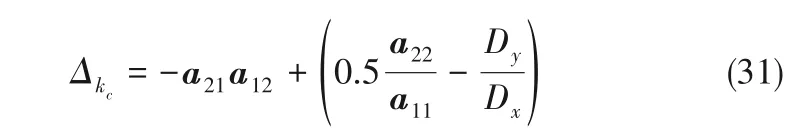
取X0、Y0分别为
解得定态解X0和Y0
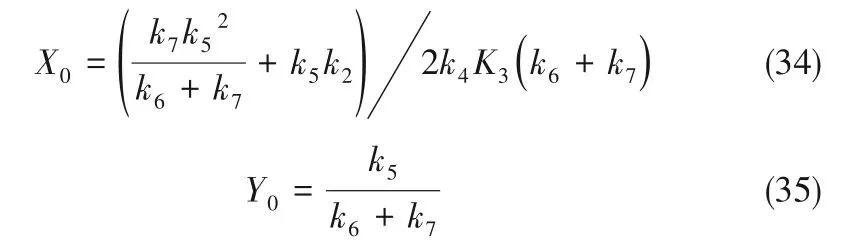
从而可以得出Jacob 行列式的秩Tr0和Δ0(取模数k=0,进行线性稳定性分析)分别为
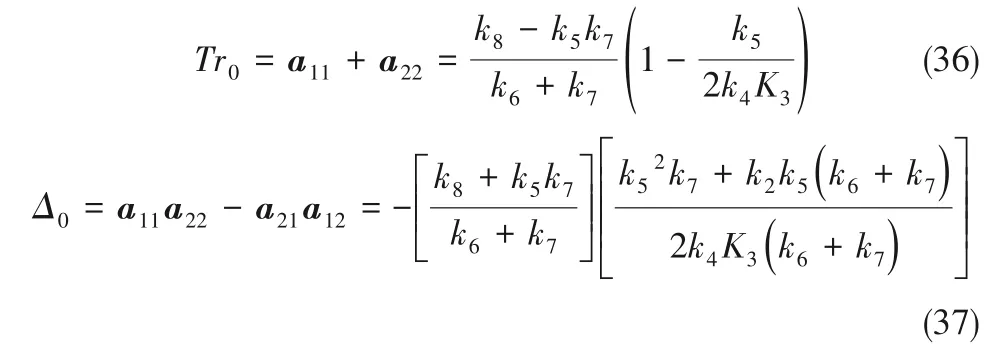
增大电压时,纳米管中H+在电场作用的迁移速率增大,反应式(14)增强,k8增大,当Δkc=0时,
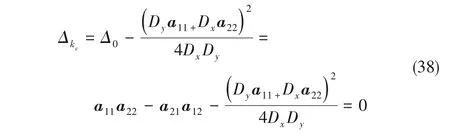
当Δ0的值如下时
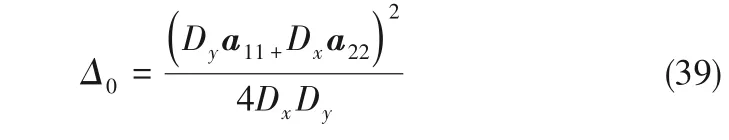
可得体系的振荡波长λ
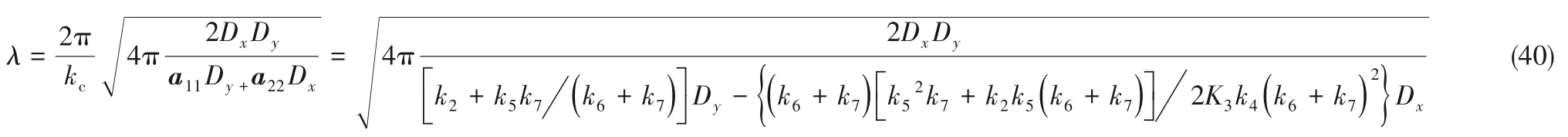
体系中阻滞子(H2O)的扩散速率远低于活化子(低聚羟基钛中间体)的扩散速度,振荡区间内体系电压增大使k8增大,对应波长缩短,相应氢氧化物纳米阵列的周期越短。
根据线性稳定性分析,当Tr0<0,Δ0>0时,若存在kc使Δkc<0,则体系可以失去空间稳定性,X 将沿电极表面作周期性分布,从而可以导致形成有序结构的氢氧化物凝胶。此时,同样可以由方程组导出X 沿电极表面作周期性分布的波长λ1为
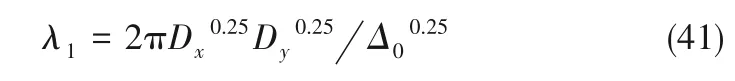
带入Δ0的值带入得到波长λ2为
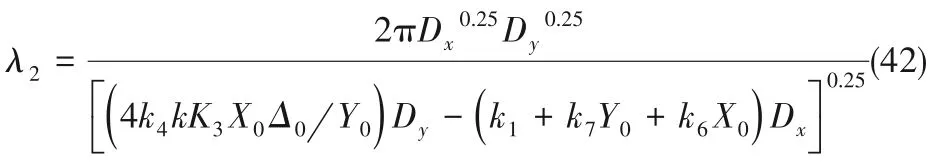
胶团或缩合离子Y的扩散系数越小,波长越短,相应氢氧化物纳米阵列的周期越短。令k7Y0=Z,则Δ0、Tr0均为Z 的高次函数。随着电解的进行各反应速率逐渐变化。Δ0和Tr0随Z、Y0的变化趋势如图6所示。刚开始时Z 较大,此时有Tr0<0,Δ0>0 并且Δkc<0。此时体系对空间失稳,出现自组织纳米管阵列。随着电解时间延长,Y0减小,对应Z 逐渐减小。根据图6 可知,随着Z 减小,Δ0也减小,对应纳米管的管心距增大。当Z 减小到1 附近时有Tr0=0,Δ0>0,此时体系对时间失稳,可能出现电流振荡。反应动力学分析表明电流振荡与有序阵列结构的形成均与反应中间体扩散反应耦合的非线性机制相关。在适合的条件下,体系能够存在电流振荡。
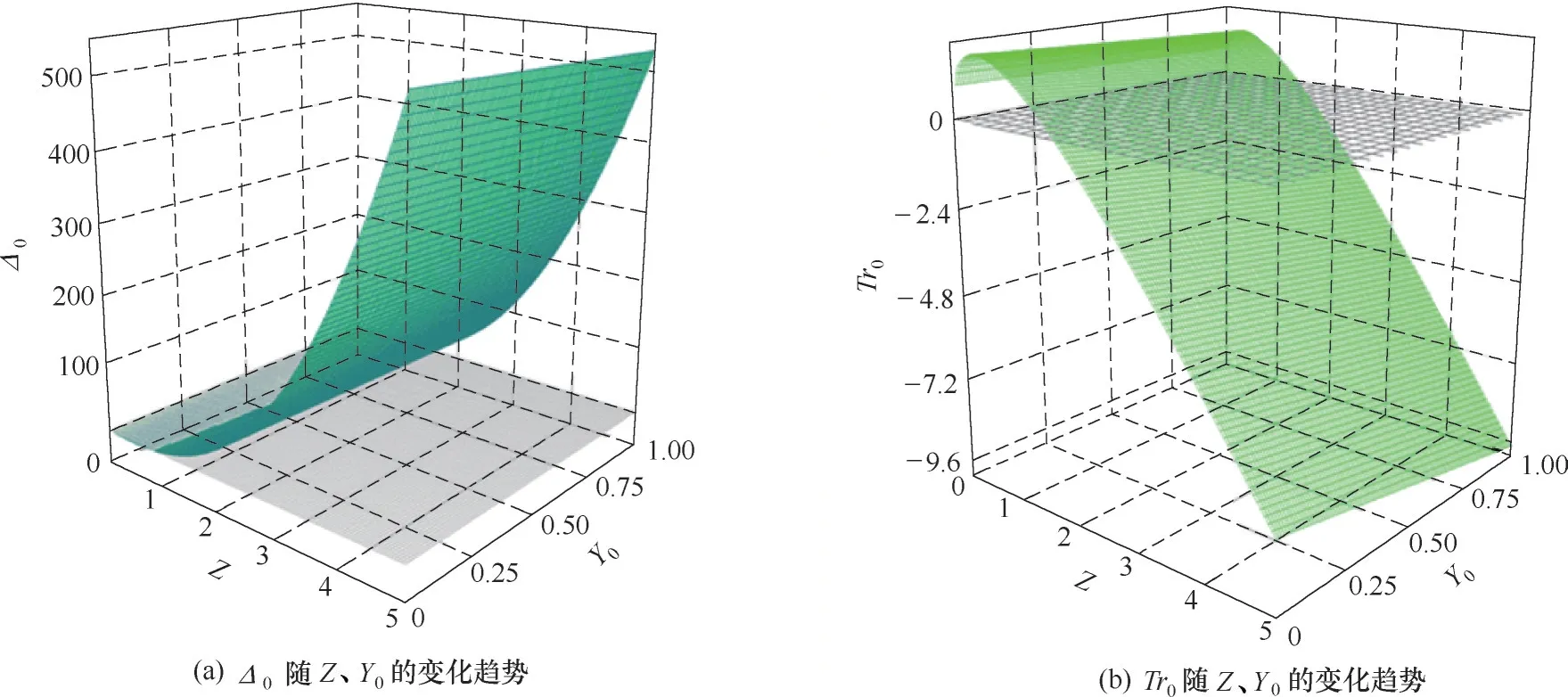
图6 Δ0以及Tr0分别随Z、Y0的变化趋势(k4k3=0.9,k1=0.01,k6=0.5)Fig.6 Δ0,Tr0 change with Z,Y0 respectively(k4k3=0.9,k1=0.01,k6=0.5)
3 结 论
本文系统考察了阳极氧化法制备TiO2纳米管阵列过程的生长机制。探索了温度、电压、氟含量及水含量等对TiO2纳米管生长速率以及不同生长阶段电化学行为的影响,并制备了结构规整的TiO2纳米管阵列。研究还利用电化学阻抗等方法测试TiO2纳米管生长初期界面电化学的演变,并分析了等效电路的变化,基于非线性动力学理论的视角探讨了TiO2纳米管阵列生长过程中非线性动力学机制。研究结果表明,TiO2纳米管生长速率与电解电压,氟含量以及温度都成正相关,与水含量负相关,并且影响生长过程中各阶段的电化学行为。水含量较高电解液中,阻抗谱是加宽的容抗弧,钛表面发生点蚀现象;氟含量较高电解液中,阳极氧化初期,等效电路由简单电路演化为带有电感元件L 的复杂电路,表明体系具有反馈性质,并且随氟含量的增加,体系的反馈性增强。研究针对大电流氧化下的TiO2纳米管阵列电合成过程,提出基于羟基钛化合物中间体的扩散−反应耦合非线性动力学机制,并解析了参数阈值。
