离子液体在稀土萃取分离中的应用
2020-10-27王道广王均凤张香平王毅霖张晓飞
王道广,王均凤,张香平,王毅霖,张晓飞
(1 中国科学院过程工程研究所离子液体清洁过程北京市重点实验室/多相复杂系统国家重点实验室,北京100190;2中国科学院绿色过程制造创新研究院,北京100190; 3 中国石油集团安全环保技术研究院有限公司石油石化污染物控制处理国家重点实验室,北京102206)
引 言
依据国际纯粹与应用化学联合会(IUPAC)的定义,稀土元素是化学元素周期表中ⅢB 族的镧系元素及钪和钇共17 种元素的总称[1−2]。由于电子层结构的特殊性,稀土元素在光、磁、电方面呈现独特的物理化学特性,在实际应用中起到不可替代的作用,被广泛应用于永磁、超导、荧光、激光、抛光、催化、储氢等高端功能材料中,覆盖能源、航天、医疗以及电子信息等领域[1−6]。我国是稀土资源大国,稀土储量、产量、消费量均居世界前列。目前全球稀土总产量为13 万~14 万吨,我国产量占比高达95%[1,7]。自然界中,稀土元素是共生的,而分离并获得高纯单一稀土元素是其高端应用的基础。因而稀土元素的分离技术对我国稀土资源的高值化利用及助力我国由稀土大国向稀土强国转变具有重要意义。
因镧系收缩导致稀土元素间电子层结构和物理化学性质的相似性使得将共生的混合稀土分离为高纯单一稀土元素的难度极大[3−4]。目前,稀土元素分离纯化技术包括溶剂萃取、分级沉淀结晶、离子交换、氧化还原、膜法等[8−12],其中,溶剂萃取因分离性能好、分离容量大、易于连续化操作等被工业上广泛采用[4−8]。长期以来,在工业化生产过程中,稀土溶剂萃取过程主要采用双(2−乙基己基)磷酸酯(P204,HDEHP,D2EHPA)和2−乙基己基磷酸单2−乙基己基酯(P507,HEHEHP,EHEHPA,PC88A)两种酸性磷类萃取剂[8],其分离系数小,萃取过程需皂化,从而造成工艺流程长、酸碱消耗大、工艺废水排放量大等问题[13−14]。随着技术要求的提高、国内环境标准的升级及人们环保意识的增强,高效绿色萃取剂的开发和应用日趋迫切。
离子液体(ionic liquid,IL)是在室温或接近室温下可呈现液体的液态有机盐。离子液体因具有一些优良的特性使其在分离、合成、催化和电化学等方面受到广泛关注[13,15−17]:(1)离子液体几乎没有挥发性,不产生大气污染,溶解能力强,被认为是环境友好的绿色溶剂;(2)结构可设计性强,阴阳离子结构均可调,可以根据需要设计出具有特定功能的离子液体;(3)离子液体不可燃、热稳定性和化学稳定性好、电化学窗口宽。在萃取分离过程中,离子液体既可作为稀释剂或溶剂,也可作为萃取剂和协萃剂[2,13,18−19]。为实现稀土元素的绿色分离,国内外科技工作者基于非功能化和功能化离子液体开发了多种萃取体系并开展了深入研究。与传统萃取体系相比,离子液体萃取体系在稀土萃取分离过程中具有萃取效率高、选择性好、稳定性好、挥发性小等优点[13−14,20]。然而,离子液体萃取剂体系在萃取过程中也存在一定的缺陷,比如某些条件下通过离子交换机理进行稀土元素的萃取分离时,离子液体的阳离子或阴离子进入到水相中[2,19,21−22],导致离子液体萃取体系无法有效重复利用的问题。因而,有必要对已有的研究成果进行总结和分析,为离子液体萃取体系的设计及更深入的研究工作提供借鉴和依据。
本文将结合近年国内外的研究成果对离子液体在稀土萃取分离的研究进行综述和分析。首先从非功能化和功能化划分离子液体,以便于对其用于稀释剂、萃取剂及协萃剂时的萃取行为和萃取机理等进行综述,在此基础上分别讨论了两类离子液体用于稀土元素萃取分离的优势和缺点,进一步提出了离子液体萃取剂用于稀土萃取分离的主要挑战并给出了建议。
1 非功能化离子液体
目前,用于稀土萃取分离的非功能化离子液体主要有咪唑类离子液体([Cnmim]+)、季铵盐类离子液体([Nxxxx]+)、季膦盐类离子液体([Pxxxx]+)和哌啶类离子液体([CnCmPip]+)。在萃取体系中,非功能化离子液体既可用作溶剂/稀释剂,也可作为萃取剂和协萃剂。
1.1 非功能化离子液体作为稀释剂
咪唑类离子液体作为稀释剂用于稀土元素的萃取分离是报道最早、截至目前研究最多的非功能化离子液体。继Huddleston 等[23]报道了离子液体作为稀释剂/溶剂用于液液萃取分离后,Nakashima等[24−25]首先开展了以咪唑类离子液体[C4mim]PF6为稀释剂用于稀土元素分离的研究,萃取剂为对正辛基苯基−N,N'−二异丁基胺甲酰甲基氧化膦(CMPO),结果表明CMPO−[C4mim]PF6体系对稀土元素的萃取分配系数是CMPO−正十二烷体系的1000 倍,而且达到同样的萃取容量时萃取剂的使用量仅为正十二烷体系的10%左右,大幅降低了萃取剂的使用量。Turgis 等[26]在用三氧化三膦(TPO)−[C2C4Pip]NTf2分离稀土元素的研究中,得出了同样的结论。斜率法表明在CMPO−[C4mim]PF6萃取体系中形成的萃合物为Ln3+·3(CMPO),平衡实验进一步证实稀土元素是以离子交换的形式进入到有机相中的,见式(1)[24−25]
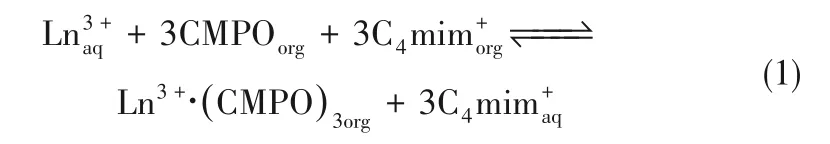
从式(1)可以看出,[C4mim]PF6除作为稀释剂起到溶解稀释的作用外,还通过离子交换过程参与萃取反应从而促进稀土元素的萃取分离,在一定程度上起到协萃剂的作用,这与分子溶剂的作用明显不同。Kubota 等[18,27]、Sun 等[28]、Shen 等[29]、Zhao 等[30]、Rout 等[31]的研究均支持这一观点。因而,该类离子液体对萃取过程的强化作用受两方面的影响最为显著:(1)阳离子的交换能力;(2)对萃取剂及萃合物的溶解能力。另外,离子液体的阴离子种类以及水相中阴离子种类与浓度也影响该萃取体系对稀土元素的分离能力。
阳离子的交换能力与其亲水性有关,而后者直接受咪唑烷烃基团链长的影响。一般来说,亲水性强的阳离子促进离子交换,疏水性强的阳离子抑制离子交换。Shimojo 等[32]考察了以N,N,N',N'−四辛基−3−氧戊二酰胺(TODGA)为萃取剂、[Cnmim]NTf2(n=2,4,6)为稀释剂的体系对Eu3+的萃取效果,结果表明体系萃取能力遵循[C2mim]NTf2>[C4mim]NTf2>[C6mim]NTf2。以[Cnmim]NTf2(n=2,4,6,8,10,12)为稀释剂、N,N−二辛基二甘醇酰胺(DODGAA)[18,27]、P204[28]、甲基咪唑(1−Mim)[29]和2,6−二[(5,6−二异己烷基)−1,2,4−三嗪−3−基]−吡啶(isohexyl−BTP)[30]为萃取剂进行稀土元素萃取分离时,得到同样的结论,即随着咪唑烷基链长的增加,离子液体体系对稀土萃取能力降低。阳离子烷基链长的增加将抑制离子交换过程,当稀释剂[Cnmim]NTf2在n≥10 时,萃取体系对稀土元素萃取的促进效果基本消失[18,27−28,31],萃取机理也趋同于分子溶剂体系[30,33]。在TPO−[C2C4Pip]/[C2C8Pip]NTf2[26]和三烷基氧化膦(Cyanex923)−[P66614]/[N1888]NTf2[31]萃取体系中得到类似的结论,研究还显示不同稀释剂中Cyanex923 对Nd 的 萃 取 能 力 遵 循[N1444]NTf2>[C4mim]NTf2>[N1888]NTf2>[P66614]NTf2≈[C10mim]NTf2[31]。
咪唑类离子液体对萃取剂及萃合物的溶解能力受萃取剂类型影响显著。作为成熟的工业化萃取剂,P204 在离子液体中的应用也受到关注。Sun等[28]以P204 为萃取剂、[Cnmim]NTf2(n=4,6,8,10)或[Cnmim]BETI(n=4,6,8,10)为稀释剂进行稀土元素萃取分离的研究,结果表明P204−[Cnmim]NTf2/BETI(n=4,6,8)体系对轻稀土和重稀土的萃取效率和分离能力均明显提高。但受到P204 在离子液体中溶解度的限制,这一体系仅可在极低浓度范围适用。即使在疏水性较强的[C10mim]NTf2中,P204的溶解度最大仅为40 mmol/L,过量的P204 将使萃取体系形成三相体系[34−35]。由于工业应用中稀土元素浓度达到1~1.5 mol/L,该萃取体系显然不能满足这一要求。Sun 等[35]、Baba 等[36]采用P507−[C12mim]NTf2体系进行稀土元素的萃取分离,其结果也证明了这一观点。CMPO、Cyanex923、TODGA、噻吩甲酰三氟丙酮(Htta)、isohexyl−BTP、1−Mim 以及DODGAA 等在咪唑类离子液体中的溶解性好因而取得较好的萃取效果。另外,Sun 等[37]、Rout 等[38]的研究表明对萃合物的相似相溶性强于分子溶剂是咪唑类离子液体强化萃取过程的另一重要原因。
一般认为,离子液体阴离子对咪唑类离子液体体系萃取性能的影响与其阳离子趋势相反,即疏水性强的阴离子有利于提高稀土元素的萃取效率[31,39]。然而情况也有例外,Baba 等[36]、Turanov 等[40]研究表明稀土元素在CMPO−[C4mim]NTf2体系中的萃取效率明显高于CMPO−[C4mim]PF6体系,主要原因是NTf2−的亲水性强于PF6−[40]。水相中阴离子对咪唑类离子液体萃取体系的行为和性能也有一定的影响,而且阳离子疏水性越强的离子液体萃取体系受影响越大。比如,在硝酸稀土体系中,增加水相中硝酸钠的浓度可明显增加Cyanex923−[P66614]/[N1888]/ [C10mim]NTf2体系对Nd3+的萃取能力,但不影响Cyanex923−[N1444]/[C4mim]NTf2体系对Nd3+的萃取效率[31],原因在于前三种体系中离子液体疏水性强,萃取过程倾向于从水相中萃取含硝酸根的缔合离子,从而增加水相中的硝酸根浓度有助于提高萃取效率。后两种体系因阳离子亲水性强使得萃取通过阳离子交换进行,水相中的阴离子不参与萃取过程因而其浓度变化不影响萃取效果。氯化稀土体系的情况与此相似,氯离子亲水性强,与稀土离子缔合能力弱,萃取时不易进入萃取相中,萃取过程倾向于阳离子交换形式,从而水相中氯离子浓度变化不影响咪唑类离子液体萃取体系对稀土元素的分离能力。
离子交换提高了萃取效率,但却造成了诸多不利后果:(1)离子液体的阳离子进入了水相,造成离子液体损失,无法有效实现离子液体的重复利用;(2)负载离子液体的洗脱困难,一些萃取剂在离子液体体系中的萃取过程不受酸浓度的影响,因而不易通过控制酸的浓度实现负载离子液体的洗脱。合理的萃取剂设计是解决上述问题的途径之一。Yang 等[41−42]发现以DODGAA 为萃取剂、[Cnmim]NTf2(n=4,8)为稀释剂的萃取体系对稀土元素的萃取机理与常规P507/P204 萃取体系相同,为质子交换机理,如式(2)所示
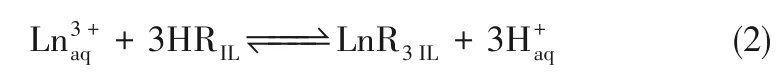
该萃取过程避免了离子液体阳离子进入水相,同时可通过调节酸浓度实现负载有机相的洗脱。DODGAA−[Cnmim]NTf2体系对稀土萃取顺序也与常规的P507/P204 萃取体系相近,且具有更高的萃取效率。Yin 等[43]则利用双(2,4,4−三甲基戊基)膦酸(Cyanex272)−[C8mim]PF6回收废旧荧光粉中的稀土元素,也取得了类似的效果。Sun 等[37]、Rout 等[38]的研究结果也表明以功能化离子液体为萃取剂时可以避免稀释剂[Cnmim]NTf2/BETI(n=4,6,8,10)发生离子交换。
非功能化离子液体为稀释剂的萃取体系,其对稀土元素的萃取机理除式(1)所示的阳离子交换机理和式(2)所示的质子交换机理外,还有一种阴离子交换机理,但这种机理报道较少。Jensen 课题组[21,44]在使用Htta−[C4mim]NTf2体系萃取分离Nd3+和Eu3+的研究中发现,萃取过程发生了NTf2−与形成的萃合物Ln(tta)4−的阴离子交换,具体见式(3)
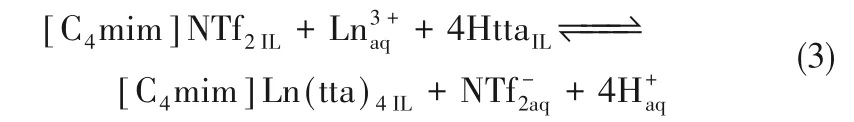
显然这种情况也导致离子液体无法有效重复利用的问题。这一机理产生的深层原因尚待进一步研究,但实际应用中应避免这一糟糕情形的发生。有效的方法之一是降低有机相中萃取剂的浓度,他们发现阴离子交换机理仅在Htta 浓度较高的情形下发生。当Htta 的浓度较低时,萃取过程按照类似于式(2)所示的质子交换机理进行[44]。除此之外,选择水相中溶解度低的阴离子有助于抑制萃取过程发生阴离子交换,相比NTf2−,NfO−则是更佳的选择。
以上三种萃取过程,目前以阳离子交换机理最为常见,该过程萃取效率高,但面临离子液体如何重复利用的问题,阴离子交换机理面临同样的问题。质子交换机理可以避免离子液体的损失和负载离子液体洗脱困难的问题,因而是开发以非功能化离子液体为稀释剂的萃取体系的重点方向。除促进稀土元素的萃取效率外,非功能化离子液体为稀释剂也可提高某些稀土元素的分离系数[31,41−42]。但总体来看非功能化离子液体为稀释剂的萃取体系对相邻稀土元素的分离系数仍然偏低,因而目前该类体系主要适用于轻稀土/重稀土或稀土与其他元素的分离。
除上述热力学方面的差异外,非功能化离子液体作为稀释剂与传统分子溶剂在萃取动力学上差异明显。Turgis 等[26]和Shen 等[29]的研究表明采用离子液体为稀释剂时萃取平衡时间为10 min,比采用常规分子溶剂二甲苯醚时增加一倍,主要原因在于离子液体的黏度比分子溶剂大,萃取过程受扩散过程影响显著,因而通常需提高萃取过程的温度以提高萃取速率。除黏度外,离子液体的密度、胶束特性、亲水性也影响萃取速率。Rout 等[31]以Cyanex 923 为萃取剂分离稀土元素时发现,不同离子液体稀释剂中的萃取平衡时间次序为:[P66614]NTf2>[N1444]NTf2>[C4mim]NTf2,与亲水性次序相反,说明稀释剂亲水性越强,萃取体系达到萃取平衡的时间越短。
1.2 非功能化离子液体作为萃取剂
由于结构形式的特殊性,非功能化离子液体除作为稀释剂与其他萃取剂混合使用外,还可以单独使用,以纯的单一离子液体萃取分离稀土元素。最早报道的是用[C8mim]PF6分离含Th4+和Ln3+的硝酸体系中Ce4+[45]。该离子液体对Ce4+/Th4+的分离系数与2−乙基己基膦酸二(2−乙基己基)酯(DEHEHP)−正己烷体系相近,且对Ce4+的萃取效率随水相中硝酸浓度的增加而增大,硝酸浓度为3.5 mol/L 时的单级萃取效率达到80%。机理研究结果表明Ce4+的萃取效率不受水相中[C8mim]Cl 浓度的影响,但随水相中KPF6浓度的增加而降低,进一步研究表明水相中形成了易与[C8mim]+结合的配合离子Ce(NO3)62−,并在萃取过程中与PF6−进行了阴离子交换,通过斜率法确定了萃取反应方程如式(4)所示。Gras 等[46]利用[C1C4Pyrr]NTf2和[P66614]NTf2萃取分离稀土元素也得到类似的结果。
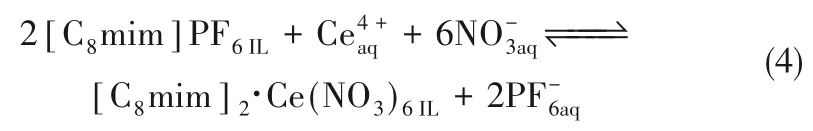
[C8mim]PF6对Ce4+的分离效果较好,但由于对Ln3+形成的萃合物Ln(NO3)nx−溶解性差而不能用于Ln3+的分离。另外,该萃取过程中向水相中释放易降解的P离子,不利于该体系的应用[47]。与该类离子液体作为稀释剂的情况类似,在强化萃取过程的同时避免离子交换造成的离子液体损失是研究的重点方向。
近年来,以季铵盐、季膦盐等为阳离子,NO3−或SCN−等无机离子为阴离子的非功能化离子液体作为萃取剂用于稀土元素的分离逐渐受到关注。Binnemans 等[48]报道了通过阴离子分割萃取方法(split−anion extraction),以[A336]SCN 或[P66614]SCN为萃取剂分离高浓度混合氯化稀土。如图1 所示,研究结果表明[P66614]SCN 对相邻稀土元素具有更高的分离因子,水相中MgCl2浓度为4 mol/L 时的饱和萃取容量在0.14 ~0.26 mol/L之间(不同稀土元素有变化),而[A336]SCN 对相邻元素的分配系数和饱和容量相对更高。该萃取机理如式(5)所示(以[P66614]SCN 为例),即为离子对萃取机理。随后该课题组[49]将[P66614]SCN 成功用于回收废旧荧光粉浸取液中Y和Eu,并取得了类似结果。
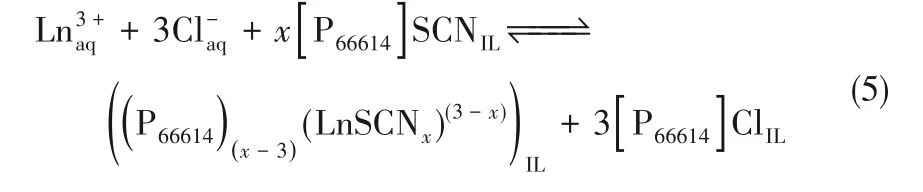
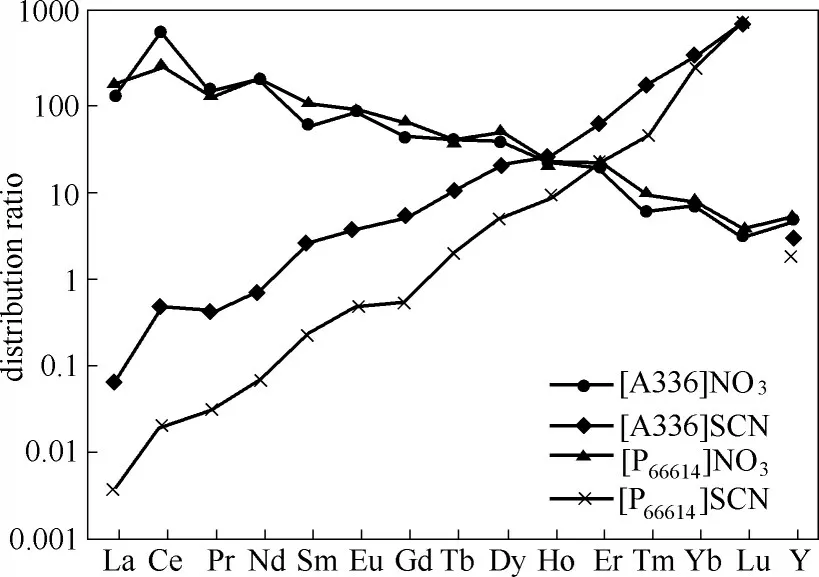
图1 [A336]/[P66614]SCN和[A336]/[P66614]NO3离子液体纯体系对稀土元素的萃取分配系数[48]Fig.1 Distribution ratio of REs by pure[A336]/[P66614]SCN and[A336]/[P66614]NO3 extraction system[48]
这一萃取体系和方法基于霍夫梅斯特序列建立,原理如图2。该方法与传统萃取过程相比具有明显的技术优势[48,50]:(1)对稀土元素的萃取能力受控于水相中氯盐的浓度,并随其浓度的增加而增大,因而可通过改变水相中的氯盐浓度完成稀土元素的萃取和洗脱,从而避免了传统萃取体系因受控于pH 而需要皂化/酸洗的缺陷;(2)离子液体既作为萃取剂也作为稀释剂,不需煤油等分子溶剂,安全性高;(3)适用于高浓度氯化稀土的分离。这一研究为离子液体萃取分离稀土提供了新思路,但这两种离子液体对轻稀土的分配系数偏低,且SCN−不稳定、易降解、有一定毒性,离绿色萃取体系的要求还有一定差距。
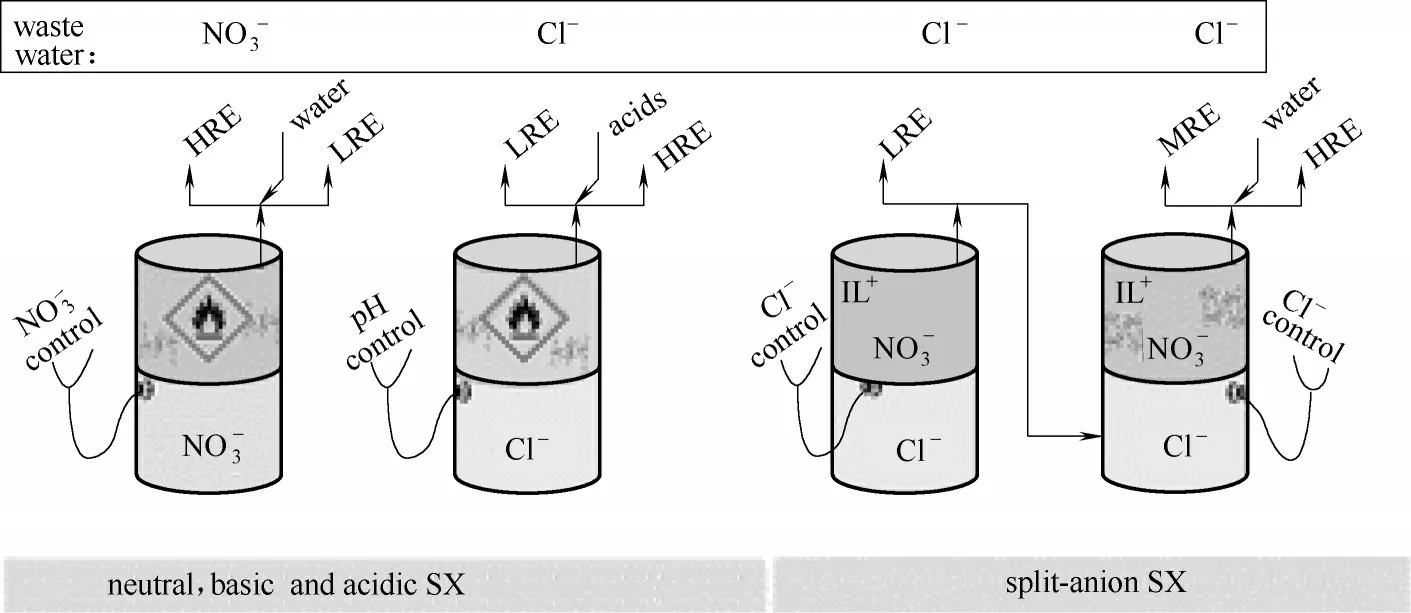
图2 阴离子分割萃取技术原理[50]Fig.2 Basic principle of split−anion extraction[50]
以NO3−为阴离子的季铵盐/季膦盐离子液体可避免这一缺陷,而且这类离子液体对轻稀土和中稀土具有更高的分配系数(图1),但对稀土元素的分离系数却远低于相应的SCN−类离子液体[48]。研究显示,该类离子液体对稀土元素呈现逆序萃取,即优先萃取分子量小的轻稀土,这说明硝酸季铵盐或季膦盐离子液体与稀土离子的相互作用随稀土元素原子序数增加而减弱,因而,通过在水相中添加络合剂如乙二胺四乙酸(EDTA)或二乙烯三胺五乙酸(DTPA)可增大相邻稀土元素间的分离因子。Kumari 等[51]在pH 为3、[NO3−]为6 mol/L 的水相中添加0.003 mol/L 的EDTA,以0.43 mol/L [A336]NO3+10%异癸醇为萃取剂、煤油为稀释剂,将Pr/Nd 的分离系数由未添加EDTA 时的1.8 增加到2.9,Larsson等[48]在[NO3−]为11 mol/L 的水相中添加0.2 mol/L EDTA、使用纯[A336]NO3为萃取剂时得到Pr/Nd 的分离系数达到13。Wang 等[52]则基于这一原理建立了动力学分离方法,使Pr/Nd 的分离系数增加到21.7。这些研究证明[A336]NO3用于轻稀土分离具有良好的前景。Sun等[53]进一步开展了[A336]NO3对稀土元素Pr 的萃取机理研究,通过斜率法和分子模拟分析认为萃取过程通过式(6)进行,式中X−代表Br−、NO3−或SCN−。Hunter 等[54]通过电 喷 雾质谱法(ESI−MS)分析证明有机相中存在[A336]2Ln(NO3)5−,这一点与式(6)中X−为NO3−时的结果一致。
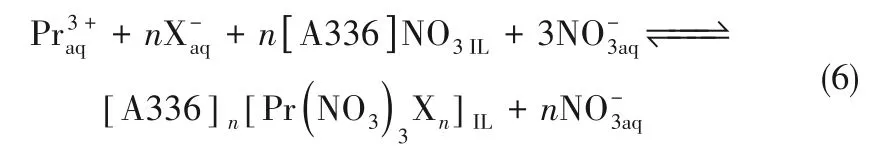
1.3 非功能化离子液体作为协萃剂
非功能化离子液体作为协萃剂,与常规的萃取剂(DEHEHP,Cyanex923,P507 等)组合协同萃取稀土元素也是研究的热点之一。与作为稀释剂的非功能化离子液体不同,作为协萃剂的非功能化离子液体通过促进萃取络合物的形成来强化稀土元素分离,而且在这一过程中不发生离子交换从而可以避免离子液体损失。Zuo 等[47]发现,与传统DEHEHP−正己烷体系或[C8mim]PF6纯体系相比,DEHEHP−[C8mim]PF6萃取体系对Ce4+的萃取效率更高。该萃取体系中起到萃取剂作用的主要是DEHEHP。研究显示该过程的萃取机理为离子对萃取,如式(7)所示,不同于[C8mim]PF6纯体系的阴离子交换过程[式(4)],从而避免了PF6−离子进入水相导致离子液体无法有效重复利用的问题。
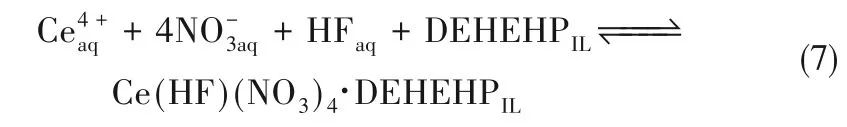
Zhu等[55]研究了DEHEHP−[A336]NO3萃取体系对硝酸稀土体系中稀土元素的分离能力,结果表明该体系对轻稀土(La−Eu)具有很好的萃取效率,对重稀土(Gd−Lu和Y)则显现出反协同作用,这一结果说明该体系可用于轻稀土与重稀土的分离。以Pr 为例,当[A336]NO3的体积比为40%时体系的协同系数最大为3.44。Zhu等[55]认为DEHEHP的存在促进了中性萃合物[Pr(NO3)3·xDEHEHP和[A336]y·Pr(NO3)3+y]的形成并有利于提高两种萃合物在有机相中的溶解性能,斜率法和红外分析对萃合物研究均确认了这一点。这一结果也表明该体系的萃取过程不发生离子交换,因此无离子液体损失。Zhu等[55]进一步研究了该体系对Pr的萃取动力学,与1.1节讨论一致,黏度仍然是影响该体系萃取动力学的重要因素,研究结果表明,将温度由25℃提高至45℃时,萃取平衡时间将由10 min降至5 min。回归得到萃取活化能为39.95 kJ/mol,说明该萃取过程受化学反应控制。Xiong等[56]利用DEHEHP−[P66614]Cl萃取体系得到类似的效果,但获得更高分配系数和萃取容量。研究显示DEHEHP−[P66614]Cl体系的萃取容量高达0.78 mol/L,远高于工业体系P507−煤油的萃取容量(0.18 ~0.2 mol/L)。Zhao 等[57]则对比了DEHEHP−[P66614]NO3、DEHEHP−[A336]NO3、DEHEHP−[P66614]Cl三种体系对稀土元素与其他金属的分离能力,结果表明DEHEHP−[P66614]NO3体系对稀土元素的萃取和分离性能更优,并将该体系应用于废旧荧光粉中稀土元素的回收和分离。
Regadío 等[50]基于阴离子分割萃取方法(split−anion extraction)研 究 了Cyanex923−[A336]NO3和Cyanex923−[P66614]NO3两种萃取体系对稀土元素的分离性能。Cyanex923 可以强化离子液体对稀土的萃取能力:一方面,Cyanex923 的加入使有机相对稀土元素的萃取顺序由优先萃取轻稀土转变为优先萃取重稀土;另一方面,Cyanex923 的加入使所有稀土元素在有机相中的分配系数和萃取容量增加。Cyanex923−[P66614]NO3体 系 中 的Cyanex923 含 量 为20%和80%时,稀土元素的饱和萃取容量分别为0.22 mol/L 和0.35 mol/L。萃取机理分析结果表明,随有机相中Cyanex923 含量的增加萃合物由[Ln(NO3)5]2−(Cyanex923=0)到[Ln(H2O)x]3+(Cyanex923=25%)再 到Ln(NO3)3·3Cyanex923(Cyanex923≥50%)变迁。另外,水相中盐析剂氯化钙的浓度对萃取体系的萃取容量和分离系数也有显著影响,这也是负载有机相中的稀土元素可以通过水洗洗脱的关键。总体上看,这两种萃取体系对稀土元素的分离系数与传统酸性萃取体系基本一致,但具有萃取/洗脱不受pH 控制、酸碱耗量低、操作成本低、环境污染小的优势。另外,该研究还表明,协萃剂Cyanex923 有助于降低萃取体系的黏度,从而提高萃取速率。
Sun等[35]利用常规的工业萃取剂P507与[N1444]NO3构筑协同萃取体系以强化稀土元素间的分离。这一体系的构筑思路与在水相中添加络合剂一致,即通过不同相中的萃取剂/络合剂与稀土元素相互作用的差异增加相邻稀土元素间的分离系数。这一体系中P507 对重稀土的作用更强,而[N1444]NO3对轻稀土的作用更强。由于P507 与[N1444]NO3互不相溶,萃取完成后轻元素留在离子液体相中,而重元素则进入P507 相中。该体系对Pr/Nd 的分离系数达到3.5 以上,接近常规P507 体系的2.5 倍,该体系也适合其他稀土元素间的分离。该研究为非功能化离子液体在稀土分离中的应用提供了新方法,但基于三相萃取体系,导致萃取过程更加复杂。
2 功能化离子液体
功能化离子液体是含有P O、C O 等功能基团的离子液体,在萃取体系中起到萃取剂或协萃剂的作用,近年来用于稀土萃取分离的功能化离子液体主要包括磷酸酯/亚磷酸/次磷酸类离子液体、羧酸类离子液体以及一些带有类似功能基团的其他离子液体。由于功能化离子液体具有较高的黏度,需采用分子溶剂或非功能化离子液体作为稀释剂开展萃取分离稀土的研究。即便如此,功能化离子液体体系所需萃取平衡时间依旧较长,通常需30~60 min。
2.1 功能化离子液体作为单一萃取剂
2.1.1 磷酸酯类离子液体(P204 类) P204 是工业上广泛应用的萃取剂之一,具有两个酯基链,给电子能力强,增加了P O基团与稀土离子间的相互作用能力。然而,随着稀土元素的原子序数的增加,其负载有机相的反萃越来越困难,尤其是重稀土负载相极难洗脱。工业上主要用其分离轻稀土,并通过皂化来获得更高的萃取容量,从而产生了大量的氨氮废水。因此,将P204合成为绿色的功能化离子液体萃取剂一直是研究的热点方向。
P204 基功能化离子液体的阴离子和阳离子均参与萃合物的形成,避免了萃取过程发生离子交换,在萃取过程中无离子液体损失[38,58]。而且在萃取过程中,该功能化离子液体的阴离子和阳离子起到较强的内协同作用,使分配系数明显增大[58]。Rout 等[38]研 究 了[C6mim]P204、[C1C6Pyrr]P204 及[N4444]P204 对硝酸体系中Nd3+的萃取分离效果,在优化条件下,[C6mim]P204−[N1444]NTf2体系对Nd3+的分配系数达到103,远高于在非功能化离子液体[C6mim]NTf2纯体系中的分配系数(约10−2)。Sun 等[5]利用[A336]P204 分离硝酸体系中的Eu3+,结果表明,该功能化离子液体对Eu3+的分配系数远高于P204及[A336]Cl−P204体系,通过斜率法分析得出萃取机理如式(8)所示,萃取配位原理示意图如图3所示。
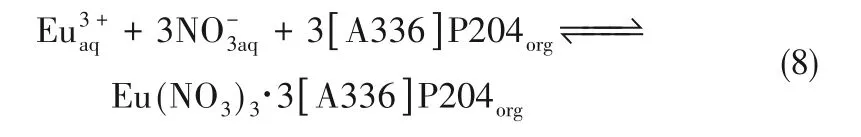
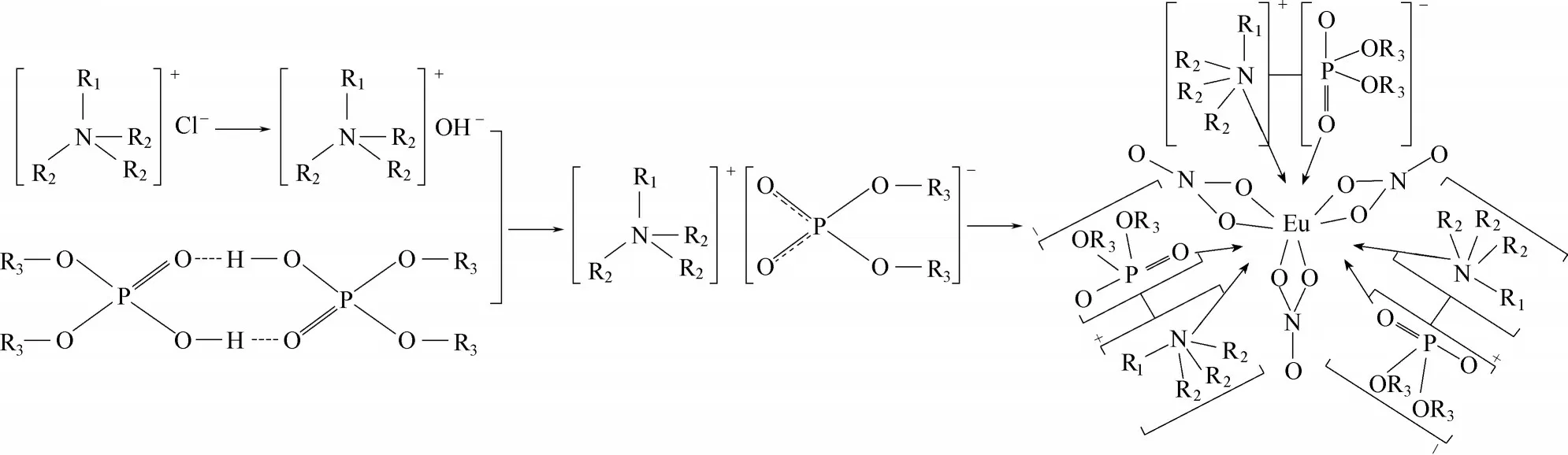
图3 P204基功能化离子液体及其与稀土元素Eu3+的络合配位方式[58]Fig.3 P204−based functional IL and its coordination with Eu3+during extraction[58]
P204 基功能化离子液体中阳离子还影响萃取剂对稀土元素的分离系数。Sun 等[59]合成了[N4444]P204、[N1888]P204 以及[P66614]P204 萃取剂,并分别以[C6mim]NTf2和对二异丙苯为稀释剂考察了从含1 mol/L 羟基乙酸、0.1 mol/L DTPA 的水溶液中分离稀土元素的效果,结果表明,由于阳离子的空间位阻效应,三种离子液体的分离系数均高于P204。深入的研究表明阳离子尺寸对P204 基功能化离子液体的萃取和分离性能影响明显。Sun 等[60]进一步研究了[N2222]P204、[N4444]P204、[N6666]P204、[N8888]P204以及[N1888]P204 在稀释剂[C10mim]NTf2/BETI 中对硝酸稀土混合物的萃取效果,结果表明上述五种P204基功能化离子液体对稀土元素的分配系数和分离系数随阳离子尺寸增大而变小,以[N2222]P204效果最优。Sun 等[14]研 究 了 正 庚 烷 中[N2222]P204、[N4444]P204、[N6666]P204 以及[N8888]P204 对5 种氯化稀土的分离效果,结果表明,阳离子对分配系数的强化能力与上述结果类似,即分配系数遵循[N2222]+>[N4444]+>[N6666]+>[N8888]+,但分离系数次序为[N2222]+<[N4444]+<[N8888]+<[N6666]+,与非功能化离子液体为稀释剂时的顺序相反,说明稀释剂影响P204基功能化离子液体对稀土元素的分离系数。不仅如此,P204 基功能化离子液体对稀土元素的分配系数也受到稀释剂的影响。比如,[N4444]/[N1888]/[P66614]P204 三种萃取剂对稀土元素的分配系数在[C6mim]NTf2中均高于在对二异丙苯中[59],原因在于离子液体萃合物与非功能化离子液体稀释剂的相似相溶性更强。Sun等[37]还研究了以[N1888]P204 为萃取剂、[Cnmim]NTf2/BETI(n=4,6,8,10)为稀释剂对稀土元素的分离性能,结果表明稀释剂阴离子相同时阳离子链长的增加对[N1888]P204 的萃取效果没有明显影响。而阳离子相同时,[N1888]P204−[Cnmim]BETI 对稀土元素的分配系数和分离系数均高于[N1888]P204−[Cnmim]NTf2。水溶液中阴离子也影响P204 基功能化离子液体的萃取性能,以[A336]P204 为例,Guo 等[20]研究表明该离子液体适合于硝酸体系中重稀土元素间的分离,或氯化物体系中轻稀土元素的分离,但由于分子量大,使得其萃取容量低于P204。
2.1.2 亚磷酸酯类离子液体(P507 类) P507 是另一种工业上常用的稀土分离萃取剂,因只含有1 个酯基链,使其与重稀土离子结合能力较P204明显减弱,从而使负载相中的稀土元素更容易洗脱,在中、重稀土分离中应用广泛,然而其洗脱酸度仍然高达6 mol/L。将P507合成为功能化离子液体后,负载相中稀土元素的洗脱性能可得到明显的改善,Sun等[14]以及Dong 等[61]的研究均证实了此观点。Dutta 等[62]研究表明[N1888]P507负载相中的Gd用50℃的去离子水洗脱的单级效率达到47%,Quinn 等[63−64]研究表明在工业浓度条件下[A336]P507可使负载相的洗脱酸度大幅降低达50%~60%(即酸浓度在3 mol/L 以下),因而推荐用于重稀土的萃取分离。
与P507 相比,P507 基功能化离子液体在稀土元素的萃取和分离能力上也有所改善。一方面,功能化离子液体可避免P507 作为萃取剂时因氢键作用而形成二聚体(图3);另一方面,该类离子液体的阴离子和阳离子间具有明显的内协同效应从而强化其萃取性能。如图4 所示,在硝酸稀土体系中[A336]P507对Eu3+的内协同效应高于[A336]P204,在氯化稀土体系中虽然内协同效应低于[A336]P204,却具有更高的分配系数[58]。Dong等[61]利用[N1888]P507对氯化稀土体系中的重稀土进行萃取分离,结果表明[N1888]P507 对重稀土元素的分配系数高于P507,也高于P507−[N1888]Br 体系,但分离效率基本与这两种体系相近。Sun等[14]对比了[N2222]P507和[N2222]P204在盐酸体系中对La、Nd、Eu、Dy、Er 五种稀土元素的萃取分离效果,结果表明[N2222]P507对稀土的分离效率高于[N2222]P204,但分配系数仅是后者的50%左右。Guo 等[20]对[A336]P507 分离14 种稀土元素的分离系数的研究表明,[A336]P507 适合于硝酸稀土体系中的重稀土元素间的分离,或氯化稀土体系中的轻稀土元素的分离(图5),这与[A336]P204 的性能一致,但Quinn等[64]认为功能化离子液体[A336]P507的萃取容量小于其前体,因而不推荐用于轻稀土的萃取分离。Guo 等[20]得到[A336]P507 在硝酸体系中对 稀 土 元 素 的 平 均 分 离 系 数β̅βz+1/z̅ 为3.61,与[A336]P204的3.67相近,而在盐酸体系中为2.75,略高于[A336]P204 的2.59。Quinn 等[64]得到结果显示[A336]P507 对稀土的分离因子略低于P507。Shen等[65]研究表明[A336]P507 还适合于硫酸体系中的中、重稀土元素进行萃取分离。
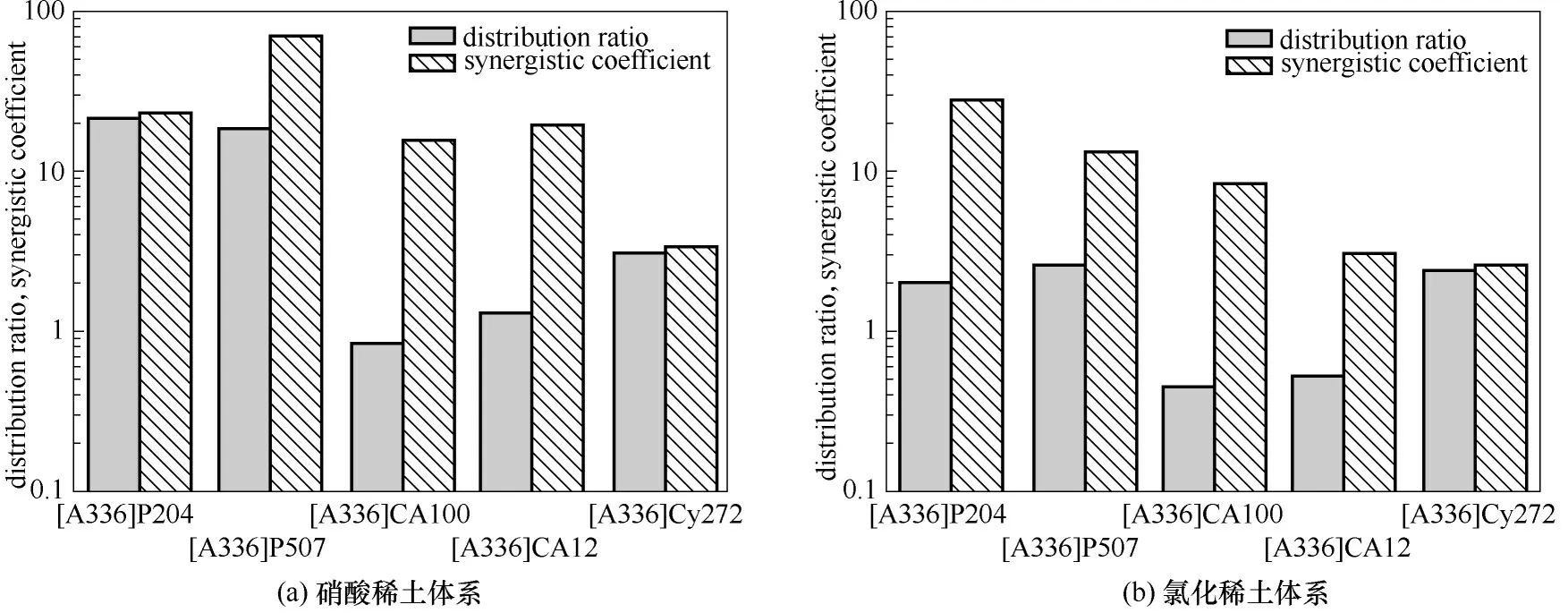
图4 不同萃取剂对Eu3+的分配系数和协同系数[58]Fig.4 Effect of extractant on the distribution ratio and synergistic coefficient of Eu3+[58]
Sun等[14]以及Dutta等[62]发现P507基功能化离子液体萃取重稀土的机理与式(8)相似。然而,Quinn等[63−64]采用[A336]P507 萃取分离氯化稀土体系中的重稀土元素,为该萃取机理提供了新的认识。Quinn等[63−64]发现功能化离子液体萃取稀土离子过程伴随着质子萃取。一方面,与P507 相比,由于[A336]+和P507−的相互作用使离子液体可在更低的pH 条件下分离水相中HCl;另一方面,水相中Cl−浓度的增加可使[A336]P507 萃取HCl 的pH 向更高处转移。该结果说明离子液体在氯化稀土体系中萃取过程的机理为表观上的离子对萃取机理和实质上离子交换机理的复杂过程,如式(9)所示,式中0<n<3。该结果也表明P507 基功能化离子液体的洗脱和再生过程可以与常规的方式一样通过酸洗和碱洗再生进行。
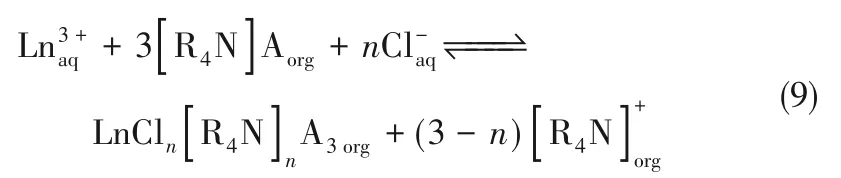
2.1.3 次磷酸酯类离子液体(Cyanex272/P227类)相比P204 和P507,Cyanex272 对稀土元素的分离系数最大,但萃取容量小、易乳化的缺点限制了其工业应用,开发Cyanex272 基功能化离子液体是解决这一问题的路径之一。 Padhan 等[66]利用[A336]Cyanex272 萃取分离Pr/Nd,结果表明对这两稀土元素的萃取效率大小次序为[A336]Cyanex272 >[A336]P204 >P204 >>Cyanex272 >A336。拉曼光谱分析结果表明阴离子中的P O 和阳离子中的C—N 均参与了萃合物的形成,这也是Sun 等[58]提出的内协同效应的基础。 Kumari 等[67]合成了[P66614]Cyanex272并用于稀土元素的萃取分离,与Cyanex272相比,[P66614]Cyanex272对所有稀土元素均具有更高的萃取效率,并对轻稀土具有更高的分离系数,但对重稀土的分离系数更小,几乎无分离效果。Sun等[60]则合成了[N2222]Cyanex272和[N2222]Cyanex301两种功能化离子液体,但二者对稀土元素的萃取能力和分离系数均小于[N2222]P204,这说明Cyanex272 基功能化离子液体对稀土元素的萃取能力受阳离子影响。
阴离子上的功能基团也影响此类离子液体对稀土元素的萃取性能,含P O基团的萃取剂相比含P S 基团的萃取剂更易于与稀土元素形成稳定的萃取物。Belova 等[68]发现不论在氯化稀土体系还是硝酸稀土体系中,该类离子液体对稀土的分配系数大小次序为[N1888]Cyanex272 >[N1888]Cyanex302 >[N1888]Cyanex301。Sun 等[60]的研究结果与此一致。萃取机理研究表明在氯化稀土体系中按照式(9)进行,而在硝酸稀土体系中,则按照式(8)进行,且萃取容量更高。
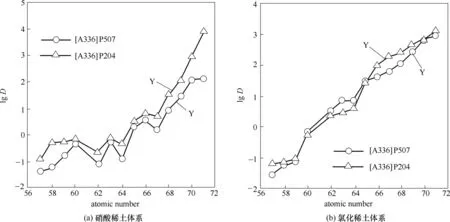
图5 稀土元素在不同萃取体系中的分配系数[20]Fig.5 Relationship between the distribution ratio and atomic number of RE(Ⅲ)[20]
Cyanex572是Cyanex272和P507的混合物,Pavón等[69]利用Cyanex572合成了[Premene 81R]Cyanex572功能化离子液体,并进行了Nd、Dy、Tb萃取分离的研究。结果表明,随溶液中Cl−浓度的增加该离子液体对稀土元素的萃取效率降低、分离系数增加,并在c(Cl−)=4 mol/L 时趋于稳定,负载相可用4 mol/L 盐酸洗脱,低于工业洗脱酸度。Chen 等[70]研究了[A336]P227 对重稀土尤其是钇的萃取分离,结果表明,此萃取剂对硝酸稀土体系中的钇具有良好的分离能力,并进一步基于[A336]P227 建立了膜分离方法以减少萃取过程中离子液体的用量。
2.1.4 环烷酸类离子液体(CA12/CA100 类) 环烷酸是一种羧酸类萃取剂,在工业上常用于Y 与重稀土的分离。因而,开发环烷酸类离子液体萃取剂也是 研 究 的 热 点。Wang 等[71]利 用[A336]CA12 和[A336]CA100 对氯化稀土体系中的稀土元素进行萃取分离,结果表明[A336]CA12 和[A336]CA100 对Y的萃取效率高于常规萃取剂仲辛基苯氧基乙酸(CA12)、仲壬基苯氧基乙酸(CA100)、磷酸三丁酯(TBP)以及甲基磷酸二甲庚酯(P350),这同样可归功于该类离子液体的内协同效应[58]。[A336]CA12和[A336]CA100 对稀土元素的萃取分离总体趋势一致,后者具有更高的分配系数,而前者的分离系数更高,尤其对La的分离系数达到6,因而[A336]CA12可用于La与其他元素的分离。机理研究表明,萃取机理与式(8)类似,不过离子液体的配合数为4,这也是其萃取容量低的原因之一。Wang 等[72]进一步研究了两者对硝酸稀土体系中La的萃取分离性能,结果与氯化稀土体系基本一致,斜率法结果表明萃合物中离子液体配合数为2,说明在硝酸稀土体系中La的萃取容量高于氯化稀土体系,机理研究显示萃取过程为类似式(9)的复杂过程。
阳离子带有[N1888]+和[P66614]+的CA12 基功能化离子液体用于氯化稀土体系中Y与其他重稀土元素的分离也受到关注。Dong 等[73]研究表明[P66614]CA12 对Y 的萃取能力高于CA12 及[P66614]Cl−CA12 体系,萃取序列为Lu >Yb >Tm >Er >Ho >Y,可实现Y 与其他重稀土的分离。Wang等[74]发现[N1888]CA12对重稀土/Y 的分配系数和分离因子高于CA12,但与[N1888]Cl−CA12 体系的分配系数和分离因子基本相同,说明[N1888]CA12 对重稀土元素的萃取无内协同效应。洗脱实验表明负载有机相可以用纯水洗脱,但在末端萃取体系乳化倾向明显。为避免乳化,Huang 等[75]采用纯水进行预洗脱,NaOH/Na2C2O4进行深度洗脱的策略,这无疑造成了洗脱过程的复杂性。另外,不论是[P66614]CA12 还是[N1888]CA12,在HCl 或NaOH 浓度大于1.2 mol/L 时均会发生化学转化生成它们的前体,不利于该类离子液体在稀土分离中的应用。
2.1.5 其他类型的功能化离子液体 在CA12 类离子液体的基础上,Sun 课题组通过在苯环上引入第二个羧酸基团设计了[P66614]2BDOAC[76]和[P66614]2IOPAA[77]两种功能化离子液体。与其他类型离子液体萃取剂不同,该类离子液体的阴离子可与稀土元素形成沉淀物,从而实现稀土元素的选择性分离,而且形成的沉淀物相比常规沉淀剂的颗粒尺寸大,易于后续处理。[P66614]2IOPAA 对稀土元素的萃取效率高于[P66614]CA12,萃取趋势与[P66614]CA12也基本一致。油酸类离子液体是另一类以长链烷烃脂肪酸根为阴离 子 的 羧 酸 功 能 化 离 子 液 体,Obón 等[78−79]采 用[A336]OL 萃取溶液中的Nd,结果表明,其萃取能力与P204 基功能化离子液体接近,而且不存在乳化现象。
Yang 等[80]研究了阴离子为双酮基的功能化离子液体([A336]TTA、[A336]TFA 和[A336]BTA)对稀土元素的萃取分离能力,发现这类离子液体同样具有内协同作用,且稀土元素的萃取效率较高,其分离系数亦大于[A336]CA12 和[A336]CA100,并推荐[A336]TTA 用于La3+与其他稀土元素的分离。Maria等[81]研究了阴离子同时具有羧酸基团和酰胺基团的功能化离子液体([N8888]DODGA、[C4mim]DEHOX 和[N8888]DEHOX)对稀土元素的萃取分离性能,并与[N8888]OL 离子液体的萃取结果进行对比,发现含有DEHOX−阴离子的离子液体对所有稀土元素的分离系数显著增加。相比其他几种离子液体,[N8888]DEHOX的萃取效率、分离效率和洗脱性能优势显著。Khodakarami 等[82]采用阴离子具有羧酸基团和酰胺基团的[A336]DHDGA 离子液体进行稀土元素的萃取分离研究,结果表明该离子液体可用于轻稀土与重稀土之间的分离。进一步将羧酸基团引入阳离子上制备了双功能化离子液体[OcGBOEt]DHDGA,该功能基团的添加提高了稀土元素的萃取效率、萃取速率以及洗脱性能,却使得分离系数明显降低。Chen等[83]则以阳离子含羧酸基团的[(CH2)nCOOHmin]NTf2(n = 3, 5, 7)为萃取剂、[Cnmim]NTf2(n = 4, 6, 8,10)为稀释剂构建了一种萃取体系,用于Sc3+与其他稀土元素的分离,研究表明通过调节pH 可使Sc3+与其他稀土元素的分离系数达到103。其中,[(CH2)7COOHmim]NTf2−[C4mim]NTf2萃 取 体 系 对Sc3+的萃取效率最高,单级萃取效率可达到99.5%。然而,该萃取机理为阳离子交换,导致离子液体损失。Guo 等[84]则设计合成了阳离子带有聚乙二醇(PEG)功能基团的咪唑类离子液体,即[PEG200(mim)2]/[PEG400(mim)2]/[PEG600(mim)2]NTf2,并用于稀土元素的分离和富集。由于该类离子液体的黏度低,纯体系可直接用于稀土元素的萃取分离,萃取能力大小顺序为[PEG600(mim)2]NTf2>[PEG400(mim)2]NTf2>[PEG200(mim)2]NTf2,与阳离子的亲水性呈正相关。而且,萃取过程为离子对萃取机理,无离子液体损失,但该类离子液体对稀土元素间的分离不具有选择性,只适用于稀土元素与其他金属离子间的分离。
2.2 功能化离子液体作为协萃剂
为进一步提高萃取性能,利用功能化离子液体与另一功能化离子液体、分子萃取剂或非功能化离子液体萃取剂构建协同萃取体系亦是热点的研究方向。
2.2.1 两种功能化离子液体协同萃取 Sun 等[85]报道了利用阳离子为[N2222]+、[N4444]+和[N8888]+,阴离子为P204−和P507−的六种功能化离子液体构筑协同萃取体系用于稀土元素的分离。在阳离子相同的情况下,任意P204 基功能化离子液体与P507 基功能化离子液体的混合体系对稀土元素均具有明显的协同萃取效应,尤其[N2222]P204−[N2222]P507 体系,其协同系数高于P204+P507 混合体系两个数量级左右,说明功能化离子液体有助于促进协同作用和提高稀土元素的分配系数。如图6 所示,混合体系的协同萃取系数大小次序为[N2222]P204−[N2222]P507 >[N4444]P204−[N4444]P507 >[N8888]P204−[N8888]P507,即阳离子上的烷基链越短,协同效应越强,说明阳离子的空间位阻制约协同作用。不同混合体系对稀土的分配系数大小顺序为:[N4444]P204−[N2222]P507 >[N8888]P204−[N2222]P507 > [N2222]P204−[N4444]P507 >[N2222]P204−[N8888]P507,分离系数的大小次序基本与此一致,即含有[N2222]P507的协同体系萃取能力和分离能力强于含有[N2222]P204的协同萃取体系。另外,仅[N4444]P204−[N2222]P507 体系对五种稀土元素(La、Nd、Eu、Dy、Er)均有协同萃取效果,其他体系则只对其中部分稀土元素有协同萃取能力。洗脱实验证明负载的稀土可以使用0.18 mol/L 的稀盐酸完全洗脱。
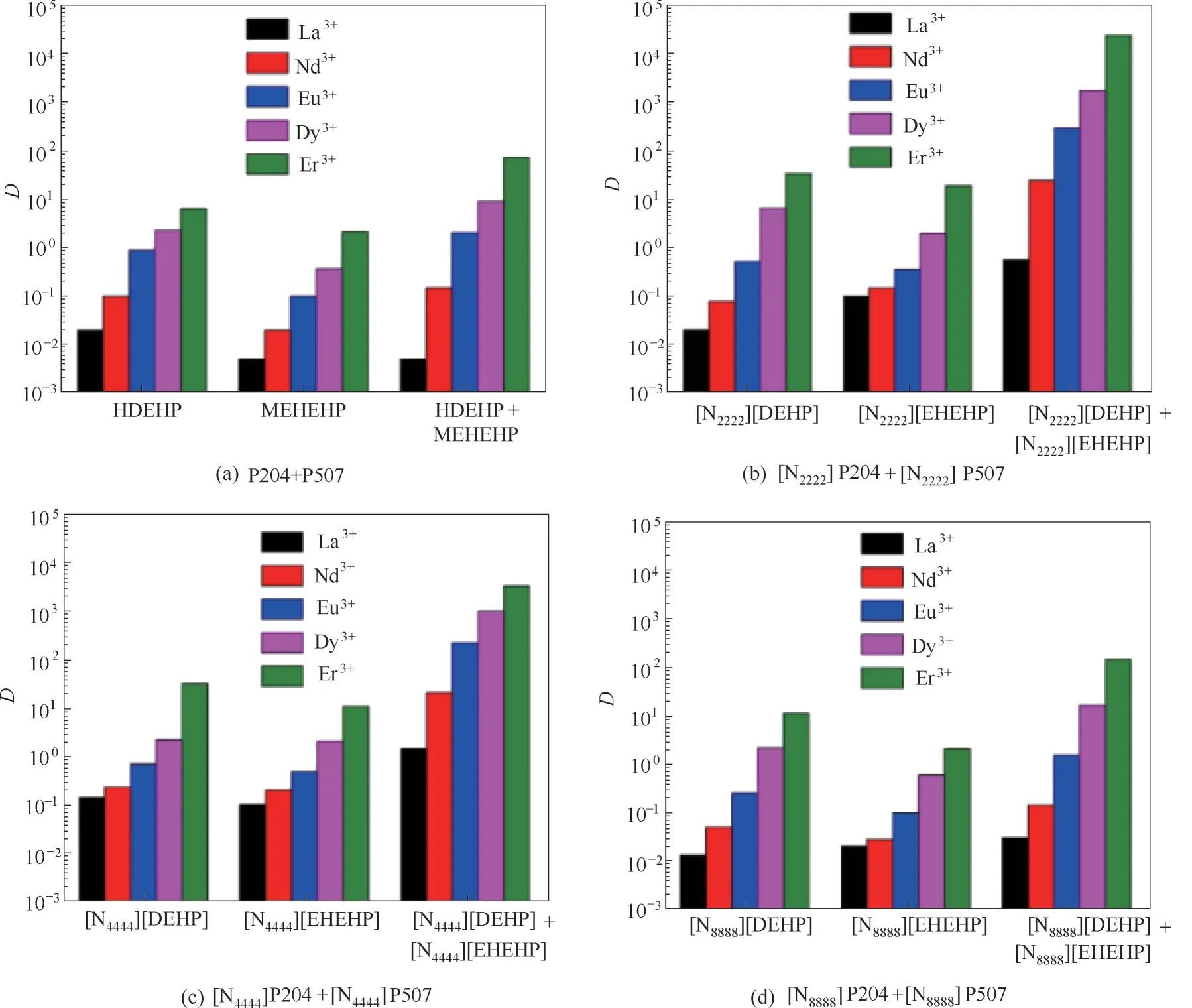
图6 稀土元素在不同萃取体系中的分配系数[85]Fig.6 The distribution ratios of REs extracted by different ILS[85]
之后,Sun等[86]又展开了以[N4444]+和[N1888]+为阳离子、P507−和Cyanex272−为阴离子的四种离子液体构筑协同萃取体系([P66614]P507 + [P66614]Cyanex272、[P66614]P507 + [N1888]Cyanex272、[P66614]Cyanex272 +[N1888]CA12 等)对重稀土元素的协同萃取研究,取得了与上述研究类似的结论。深入的机理研究显示萃取过程非常复杂,不仅在于协同萃取体系中的两个阴离子和两个阳离子均参与到萃取络合物中,而且不同离子液体组成的协同萃取体系或同一体系离子液体含量不同时形成萃取络合物均有所变化,研究显示[N4444]P507 + [N4444]Cyanex272 协同萃取体系中两者按照1∶1 参与了萃取络合物的形成,见式(10)[86],而[P66614]P507 和[N1888]Cyanex272组成的萃取体系中两者按照1∶3 的比例参与萃取络 合 物 的 形 成[87]。Dong 等[88]则 报 道 了[P66614]P507 和[P66614]Cyanex272 组成的协同萃取体系随其中[P66614]Cyanex272 浓度变化时萃取过程机理,显示在低浓度下[P66614]Cyanex272 与稀土离子按照1.5∶1 形成萃合物,而在高浓度下这一比例变为7.5∶1,而[P66614]P507与稀土离子在萃合物中的比例保持4.5∶1不变。
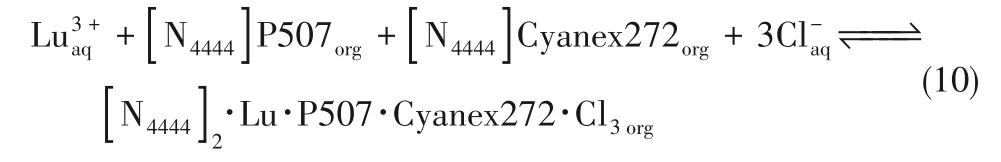
2.2.2 功能化离子液体与非功能化离子液体协同萃取 Rout 等[89−90]的研究显示功能化离子液体可与非功能化离子液体构成协同萃取体系。他们首先构筑了[P66614]MA−[P66614]NO3及[P66614]MA−[P66614]Cl 萃取体系[89],分别研究了硝酸稀土体系和氯化稀土体系中Eu3+的分离效果。结果表明,[P66614]MA−[P66614][NO3]体系在硝酸稀土体系中协同萃取效应显著,其对Eu3+的分配系数是MA−[P66614]NO3体系的103倍,可用于轻稀土元素间的分离或稀土/过渡金属的分离,而[P66614]MA−[P66614]Cl 体系的协同效应较弱。萃取动力学研究显示,上述两种体系的萃取平衡时间在1 h 左右,研究也表明在萃取前将上述体系与相应水溶液进行预饱和可有效降低有机相的黏度,从而提高萃取速率。之后他们又构筑了[A336]DGA−[A336]NO3体 系 用 于Nd 的 萃 取 分 离[90],该 体 系 在pH>2 时协同效应明显,这是由于[A336]NO3的存在强化了[A336]+与DGA−的协同作用。在pH<2 时[A336]DGA 优先萃取HNO3并转化为[A336]NO3及N,N−二辛基二甘醇酰胺酸(HDGA),导致该体系失去协同作用。同样,[A336]DGA−[A336]NO3体系对硝酸稀土体系中Nd3+的萃取效率远高于[A336]DGA−[A336]Cl 体系对氯化稀土中Nd3+的萃取效率,在盐析剂(NaNO3/NaCl)浓度均为1 mol/L 时,Nd3+在前一体系中的分配系数接近后者的200倍。负载相中的Nd3+可以通过0.5 mol/L 的硝酸完全洗脱。该体系对轻、中稀土均具有较好的分离性能,但仅从Ho/Yb的萃取效果看对重稀土分离性能不足。
2.2.3 功能化离子液体与分子萃取剂协同萃取Sun 等[91]将中性萃取剂Cyanex923 分别与[N2222]P507和[N2222]P204构成协同萃取体系,用于水相中稀土元素的萃取分离。研究结果表明,这两种协同萃取体系对多数稀土元素的分配系数高于单一萃取剂,即显示出协同效应,而La3+例外,显示出反协同效应。这一结果说明该协同萃取体系可适用于中、重稀土的萃取分离。进一步研究显示Cyanex923−[N2222]P507的分配系数高于Cyanex923−[N2222]P204 萃取体系,说明[N2222]P507 的协同作用高于[N2222]P204,这一结论与前面讨论的结果一致。除具有更高的分配系数外,协同萃取体系还使稀土元素间的分离系数增大,且Cyanex923−[N2222]P507 体系的分离系数高于Cyanex923 + [N2222]P204。洗脱实验显示负载有机相容易洗脱,洗脱酸度仅0.15 mol/L。Sun 课题组[92]又利用TBP 和[N1888]CA12 构成的协同萃取体系分离稀土元素,结果表明与前者类似,该体系对重稀土协同萃取分离效果最为显著。机理研究表明萃取过程为离子对萃取机理,TBP 和[N1888]CA12按照1∶1 参与了萃取络合物的形成,具体见式(11)。
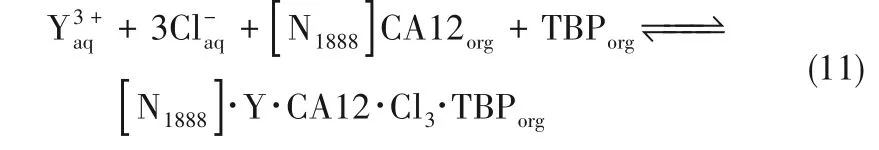
3 结论和展望
不论是非功能化离子液体还是功能化离子液体,其作为稀释剂、萃取剂或协萃剂用于稀土元素的萃取分离具有以下优势:(1)提高了萃取体系对稀土元素的分配系数;(2)增加了萃取体系对稀土元素的选择性;(3)优化了负载相的洗脱和再生条件。非功能化离子液体萃取体系还具有黏度小、纯体系可用于稀土元素的萃取分离的特点,尤其基于阴离子分割法建立的[A336]/[P66614](SCN/NO3)等离子液体体系,已应用到工业浓度水平,萃取容量也远高于目前的工业萃取体系,不足之处在于水相中需添加高浓度的盐析剂,形成大量高浓含盐废水。功能化离子液体因其功能化基团与稀土元素的结合能力更强,萃取效率更高,分离系数也较大,P507基离子液体是典型的代表,不足之处在于黏度大因而需要稀释剂,而且萃取容量偏低。总体看来,基于目前的研究成果,可通过调节阴阳离子上功能基团的结构、调控阴阳离子的种类、优化萃取体系组成等实现稀土元素的高效分离及萃取体系的绿色循环利用。
基于过去几年所取得进展,要实现离子液体在稀土萃取分离中的工业化应用,还面临以下挑战:(1)目标离子液体及萃取体系的设计和筛选。离子液体种类繁多,设计和筛选出对目标稀土具有高效选择分离能力的离子液体及萃取体系至关重要,计算机辅助设计和模拟(CADS)方法是解决这一挑战的有效措施。(2)离子液体萃取体系对稀土元素的萃取机理还需进一步解析和完善。已有的研究表明,离子液体萃取体系的萃取机理相比传统萃取体系复杂得多,且随离子液体萃取体系变化而变化。透彻认识该过程的萃取机理,明确每个粒子在萃取过程中的传递和扩散过程及其在萃取界面处的分离行为,对萃取体系选择乃至整个萃取工艺优化具有重要意义。(3)萃取剂的设计原则应满足9S原则,离子液体作为萃取剂,其黏度大、成本高,在萃取过程中存在损失、萃取容量低等问题需要进一步改进。其中,对于非功能化离子液体体系,最大的瓶颈在于萃取体系的重复利用能力问题;对于功能化离子液体体系,最大的瓶颈在于因黏度大而稀释造成的萃取容量低的问题。总之,持续开发新型离子液体及萃取体系,深入开展离子液体萃取体系对稀土元素的萃取机理,实现稀土元素的绿色、经济、快速、高效的萃取分离,是目前离子液体萃取分离稀土研究的主要内容与目标。
致谢:感谢张锁江院士对论文提出的宝贵建议。
