葛枳总黄酮口服脂质体的制备及质量评价
2020-09-24郭永梅胥彦琪
郭永梅 胥彦琪
化学性肝损伤是我国常见疾病之一,其发病率在呈现逐年上升的趋势,且无有效的治疗手段。根据现代研究表明,在人及哺乳动物的肝脏内,乙醇脱氢酶(ADH)和乙醛脱氢酶(ALDH2)构成了乙醇脱氢酶体系,参与体内乙醇代谢[1]。乙醇脱氢酶氧化体系是肝脏代谢酒精的一条重要途径。葛根和枳椇子都是中国传统医学中极具代表性的护肝药物,二者对化学性肝损伤均具有显著的保护作用[2-3],其主要有效成分为黄酮类的化合物,但其溶解度低、稳定性差、口服具有首过效应,生物利用度低,如何提高黄酮类天然药物的生物利用度,一直是药剂学领域的一个难题[4]。
脂质体作为一种新型药物载体,具有提高制剂稳定性及药物溶出的优点[5]。将PHTF 制备成口服脂质体制剂,以期其具备脂质体优点,并能克服传统剂型生物利用度低的缺点,最终增加PHTF 在机体中吸收和口服生物利用度[6]。目前,尚无关于制备葛根-枳椇子配伍制备脂质体的报道,故本实验将进行相关研究,并对PHTF 口服脂质体的质量进行评价。
1 仪器与材料
1.1 仪器
T6 紫外-可见分光光度计(北京普析通用仪器有限责任公司);FA2004 电子天平(上海舜宇恒平科学仪器有限公司);旋转蒸发仪;JSM-7500F 扫描电镜(日本电子株式会社);MS-2000激光粒度分析仪(英国malvern 公司);KQ3200DB 型数控超声波清洗器(昆山市超声仪器有限公司);TGL-16G 高速离心机(上海安亭科学仪器厂)
1.2 药品及试剂
葛根总黄酮提取物(陕西森弗天然制品有限公司,批号:GGE20180722 总黄酮≥85.0%);枳椇子总黄酮提取物(陕西森弗天然制品有限公司,批号:JJZ20180814 总黄酮≥75.0%);芦丁(中国食品药品检定研究院,批号:100080-201810);乙醇脱氢酶(sigma 公司,批号:A3263)、乙醛脱氢酶(上海源叶生物科技有限公司,批号:S10195);β-烟酰胺腺嘌呤二核苷酸(NAD+,Roche 公司);磷酸二氢钾(上海展云化工有限公司)、氢氧化钠(上海展云化工有限公司);大豆卵磷脂(德国Lipoid Gmbh 公司);胆固醇(德国Merck 公司)。
2 方法与结果
2.1 PHTF 的配比对酶活性的影响
2.1.1 ADH/ALDH2 酶活性的测定方法
取具塞试管,加入pH7.4 磷酸盐缓冲液2.0 ml、NAD+溶液0.188 mmol/ml,并加入一定浓度的样品溶液及酶溶液(ADH 或ALDH2)0.2 ml,加盖,25 ℃温育5 min,加入相应的底物溶液,立即用紫外-可见分光光度计于340 nm 测定吸光度A 值,以后每隔10 s 读数一次,连续测定5 min,记录结果,计算酶活力激活率。
2.1.2 PHTF 配比对ADH 酶和ALDH2 酶活性的影响
将PTF 与HTF 分别按照5∶1、4∶1、3∶1、2∶1、1∶1、1∶2、1∶3、1∶4、1:5的比例进行配比,即得PHTF。分别精密称取一定量不同比例的PHTF,制备成5.0 mg/ml 的供试品溶液,固定加样量为0.5 ml。并对其复合物的酶激活能力进行研究。不同比例的PHTF 对ADH酶和ALDH2 酶的影响如图1 所示。从图中可以看出,当复合物中PTF 与HTF 的比例为1∶2 时,复合物对ADH 酶的激活率为59.3%,对ALDH2 的激活率为54.5%,均维持较高水平,因此确定PTF 与HTF 配比为1∶2。

图1 葛根总黄酮-枳椇子总黄酮复合物对AND 酶和ALDH2酶活性的影响
2.2 PHTF 含量测定
2.2.1 对照品溶液的制备
精密称取芦丁对照品10.32 mg,置于25 mL 容量瓶中,加60%乙醇适量,超声溶解,再加60%乙醇稀释至刻度摇匀,即得对照品溶液。
2.2.2 供试品溶液制备
精密称取一定量的PHTF(约相当于总黄酮10 mg),置于25 ml 容量瓶中,用适量60%乙醇超声溶解,摇匀过滤,即得供试品溶液。
2.2.3 UV 检测波长的确定
采用亚硝酸钠-硝酸铝-氢氧化钠比色法测定总黄酮含量。标准品和样品溶液按显色后,以随行试剂为对照空白,于200~600 nm 波长范围扫描,见图2。标准品和样品在508 nm 波长处均具有最大吸收,故确定检测波长为508 nm。
2.2.4 标准曲线绘制
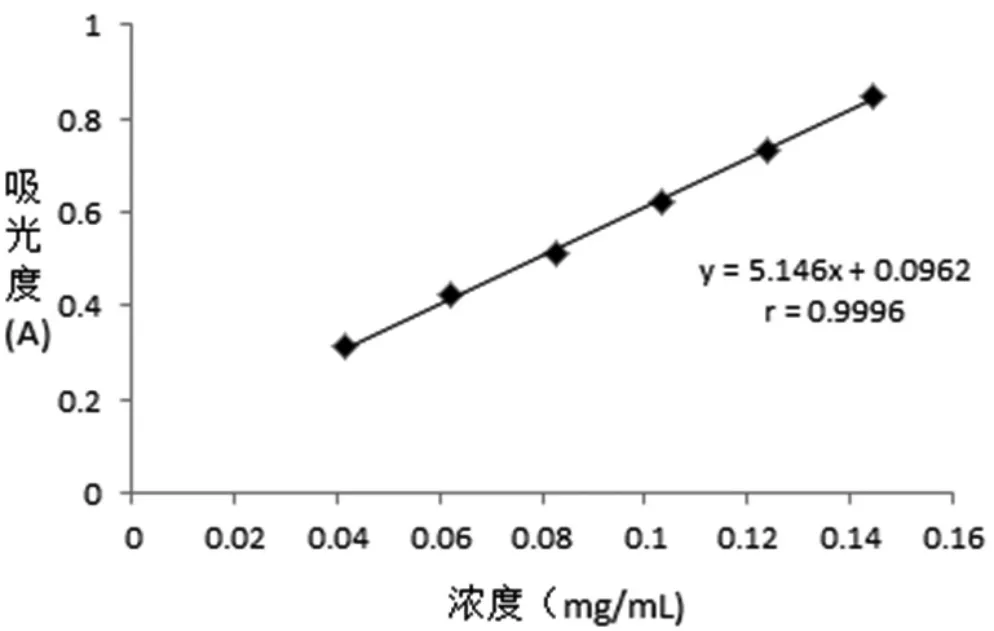
图2 芦丁标准曲线
精 密 吸 取对 照 品 溶 液1 mL,1.5mL,2mL,2.5mL,3mL,3.5 mL,置于10 ml 容量瓶中,按“2.2.3”项下方法显色,以随行试剂为对照空白,照紫外-可见分光光度法在508 nm 的波长处测定吸收度值。以芦丁浓度(mg/mL)为横坐标,吸光度值(A)为纵坐标,绘制标准曲线,得回归方程Y=5.1 460X+ 0.0 962(r = 0.9 996),结果表明,在0.0413 mg/mL~0.1445 mg/mL 范围内与吸光度值呈良好的线性关系。结果如图2。
2.3 工艺优化
2.3.1 脂质体制备采用逆向蒸发法
分别取大豆卵磷脂、胆固醇适量,溶于30 mL 无水乙醇中,作为有机相;取总黄酮适量,溶于10 mL PBS(PH7.0)中,作为水相。将水相与有机相混合,水浴超声处理,直至形成均匀乳剂,移至梨形瓶中,水浴减压除去无水乙醇,达到胶态后滴加适量PBS 溶液(PH7.0),继续减压蒸发使其充分水化,0.45 μm 微孔滤膜过滤,即得。
2.3.2 脂质体包封率测定
采用离心法。精密量取脂质体1 mL,加50 mL 甲醇破乳后再稀释10 倍,于508 nm 处测吸光度,计算PHTF 含量(W 总)。精密量取脂质体上清液1 mL,10 000 r/min 离心30 min,取上清液10 μL,甲醇定容至5 mL,测定吸光度,计算游离PHTF 含量(W 游),计算包封率。
2.2.3 药物与卵磷脂比对包封率的影响
固定处方及工艺中的其他因素不变,改变卵磷脂:药物(w/w)的比例,分别按6∶1、8∶1、10∶1、12∶1、14∶1 制成PHTF 脂质体,测定其包封率分别为54.2%、58.3%、62.9%、59.6%、58.7%。结果表明药物与卵磷脂的比例(w/w)为1∶10 时所制得的PHTF 脂质体包封率最高。
2.3.4 卵磷脂与胆固醇比例对包封率的影响
固定处方及工艺中的其他因素不变,改变卵磷脂:胆固醇(w/w)的比例,分别按2∶1、3∶1、4∶1、5∶1、6∶1 制成PHTF 脂质体,测定其包封率分别为53.4%、56.7%、61.2%、59.3%、55.2%。结果表明卵磷脂与胆固醇的比例(w/w)为4∶1 时所制得的PHTF 脂质体包封率最高。
2.3.5 有机相与水相比例对包封率的影响
固定处方及工艺中的其他因素不变,改变有机相:水相(V/V)的比例,分别按1∶1、2∶1、3∶1、4∶1、5∶1 制成PHTF 脂质体,测定其包封率分别为52.5%、58.6%、62.4%、59.4%、55.2%。结果表明卵磷脂与胆固醇的比例(w/w)为4∶1 时所制得的PHTF 脂质体包封率最高。
2.3.5 水浴温度对包封率的影响
固定处方及工艺中的其他因素不变,考察水浴温度分别为30℃、35℃、40℃、45℃、50℃,制备PHTF 脂质体,测定其包封率分别为56.3%、58.3%、61.8%、60.3%、59.9%。结果表明,水浴温度为40℃时,PHTF 脂质体包封率最高。
2.3.6 正交实验优化
以包封率为主要指标,结合单因素试验结果,对水浴温度(A);有机相与水相比例(V/V)(B);卵磷脂与胆固醇比例(w/w)(C);药物与卵磷脂比(w/w)(D);四个因素进行4 因素3 水平实验,选用L9(34)正交表安排实验,制备PHTF 脂质体,测定包封率。结果见表1。
从表中按极差R 值大小排序,C>D>B>A,即卵磷脂与胆固醇的质量比是影响包封率的主要因素。按照A2B3C2D1 组合制备的PHTF 脂质体包封率为68.1%,优于其他组合的包封率。因此确定水浴温度为40℃,有机相与水相的比例为4∶1,卵磷脂与胆固醇的比例为4∶1,药物与卵磷脂比例为1:8 为最优处方。
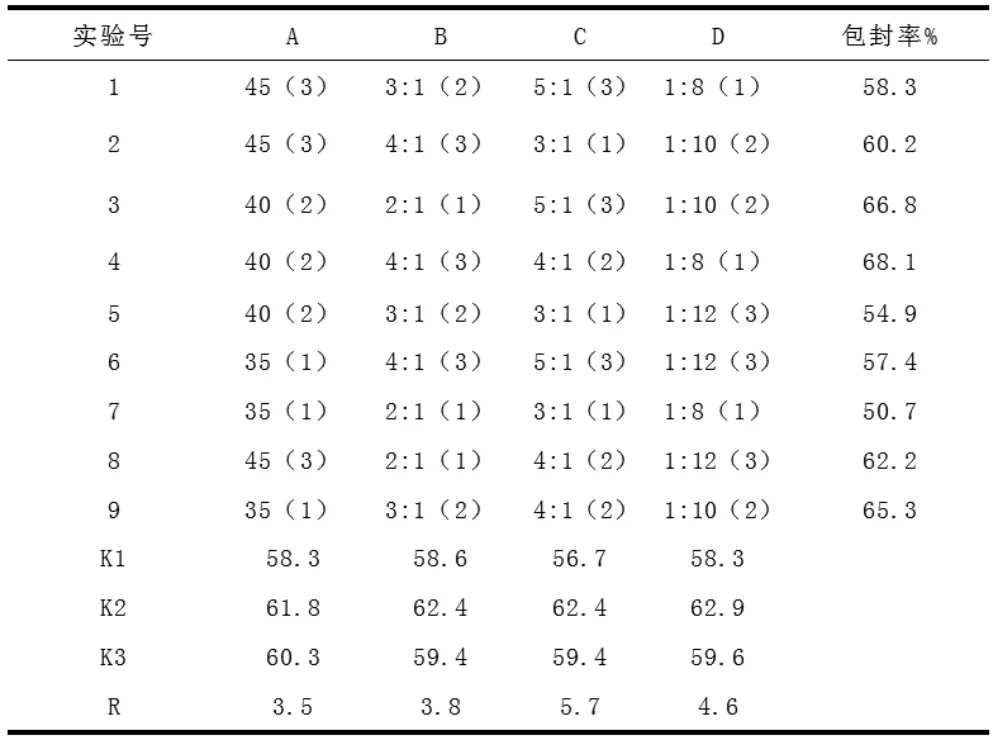
表1 正交实验结果
2.4 验证试验
按最优处方制备3 批PHTF 脂质体,测定其包封率分别为68.2%、68.4%、67.7%。平均包封率为68.1%。由测定结果可知该处方制备条件稳定可行。
2.5 PHTF 脂质体的质量评价
2.5.1 PHTF 脂质体的外观形态
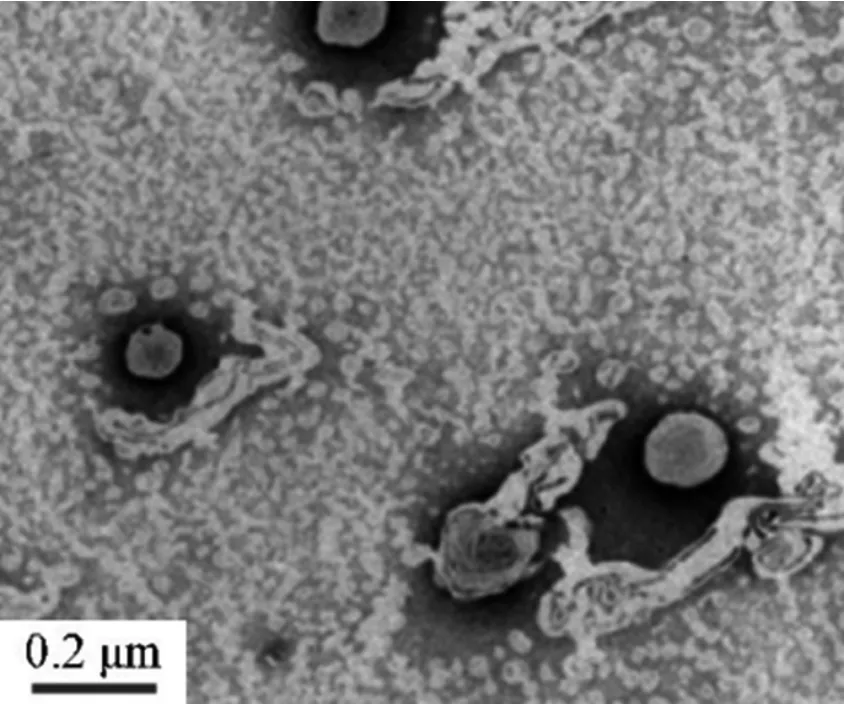
图3 脂质体电子显微镜图
按最优处方制备脂质体,外观为淡黄色乳状液体。PBS(PH7.0)稀释至适当浓度,取适量滴于铜载体,1 min 后滤纸吸去多余样液,2%磷钨酸溶液进行负染,30 s 后滤纸吸去余液,晾干,于电镜在观察PHTF 脂质体形态并拍照,结果见图3。由图可见,脂质体外观圆整,粒径均一,为球状或类球状的小囊泡。
2.5.2 粒径分布
取逆向蒸发法制得的PHTF 脂质体,纯水稀释后测定粒径,平行3 次,结果见图5,测得平均粒径为(160.7±12.0)nm,粒度分布较为均匀。
2.5.3 Zeta 电位的测定
取PHTF 脂质体适量,纯水稀释后测定,结果见图5,3 批脂质体Zeta 电位为(-41.4±2.3)mV,表明PHTF 脂质体具有较好的稳定性。
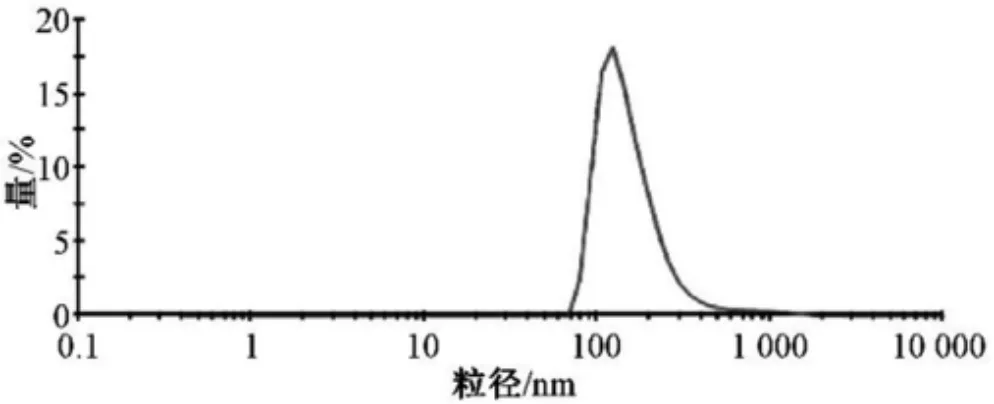
图4 脂质体粒径分布
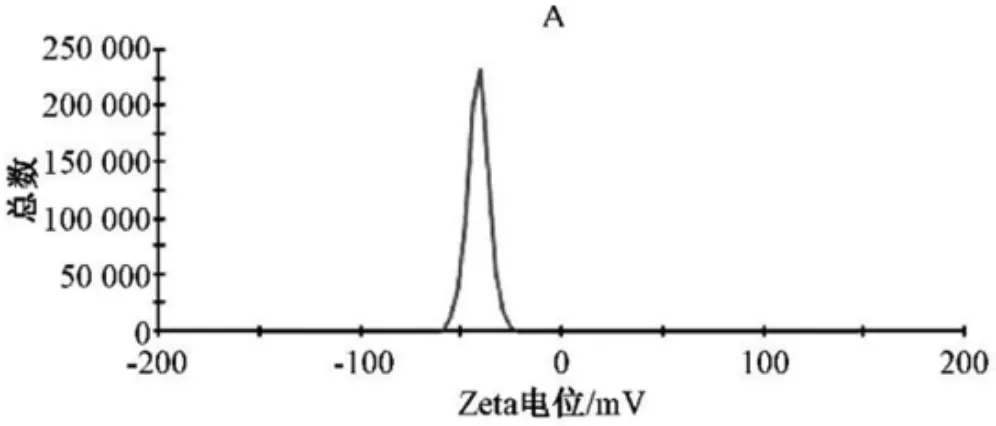
图5 脂质体Zeta 电位
2.5.4 PHTF 脂质体的载药量
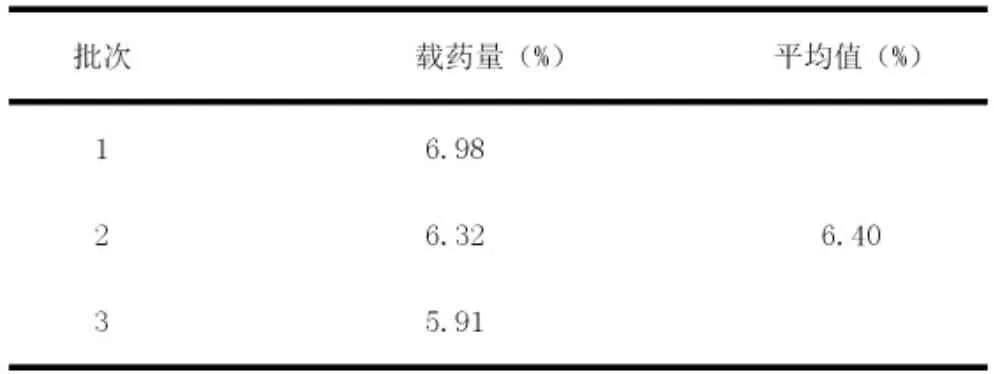
表2 总黄酮含量测定结果
取最优工艺制备的3 批PHTF 脂质体,通过离心法测定其载药量,计算公式为,结果见表2。实验证明逆向蒸发法制得的PHTF 脂质体具有较高的载药量,符合要求。
2.5.5 稳定性考察
取3 批PHTF 脂质体置于玻璃瓶中,将其在室温条件(25℃)下放置60d,分别于0、7、15、30、60d 观察其形态变化、平均粒径、包封率、Zeta 电位及pH 值,结果见表2。在60d 的稳定性考察中,PHTF 脂质体外观无变化,无浑浊,平均粒径、包封率、Zeta 电位及pH 值基本不变,说明PHTF 脂质体在25℃条件下60d 内稳定。

表3 稳定性考察结果
3 讨论
本实验采用逆向蒸发法成功制备PHTF 脂质体,并分别用单因素实验考察了各个因素对制备脂质体的影响。在单因素实验的基础上用正交试验进行了处方优化。考察了水浴温度、有机相与水相比例(V/V)、卵磷脂与胆固醇比例(w/w)、药物与卵磷脂比(w/w),结果显示逆向蒸发法制备的脂质体方法简单、效果良好。通过Valle-Hoch 法检测不同比例的PHTF 对ADH 和ALDH2 的激活率的影响,确定PTF 和HTF 最优配比为1∶2。通过正交试验确立了逆向蒸发法制备PHTF 脂质体的最佳处方为药脂比1∶8,磷脂胆固醇比4∶1,有机相与水相比例4∶1。并确定了制备工艺中旋转蒸发时的最佳水浴温度为40℃。制得的PHTF 脂质体为浅黄色的液体。
通过三批次验证试验,测得PHTF 脂质体平均包封率为68.1%,平均总黄酮含量为18.40%,证明制备方法可行,具有较好的含药量。并通过初步稳定性考察显示,PHTF 脂质体在常温条件(25℃)下具有良好的稳定性,60d 无明显变化,从而确保了PHTF 脂质体用药安全性和稳定性。
本次实验仅考察了PHTF 体外分析方法的建立,且方法单一,不能有效评价PHTF 脂质体的药效及生物利用度。后续课题组将建立系统的、多指标的评价分析方法,并进行体内的药代动力学实验。
