板蓝根中淀粉含量与活性成分含量的相关性研究*
2020-09-07李晓晨张建逵
李晓晨,魏 巍,张建逵,李 丽,牛 蕾
(辽宁中医药大学 药学院,辽宁 大连 116600)
板蓝根为十字花科植物菘蓝Isatis indigotica Fort.的干燥根,性苦,寒,气微,归心、胃经。具有清热解毒,凉血利咽之功效[1]。传统认为:板蓝根药材以“粉性大(足)者为佳”[2]。粉性强即为淀粉含量高,但研究表明,其活性成分为(R,S)-告依春、靛蓝和靛玉红[3]等。本实验研究板蓝根淀粉含量与其活性成分含量之间的相关性,为板蓝根栽培药材提供质量控制依据,并检验“粉性大者为佳”的适用性。
1 实验材料
1.1 仪器与材料
UV-3010紫外可见双光束扫描分光光度计(日本日立集团);BP 211D型电子分析天平(德国赛多利斯公司);1100型高效液相色谱仪(G1314A型VWD检测器,G1311A型四元泵,AT-130型柱温箱)(大连中汇达科学仪器有限公司)。
1.2 试剂与试药
甲醇(色谱纯);甲醇、无水乙醇、高氯酸、乙酸乙酯等均为分析纯;蒽酮(上海源叶生物科技有限公司);浓H2SO4(国药集团化学试剂有限公司);可溶性淀粉(Solarbio科技有限公司);(R,S)-告依春对照品、靛蓝对照品、靛玉红对照品均购于上海源叶生物科技有限公司,批号分别为:KA0816CA14、K18M7C1和Z25N8B48799。纯度均≥98%。
1.3 样品
从不同收集地药店购进10批不同产地的板蓝根饮片,均经辽宁中医药大学药学院张建逵副教授鉴定,为十字花科植物菘蓝Isatis indigotica Fort.的干燥根,具体来源见表1。
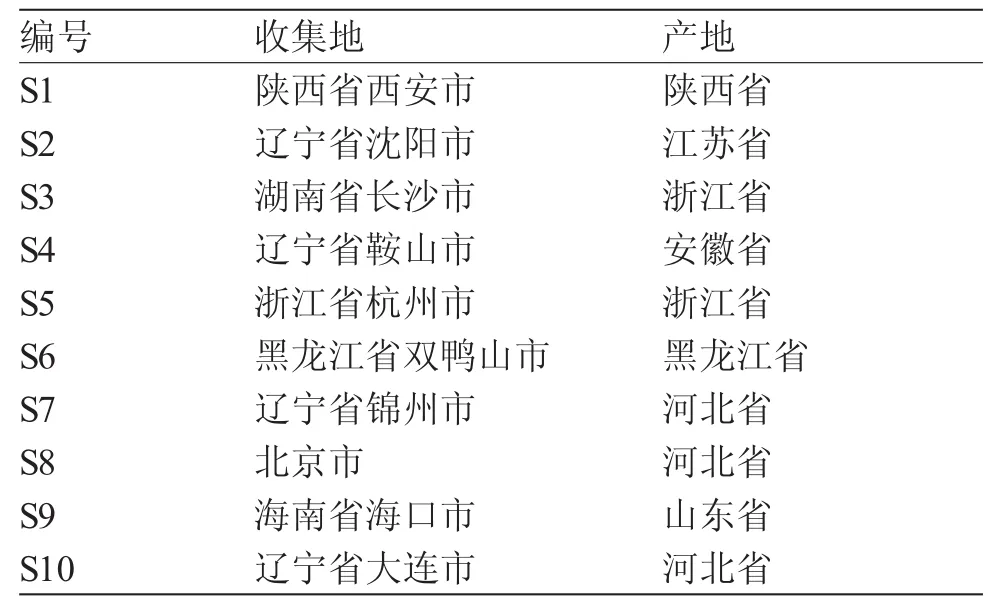
表1 饮片样品来源表Tab.1 Source of prepared slices
2 实验方法[5]
2.1 板蓝根淀粉含量测定
2.1.1 试液的配制 2%蒽酮试剂:精密称取1g蒽酮于50mL乙酸乙酯中溶解,置4℃暗处贮藏;80%乙醇;9.2mol·L-1HClO4[6]。
2.1.2 供试品溶液的制备 精密称量0.03g样品粉末于15mL离心管中,加入80%乙醇溶液8mL,80℃水浴提取 3 次(30、10、10min),弃去上清液,残留物加入 6mL 的 9.2mol·L-1HClO4,快速振荡摇匀,反应5min,静置,沉淀后上清液移置100mL容量瓶中,重复3次,蒸馏水定容,摇匀,即得。
2.1.3 样品测定 精密量取1mL供试品溶液于15mL离心管中,蒸馏水补足至2mL,并加入2%蒽酮试剂0.5mL,缓慢加入5mL 98%的浓H2SO4,快速摇匀,于沸水中显色1min,快速取出置于冰水浴中冷却5min,取出后室温放置5min,另取2mL蒸馏水为空白对照,同法处理,于630nm处测定吸光度值。
2.1.4 标准曲线的绘制 精密称取0.05g淀粉于小烧杯中,加入 18mL 9.2mol·L-1HClO4,溶解后转移到100mL容量瓶中,加蒸馏水置刻度。分别量取该溶液0、0.3、0.6、0.9、1.2、1.5mL,照 2.1.3 项下方法测定吸光度,以浓度为横坐标,吸光度为纵坐标,绘制标准曲线,回归方程为Y=9366.7X+0.0021,r=0.9997。结果表明,淀粉含量在0~0.375mg·mL-1内具良好的线性关系。
2.1.5 方法学考察
(1)经方法学考察,重现性、稳定性、重复性均符合试验要求。
(2)加样回收率实验 精密称取S2样品粉末5份,每份 10mg(淀粉含量为 35.18%),按“2.1.2”项下方法制备成供试品溶液,精密吸取1mL供试品溶液于15mL离心管中,并加入0.4mL淀粉标准品溶液,蒸馏水补足至2mL,将所得淀粉标准品溶液及供试品溶液混合后显色并测定其吸光度,结果见表2。
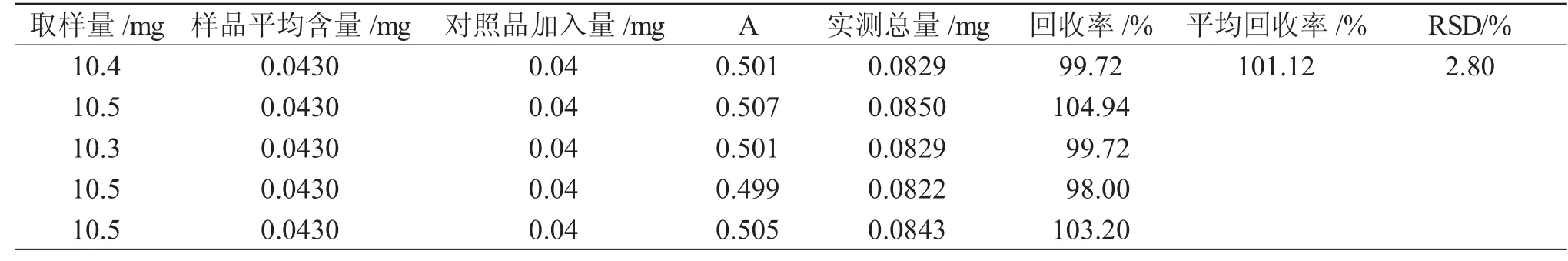
表2 加样回收率测定结果Tab.2 Results of additive recovery
测得板蓝根淀粉的平均回收率为101.12%,RSD值为2.80%。
2.2 (R,S)-告依春、靛蓝、靛玉红含量测定
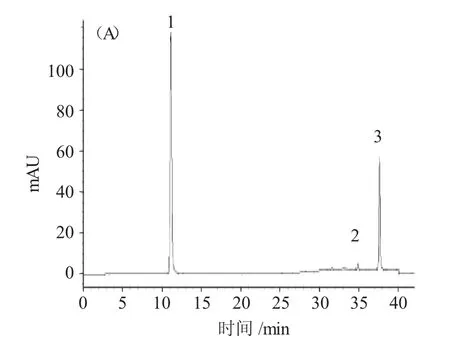
2.2.1 色谱条件采用Waters symmetry-C18(250mm×4.6mm,5μm)色谱柱,以 A- 甲醇,B- 水为流动相,梯度洗脱程序为:0~15min,90%~85%B;15~20min,85%~78%B;20~30min,78%~20%B;30min~40min,20%B;流速:1mL·min-1;检测波长采用切换波长,0~20min,254nm;20~40min,285nm;柱温,30℃;进样量,10μL。在此色谱条件下(R,S)-告依春,靛蓝,靛玉红分离度均大于1.5,其拖尾因子在0.95~1.05,分离度良好,在该色谱条件下,对照品溶液和供试品溶液色谱图见图1。

图1 对照品溶液(A)和供试品溶液(B)的色谱图Fig.1 Reference substance solution(A)and(B)the chromatogram of test sample solution
2.2.2 对照品溶液的制备 取(R,S)-告依春、靛蓝、靛玉红对照品适量,精密称定,同置于10mL的棕色容量瓶,用甲醇定容至刻度,摇匀,超声0.5h,0.45μm微孔滤膜滤过,制成每1mL含(R,S)-告依春,靛蓝,靛玉红各 0.90,0.85,0.40mg 的混合溶液,即得。
2.2.3 供试品溶液的制备 精密称定各样品2g,加200mL 75%的乙醇,回流提取2h,过滤,浓缩并用甲醇定容至10mL容量瓶中,作为供试品溶液备用。
2.2.4 线性关系考察 精密吸取(R,S)-告依春、靛蓝、靛玉红的混合对照液 2,4,6,8,10,12μL,进样分析。将各对照品的质量作为横坐标,峰面积作为纵坐标,按“2.2.4”项下方法进行测定绘制标准曲线,回归方程,见表3。

表3 3种成分线性关系Tab.3 Linear relationship of the three components
3 实验结果
对上表中淀粉含量及(R,S)-告依春含量进行相关性分析,淀粉含量与(R,S)-告依春含量的回归方程为:Y=0.0013X-0.0076,r=0.1122(P>0.05 为差异没有统计学意义),淀粉含量与靛蓝含量的回归方程为:Y=-0.9511X+38.742,r=0.3422(P>0.05 为差异没有统计学意义),淀粉含量与靛玉红含量得到回归方程为:Y=8×10-5X-0.0014,r=0.3547(P>0.05 为差异没有统计学意义)。因此,板蓝根淀粉含量与其主要药用成分之间并无明显相关性。
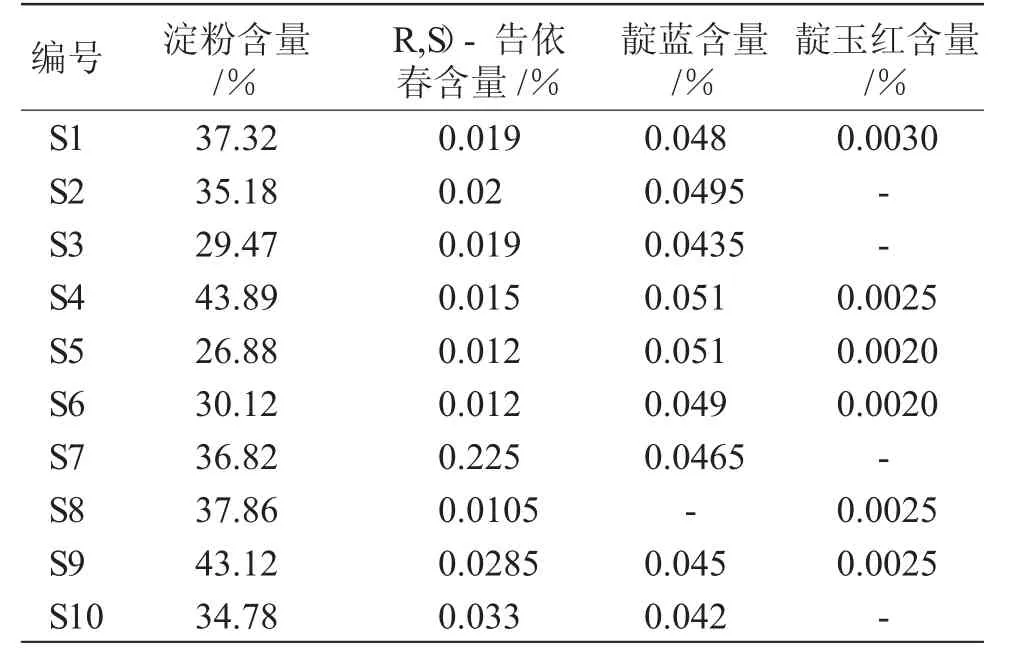
表4 板蓝根淀粉及(R,S)-告依春、靛蓝、靛玉红含量测定结果Tab.4 Determine the contents of(R,S)-epigoitrine,indigo and indirubin
4 讨论与结论
按照2015版《中国药典》的规定[1],板蓝根中(R,S)-告依春含量不得少于0.02%,照此标准,上述10批药材中仅有4批合格,合格率仅为40%,因此,相关部门对该药材的质量应加强监管。
相关性分析结果表明,板蓝根淀粉含量与主要活性成分无相关性。“粉性大(足)者为佳”这一经验并不适用。笔者认为,古代板蓝根药材来源多为野生品,而目前药用的板蓝根几乎全部为栽培品,通过施肥促进初生代谢产物淀粉含量的增加,而未必能促进活性成分含量的提高,因此,才会出现“粉性大(足)者为佳”这一经验不适用的情况。
本实验结果提示,栽培中药过程中要注意到生长环境对药材质量的影响。活性成分多为次生代谢产物,环境的胁迫作用可能是促进其形成的主要原因。因此应该对栽培的板蓝根予以适当的环境胁迫,来提高活性成分含量。并抑制淀粉生成量或增大其消耗量,来提高活性成分含量。该药材的栽培技术还需要更加深入的研究。
本实验探讨了板蓝根药材淀粉含量与其活性成分含量之间的相关性,本研究可为板蓝根药材的质量评价以及板蓝根栽培品的质量控制提供参考。
