方解石对复合重金属污染土壤的修复研究
2020-09-02徐艳郭振
徐艳 郭振
摘要:通过在人工配置的复合铜铅锌重金属污染土壤中添加不同比例的方解石粉,开展原位钝化修复试验,研究不同比例不同修复时间(30d、60d和90d),方解石对该复合污染土壤的修复效果。结果表明:方解石浓度增加及培养周期的延长对供试土壤pH无显著影响;方解石粉对供试土壤重金属有一定修复效果。相同培养周期内,土壤可提取态重金属含量并不随方解石剂量增加而显著变化;随培养周期延長,修复效果逐渐增强。培养30d时,1%的添加剂量修复效果较好;培养60d时,2%的修复效果较好;培养90d时,1%和2%的修复效果均有所增加,但均小于1.5%的修复效果。就不同重金属而言,培养30~60d时,各处理组方解石添加对供试土壤3种可提取态重金属修复效果依次为Pb>Cu>Zn;培养90d时,修复效果为Cu>Pb>Zn。综上,后期采用方解石进行重金属污染原位修复时,最适添加剂量为1.5%(质量比,风干土计),最佳修复时间≥90d。
关键词:方解石;铜铅锌复合污染;土壤修复;可提取态
中图分类号:S181文献标识码:ADOI:10.19754/j.nyyjs.20200815037
收稿日期:2020-06-23
基金项目:陕西地建土地工程技术研究院预研项目(项目编号:NBYY2019-17)
作者简介:徐艳(1989-),女,硕士,工程师。研究方向:土地工程、土壤修复。
引言
随着我国工业化和城镇化进程不断加快,土壤重金属污染问题日益严重,导致土壤环境质量破坏,农作物产量和质量下降,同时重金属在作物体内富集,通过食物链进入人体,直接影响人体健康[1,2]。因此,土壤重金属污染修复已经刻不容缓,亟待研究。
原位钝化修复是一种成本较低、操作简单、见效快且适合大面积推广的修复方式,在土壤污染修复中应用较广[3,4]。原位无机钝化材料中方解石是一种碳酸盐岩矿物,由三方晶系组成,主要成分是碳酸钙,在自然界中最为常见且分布较广[5,6]。其比表面积大,吸附性能好,无毒无害,易得且价格便宜。作为石灰类钝化剂进行土壤重金属污染修复时,主要是通过提高土壤pH,使土壤颗粒表面负电荷增加,土壤有机质、黏土矿物和水合氧化物及钝化剂表面的负电荷增多,土壤对重金属的吸附能力增强[7],同时促进重金属离子形成氢氧化物沉淀或碳酸盐岩沉淀而降低其有效性[8]。与其它碱性较强的物质(赤泥、石灰)相比,方解石碱性较弱,长期使用不易使土壤发生盐碱化、板结从而影响土壤结构[9,10],因此方解石已逐渐成为重金属污染土壤及其它场地的修复材料[11,12]。已有研究将方解石应用于水体污染修复及土壤镉污染修复,并取得了较好成效[13,14],但关于方解石修复重金属复合污染土壤的研究较少。本试验选用方解石作为原位钝化修复材料,研究其对铜铅锌复合污染土壤的修复效果,为重金属复合污染土壤原位钝化修复探究更好的钝化剂提供重要理论依据。
1材料与方法
1.1供试材料
供试土壤选自陕西地建研究院富平中试基地无污染土壤,pH为6.74,有机质为7.09g·kg-1。供试土壤中重金属配制试剂选用CuSO4、Pb(NO3)2、Zn(NO3)2·6H2O,分析纯;供试方解石粉(200目)购自石家庄雨馨建筑材料公司,pH为7.45。供试透明培养皿购自杨凌实验用品器材店。
1.2试验设计
将采自富平中试基地的无污染土壤研磨过20目筛后,准确称取5kg土壤放入自封袋中,根据土壤环境质量标准[15],按照Cu为400mg·kg-1、Zn为500mg·kg-1、Pb为500mg·kg-1(大于土壤污染风险筛选值,存在潜在污染风险)称取相应含量的CuSO4、Pb(NO3)2、Zn(NO3)2·6H2O颗粒,与土壤充分混匀[16],用去离子水调节土壤含水量保持在田间持水量的70%,在25±2℃下恒温培养箱中开口培养30d后,自然风干,作为复合重金属污染土壤用于培养试验。
将配置的复合重金属污染土壤研磨过2mm筛,分成5等份,方解石粉添加剂量分别为土壤重量的0.5%(F0.5)、1%(F1)、1.5%(F1.5)、2%(F2)、3%(F3),共设5个处理,每个处理3个重复。将污染土壤与方解石粉末充分混匀,分别放置在透明的塑料培养皿内,在培养箱内开口培养。每隔1d用去离子水给土壤补充水分,保持在田间持水量的70%左右,在25±2℃下恒温箱中开口培养。
1.3样品测定与分析
在培养试验30d、60d、90d时取出土样,风干研磨,分别过2mm和0.149mm筛待测。土壤pH采用DELTA 320 pH计测定(水土比2.5∶1);土壤中重金属有效态含量及其有效性能更好地反映出其环境效应,DTPA提取态含量与作物对重金属吸收有较高的相关性,常用来衡量生物对重金属的可吸收性[17]。因此,本文选用DTPA法测定土壤中可提取态重金属Cu、Pb、Zn进行分析。采用SPSS17.0软件进行方差分析及显著性检验,计算标准差;采用Origin 2018绘制直方图。
2结果与讨论
2.1添加后土壤pH变化
未添加方解石粉末前,供试土壤pH为6.74,方解石粉pH为7.45。添加不同比例方解石粉末后,就同一处理而言,各处理土样pH均值依次为6.88(F1.5)>6.81(F3)>6.80(F2)>6.79(F1)>6.76(F0.5)。添加1.5%的方解石后,土壤pH平均增加了0.14个单位,培养90d时,pH为6.92,增幅最大,为0.18个单位。添加3%、2%和1%的方解石后,土壤pH平均增幅非常接近,分别增加了0.07、0.06和0.05个单位。综上,本试验中土壤pH随方解石添加剂量增加略有增加,这一结果与张亚男研究结果类似[18]。
就不同培养周期而言,仅3%的方解石添加比例下,pH随培养时间延长而略微增加,其余各处理土壤pH并未随培养时间增加而逐渐增大。本试验结果与朱德强等、梁丽芹等[11,19]研究结果类似。在方解石—土壤体系中,方解石主要通过水解作用产生OH-而使土壤pH升高。由于方解石的溶解及其中Ca2+的平衡浓度释放主要受CO2分压控制,CO2又受微生物呼吸及有机质分解作用的影响,且方解石本身的水解能力较弱,与供试土壤pH差异较小,因此本试验中随方解石剂量增加、时间延长,土壤pH无显著性差异[20]。
2.2添加后土壤可提取态重金属含量
供试土壤按照总Cu 400mg·kg-1、总Zn 500mg·kg-1、总Pb 500mg·kg-1进行配置,静置培养30d后对供试土壤可提取态重金属Cu、Zn和Pb进行测定。结果表明,未添加方解石粉时,土壤可提取态Cu为176.63mg·kg-1,可提取态Zn为172.12mg·kg-1,可提取态Pb为243.72mg·kg-1,依据土壤环境质量标准(GB15618-2018)[15],属于铜铅锌复合污染土壤。
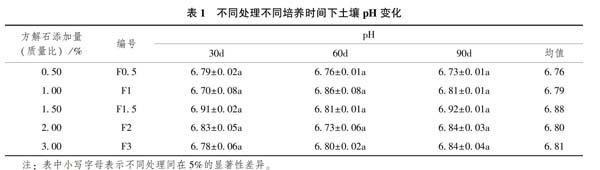
由图1可知,培养30d时,各处理组添加方解石粉对供试土壤Pb的整体修复效果较好,平均为3.7%,Cu次之,为2.6%,对Zn的修复效果最差,仅1.9%。相较其它处理,添加1%的方解石含量对供试土壤的修复效果较好,可提取态Cu和Pb分别减小了7.4%和7.1%;添加0.5%的方解石含量对供试土壤Zn的修复效果较好,可提取态Zn减小了5.0%。3者的修复效果不同,与方解石在土壤中的溶解平衡及3种重金属可提取态存在竞争吸附有关。30d的培养时间内,对这3种可提取态重金属的修复效果并不随方解石粉剂量增加而增加。
注:图柱上小写字母表示同一处理下不同指标间在5%的显著性差异,下同。
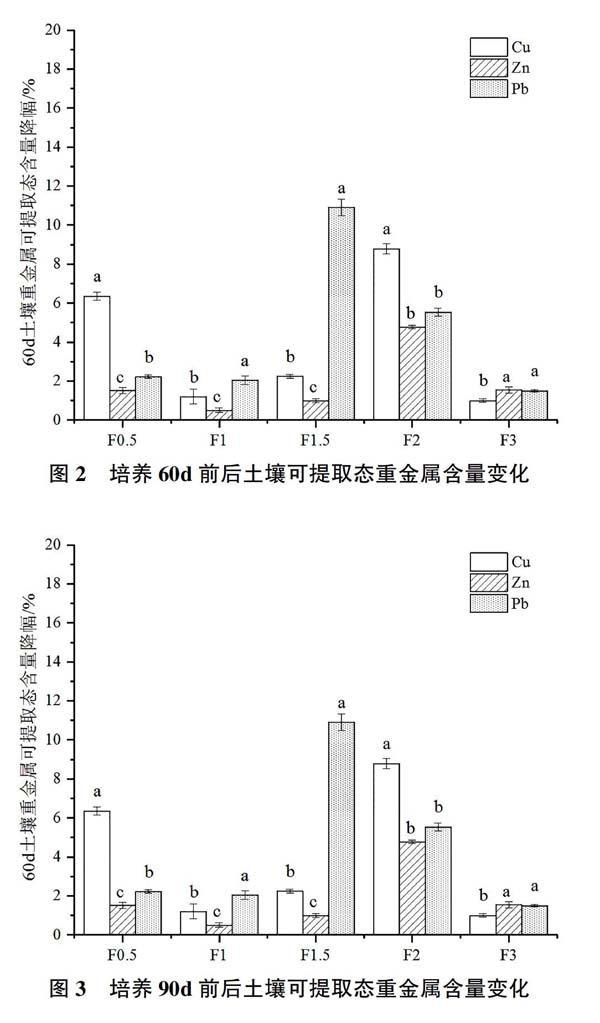
由图2可知,培养60d时,各处理组方解石添加对供试土壤可提取态重金属的平均修复效果依次为Pb(4.6%)>Cu(3.9%)>Zn(1.9%),随修复时间延长,各处理对Pb和Cu的平均修复效果增加较为显著,对Zn的修复效果不明显。添加0.5%的方解石粉,可提取态Cu含量有所下降,对Pb和Zn无显著修复效果;添加1%的方解石粉,可提取态整体修复效果不显著;添加1.5%的方解石,可提取态Pb和Cu分别减小了10.9%和2.2%;而添加2%的方解石对3种重金属可提取态均有一定效果,可提取态Cu、Pb和Zn含量依次减小了8.8%、6.0%和4.7%。综上,随修复时间延长,各处理对Pb和Cu的修复效果有所增加,对Zn修复效果不明显。修复效果不随方解石添加含量增加而增加,且添加2.0%的方解石对供试土样修复效果较好。
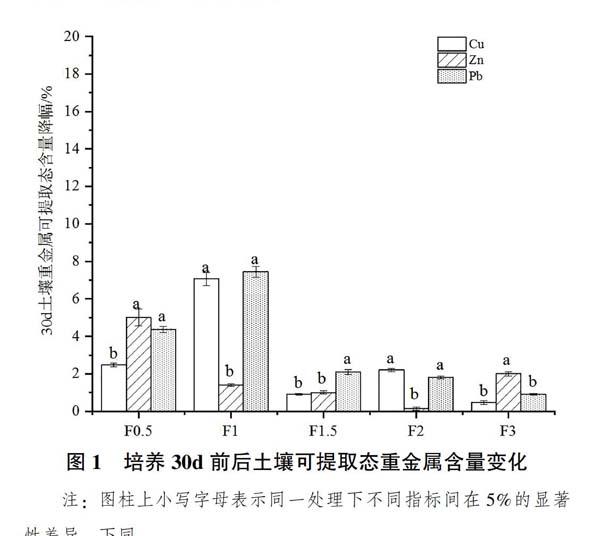
由图3可知,培养90d时,各处理组方解石添加对供试土壤3种可提取态重金属的修复效果均有所增长,依次为Cu(9.6%)>Pb(6.3%)>Zn(4.7%)。相较其它4种处理,添加1.5%的方解石对3种可提取态重金属Cu、Pb、Zn修复效果显著增加,依次为18.2%、12.1%和7.8%。此外,仅添加1%的方解石处理对可提取态Cu的修复效果超过了10.0%,其余均小于8.0%,随周期延长,修复效果变化不显著。综上,培养90d时,添加1.5%的方解石对供试土样修复效果较好。
目前,方解石对土壤重金属的钝化机制研究可分为离子交换和碳酸盐沉淀2个方面[17]。方解石内部Ca2+与6个氧原子配位,表面Ca2+往往配位不全。当把方解石加入土壤后,带负电的土壤颗粒会吸附表面的Ca2+,为方解石吸附土壤中的重金属离子提供了点位。相同培养周期内,各处理方解石添加对供试土壤铜铅锌的修复效果并不随添加剂量增加而增加,可能由于在方解石粉较低剂量时,重金属离子既可与方解石发生配位吸附,和其表面的CO32-生成碳酸盐岩结合态,也可发生离子交换吸附,与表面Ca2+发生交换;而在较高剂量时,高浓度的Ca2+与重金属离子形成竞争吸附,影响其钝化效果。这一结果与张亚男[18]研究结果相近。
此外,重金属离子竞争吸附能力的大小与该离子的一级水解常数、离子半径、电负性及其与吸附位点能否形成共价键等因素有关[21,22]。赵民等[23]、刘晶晶[24]研究表明,从离子整体吸附量来看,竞争吸附能力Pb2+>Cu2+>Zn2+,因此,Pb2+更容易进入方解石晶格内部进行钝化。添加方解石后,方解石在短时间内迅速溶解而后稳定,导致土壤中Ca2+、CO32-浓度迅速升高后稳定。培养30d和60d周期内,Pb2+优先被吸附固定,可提取态含量降幅较大;至培养后期,CO32-也随之水解,Cu2+和Zn2+竞争压力减小,可提取态含量降幅也逐渐增大,且Cu2+更易与OH-形成沉淀,所以培养后期土壤中可提取态Cu降幅更加明显。
3结论
方解石作为一种原位钝化剂,对供试土壤重金属有一定修复效果。培养试验结果表明,供试土壤pH为6.74,偏中性;方解石浓度增加及培养周期的延长对供试土样pH无显著影响。相同培养周期内,土壤可提取态重金属含量并不随方解石剂量增加而显著变化;随着培养周期延长,修复效果逐渐增强。培养30d时,1%的添加剂量修复效果较好;培养60d时,2%的修复效果较好;至90d时,1%和2%的修复效果均有所增加,但均小于1.5%的修复效果。就不同重金属而言,培养30d和60d时,各处理组方解石添加对供试土壤3种可提取態重金属修复效果依次为Pb>Cu>Zn;培养90d时,平均修复效果依次为Cu>Pb>Zn,与3者之间存在竞争吸附及离子本身属性有关。综上,后期采用方解石进行重金属污染修复时,最适添加剂量为1.5%(质量比,风干土计),最佳修复时间≥90d。
参考文献
[1] 梁媛,王晓春,曹心德.基于磷酸盐、碳酸盐和硅酸盐材料化学钝化修复重金属污染土壤的研究进展[J].环境化学,2012,31(01):16-25.
[2]周旋,郑琳,胡可欣.污染土壤的来源及危害性[J].武汉工程大学学报,2014,36(07):12-13.
[3]陈远其,张煜,陈国梁.石灰对土壤重金属污染修复研究进展[J].生态环境学报,2016,25(08):1419-1424.
[4]张茜,徐明岗,张文菊,等.磷酸盐和石灰对污染红壤与黄泥土中重金属铜锌的钝化作用[J].生态环境,2008,17(03):1037-1041.
[5]廖喜林.方解石矿床及工业利用[J].矿产与地质,1999,1(13):44-46.
[6]秦善,王长秋.矿物学基础[M].北京:北京大学出版社,2006.
[7]徐粲然,卢滇楠,刘永民.生物钝化修复镉污染土壤研究进展[J].化工进展,2014,33(08):2174-2179.
[8]黎大荣,吴丽香,宁晓君,等.不同钝化剂对土壤有效态铅和镉含量的影响[J].环境保护科学,2013,39(03):46-49.
[9]谢飞,梁成华,孟庆欢,等.添加天然沸石和石灰对土壤镉形态转化的影响[J].环境工程学报,2014(08):3505-3510.
[10]李剑睿,徐应明,林大松,等.农田重金属污染原位钝化修复研究进展[J].生态环境学报,2014,23(04):721-728.
[11]朱德强,梁成华,杜立宇,等.含方解石物质对土壤镉赋存形态的影响[J].水土保持学报,2016,30(01):326-330.
[12]刘云,董元华,杭小帅,等.环境矿物材料在土壤环境修复中的应用研究进展[J].土壤学报,2011,48(03):629-638.
[13]化海兵,姜雅婿,刘成,等.方解石粉钝化太湖水中磷的能力及影响因素[J].环境工程学报,2011,5(02):337-342.
[14]吴学丽,杨永亮,徐清,等.沈阳地区河流灌渠沿岸农田表层土壤中重金属的污染现状评价[J].农业环境科学学报,2011,30(02):282-288.
[15]GB15618-2018,土壤环境质量标准[S].北京:中国标准出版社,2018.
[16]章骅,何品晶,吕凡,等.重金属在环境中的化学形态分析研究进展[J].环境化学,2011,30(01):130-137.
[17]朱德强.含方解石物质修复镉污染土壤及机理初探[D].沈阳:沈阳农业大学,2016.
[18]张亚男.石灰类钝化剂对土壤镉修复化理及油麦菜吸收镉的影响[D].沈阳:沈阳农业大学,2017.
[19]梁丽芹,章力干,周可金,等.硫和白云石对皖中黄褐土铅形态分布的影响[J].土壤,2007,39(06):919-923.
[20]吴贻中,李保国.土壤学[M].北京:中国农业出版社,2006.
[21]林青,徐绍辉.土壤中重金属离子竞争吸附的研究进展[J].土壤,2008,40(05):706-711.
[22]林青.土壤中重金属Cu、Cd、Zn、Pb吸附及迁移的实验研究[D].青岛:青岛大学,2008.
[23]赵民,王森,李悦,等.新型钛酸钠填料对Cu2+、Pb2+、Zn2+和Cd2+的競争吸附研究[J].环境科学学报,2019,39(02):390-398.
[24]刘晶晶.Pb2+、Cu2+、Cd2+在黄土上竞争吸附及解吸特性研究[D].杭州:浙江大学,2014.
(责任编辑贾灿)
