杜鹃兰酮的制备方法研究
2020-08-23陈卓谭李玉杨月乌雪娟夏锐
陈卓 谭李玉 杨月 乌雪娟 夏锐


摘 要:为了探究抗糖尿病性视网膜病变活性天然产物杜鹃兰酮的制备工艺,本研究以市售可得的4-苄氧基-6-羟基-2,3-二甲氧基苯乙酮为原料,经缩合、氢化、苄基化及选择性去甲基化等6步反应,以9.6%的总收率制备了杜鹃兰酮。最后考察了选择性去甲基化反应中反应溶剂、反应温度对目标产物得率的影响。
关 键 词:杜鹃兰酮;选择性去甲基化反应;高异黄酮
中图分类号:R9; TQ463 文献标识码: A 文章编号: 1671-0460(2020)07-1265-04
Study on Preparation of Cremastranone
CHEN Zhuo, TAN Li-yu,YANG Yue, WU Xue-juan, XIA Rui
(Xian Medical University, Xian Shaanxi 710021, China)
Abstract: In order to explore the preparation process of cremastranone, a natural product of anti-diabetic retinopathy activity, cremastranone was prepared with 4-oxyoxanoe-6-hydroxy-2, 3-dioxybenzone as raw material via six-step reactions, such as condensation, hydrogenation, benzylation,selective demethylation and so on,and the total yield was 9.6%. The effect of reaction solvent and reaction temperature on the yield of the target product was also investigated in the selective demethylation reaction.
Key words: Cremastranone; Selective demethylation reaction; Homoisoflavonoids
糖尿病視网膜病变(diabetic retinopathy, DR)是糖尿病最常见的微血管并发症之一,最终可导致不可逆的视力丧失[1]。血管内皮生长因子(vascular endothelial growth factor, VEGF)是导致糖尿病视网膜微血管病变的关键因子[2],是临床药物治疗糖尿病视网膜病变的主要靶点。
目前,针对VEGF通路的主要一线临床治疗药物是抗VEGF单抗[3]。然而,抗VEGF单抗球内注射治疗在DR治疗中仍存在着一系列显著问题:首先,由于抗VEGF单抗是分子量148 KD的蛋白质大分子,无法经角膜或血-视网膜屏障吸收入眼,必须通过玻璃体腔注射。反复的玻璃体腔注射破坏玻璃体的正常微环境[4],不仅给患者带来极大的痛苦,也增加了对眼球组织的结构损害,临床多见眼内感染、晶状体损伤、高眼压、动脉阻塞、结膜出血、玻璃体内浮游物等。第二,非选择性的VEGF抑制可能导致视网膜正常组织结构的萎缩[5]。视网膜的多种VEGF分泌细胞中,只有视网膜微血管内皮细胞产生的VEGF在DR的发展中是病理性的。而视网膜色素上皮细胞 (retinal pigment epithelium, RPE) 产生的生理性VEGF有助于维持脉络膜微循环的正常生理状态。VEGF单抗的非选择性可能引起残余正常视网膜神经细胞的凋亡变性,并且增加了脉络膜毛细血管循环障碍的危险[6]。第三,抗VEGF单抗制备、纯化困难,生产成本高,导致价格昂贵,许多患者因而放弃治疗。
因此,开发基于易制备的小分子化合物、具有高度选择性的VEGF通路拮抗剂,如VEGF受体抑制剂,是目前的新药研究及开发的热点。杜鹃兰酮(Cremastranone,结构如图1)是一种天然产物,属于3-苯基-4-色满酮(chromanone),或高异黄酮(homoisoflavanone),于1987年在葡萄风信子(Muscari armeniacum)中首次发现[7],近年来在我国常见植物杜鹃兰(Cremastra appendiculata (D.Don) Makino)中亦有发现[8],杜鹃兰的假鳞茎入药称毛慈菇,录于《本草拾遗》。
体内研究发现,杜鹃兰酮具有显著的新生血管抑制作用,对眼部微血管上皮细胞具有较强的选择性抑制作用,但对眼部的其他细胞系,甚至大血管上皮细胞并未观察到脱靶作用[9]。在小鼠视网膜病变模型研究中具有良好的新生血管抑制作用,也未观察到明显的副作用[10]。因此,对杜鹃兰酮类结构进行深入研究,有望解决上述药物所面临的问题。
杜鹃兰酮属于二甲基取代的高异黄酮类化合物,其母核上的5个羟基中仅有两个被甲基取代,在合成过程中实现选择性甲基化/去甲基化具有显著的挑战性。目前,国内外对杜鹃兰酮类结构的研究较少[11-13],本研究对其制备方法[11]进行了考察(图2),尤其针对其选择性去甲基化反应进行了工艺改进。对于针对此类结构的深入研究及构效关系分析有着重要的基础意义,此工艺研究目前未见文献报道。
1 儀器与试剂
磁力搅拌低温槽,PSL-1810型,日本东京理化株式会社;Agilent TM 1260 型高效液相色谱仪。
4-苄氧基-6-羟基-2,3-二甲氧基苯乙酮, 95%,上海隆盛化工有限公司;异香草醛,98%,Macklin Inc.;钯碳,10%Pd,Macklin Inc.;N,N-二甲基甲酰胺二甲缩醛,97%,Macklin Inc.;三甲基碘硅烷,97%,含铜作稳定剂,Macklin Inc.;苄溴,化学纯,安耐吉化学;柱层析所使用薄层硅胶为硅胶H,青岛海洋化工;其他常见有机溶剂、试剂均为分析纯,必要时干燥。
2 杜鹃兰酮的制备研究[11]
2.1 4'-苄氧基-2',3',4-三甲氧基-6',3-二羟基查尔酮(化合物1)的合成研究
称取4-苄氧基-6-羟基-2,3-二甲氧基苯乙酮 3 g加至事先装有温度计及恒压滴液漏斗的三颈瓶中,向三颈瓶中用量筒加入 30 mL 无水乙醇,搅拌至完全溶解。称取事先无水处理过的KOH 0.67 g,搅拌混匀。称取异香草醛 1.6 g,以40 mL无水乙醇溶解后,通过恒压滴液漏斗缓缓滴加至反应液中, 滴加完毕通入氮气保护,加热搅拌至回流开始计时,反应12 h。 反应结束后,静置冷却至室温。滤去不溶物,滤液减压浓缩至约20 mL左右,抽滤,滤饼用10 mL无水乙醇洗涤,滤液继续浓缩至干。所得油状物用乙酸乙酯溶解,依次用5%盐酸、饱和食盐水洗涤,干燥,蒸干。所得黑色油状物以硅胶柱层析法(环己烷∶乙酸乙酯3∶1至1∶1)纯化,得到产物黄色油状物2.02 g,产率46.3%,经核磁共振波谱法验证为4'-苄氧基-2',3',4-三甲氧基-6',3-二羟基查尔酮(化合物1),1H-NMR (400 MHz, CD3OD) δ 8.07 (s, 1H),7.21~7.43 (m, 9H),6.29 (s, 1H), 5.19 (s, 1H),3.81 (d, 6H),3.74 (s, 3H)。
2.2 2',3',4-三甲氧基-4',6',3-三羟基二氢查尔酮(化合物2)的合成向100 mL 厚壁圆底烧瓶中依次加入化合物
1 1.09 g,钯碳0.7 g,无水乙醇30 mL,安装三通换气阀。以氮气置换体系中的空气3次后,检漏。以配置减压阀的氢气瓶将体系内氮气置换为氢气,最终维持在约0.1 MPa的内压下,室温下搅拌反应4 h。反应完毕后,将反应液小心地常压过滤以回收钯碳,滤饼用30 mL无水乙醇分多次洗涤,滤液浓缩至干。所得红棕色胶状物以硅胶柱层析法(环己烷∶乙酸乙酯3∶1至1∶1)纯化,得到产物黄色油状物0.65 g,产率74.9%,经核磁共振波谱法验证为4',3-二苄氧基-2',3',4-三甲氧基-6'-羟基二氢查尔酮(化合物3),1H-NMR (400 MHz, CD3OD) δ 9.62 (br, 1H),6.72 (s, 1H),6.59 (s, 2H),6.07 (s, 1H),3.88 (s, 3H),3.86 (s, 3H),3.61 (s, 3H),2.61 (t, 2H),2.52 (t, 2H)。
2.3 4',3-二苄氧基-2',3',4-三甲氧基-6'-羟基二氢查尔酮(化合物3)的合成
向装有温度计及恒压滴液漏斗的三颈瓶中加入0.7 g化合物2及碳酸钾0.83 g,丙酮30 mL。将此反应装置置于磁力搅拌低温槽中,低温槽温度设为-3 ℃。搅拌均匀后,从恒压滴液漏斗中滴加0.82 g苄溴。滴毕,转移至室温下搅拌2 h,升温至回流反应2 h。反应结束后,静置冷却至室温,倒入水中以去除苄溴。将该混合物减压蒸去丙酮,以乙酸乙酯50 mL分3次提取残余水溶液,乙酸乙酯层合并后依次用饱和碳酸钠溶液、饱和食盐水洗涤,干燥,蒸干。所得黑色油状物以硅胶柱层析法(环己烷∶乙酸乙酯10∶1至2∶1)纯化,得到产物褐色固体0.75 g,产率71.4%,经薄层色谱法初步证实后,用于下步反应。
2.4 5,6,4'-三甲氧基-7,3'-羟基二氢高异黄酮(化合物4)的合成
向50 mL 厚壁圆底烧瓶中依次加入0.53 g化合物3,0.24 g DMF-DMA,甲苯30 mL,搅拌溶解后,安装冷凝管,加热至回流反应6 h。
冷却至室温后,向体系投入钯碳0.2 g,安装三通换气阀。以氮气置换体系中的空气3次后,检漏。以配置减压阀的氢气瓶将体系内氮气置换为氢气,最终维持在约0.1 MPa的内压下,室温下搅拌反应2 h。反应完毕后,将反应液小心地常压过滤以回收钯碳,滤饼用30 mL甲苯分多次洗涤,滤液浓缩至干。所得红棕色胶状物以硅胶柱层析法(环己烷∶乙酸乙酯1∶1)纯化,得到产物黄色油状物198 mg,产率54.9%。经核磁共振波谱法验证为化合物4,1H-NMR (400 MHz,CD3OD) δ 6.79 (d, J =9.6Hz,1H),6.69 (s,1H),6.66 (dd,1H),6.21 (s,1H),4.34 (dd,J=7.6, 2.8Hz,1H),4.19 (dd,J=7.6,2.4 Hz,1H),3.77 (s, 3H), 3.75 (s, 3H),3.62 (s, 3H),2.93 (dd,J=8.6,2.3Hz,1H),2.67 (m,1H),2.51 (dd,J =9.6,7.2Hz,1H)。
2.5 杜鵑兰酮的合成
将72 mg化合物4加入10 mL圆底烧瓶中,加入氯仿2 mL,搅拌溶解,将此反应装置置于磁力搅拌低温槽中,低温槽温度设为-10 ℃。于搅拌下向反应液中滴入碘代三甲硅烷 90 mg的4 mL氯仿溶液。滴毕,保持在低温槽中搅拌10 min,然后将反应体系温度上升到室温反应1 h,薄层色谱法监控反应,待反应结束后,将反应液倒入10 mL甲醇中。减压蒸馏,剩余物以30 mL氯仿溶解后,分别用亚硫酸氢钠水溶液和饱和碳酸氢钠溶液洗涤,饱和食盐水洗涤,干燥,蒸干。所得黑色油状物以硅胶柱层析法(环己烷∶乙酸乙酯2∶1至1∶1)纯化,得到产物褐色固体48.6 mg,产率70.3%。经核磁共振波谱法验证为目标产物杜鹃兰酮,1H-NMR (400 MHz, CD3OD)δ 7.02 (d, J =5.8 Hz,1H),6.87 (s,1H),6.64 (m, 1H),5.89 (s, 1H),4.47 (dd, J=7.6,2.8 Hz,1H),4.11 (dd, J=7.6,4.8 Hz,1H),4.01 (s, 3H), 3.93 (s, 3H),3.14 (dd, J=9.2,3.2 Hz, 1H),2.78 (m, 1H),2.50 (dd, J=9.2,3.2 Hz ,1H)。
3 杜鹃兰酮制备中选择性去甲基化工艺探索
在杜鹃兰酮的合成中,其7位羟基可以通过苄基进行保护,并在制备过程中通过氢化反应脱去苄基。然而,5位羟基从起始原料4-苄氧基-6-羟基-2,3-二甲氧基苯乙酮开始,在制备过程中始终被甲基保护,最终如何在不影响6,4'位的两个甲氧基的情况下,选择性地断开醚键,脱去5位羟基上的甲基,是杜鹃兰酮制备过程中的重要科学问题。
笔者考察了在该选择性去甲基化反应中反应溶剂、反应温度对目标产物得率的影响。
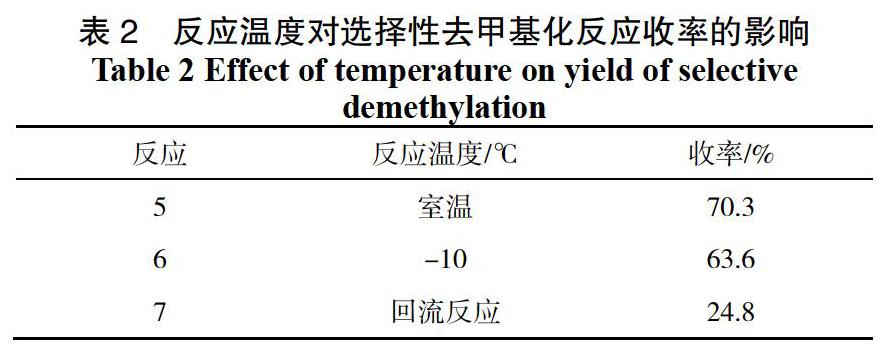
考察反应溶剂对选择性去甲基化反应收率的影响时,考察了质子溶剂、非质子极性溶剂、中等极性溶剂及低极性溶剂等体系,考察结果如表1、表2。
考察反应温度对选择性去甲基化反应收率的影响时,采用氯仿为溶剂,考察结果如下。
从表1及表2中可以看出, 化合物4的最佳选择性去甲基化反应条件为以氯仿为溶剂,室温下反应。
4 结束语
本研究以碘代三甲硅烷作为去甲基化试剂,在温和的条件下实现了杜鹃兰酮5位的选择性去甲基化。该选择性的实现,可能是由于该甲氧基旁边4,6位的羰基和甲氧基的位阻效应,迫使该甲氧基略离开了苯环平面,使该甲氧基的氧原子无法与苯环共轭,氧无法接受苯环电子云的共轭效应,电负性增加,从而易接受亲电进攻。在研究中,我们考察反应温度时发现,在较高温度下难以实现更高的收率,可能是因为在较高的温度下,其他甲氧基上氧原子的反应活性提高了,难以实现区域选择性的缘故。
本研究发现,去甲基化反应的最适合溶剂为氯仿,采用其他质子溶剂、非质子极性溶剂、低极性溶剂均无法获得较好的结果。这可能是因为该反应机理为先生成离子化的碘化鎓盐中间体,该鎓盐再生成硅氧烷中间体,这一步反应为较慢的限速步骤。因此,可以合理推测[14-15],在极性溶剂中鎓盐得到了较好的溶剂化,使其参与的反应的活化能垒提高,不利于反应的进行。当使用低极性的甲苯作为溶剂时,收率降低可能是因为鎓盐中间体的溶解性问题或区域选择性较差导致的,该原因有待在后续研究中进一步探讨。
参考文献:
[1]YAU J W, ROGERS S L, KAWASAKI R, et al. Global prevalence and major risk factors of diabetic retinopathy[J]. Diabetes Care, 2012, 35 (3): 556-564.
[2]MISHRA M, RESSLER A, SCHLESINGER L S, et al. Identification of OprF as a complement component C3 binding acceptor molecule on the surface of Pseudomonas aeruginosa[J]. Infection & Immunity, 2015, 83(8): 3006-3014.
[3]ELMAN M J, HAIJING Q, LLOYD P A, et al.Intravitreal Ranibizumab for Diabetic Macular Edema with Prompt versus Deferred Laser Treatment : Three-Year Randomized Trial Results[J]. Ophthalmology, 2012, 119(11): 2312-2318.
[4]ELMAN M J, ALLISON A, BRESSLER N M, et al. Intravitreal Ranibizumab for Diabetic Macular Edema with Prompt versus Deferred Laser Treatment: 5-Year Randomized Trial Results[J]. Ophthalmology, 2015, 122(11): 375-381.
[5]SIBEL D, SENGUL O. Pigment epithelial tears associated with anti-VEGF therapy: incidence, long-term visual outcome, and relationship with pigment epithelial detachment in age-related macular degeneration[J]. Retina, 2014, 34(6):1156-1162.
[6]D'AMORE P A. Vascular Endothelial Cell Growth Factor-A: Not Just For Endothelial Cells Anymore[J]. American Journal of Pathology, 2007, 171(1):14-18.
[7]ADINOLFI M, CORSARO M, LANZETTA R, et al. Ten homoisoflavanones from two Muscari species[J]. Phytochemistry, 1986, 26(1):285-290.
[8]SHIM J S, KIM J H, LEE J, et al. Anti-angiogenic activity of a homoiso-flavanone from Cremastra appendiculata[J]. Planta
Medica, 2004, 70(2): 171.
[9]SULAIMAN RS, BASAVARAJAPPA HD, Corson TW. Natural product inhibitors of ocular angiogenesis[J]. Exp. Eye Res, 2014, 129:161-171.
[10]KIM J H, KIM K H, YU Y S, et al. Homoisoflavanone inhibits retinal neovascularization through cell cycle arrest with decrease of cdc2 expression[J]. Biochem. Biophys. Res.Commun,2007, 362 (4): 848-852.
[11]LEE B, BASAVARAJAPPA H D, SULAIMAN R S, et al. The first synthesis of the antiangiogenic homoisoflavanone, cremastranone[J]. Org Biomol Chem. , 2014, 12 (39): 7673-7677.
[12]LEE H, YUAN Y, RHEE I,et al. Synthesis of Natural Homoisoflavonoids Having Either 5,7-Dihydroxy-6-methoxy or 7-Hydroxy-5,6-dimethoxy Groups [J]. Molecules, 2016, 21(8): 1058-1068.
[13]BASAVARAJAPPA H D, LEE B, LEE H, et al. Synthesis and Biological Evaluation of Novel Homoisoflavonoids for Retinal Neovasculariza- tion[J]. J. Med. Chem.,2015,58 (12): 5015-5027.
[14]屈剛,李宏,刘玉荣,等. 润滑油基础油络合脱氮的溶剂选择[J].当代化工,2004,33(4):197-199.
[15]李长海. 溶度参数对聚α-烯烃油溶剂选择的影响[J]. 当代化工,2011,40(11):1131-1132.
基金项目:陕西省教育厅专项科研计划项目(项目编号:19JK0772);西安医学院大学生创新创业训练计划项目(项目编号:2018DC-32,
2018DC-75)。
收稿日期:2020-04-04
作者简介:陈卓,男,副教授,研究方向:新药开发。E-mail:chenzhuo_chem@outlook.com。
