腹腔感染患者感染源控制时机与预后的关系
2020-07-17文静汤展宏
文静 汤展宏
摘要:目的 探討腹腔感染患者采取感染源控制措施的时机对疾病预后的影响。方法 回顾性分析广西医科大学第一附属医院重症医学科二病区2015年7月~2018年12月收治的101例腹腔感染患者的临床资料,根据入院时间或住院期间出现腹腔感染的时间到采取感染源控制措施的时间间隔将患者分成≤6 h组、6~12 h组、12~24 h组、24~48 h组、>48 h组5组,并将6~12 h组、12~24 h组、24~48 h组及>48 h组设为>6 h组,比较各组死亡率、≤6 h组与>6 h组在住院时间、重症监护室(ICU)监护时间、呼吸机治疗时间、连续性血液净化治疗(CRRT)时间、住院费用及并发症发生情况。结果 患者总体死亡率为34.65%(35/101),≤6 h组死亡率为29.17%,低于6~12 h组(35.71%)、12~24 h组(42.11%)、24~48 h组(33.33%)、>48 h组(34.62%)4组死亡率,但差异无统计学意义(P>0.05)。≤6 h组在住院时间、住院费用、腹腔出血的并发症方面优于>6 h组,差异有统计学意义(P<0.05);≤6 h组在肺炎及血流感染的发生率、ICU监护时间、呼吸机治疗时间、CRRT治疗时间均少于>6 h组,在呼吸衰竭、腹腔脓肿的发生率与>6 h组相当,在急性肾衰竭、多器官功能障碍综合征(MODS)、肠梗阻、腹腔间隙综合征发生率方面则高于>6 h组,但差异均无统计学意义(P>0.05)。结论 在6 h时间窗内尽早采取感染源控制措施并未明显改善腹腔感染患者的不良预后,但在缩短患者的住院时间,减少住院费用,以及减少腹腔出血并发症的发生方面可能具有一定的优势。
关键词:腹腔感染;感染源;控制措施;时机;预后
中图分类号:R656 文献标识码:A DOI:10.3969/j.issn.1006-1959.2020.11.025
文章编号:1006-1959(2020)11-0086-06
Abstract:Objective To investigate the impact of the timing of infection source control measures on the prognosis of patients with abdominal infection.Methods To retrospectively analyze the clinical data of 101 patients with abdominal infections admitted to the Second Ward of the Department of Critical Medicine of the First Affiliated Hospital of Guangxi Medical University from July 2015 to December 2018. The time interval of source control measures divided the patients into ≤6 h group, 6~12 h group, 12~24 h group, 24~48 h group,>48 h group 5 groups, and 6~12 h group, 12~24 h group , 24~48 h group and group>48 h were set as group>6 h, comparing the mortality in each group, group ≤6 h and group>6 h in hospital stay, intensive care unit (ICU) monitoring time, ventilator duration of treatment, the duration of continuous blood purification therapy (CRRT), the cost of hospitalization, and the occurrence of complications.Results The overall mortality rate of the patients was 34.65% (35/101), and the mortality rate in the ≤6 h group was 29.17%, lower than the 6-12 h group (35.71%), 12~24 h group (42.11%), 24~48 h group (33.33%),>48 h group (34.62%) 4 groups mortality, but the difference was not statistically significant (P>0.05). The ≤6 h group was superior to the ≥6 h group in terms of hospitalization time, hospitalization costs, and complications of abdominal bleeding,the difference was statistically significant (P<0.05); the ≤6 h group had the incidence of pneumonia and bloodstream infection, ICU Monitoring time, ventilator treatment time, and CRRT treatment time were all less than>6 h group. The incidence of respiratory failure and abdominal abscess was similar to that of>6 h group. In acute renal failure, multiple organ dysfunction syndrome (MODS), The incidence of intestinal obstruction and celiac space syndrome was higher than that in the group> 6 h, but the difference was not statistically significant (P>0.05).Conclusion Taking the source control measures as early as possible within the 6 h time window does not significantly improve the poor prognosis of patients with abdominal infections, but may have certain advantages in shortening the hospitalization time of patients, reducing hospitalization costs, and reducing the incidence of abdominal bleeding complications.
Key words:Abdominal infection;Source of infection;Control measures;Timing;Prognosis
脓毒症(sepsis)是目前全球重大的公共卫生问题之一[1],全球每年有超过1900万的脓毒症患者,其中的死亡人数高达530万[2,3],腹腔感染(intra-abdominal infection,IAI)是脓毒症及感染性休克的第2大病因,同时也是重症监护病房(ICU)中感染性疾病患者的第2大死因,如不能及时有效处理可进一步发展为脓毒症、感染性休克,最终可导致多器官功能衰竭,从而增加患者的死亡率。腹腔感染治疗的关键措施包括复苏、感染源控制以及抗菌药物的使用,其中感染源控制是治疗的基础,给予感染源控制措施的时机可能影响患者预后,2012年版本的脓毒症与感染性休克治疗国际指南(SSC 2012)建议感染源控制措施应在确诊的12 h内启动[4],而 2016年版本的脓毒症与感染性休克治疗国际指南(SSC 2016)要求在符合医疗原则的情况下尽可能快的控制感染源[5]。美国外科感染学会2017年发布的腹腔感染管理指南(SISAcIAI2017)建议除临床证据表明非介入治疗或延迟治疗是适当的,否则应在诊断腹腔感染后的24 h内进行感染源控制,对合并有脓毒症以及感染性休克的患者,应以更紧急的方式进行感染源控制[6],可见目前对于感染源控制措施实施的时机尚存在争议。本研究通过回顾性分析101例腹腔感染患者的临床资料,旨在探讨腹腔感染患者采取感染源控制措施的时机对该疾病预后的影响,现报道如下。
1资料与方法
1.1一般资料 收集2015年7月~2018年12月广西医科大学第一附属医院重症医学科二病区收治的101例腹腔感染患者的临床资料,其中新入院患者以入院时间作为时间“零点”,住院期间获得腹腔感染的患者以出现相关临床、体征的时间作为时间“零点”,根据患者的时间“零点”到首次感染源控制措施开始的时间间隔将患者分为5组,分别为≤6 h组(24例)、6~12 h组(14例)、12~24 h组(19例)、24~48 h组(18例)、>48 h组(26例),其中6~12 h组、12~24 h组、24~48 h组、>48 h组4个组的患者统称为>6 h组(77例),对各组患者的资料进行回顾性分析。纳入患者符合:①出院主要诊断为腹腔感染,按广义的腹腔感染的定义,包括肠坏死、肠梗阻、胃肠穿孔以及阑尾炎等空腔脏器引起的腹腔内的细菌性炎症,也包括肝、脾等实质性脏器感染病原体而形成脓肿的情况,还包括胰腺等腹膜后脏器炎症引起的腹膜后感染;根据美国外科感染学会2010年腹腔感染管理指南,通过患者的临床症状、体征、实验室检查及CT检查结果进行诊断,且均经感染源控制措施留取标本进一步确诊;②年龄>18岁;③首次感染源控制措施在本院进行;④临床资料完整。
1.2方法 在时间“零点”收集患者的一般资料,包括性别、年龄、合并症、生命体征、血常规、肝功能、肾功能、电解质、血气分析、腹部X线片和(或)腹部超声和(或)腹部计算机断层扫描(CT)等评估结果、Glascow昏迷评分、急性生理学和既往健康评分(APACHE Ⅱ评分)和脏器功能障碍严重度评分(SOFA评分)等指标。
1.3观察指标 比较≤6 h组、6~12 h组、12~24 h组、24~48 h组、>48 h组的死亡率,另外分析比较≤6 h组与>6 h组在死亡率、住院时间、ICU 监护时间、呼吸机治疗时间、连续性血液净化治疗(CRRT)时间、住院费用以及各种并发症等指标上的差异。
1.4统计学处理 使用SPSS 22.0统计软件,分类变量使用(n)和(%)表示,连续变量使用(x±s)或四分位数表示,对连续变量进行分组,根据数据类型分别采用?字2检验、Wilcoxon秩和检验和方差分析3种不同的方法进行组间差异比较。本研究设定假设检验为双尾检验,P<0.05表示差异有统计学意义。
2结果
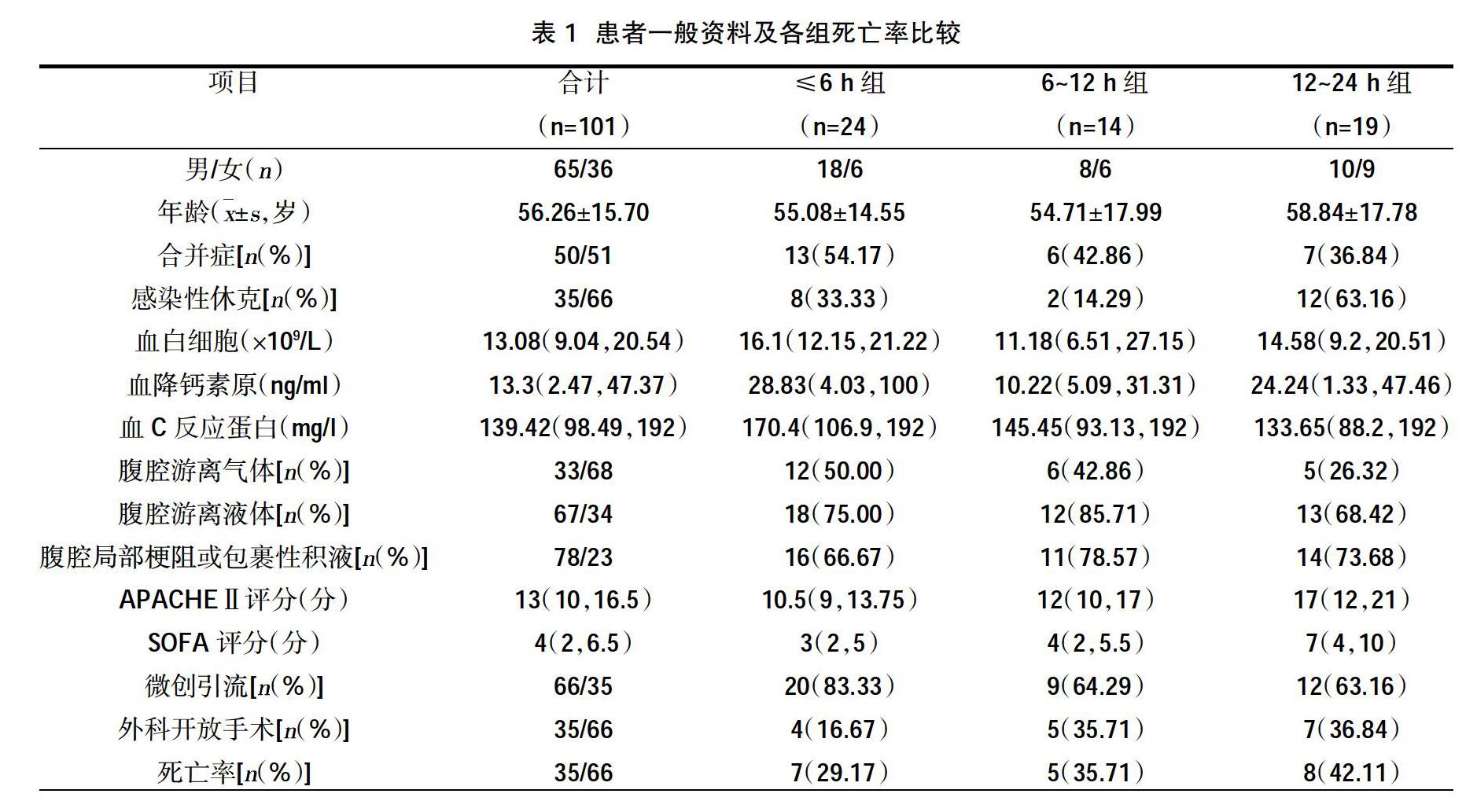
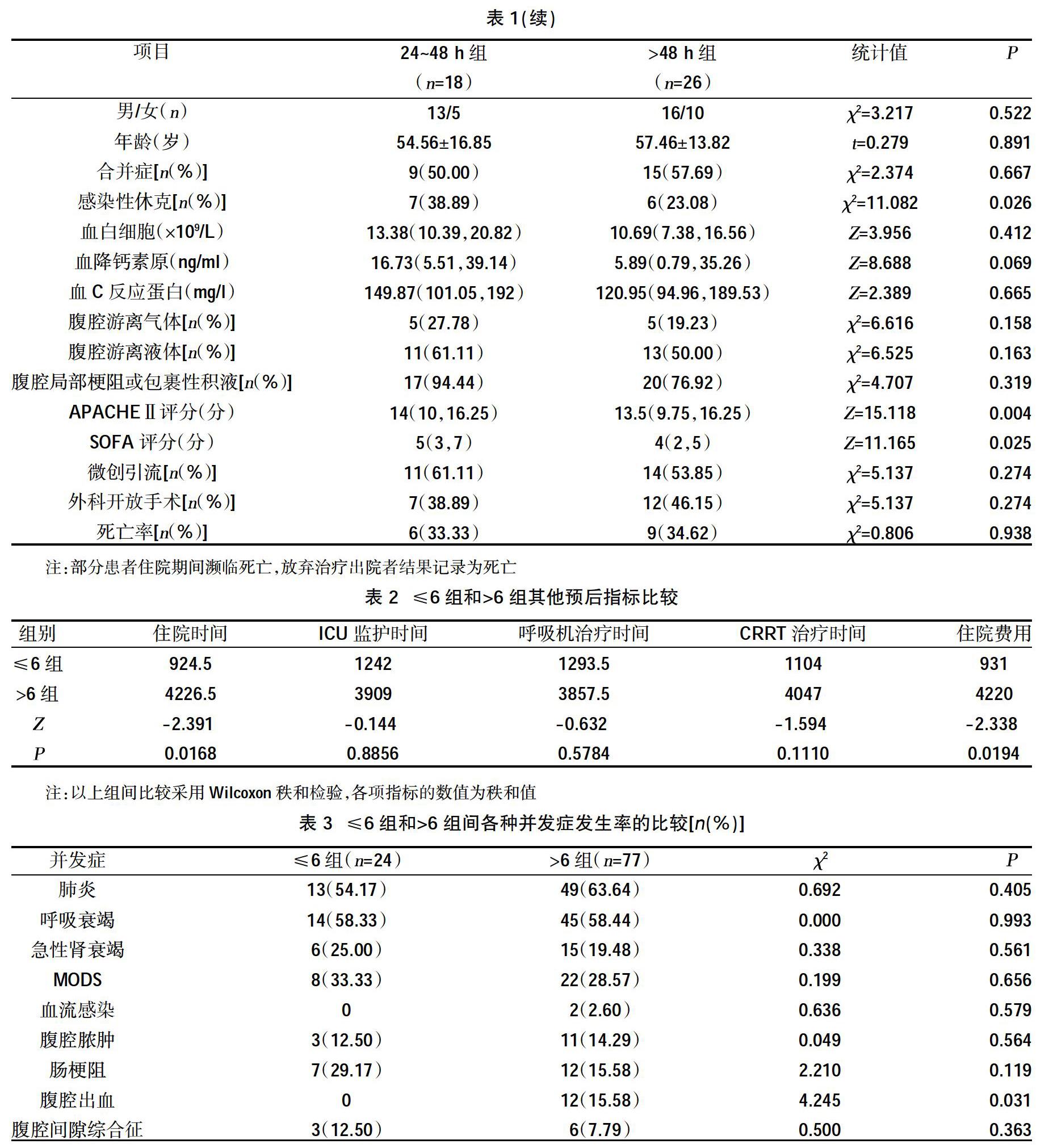
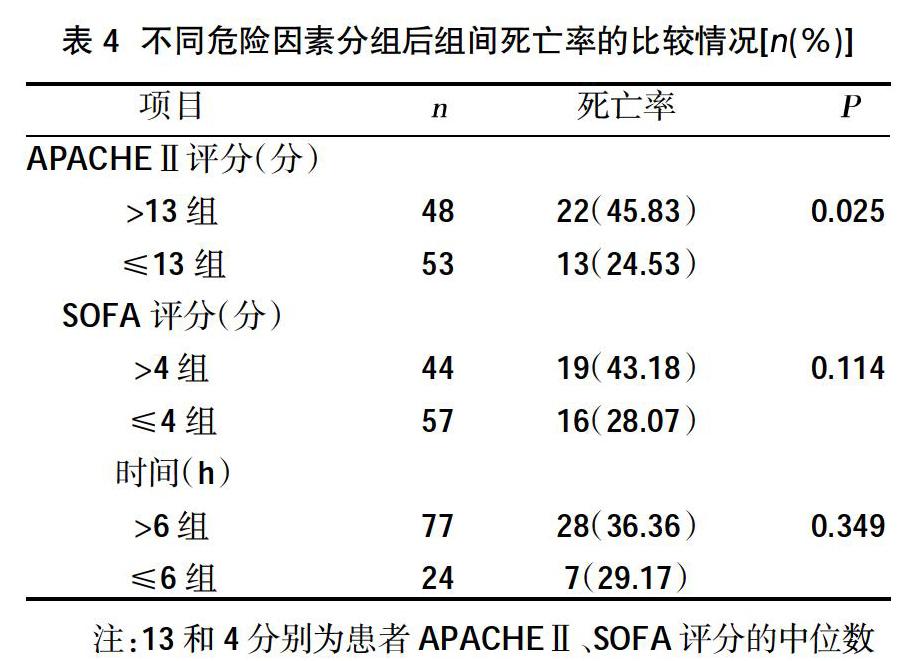
列入研究的101例患者中有21例为住院期间腹部手术后继发感染,占20.79%,其余为院外感染后新入院患者(79.21%)。病变部位的分布情况:胆道系统占比最多,为25.74%,其次为大肠(18.81%)、小肠(17.82%)、胃(11.88%),十二指肠、胰腺、肝、阑尾的比例在10%以下,其中阑尾最少、约为2.97%。病因方面,有18例为恶性肿瘤患者,占17.82%,其余为良性疾病患者(82.18%)。感染源控制时间窗范围为21(0.5~600)h。控制感染源的措施主要为B超引导下的穿刺引流或ERCP等微创介入技术和外科开腹手术2种,见表1~表4。
3讨论
腹腔感染是一种涉及腹腔内多个部位、多种病因的综合征,临床表现多样化,个体差异大,又不能完全分割,多数情况下需要紧急处理,且处理措施中包括微創的或开放的手术操作,不同个人、不同医疗机构、不同地区之间的操作水平差异难以衡量,同时考虑伦理道德方面的限制等原因,不仅很难实施大型的多中心前瞻性研究,常规的临床研究也面临重重困难。到目前为止,现有证据标明感染源控制的最佳时机[6]。
研究显示[7],从诊断到感染源控制时间间隔是腹腔感染患者死亡的预测因素。然而,既往研究并未见明确标准说明应该何时启动感染源控制措施。临床医师在是否开始感染源控制的决策上往往较为谨慎,常需行充分的实验室检查以达到精确的病情评估、CT检查以对病变部位进行更准确的定位、进行充分的液体复苏实现血流动力学稳定等处理后再开始感染源控制的措施,但上述措施全部完善后可能会导致感染源控制延迟,增加感染源控制失败的风险。
既往研究显示[8,9],对于血流动力学不稳定的脓毒症患者,可能需要短时间延迟开始感染源控制的时间才能快速复苏。2008年版本的脓毒症与感染性休克治疗国际指南(SSC 2008)亦建议只有在成功的初始复苏后才能开始进行针对感染源的干预措施[10]。
但最新版本的SSC(SSC 2016)和SISAcIAI2017不再强调必需成功复苏后才能开始控制感染源[5,6]。De De Waele JJ的研究提出消化道穿孔及弥漫性腹膜炎患者应在诊断后1~2 h内进行手术,不论其对复苏尝试的反应如何[11]。Azuhata T等[12]的一项对154例胃肠穿孔患者的前瞻性观察性研究显示,入院到实施感染源控制的时间是影响患者存活率的独立因素,研究表明,按照目标导向性复苏策略对患者进行初始复苏,即使在患者血流动力学不稳定的情况下,及早手术仍可显著改善患者预后,随着入院到手术时间的延长,存活率下降,当入院到手术开始时间超过6 h时,60 d存活率为0。Rausei S等[13]回顾性分析了111例使用腹腔开放疗法作为感染源控制措施的严重腹腔感染患者的临床资料后发现,早期手术可以显著改善患者的预后,6 h内进行手术治疗的患者死亡率较超过6 h才手术的患者低,而初级筋膜关闭率较后者高,且手术每延迟 6 h,患者的死亡率逐渐增高,初级筋膜关闭率逐渐下降。但值得强调的是该研究里的死亡率以及初级筋膜关闭率的高峰出现在了与预后相关的APACHEⅡ评分及SOFA评分得分最高的6~12 h组,说明相较于手术时机对预后的影响,患者病情的严重程度对预后的影响更为关键。同时,另有研究提出病情对预后的影响比手术时机的影响更 大[5,14,15]。因此,血流动力学不稳定的情况下是否应开始感染源控制措施,给予了积极的复苏治疗血流动力学状态仍无法改善的重症感染患者的处理仍存在争议,有待进一步研究。
本研究模拟了Rausei S等[13]的方法对研究对象进行观察,从各组实际死亡率上看,呈现的趋势如下:≤6 h组的死亡率在各组中最低,且≤6 h组、6~12 h组、12~24 h组3组的死亡率随着手术时间的延迟逐渐递增,死亡率高峰出现在12~24 h组,24~48 h组死亡率稍低于>48 h组,但24~48 h组、>48 h组两组的死亡率均低于6~12 h组及12~24 h组。同时,各组死亡率的高低与它们的APACHEⅡ评分及SOFA评分的平均分值的高低基本一致。并且,101例患者中APACHEⅡ评分>中位数分数13分的患者死亡率高于APACHEⅡ评分≤13分的患者,差异有统计学意义(P<0.05),与Rausei S等[13]的研究中观察到的情况是一致的。但此本研究各组死亡率比较,差异无统计学意义(P>0.05)。
本研究的没有限定控制感染源的具体措施,Rausei S等[13]研究的对象均为接受腹腔开放疗法治疗的严重腹腔感染患者,而本研究入组的患者感染源控制措施主要为B超引导下的穿刺引流或ERCP等微创介入技术以及外科开腹手术2种,具体方式的选择是根据当时患者的病情、患者及家属的意愿、外科医师的经验以及医院的条件等因素决定的。目前被认为有效的感染源处理措施包括传统的剖腹探查和脓肿切开引流、经皮脓肿穿刺引流、腹腔镜探查和引流、腹腔开放疗法等[16]。指南(SISAcIAI2017)建议在能够达到有效控制感染源的目标的前提下,优先选择损伤最小的干预措施。但SISAcIAI2017指南同时指出:对局部腹腔感染患者而言,选择经皮穿刺引流等微创手术治疗是合理的;对弥漫性腹膜炎患者而言,需要进行剖腹手术,部分重症患者甚至需要采取腹腔开放疗法[6]。对此,王革非等[17]亦提出了递增式的感染源治疗策略:首先选择微创手术达到改善引流的目的或者建立主动的引流途径;上述方式无法有效的控制感染源时应考虑行开腹手术引流,手术需遵循损伤控制的原则;合并腹腔高压的患者应积极采用腹腔开放疗法进行干预。在本研究中,所有患者感染源控制方式的选择基本符合指南以及专家的建议。但是受医院及外科医师技术条件的限制、患者及家属的意愿、社会风俗习惯等因素的影响,本次纳入研究的患者极少采用腹腔开放治疗,因此部分患者可能存在感染源控制措施选择欠合理、感染源控制欠充分的情况,而感染源控制不足可導致包括死亡率增加在内的多种不良后果[18]。
另外,为了更好地观察感染源控制时机与预后的关系,本研究增加了≤6 h组和>6 h组在住院时间、ICU 监护时间、呼吸机治疗时间、连续性血液净化(CRRT)治疗时间、住院费用以及各种并发症方面的比较,结果显示≤6 h组在住院时间、住院费用、腹腔出血的并发症方面优于>6 h组,差异有统计学意义(P<0.05),在肺炎及血流感染的发生率、ICU监护时间、呼吸机治疗时间、CRRT治疗时间均少于后者,但差异无统计学意义(P>0.05),而在呼吸衰竭、腹腔脓肿的发生率与后者相当,甚至在急性肾衰竭、多器官功能障碍综合征(MODS)、肠梗阻、腹腔间隙综合征发生率方面高于后者,这可能与手术影响复苏方案的充分实施以及复苏目标的监测与判断、手术损伤等因素有关,手术创伤对危重患者而言有时是不可忽视的,损伤控制外科理念的存在即很好的证明了这一点,但以上项目的比较差异无统计学意义(P>0.05),需进一步的研究了解其间的关系。
总之,本次研究仍存在不足之处。首先,小样本量的回顾性分析的方法限制了结果的准确性。其次,本次研究样本是不均匀,既有在院外已获得感染的新入院患者,又有手术后并发腹腔感染的患者;既有消化性溃疡穿孔、胆石症并感染等良性疾病的患者,也有恶性肿瘤患者;各组患者间的一般资料比如APACHEⅡ评分及SOFA评分的分布也是不均匀的,这些干扰因素无疑会影响结果的判断。再次,因为有时候出现症状的时间是很难确定的,所以“零点”时间的定义未包括新入院病人从出现症状到入住医院期间的时间长短,这些都可能会影响研究的结果。
参考文献:
[1]Singer M,Deutschman CS,Seymour CW,et al.The Third International Consensus Definitions for Sepsis and Septic Shock(Sepsis-3)[J].JAMA,2016,315(8):801-810.
[2]Sep Net Critical Care Trials Group.Incidence of severe sepsis and septic shock in German intensive care units:the prospective,multicentre INSEP study[J].Intensive Care Medicine,2016,42(12):1980-1989.
[3]Angus DC,van der Poll T.Severe sepsis and septic shock[J].N Engl J Med,2013,369(9):840-851.
[4]Dellinger RP,Levy MM,Rhodes A,et al.Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septicshock,2012[J].Crit Care Med,2013,41(2):580-637.
[5]Rhodes A,Evans LE,Alhazzani W,et al.Surviving Sepsis Campaign:International Guidelines for Management of Sepsis and Septic Shock:2016[J].Critical Care Medicine,2017,45(3):486-552.
[6]Mazuski JE,Tessier JM,May AK,et al.The Surgical Infection Society Revised Guidelines on the Management of Intra-Abdominal Infection[J].Surgical Infections,2017,18(1):1-76.
[7]Kim JJ,Liang MK,Subramanian A,et al.Predictors of relaparotomy after nontrauma emergency general surgery with initial fascial closure[J].American Journal of Surgery,2011,202(5):549-552.
[8]Solomkin JS,Mazuski JE,Bradley JS,et al.Diagnosis and management of complicated intra-abdominal infection in adults and children:Guidelines by the Surgical Infection Society and the Infectious Diseases Society of America[J].Surg Infect(Larchmt),2010,11(1):79-109.
[9]Friedrich AKU,Cahan M.Intraabdominal Infections in the Intensive Care Unit[J].Journal of Intensive Care Medicine,2014,29(5):247-254.
[10]Dellinger RP,Levy MM,Carlet JM,et al.Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock:2008[J].Crit Care Med,2008,36(1):296-327.
[11]De Waele JJ.Early source control in sepsis[J].Langenbecks Arch Surg,2010,395(5):489-494.
[12]Azuhata T,Kinoshita K,Kawano D,et al.Time from admission to initiation of surgery for source control is a critical determinant of survival in patients with gastrointestinal perforation with associated septic shock[J].Crit Care,2014,18(3):R87.
[13]Rausei S,Pappalardo V,Ruspi L,et al.Early Versus Delayed Source Control in Open Abdomen Management for Severe Intra-abdominal Infections:A Retrospective Analysis on 111 Cases[J].World Journal of Surgery,2017,42(3):707-712.
[14]Tavaré A,O'Flynn N.Recognition,diagnosis,and early management of sepsis:NICE guideline[J].British Journal of General Practice,2017,67(657):185-186.
[15]Sartelli M,Catena F,Ansaloni L,et al.Complicated intraabdominal infections worldwide:the definitive data of the CIAOW study[J].World J Emerg Surg,2014(9):37.
[16]任建安.腹腔感染風险因素分析与对策[J].中华消化外科杂志,2017,16(12):1167-1171.
[17]王革非,任建安,黎介寿.腹腔感染源的递增式治疗策略[J].医学与哲学,2017,38(12B):8-10.
[18]Tellor B,Skrupky LP,Symons W,et al.Inadequate source control and inappropriate antibiotics are key determinants of mortality in patients with intra-abdominal sepsis and associated bacteremia[J].Surg Infect(Larchmt),2015,16(6):785-793.
收稿日期:2020-04-15;修回日期:2020-04-25
编辑/肖婷婷
