纳米硒化锌制备中的条件控制与优化实验研究
2020-06-30刘力嘉刘静静张丛丛张晓凯
刘力嘉 刘静静 夏 蕾 张丛丛 张晓凯
(1) 山东师范大学物理与电子科学学院,250358,济南; 2) 山东师范大学化学化工与材料科学学院,250014,济南)
近年来,ⅡA-ⅥB(A=Cd, Zn, B=S, Se,Te)族半导体[1]纳米材料的合成吸引了人们大量的兴趣.使用该类纳米材料制作的光电器件能够显示出宏观的优良性能,研究人员正努力探索如何微调与调控纳米半导体材料的超微结构,阐明影响器件宏观物理性质与微观结构之间的内在联系.ZnSe纳米粒子是一种宽带隙[2,3]半导体材料,其带隙宽达2.7 eV.目前,有许多方法用来合成ZnSe纳米晶体,如水热法、化学气相沉积(CVD)、电沉积和模板定向生长,以及Zn和Se颗粒的机械化学合成[4-7].1998年,Hines[8]等人采用有机金属法初次用二乙基锌为前驱体在配体烷基胺中合成了荧光强度较高的紫外-蓝光ZnSe纳米晶.2003年,李焕勇[9]等人创新实验方法,他们在实验过程中改良溶剂热方式制备出一维ZnSe闪锌矿纳米材料.2004年,Shavel[10]等采取水相合成法顺利合成2~3 nm的ZnSe量子点.2005年,Chand[11]等人以Au颗粒作催化,GaAs为衬底,采取分子束外延法顺利制出ZnSe纳米线.2007年,Zheng[12]等人采用GSH作为稳定剂制备出质量较好的ZnSe量子点,合成的量子点颗粒较大且稳定性强,并利用不同Zn/Cd比例来调控量子点荧光波长.2010年,石宝琴[13]等人采用胶体水相法,用具有还原性的L-谷胱甘肽作为稳定剂,在低温下(90~100 ℃)制备出荧光性能较好的ZnSe量子点,其荧光产率达到51%.2014年,Ashrafi[14]等人用氯化锌作锌源,配体是(CH2OH)2和(CH2NH2)2,在200 ℃下制备出纯度很高的ZnSe量子点.ZnSe纳米粒子的应用十分广泛,主要应用于LED显示[15].此外,核壳和空心微球结构[16-18]在催化、传递和控制释放、人工细胞、光电子、微腔共振和光子晶体、太阳能电池、生物医学标签等方面有潜在应用[19,21].本文采用水相合成法制备纳米结构硒化锌,通过调节实验条件及优化方案,最终得到制备ZnSe的最佳优化条件.
1 实验部分
1.1仪器与试剂实验仪器和试剂见表1和表2.
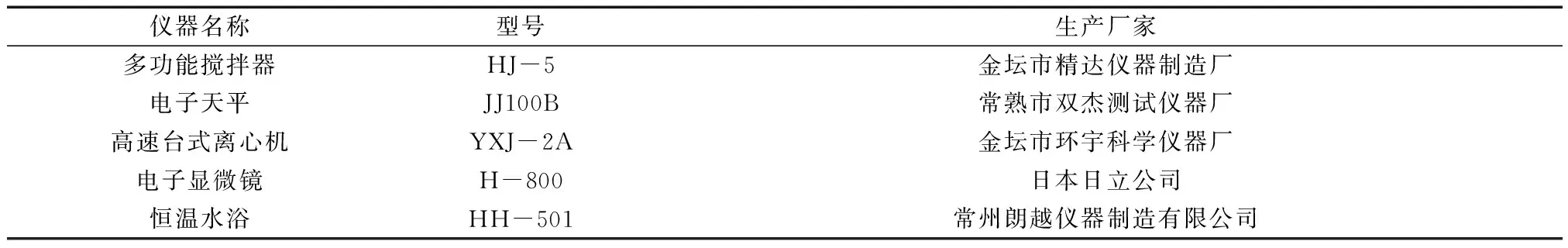
表1 实验仪器
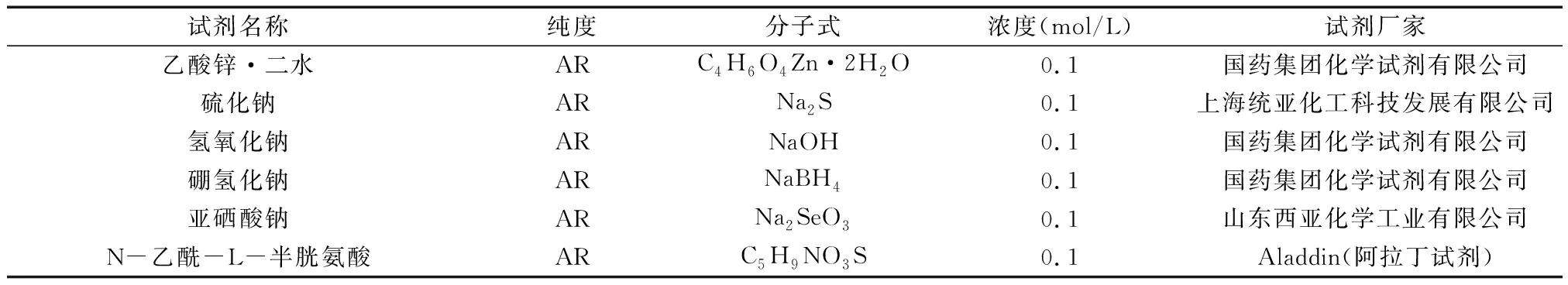
表2 实验试剂
1.2实验机理分析用水热法制备ZnSe纳米粒子,在这个实验过程中重要的三步分别是:NaHSe的制备、Zn前驱体的制备以及ZnSe纳米粒子的水热合成.
1.2.1 NaHSe的制备 采用Na2SeO3作为Se源制备ZnSe纳米粒子,使用NaBH4进行还原,反应现象较为迅速,并且不需要严格的温度与压强,室温下就能生成NaHSe,且反应只能顺向进行.因此,Se前驱体采用NaHSe.硒氢化钠前驱体的制备反应方程式如式(1)所示.
4NaBH4+ 2Na2SeO3+ 5H2O=2NaHSe + Na2B4O7+ 10H2+ 4NaOH.
(1)
1.2.2 Zn前驱体的制备 取适量事先配置好的Zn(CH3COO)2溶液倒入N-乙酰-L-半胱氨酸,搅拌下逐滴加入的NaOH溶液调节pH值,在多功能搅拌器上进行搅拌即得Zn前驱体溶液.
1.2.3 ZnSe纳米粒子的水热合成 把制备好的NaHSe溶液快速倒入Zn前驱体溶液中,反应得到ZnSe纳米粒子.反应方程式如式(2)所示.
Zn(Ac)2+ NaHSe + NaOH = ZnSe + 2NaAc + H2O.
(2)
1.3实验步骤本实验通过水相合成法制备ZnSe纳米粒子,原料为乙酸锌、N-乙酰-L-半胱氨酸、氢氧化钠、亚硒酸钠、硼氢化钠、硫化钠,以三次蒸馏水为溶剂.采用控制变量法研究不同条件对制备ZnSe产物的影响,实验参数变量分别是反应时间、Zn(Ac)2的用量、N-乙酰-L-半胱氨酸的用量,改变变量参数能产生出不同形貌的ZnSe,从中确定制备ZnSe的最佳条件.
在100 mL的锥形瓶中先加入5 mL 0.1 mol/L的Zn(Ac)2,然后加入适量0.1 mol/L的N-乙酰-L-半胱氨酸, 再加入30 ml的蒸馏水,之后再用1 mol/L的NaOH溶液将pH调为中性.在小烧杯中放入适当的0.1 mol/L的Na2SeO3,再加入2.5 mL适量的NaBH4反应生成NaHSe,将小烧杯中的溶液加入到上面的溶液中,通过DHT恒温搅拌电热套搅拌20 min,与此同时,滴加少量的Na2S溶液,这样制备的ZnSe纳米粒子溶液的外表皮包覆着ZnS.最后在恒温水浴锅中老化一定时间,再冷却至室温,ZnSe纳米粒子的制备完成.
2 结果与讨论
2.1ZnSe纳米粒子的透射电镜观察实验中,将ZnSe纳米粒子溶液放入1.5 mL离心管中,然后放入超声波振荡器中进行超声分散, 取一滴样品滴加到铜网上,待观察.
1) Zn∶Se比值为4∶1,Zn(Ac)2∶N-乙酰-L-半胱氨酸=1∶1.2,实验以反应时间为变量分析,分为三组,第一组反应时间为30 min,第二组反应时间为60 min,第三组反应时间为90 min.
图1所示,分别为反应时间30、60和90 min的ZnSe纳米粒子透射电镜图像.由图1(a)看出,在反应时间为30 min时,ZnSe呈颗粒状聚集一起,颗粒大小均匀,其粒径大约在20 nm左右.由图1(b)看出反应时间为60 min时,可以清楚的看到硒化锌呈球状,分散均匀,球径由25 nm到120 nm不等.图1(c)所示的是反应时间为90 min的ZnSe纳米粒子,呈现出颗粒状ZnSe纳米粒子聚集形成的网状结构,其粒径大约在30 nm到120 nm之间.可以得出结论:反应时间与硒化锌的生长形态与分布密切相关.可以推测出,随着反应时间的延长,硒化锌由集中分布的颗粒状逐渐生长成为分散分布的独立球状,反应时间再度延长,球状硒化锌越来越密集并相互连接形成网状.因此,当反应时间为60 min时,硒化锌纳米粒子生长形态比较规律,最有利于球状硒化锌的生成.
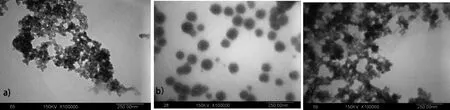
图1 不同反应时间的ZnSe纳米粒子透射电镜图像(a)反应时间30 min; (b)反应时间60 min; (c)反应时间90 min.
2) 试验反应时间为60 min, Zn(Ac)2∶N-乙酰-L-半胱氨酸=1∶1.2,实验以Zn∶Se比值为变量分析.

图2 不同Zn:Se比值的ZnSe纳米粒子透射电镜图像(a)Zn∶Se=1∶1; (b)Zn∶Se=2∶1; (c)Zn∶Se=4∶1.
图2为3种Zn∶Se比值为变量的ZnSe纳米粒子透射电镜图像,由图2(a)可以看出Zn∶Se=1∶1时,ZnSe分布密集形成片状,密度较大,其片状宽度在600 nm左右,长度大约在1 000 nm.图2(b)可以看出Zn∶Se=2∶1时,ZnSe呈现杆状和条状,分布较为均匀,其杆状直径大约在10 nm到20 nm之间.图2(c)观察到Zn∶Se=4∶1时ZnSe呈规则的球状,分散均匀,球径大约在30 nm到120 nm 之间.实验结果发现Zn与Se的比例对ZnSe纳米粒子的密度以及形状有较大的影响.当Zn∶Se=4∶1时,ZnSe纳米粒子分布与分散较好,且呈现为球状.
3) 试验Zn∶Se比值为4∶1,反应时间为60 min,实验以N-乙酰-L-半胱氨酸保护剂与Zn(Ac)2的摩尔比为变量分析.
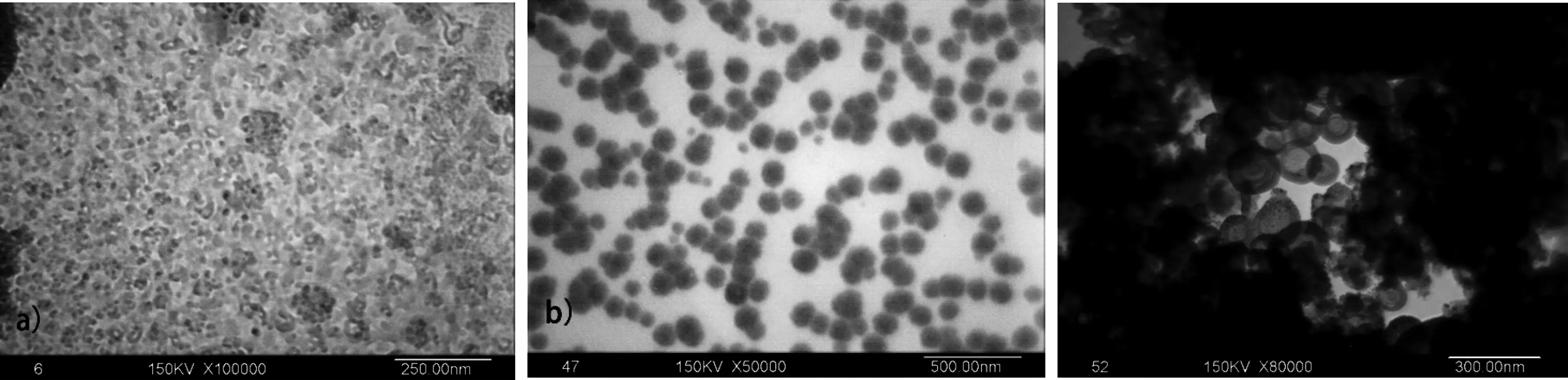
图3 不同Zn(Ac)2与N-乙酰-L-半胱氨酸摩尔比的ZnSe纳米粒子透射电镜图像(a)Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1; (b)Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1.2;(c)Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1.8.
图3为3种Zn(Ac)2与N-乙酰-L-半胱氨酸摩尔比的ZnSe纳米粒子透射电镜图像.由图3(a)可以看出Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1时,ZnSe纳米粒子的形貌呈现规则且密集的颗粒状,其粒径大小基本一致在25 nm左右.当Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1.2时,由图3(b)可知此时生成了分散分布且规则的球状ZnSe,其球径大约在40 nm到120 nm之间.由图3(c)可以看出Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1.8时,ZnSe为环状结构,密度大分布广,且形态十分规律,其内环直径大约在30 nm到60 nm之间,外环直径大约在50 nm到150 nm之间.由以上分析可以看出N-乙酰-L-半胱氨酸保护剂与Zn(Ac)2的摩尔比对ZnSe的形貌影响显著.当Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1时,ZnSe纳米粒子的形貌倾向于呈现为颗粒状;当Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1.2时,ZnSe纳米粒子的形貌倾向于呈现为球状;当Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1.8时,ZnSe纳米粒子的形貌倾向于呈现为环状.
由此可得,当反应时间为60 min,Zn(Ac)2∶N-乙酰-L-半胱氨酸=1∶1.2,Zn∶Se比值为4∶1时硒化锌的形貌结构最为规律,呈现为规则的球状结构.图1(b)、图2(c)和图3(b)均是在此条件下生成的ZnSe纳米粒子电镜图像,选择图2(c)的粒径分布为例进行分析.表3为其粒径分布的统计表,图4为其粒径分布柱状图.由表3中可以分析得到球径范围是33~122 nm,其中79~87 nm之间的硒化锌纳米粒子最多,33~42 nm以及104~122 nm之间的硒化锌纳米粒子最少,绝大部分纳米粒子分布在68 nm到104 nm之间.ZnSe纳米粒子的粒径分布大致呈正态分布,平均粒子直径大约为82 nm.
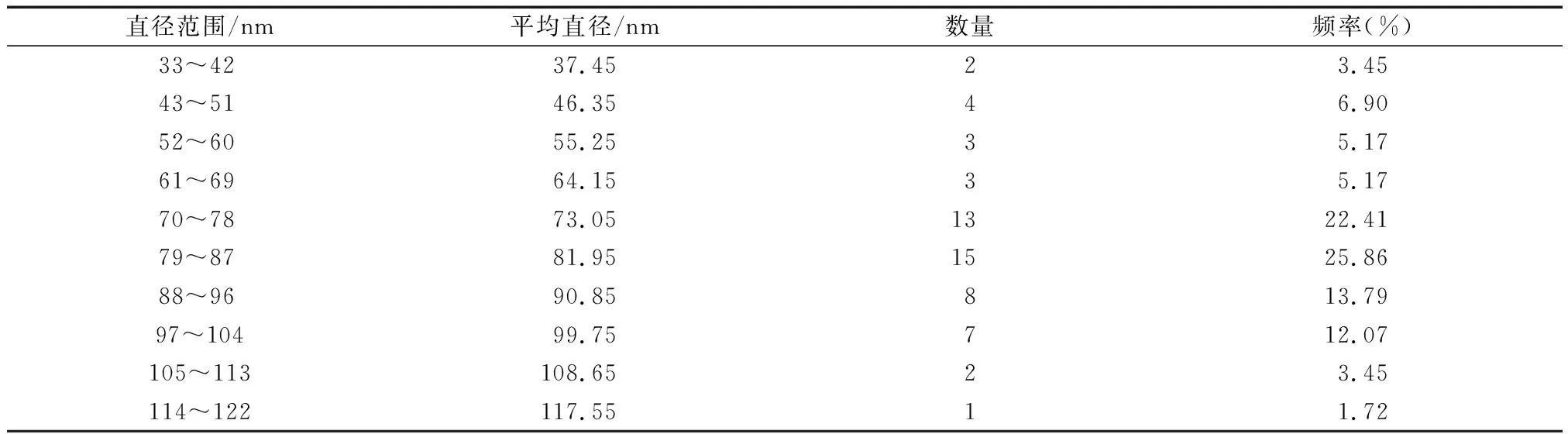
表3 ZnSe纳米粒子粒径分布统计表

图4 ZnSe纳米粒子粒径分布柱状图

图5 ZnSe纳米粒子环状形貌
同时我们也能发现当反应时间为60 min,Zn∶Se比值为4∶1,Zn(Ac)2∶N-乙酰-L-半胱氨酸为1∶1.8时,ZnSe纳米粒子的形貌呈现为规则的环状.图5是由图3(c)中截取放大的一部分,在图5中我们可以分析得到内环1的直径约为为50 nm,次外环2的直径约为100 nm,外环3的直径约为165 nm.同时,在其它环状结构中,还可以看到周围有许多由小颗粒聚集而成的环轮廓,可以推测ZnSe纳米粒子可能是由小颗粒的ZnSe晶核层层堆积在相对较大的纳米颗粒的表层,形成了更大些的纳米颗粒.
2.2ZnSe纳米粒子的红外光谱图6为Zn(Ac)2∶N-乙酰-L-半胱氨酸=1∶1.8的环状ZnSe纳米粒子的红外光谱,图7为Zn(Ac)2∶N-乙酰-L-半胱氨酸=1∶1.2的球状ZnSe纳米粒子的红外光谱,依据其峰值位置变化的不同和分子间的连接情况等信息来分析,由吸收谱可得出如下结论.
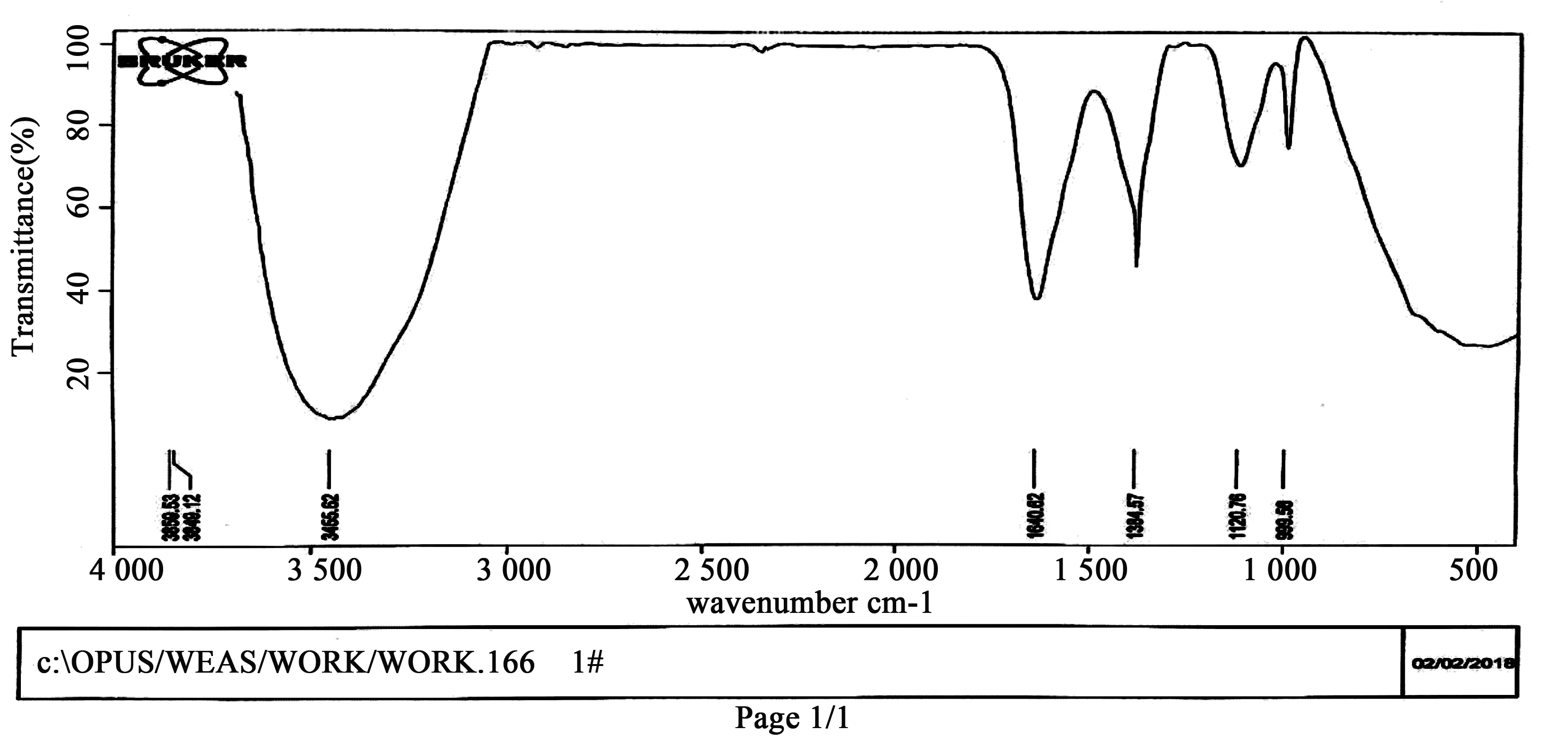
图6 环状ZnSe纳米粒子红外光谱
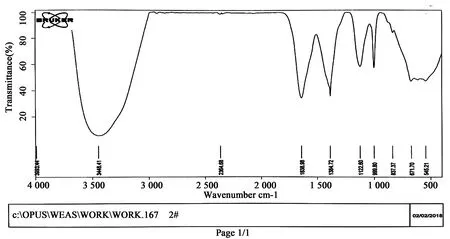
图7 球状ZnSe纳米粒子红外光谱
1) 图6中3 455.62 cm-1处的峰是因为样品没有蒸发掉全部水分而引起的O-H 的伸缩振动峰(νO-H)或是N-H键的伸缩振动(νNH)吸收峰组成,图7中3 448.41 cm-1的峰同理.
2) 图6中若3 455.62 cm-1(vNH,N-H键的伸缩振动)是酰胺基团的振动峰,同时在1 640.62 cm-1处反对称伸缩振动(COO-aS) 和 1 384.57 cm-1处对称伸缩振动(νCOO-S) 相应出现,则说明了N-乙酰-L-半胱氨酸包裹在ZnSe纳米粒子表面.图7中若由3 448.41 cm-1(vNH,N-H键的伸缩振动) 与1 638.98 cm-1处反对称伸缩振动(COO-aS)和1 384.72 cm-1处对称伸缩振动(νCOO-S)也可以得到N-乙酰-L-半胱氨酸包裹在 ZnSe纳米粒子表面的结论.
3) 将图6与巯基乙酸钠的红外光谱图[22]进行对比,可以得出在ZnSe纳米粒子2 600~2 550 cm-1的范围中没有S-H 的伸缩振动(νS-H)峰,由此可以看出S-H 键已断裂,N-乙酰-L-半胱氨酸中的巯基首先和羧酸进行水解,然后与Zn2+配位并包覆于 ZnSe纳米粒子表面,因为ZnSe与 ZnS具有相近的晶格匹配度,所以表面修饰了巯基乙酸的硒化锌粒子更稳定的存在于溶液中.图7同理可解释.
4) 图6中999.56 cm-1(OH)处的吸收峰是羟基的面外变形的振动峰,图7中不仅在999.80 cm-1处有一个峰并且在671.70 cm-1处有一个和ZnS相同的吸收峰,由此更加证明了ZnSe纳米粒子中ZnS层的存在.
由此可见无论是环状ZnSe 纳米粒子还是球状ZnSe 纳米粒子,均为核壳式结构,其表面有ZnS层和N-乙酰-L-半胱氨酸层.
2.3ZnSe纳米粒子的紫外可见吸收光谱图8为Zn(Ac)2∶N-乙酰-L-半胱氨酸=1∶1.2的球状ZnSe纳米粒子的紫外吸收光谱.我们可以看到图8中样品的紫外吸收峰位于300~350 nm左右,与吸收峰为460 nm的块状ZnSe材料比较来说,产生了显著的蓝移.这种向更高能量的蓝移可以归因于ZnSe纳米晶体的量子尺寸效应,因此充分证明了ZnSe纳米粒子是属于纳米尺寸.
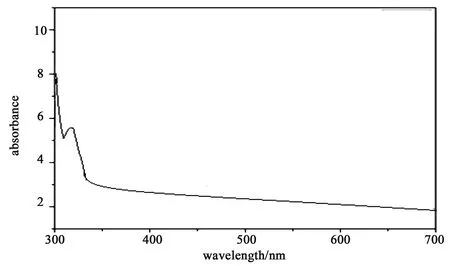
图8 ZnSe纳米粒子的紫外吸收光谱
3 结 语
根据实验结果,优化后的可控最佳实验条件为∶Zn(Ac)2∶Na2SeO3=4∶1,Zn(Ac)2∶N-乙酰-L-半胱氨酸=1∶1.2,反应的时间为60 min,在该条件下制得的ZnSe纳米粒子为规则的球状.由ZnSe 纳米粒子红外光谱的分析,可以得知无论是环状ZnSe 纳米粒子还是球状ZnSe 纳米粒子,均为核壳式结构,其表面有ZnS层和N-乙酰-L-半胱氨酸层.由ZnSe 纳米粒子紫外吸收光谱的分析,证明了ZnSe纳米粒子是属于纳米结构尺寸.依据实验分析认为ZnSe 纳米粒子生长机理符合Ostwald 熟化机理.采用水相合成法制备ZnSe纳米粒子,其方法简便易行、制备条件易控、所消耗原材料成本较低.
