燃煤烟气脱汞处理技术
2020-06-13叶智青
叶智青
(亚太环保股份有限公司,国家环境保护工业资源循环利用工程中心,云南 昆明 650118)
0 前言
汞是有毒重金属元素。我国试验煤样中汞质量分数为0.156×10-6~0.267×10-6,国内煤中汞平均质量分数0.22×10-6(0.22mg/kg)。煤中汞燃烧后除少量进入飞灰(23%~26%)及底渣(2%)之外,大部分以气态形式进入烟气中(56%~69%)。各国相继颁布法律法规限定燃煤电厂汞排放浓度,我国燃煤火电行业的汞排放总量较高,根据《GB13223-2011火电厂大气污染物排放标准》,燃煤锅炉汞及其化合物的排放限值为30μg/m3。2003年联合国环境规划署(UNEP)在内罗毕发表的《全球汞状况评估》(Global mercury assessment)报告指出:人类活动是造成全球汞含量持续增加的主要原因,每年各种人为污染源向大气排放汞总量为1900~2200t,其中每年煤燃料火力发电和焚烧垃圾向大气中排放的汞为1500t,占大气排放汞的70%,全球最高的亚洲排放汞量为860t。如何控制燃煤电厂中烟气汞的排放浓度,已经成为了全球范围内的研究焦点,现有装置组合脱除汞是研究的重点。
燃煤烟气中汞有3种存在形态:单质汞Hg0、二价汞Hg2+和颗粒态汞Hgp,其中Hg0不溶于水、挥发性极强、难以捕获、难以去除[1-8]。目前,燃煤烟气脱汞以增加脱汞设施和利用现有烟气净化设备协同脱汞技术为主,前者投资较高、占用空间、增加运行成本,中国燃煤汞含量低协同脱汞技术是较为可行的技术路线。燃煤机组大部分已经完成超低排放的改造工作,原有的烟气净化设备提高了协同处理多污染物的能力。
在烟气中的汞浓度含量只有ppb级别,当前实验室研究和工程试验主要有两个方向[10-24]:① 吸附法脱除技术:吸附材料主要吸附单质汞,对二价汞的吸收效果较小,通过解吸释放收集得到一定浓度的纯汞蒸气,工程中以喷射活性炭技术(ACI)吸附烟气单质汞Hg0,但是去除效果较低,技术难点是过高的活性炭消耗量、再利用困难、运行成本高、吸附效果差;② 氧化法氧化汞技术:用氧化剂、催化剂、光催化、紫外光等方法氧化单质汞为二价汞,用脱汞剂处理溶解于溶液中的二价汞得到固体沉淀HgS,再用亚硫酸铵溶液处理多余的脱汞剂,技术难点是氧化效率低、吸收效率受不同汞形态的制约,还有吸收后汞与溶液混合难于分离造成汞与副产品混合为一体。对于脱汞还需要攻克很多技术难题,从工程应用方面考虑,汞含量极低单独设置处理设备经济效果不合理,所以,研究方向还是需要考虑利用已有的烟气净化装置协同处理汞,如脱硝设备、除尘设备、脱硫设备,通过合理改进使得其兼有脱汞的作用。
燃煤烟气处理流程主要有:脱硝、除尘、脱硫、湿式电除尘器。每个烟气处理技术都有一定的脱汞效果,不同流程处理不同形态的烟气汞,由于汞的化学性质,不同价态汞有略微的变化。本文重点论述了脱硝、除尘、脱硫的协同脱汞技术,还论述了催化氧化剂的研究应用和相关工程应用中的技术效果。
1 协同脱除汞的技术研究
1.1 脱硝+除尘+脱汞的研究内容
脱硝过程中主要是催化剂作用达到协同脱汞效果,在燃烧温度为1000~1500℃的情况下煤中汞完全释放为Hg0形式,选择性催化还原SCR催化剂能够促进Hg0氧化为Hg2+,在这个过程中,脱硝催化剂同时也是单质汞氧化剂。许月阳等[4]测试了国内20多个典型燃煤电厂,测试结果显示烟气通过SCR催化剂装置后,明显降低了Hg0浓度,而Hg2+含量大幅增加,说明脱硝催化剂对Hg0有很强的催化氧化作用,但烟气中总汞(HgT)含量下降不明显。SCR装置虽然不能直接脱汞,但是可以提高烟气中Hg2+的比例,能为后续湿法脱硫装置脱汞创造有利条件,可以有效提高后续除尘和脱硫设备的吸附、吸收脱汞效率[5-16]。
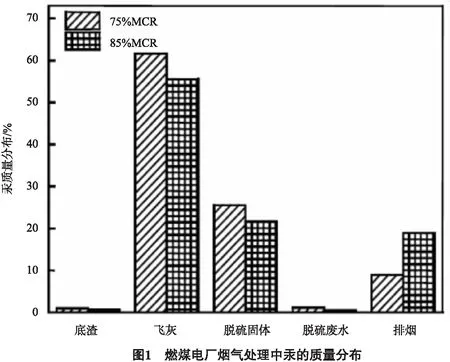
除尘设备可以同时去除烟气中颗粒物和颗粒态Hgp,Hgp的含量比例较小[1-6],低温电除尘技术脱除总汞的效率达到40%,实际运行条件下湿式电除尘器没有明显的协同脱汞效率,脱硫塔中的高效丝网除尘除雾器协同脱汞效率达到96%。高效丝网除雾器有如此高的脱除效果,很可能是经过湿法装置后湿式气溶胶以颗粒物作用吸附汞达到同时脱除效果。图1为燃煤电厂烟气处理中汞的质量分布。
1.2 脱硫+脱汞的研究内容
石灰石-石膏法脱硫(WFGD)的系统温度较低,可以抑制二价汞的还原,但是没有明显的Hg0脱除效果。WFGD对燃煤烟气有较高的协同脱汞效率,主要是因为脱硝催化剂氧化了烟气中汞。脱硫装置中一定范围内的液气比和pH值可以有效提高脱汞效率,但是也会有少量的Hg2+与2价离子反应(如SO32-、Mn2+、Fe2+等)被还原为Hg0,液气比继续增大则吸收效果下降、还原概率增加,因此一定情况下改进工艺后的单塔脱硫装置出口汞排放浓度较进口有少量增加[2-10]。湿法烟气脱硫装置(WFGD)对Hg2+协同脱除效率达到90%,但对不溶于水的Hg0的脱除效果不明显,WFGD系统脱汞作用主要受总汞中Hg2+的比例大小影响。此外脱硫浆液中Hg2+的还原和再释放问题也影响了WFGD系统对于汞的脱除效率。所以,在湿法脱硫中如何抑制二价汞被还原是研究工程应用的技术难点。
工程应用中脱硫塔增加均流装置可以使得气固液三相充分接触增加反应面积,脱硫协同脱汞的双塔双循环工程技术能增加烟气与浆液的接触面积和塔内停留时间,同时提高脱硫对汞的脱除效率[20-24]。由于目前还没有系统的监测数据,难以做出有效判断,更多的试验数据需要监测不同燃煤锅炉烟气予以证实,不同的煤质、燃煤量、锅炉参数、燃烧气量等因素中烟气汞含量也不同。
湿法脱硫技术协同脱汞的原理[21]:
Hg2++Hg0+2OH→H2O+HgO+Hg0↑
HgO+SO2→Hg0↑+SO3
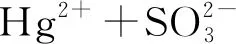
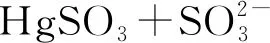
HgSO3+H2O→Hg0↑+SO42-+2H+
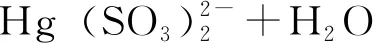
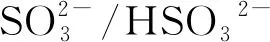
氨法脱硫中的脱汞效率如何,还没有具体的文献报道。从石膏法脱硫情况看,因为氨法脱硫中同样含有亚盐同时存在NH3,应该也会存在二价汞的二次释放问题。其反应原理需要通过化学反应和监测数据进一步推断,通过监测才能分析其脱汞效果。
2 固体吸附剂、催化剂在脱汞中的应用
2.1 脱汞吸附剂的研究内容
吸附剂有吸附和氧化双重作用,可同时脱除不同价态的汞[15-20]。贵金属吸附剂可达到很高的脱汞效率,但是高昂的价格限制其经济可行性。常见的应用负载型吸附剂有活性炭、Al2O3等载体吸附剂。过渡金属元素的氧化物如Fe、Mn、Ce等具有特殊的晶体结构,具有一定的储氧能力,通过晶格氧和化学吸附氧作用氧化烟气中的Hg0,被消耗的晶格氧和化学吸附态氧可以由烟气中的O2补充,以此达到持续高效脱汞效率。吸附剂中的Hg0通过高温处理解吸收集一定纯度的汞蒸气。
吸附法中脱汞效率的影响因素有烟气温度、烟气组分、煤质、吸附剂结构、化学性质、有效孔面积、孔隙度、比表面积等,烟气中的SO2、H2S等酸性组分生成金属硫化物覆盖脱汞活性点位影响吸附剂的脱汞效率,竞争吸附和物理吸附减少了汞与活性点位的结合概率,降低脱汞效率,实验表明适当的O2浓度可以促进Hg0转化为Hg2+。吸附剂适用温度大多位于100~200℃,吸附剂装置应该设置在烟温较低的位置,同时兼顾吸附剂回收再生工艺。工程应用中根据吸附剂适用温度范围可以在脱硝出口后或电除尘ESP后设置吸附层[18-22]。
要同时实现高脱汞效率和较低装置运行成本,脱汞吸附剂应该满足以下基本条件:较高脱汞效率,脱汞后有效回收吸附剂以再生循环使用,可富集回收吸附剂再生过程中解吸的汞,避免汞进入环境造成二次污染。由此可以得到再生处理吸附剂,吸附剂技术的工程应用关键技术是能否高效回收处理吸附剂,而且吸附剂的占用空间大,改性吸附剂和再生技术将是吸附法工程应用的技术瓶颈。能否让固体吸附剂同时具有吸附和氧化效果也同样是研究难题,结合现有的脱硝催化剂,如何在脱硝效率和吸附氧化汞中找到技术平衡也是研究内容。因此有必要开发高效的可再生脱汞吸附剂。
2.2 催化剂氧化汞的技术研究
汞的固体催化氧化技术主要是氧化单质Hg0,单质汞氧化剂有碳基催化剂、金属及金属氧化物催化剂、SCR催化剂,由于单质汞强挥发性和难溶于水的化学性质,已有的空气污染物控制设备难以脱除单质Hg0。而氧化态的Hg2+易溶于水,可以被湿法脱硫系统吸收脱除,故Hg0转化Hg2+是汞控制脱除技术的研究重点。主要类型的汞氧化物催化剂有过渡金属、贵金属、SCR脱硝催化剂和燃煤烟尘飞灰[6-13]。具体催化剂如表1所示。

表1 催化剂种类及相应物质
研究表明[3,11,22]CuO、Fe2O3、Co3O4、CeO2等过渡金属氧化物对氧化Hg0具有较好的氧化活性。在燃煤电厂要广泛应用这项技术还需要解决一些技术问题,如:如何提高催化剂自身抗SO2性能,同时保证高的Hg0氧化效率;反应催化温度大部分在150~300℃,需要进行更深入研究和现场测试得到更多的实验数据。催化氧化法的缺点:催化剂催化氧化单质汞的温度在100℃以上,烟气中的SO2被氧化为SO3出现腐蚀问题,气溶胶颗粒物堵塞催化剂生成亚盐沉积降低催化剂活性;SCR催化还原NOx的烟气中NH3的抑制作用使得催化性能降低,要保证高效催化氧化Hg0,需要研究更加平衡脱硝脱汞的SCR催化剂[5,17]。同时保持较低的SO2/SO3转化率将是燃煤烟气催化剂应用技术的污染控制技术的重点研究内容。
2.3 添加卤素脱汞的促进作用
添加少量卤素化合物可以有效提高脱汞效率,在烟气中利用添加卤素将单质汞转化为容易吸收的汞形态,其原理还是氧化+吸收方法。添加的卤素化合物主要有NH4Br、CaCl2、NaCl、CaBr2等,卤素氢化物与汞生成卤素分子或卤间化合物,卤化物对Hg0氧化有很强的促进作用,在催化剂的作用下可以氧化Hg0为二价汞[14-23]。
研究表明[21]烟气中的HCl气体、Cl2和Cl-浓度对汞的氧化有促进作用,氧化温度一般为200~600℃,添加HCl后Hg0的氧化率和脱汞效率随着温度升高先增大后减小,在350℃时达到最大值,超过400℃,Hg0氧化率急剧下降,这是由于过高的温度阻碍了单质汞吸附在催化剂的表面影响了氧化效果。SCR对汞氧化的效率随着HCl含量的增大而有所提高,在无HCl的卤素条件下单质汞的催化氧化性能较低。燃煤烟气脱汞中溴的氧化作用比氯的效果更好[22],影响作用为HBr﹥HI﹥HCl﹥HF。
由此可见,添加卤素去除汞需要较高的反应温度,还需要有催化剂协同作用。研究方向可以考虑与脱硝结合,在脱硝段添加卤素,以达到协同效果;也可以在锅炉中把卤素氧化物与煤一起喷入锅炉,可以直接到燃煤锅炉中做工程试验。
3 部分燃煤锅炉烟气的监测情况
2017年福建龙净环保有限公司对4个超低排放项目进行汞数据和工程参数监测,进行各段进出口同时监测,监测点在SCR出口、ESP出口、FGD出口、WESP出口,但是没有测燃煤锅炉出口(即SCR进口),4个项目的发电厂装机容量为300~660MW,分析不同煤质、锅炉条件、燃烧情况、烟气处理工艺路线下汞浓度及分布特征。湿法脱硫对汞的脱除效率为22%~80%,湿式电除尘器对汞的脱除效率为30%~71%,湿法脱硫对汞的脱除效率与脱硫系统入口汞形态分布及负荷、气液传质强度等有关;湿式电除尘器在汞入口浓度较低时,脱汞效果不明显[4]。4个侧点的汞浓度最高为20μg/m3,烟囱出口的总汞浓度低于2μg/m3,满足我国火电厂的汞排放标准30μg/m3,但经过煤的发热量、烟气量计算的汞浓度超过美国汞排放限值0.004lb/(GW·h)[20]。
江西省电力科学研究院监测了江西4台燃煤机组的汞排放浓度[21,24],为了解燃煤电厂汞的排放规律以及现有的污染控制设备对烟气中汞的协同脱除效果,采用安大略法对4台机组进行汞排放及控制试验研究,得到现阶段燃煤电厂配置条件下汞的排放特性。燃煤锅炉烟气出口(SCR脱硝系统入口)烟气中总汞质量浓度为22.6~35.78μg/m3,4 台测试机组除尘器可以协同脱除大部分的颗粒态汞,脱汞效率在16.60%~30.32%, 平均脱汞效率为24.37%;湿式脱硫系统对Hg2+的脱除效率为88.39%;监测结果表明:未投入汞氧化剂的机组污染控制设备协同脱汞效率在69.01%~75.63%,投入汞氧化剂的机组脱汞效率可达89.69%。
监测结果显示,SCR脱硝装置对烟气总汞的减排效果不明显,但能促使Hg0成为易于脱除的Hg2+和颗粒态汞,机组投入汞氧化剂后可大幅提高Hg0氧化为Hg2+的比率;烟气经过脱硝、除尘、湿式脱硫装置后,最终排放气体中汞的质量浓度在3.91~8.89μg/m3,远小于国家排放标准限值。SCR 脱硝工艺和汞氧化剂本身并不能脱汞,但能将Hg0转化为相对比较容易脱除的Hg2+和Hgp,从而增加烟气除尘系统和脱硫系统对汞的脱除效率,达到协同脱除汞的技术效果。
4 总结
通过SCR脱硝+ESP除尘+WFGD脱硫+WESP湿式除尘除雾组合工艺技术路线协同作用后,Hgp和Hg2+可被现有的污染控制设备脱除,而Hg0因其极高的挥发性和极低的水溶性是汞的主要排放形式,因此汞的化学形态是影响汞污染控制的关键因素,选择适宜的催化剂或氧化剂将烟气中的Hg0转化为Hg2+和Hgp,并充分利用现有的污染控制设备协同脱汞将是经济有效的燃煤汞控制技术。经过多步处理后烟气中汞含量远低于30μg/m3的国家标准,实现了烟气高效脱汞,但脱除的汞进入脱硫石膏和飞灰等固相产物,仍会造成汞的二次污染,未能从根本上解决汞污染环境问题,而且汞的脱除效果受烟气流速影响较大,脱汞效率不稳定,且脱除的汞进入废水中,后续净化处理成本较高。
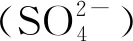
根据我国燃煤烟气处理技术现状,工业应用中协同脱硝脱硫脱汞需要深入研究单质汞的催化氧化机理、催化剂选择和吸收效率,需要提高SCR催化剂的催化氧化单质汞活性,催化剂的抗硫性及稳定性。以后的研究重点应该结合现有工程技术情况,研究可以同时催化氧化NOx和单质汞的催化剂,卤素的添加方式和添加量,不同的燃煤烟气的适用范围和应用条件,选择最佳反应温度,提高脱硫装置的吸收效率。对于工程化应用需要考虑更多的技术参数,如喷淋量、溶液密度、气液比例、装置抗卤素的腐蚀性能等技术难点。
