三元体系NH4Cl-NaCl-H2O 298 K介稳相平衡研究
2020-06-12邬莉婷程兴龙
邬莉婷,李 晨*,陈 鹏,程兴龙
(1.四川省地质矿产勘查开发局成都综合岩矿测试中心,四川 成都 610081;2.琥珀科技(天津)有限公司,天津 300350;3.上海电气集团股份有限公司中央研究院,上海 200070)
地下卤水是天然存在的水盐共存资源,我国地下卤水具有资源丰富、品质优异等优点,现代生产中化工、轻工、航空等企业仍将其作为生产的重要原料[1-2]。常见地下卤水生产的无机盐大都包含NH4+、Na+、Cl-三种离子。研究NH4Cl-NaCl-H2O三元体系在蒸发过程中的析盐、浓缩规律,将为实现卤水资源的综合利用提供一定的理论指导。
目前含氨水盐体系的研究较多,如三元体系NH4+,Al3+//Cl--H2O[3](298 K)、Na+,NH4+//Cl--H2O[4-5](298 K、313 K)、NH4+,Mg2+//Cl--H2O[6](298 K)、K+,NH4+//Cl--H2O[7](298 K)稳定相平衡研究,三元体系Na+,NH4+//Cl--H2O[8](323 K)、NH4+,Mg2+//Cl--H2O[9](298 K)、K+,NH4+//Cl--H2O(298 K) 介稳相平衡研究。四元体系NH4+,Na+,Mg2+//Cl--H2O[10](348 K)、K+,NH4+//Cl-,SO42--H2O[11](273 K)稳定相平衡研究,四元体系Mg2+,NH4+//Cl-,SO42--H2O 298 K[12]介稳相平衡研究。五元体系K+,NH4+,Mg2+//Cl-,SO42--H2O[13](273 K、298 K)的稳定相平衡研究。研究发现:钠离子对铵盐的结晶形式也有一定的影响,在298~313 K温度范围内,稳定相平衡研究过程中形成了固溶体,而在323 K的介稳相平衡研究中没有形成固溶体或者复盐。
综上所述,现有含氨水盐体系的研究大多为稳定相平衡,氯化铵和氯化钠的结晶形式会受到温度和研究方法的影响。介稳相平衡比稳定相平衡更接近自然状态,三元体系NH4Cl-NaCl-H2O在323 K的介稳相平衡研究过程中没有固溶体或复盐的形成。此三元体系在298 K的介稳相平衡研究过程中盐类的析出形式与结晶区域的大小是否会随着温度的变化而改变,还需进行实验进一步验证。因此,开展三元体系NH4Cl-NaCl-H2O在298 K的介稳相关系研究,可为实现卤水资源的综合利用提供基础数据。
1 实验部分
1.1 实验试剂
实验过程中使用去离子水(电导率<1.5×10-4S/m)配制样品和分析标准溶液,pH≈6.6,实验所需试剂 NaCl(A.R),NH4Cl·6H2O(A.R)。
1.2 实验仪器
实验所用仪器:SHH-250型恒温箱,BSA124S型电子天平,WYA型阿贝折射仪,DX-2700型X射线粉晶衍射仪。
1.3 实验方法
1.3.1 介稳相平衡研究方法
采用等温蒸发法。在硬质塑料盒中配制NH4Cl或NaCl的饱和水溶液,添加一定量的另一种盐,盐类完全溶解后,将其放入恒温箱中进行等温蒸发。观察固相析出渐变过程,待析出一定量固相时分离固液相,并对固相和液相进行化学分析。测定平衡液相的密度和折光率,并鉴定固相。重复以上步骤,直至蒸干。
1.3.2 分析方法[14]
Cl-:AgNO3容量法测定;NH4+:甲醛法测定;Na+:差减法计算。
1.3.3 平衡固相分析
采用Schreinemarkers湿渣法[15],再结合X射线粉晶衍射法进一步确定。
2 结果与讨论
2.1 三元体系NH4Cl-NaCl-H2O 298 K介稳相平衡研究
三元体系NH4Cl-NaCl-H2O 298 K下的固液相化学组成以及溶液的物化性质,见表1。
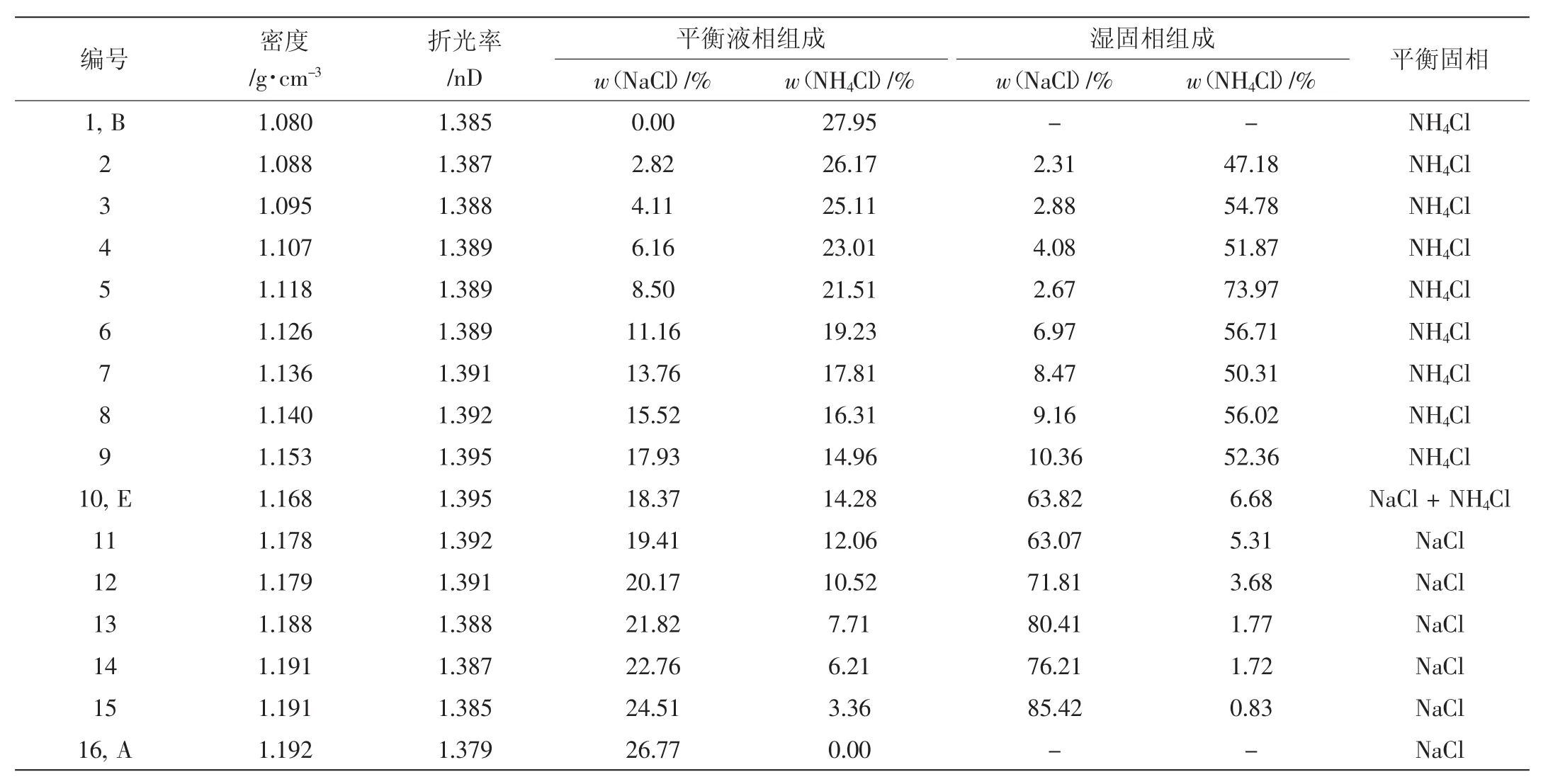
表1 三元体系NH4Cl-NaCl-H2O 298 K的固液平衡组成及溶液物化性质数据Table 1 Experimental values of densities,refractive indices,and solubility of the equilibrium solution in the ternary system NH4Cl-NaCl-H2O at 298 K
绘制出此三元体系的介稳相图,见图1。图2为该三元体系共饱点E处固相的XRD图谱。为探究温度的变化对此三元体系盐类析出情况的影响,绘制了三元体系NH4Cl-NaCl-H2O在298 K与323 K的对比介稳相图,如图3。
由图1、图2可知,三元体系NH4Cl-NaCl-H2O在298 K下有一个共饱点E,两条单变量曲线 (AE、BE),两个单盐结晶区域 (NH4Cl、NaCl),一个未饱和溶液区AEBHA。该体系无复盐或固溶体的形成,为简单三元体系。其中A、B分别为两个二元子体系NaCl-H2O、NH4Cl-H2O的共饱点,C、D为两种单盐的纯盐点。E点处NaCl、NH4Cl均处于饱和状态,其质量分数为w(NaCl)=18.37%、w(NH4Cl)=14.28%。NaCl和NH4Cl两个结晶区域的大小差异并不明显,在此体系中NaCl和NH4Cl的溶解度相当。
由图3可知,298 K和323 K时,三元体系NH4Cl-NaCl-H2O盐类析出类型没有发生变化,为简单三元体系。随着温度的升高,NaCl的结晶区域明显增大,而NH4Cl的结晶区域明显变小,说明此三元体系在升温过程中会使NH4Cl的溶解度增加,与NaCl的溶解度拉出差距。与同温度下的稳定相平衡比较,发现介稳相平衡研究过程中,没有氨钠固溶体形成,只有单盐析出。研究方法的改变使盐类析出形式发生了变化。

图1 三元体系NH4Cl-NaCl-H2O 298 K的介稳相图Figure 1 Metstable phase diagram of the ternary system NH4Cl-NaCl-H2O at 298 K
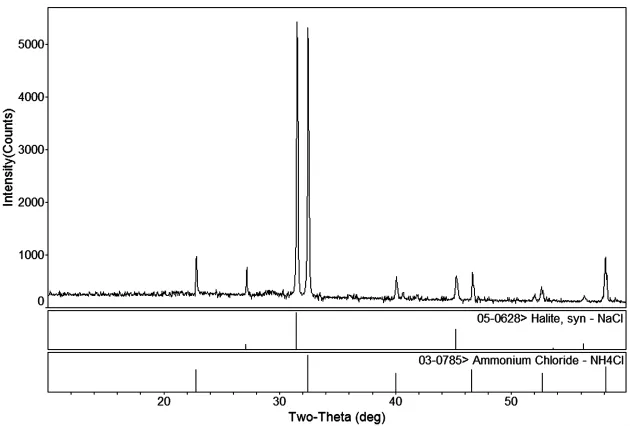
图2 共饱点E处平衡固相XRD图Figure 2 X-ray diffraction pattern for the cosaturated salts corresponding to the invariant point E
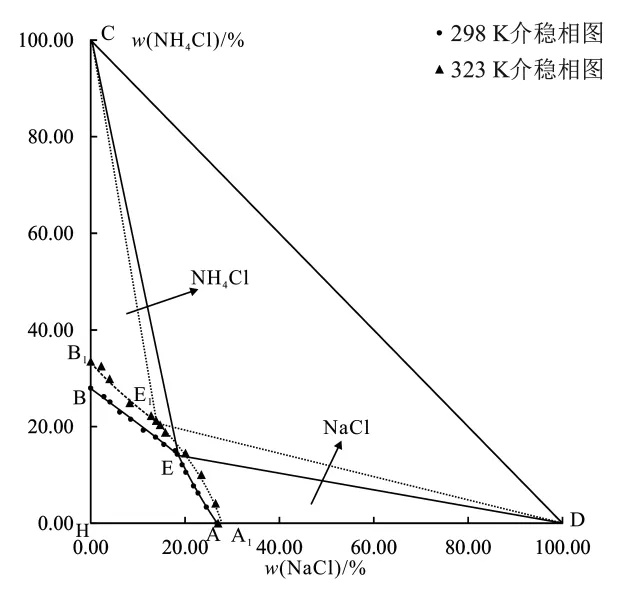
图3 三元体系NH4Cl-NaCl-H2O 298 K、323 K的介稳对比图Figure 3 Compared phase diagram of the ternary system NH4Cl-NaCl-H2O at 298 K and 323 K
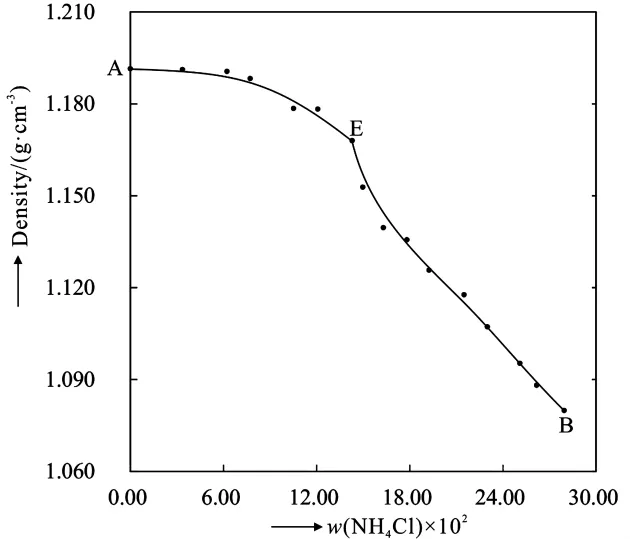
图4 三元体系NH4Cl-NaCl-H2O 298 K密度-组成图Figure 4 Densities vs composition diagram of the ternary system NH4Cl-NaCl-H2O at 298 K
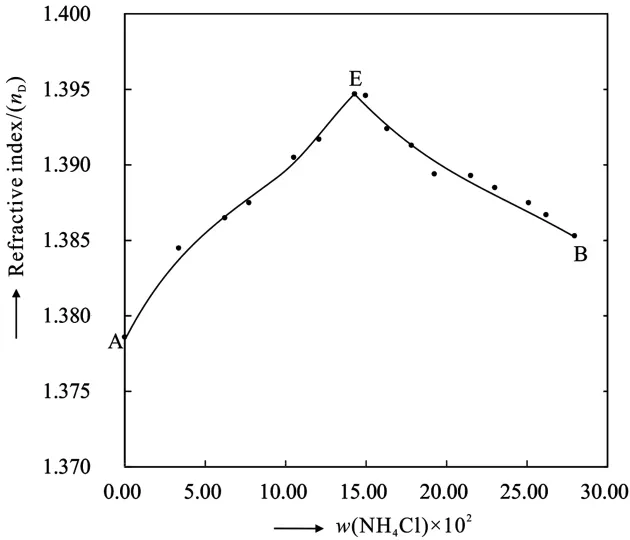
图5 三元体系NH4Cl-NaCl-H2O 298 K折光率-组成图Figure 5 Refractive indices vs composition diagram of the ternary system NH4Cl-NaCl-H2O at 298 K
如图4、图5所示,蒸发实验分别从二元共饱点A、B处附近开始。随着氯化钠或者氯化铵的析出,两种溶液中各种溶质的质量分数发生变化,并随蒸发的进行,溶质组成逐渐趋于相似。随着蒸发实验的进行,溶液的密度和折光率也逐渐接近,直到在共饱点处达到相等。总体上溶液的密度随氯化铵质量分数的增大而减小,折光率随氯化铵质量分数的增大呈现出先增大后减小的趋势。
3 结论
三元体系NH4Cl-NaCl-H2O 298 K等温蒸发实验中出现一个共饱点E、两条单变量曲线、两个单盐结晶相区。该体系无复盐和固溶体形成,为简单三元体系。其中氯化铵、氯化钠两个结晶区域的大小差异并不明显,在此体系中NH4Cl和NaCl的溶解度差异不大。随着蒸发进行,平衡液相的密度和折光率随着NH4Cl质量分数的增加呈现出规律性变化。三元体系NH4Cl-NaCl-H2O在298~323 K温度范围内,随着温度的增加,NaCl的结晶区域明显增大,而NH4Cl的结晶区域明显变小,说明降温有利于NH4Cl的析出。
