高血压合并焦虑抑郁病人血压变异性与血浆肾素活性、醛固酮水平的关系
2020-06-01崔淑娴赫连曼赵海鹰
崔淑娴,赫连曼,赵海鹰
高血压是一种心身疾病,国内流行病学调查显示,焦虑、抑郁病人合并高血压的发生率分别为11.6%~38.5%和5.7%~15.8%[1]。一项国外荟萃分析表明,在高血压人群中焦虑患病率为8.9%~55.3%[2],焦虑病人高血压患病率为一般人群的2~3倍[3]。焦虑、抑郁通过多种机制参与高血压的发病过程,如肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone system,RAAS)激活[4-5],交感神经亢奋[6-7],垂体-下丘脑-肾上腺轴功能紊乱[8]等。高血压合并焦虑抑郁病人临床症状无特异性,可表现为头晕、乏力、心悸、胸闷、烦躁不安、睡眠障碍等多种症状,血压波动性大,常规降压治疗收效甚微,更易形成难治性高血压。了解该类病人血压变异性(blood pressure variability,BPV)及RAAS的改变,可以为临床降压药物的优化选择提供指导。本研究观察高血压合并抑郁焦虑病人全天BPV的特点,检测血浆肾素活性(plasma renin activity,PRA)、醛固酮(adlosterone,ALD)水平的变化情况,现报道如下。
1 资料与方法
1.1 观察对象 选取2016年3月—2018年6月在河南省人民医院高血压科住院,且明确诊断为高血压合并抑郁焦虑病人186例为高血压并焦虑抑郁组,男88例,女98例,年龄23~68(49±12)岁。原发性高血压(essential hypertension,EH)病人153例为原发性高血压组,男79例,女74例,年龄25~70(46±13)岁。所有入组病人均排除其他继发性高血压疾病。高血压诊断参照2013年《中国高血压防治指南的诊断标准》。本项研究已通过河南省人民医院伦理委员会审查。所有入组病人自愿参与研究,签署知情同意书。
1.2 焦虑抑郁状况测评 所有入组高血压病人均通过仔细问诊, 了解个性特征及有无焦虑抑郁病史, 同时采用汉密尔顿焦虑量表(HAMA) 评分和汉密尔顿抑郁量表(HAMD)评分(17项版)对病人进行焦虑抑郁状况测评。合并焦虑判定方法: 现场HAMA评分≥11分; 既往有焦虑人格特征或有反复出现的焦虑相关症状。合并抑郁判定方法: 现场HAMD评分≥13分; 既往有抑郁人格特征或有反复出现的抑郁相关症状。高血压同时合并HAMA和(或)HAMD评分大于上述标准,且排除其他继发性高血压病变者诊断为高血压合并焦虑抑郁。
1.3 24 h动态血压监测 病人入院后采用无锡中健科仪有限公司 24 h 动态血压监测仪,进行无创动态血压监测,白昼时间为06:00~22:00,夜间为 22:00 至次日06:00,测量间隔白昼为15 min,夜间为 30 min。24 h获取数据的成功率为 85%以上,病人在每次测量时前臂放于体侧,保持静止,避免说话及肢体活动。以各时间段血压的变异系数(coefficient of variation,CV)作为血压变异性(BPV)的指标,包括 24 h收缩压(24 hSBP) 变异(24 hSCV)及24 h舒张压(24 hDBP) 变异(24 hDCV);白昼SBP变异(dSCV)及DBP 变异(dDCV);夜间SBP 变异(nSCV)及DBP 变异(nDCV)。
1.4 血浆PRA与ALd检测 入院前未服用降压药的病人,于入院后第2天清晨06:00~08:00平卧2 h后采血查卧位PRA与Ald水平,然后于08:00~10:00站立2 h后采血查立位PRA与ALD。既往服用钙离子拮抗剂、血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂或β-受体阻滞剂的病人需停药2周,服用利尿剂的病人需停药4周,给予维拉帕米缓释片0.12~0.24 g/d和(或)特拉唑嗪2~8 mg/d洗脱后再行PRA与Ald水平测定。所有指标采用放射免疫法检测。
2 结 果
2.1 两组临床资料比较 两组之间性别、年龄、体质指数、肌酐、空腹血糖、血脂、尿酸之间比较差异无统计学意义(P>0.05)。详见表 1。
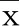
表1 两组病人临床资料比较(±s)
2.2 两组血压变异系数比较 收缩压:与原发性高血压组相比,高血压并焦虑抑郁组24 hSCV、dSCV均明显高于原发性高血压组(P<0.01),夜间nSCV与原发性高血压组比较,差异有统计学意义(P<0.05)。舒张压:高血压并焦虑抑郁组24 hDCV、dDCV明显高于原发性高血压组,夜间nDCV与原发性高血压组比较差异有统计学意义(P<0.001)。详见表2。
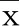
表2 两组病人血压变异系数比较(±s) 单位:%
2.3 两组病人PRA及ALD的变化 高血压并焦虑抑郁组卧位PRA及ALD均明显升高,立位2 h后PRA与ALD也高于原发性高血压组,差异均有统计学意义(P<0.05或P<0.01)。详见表3。
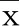
表3 两组卧位、立位PRA及Ald的变化比较(±s)
3 讨 论
目前,高血压合并焦虑抑郁病人日渐增多,且发生率有逐年增高的趋势。研究显示,焦虑、抑郁与高血压发病有较强的相关性,焦虑使非高血压人群患高血压风险增加约2倍,抑郁使非高血压人群患高血压风险增加约 3.5 倍[3]。高血压专科门诊就诊病人中常伴有精神症状,高血压病人中抑郁、焦虑、睡眠障碍的检出率为5%、40%和60%,高血压患病率随着抑郁焦虑情绪和睡眠障碍程度的加重而升高[9-10]。我科住院病人中高血压合并焦虑抑郁的比例达50%以上,且多为难治性高血压,因血压不易控制病人多反复到多家医院就诊,反复更换不同种类的降压药物,给家庭造成沉重的经济负担。病人常有以下临床特征:血压波动性较大,严重时呈发作性血压升高,血压突发升高时常伴随一系列躯体化症状,如头痛、头晕、出汗、胸痛、心悸、濒死感等,临床表现酷似嗜铬细胞瘤[11-12]。发作频率从数天、数月1次到每天数次不等,每次持续时间从几分钟至几天不等,发作间期血压正常或轻度升高,或间断、持续出现的头晕、乏力、胸闷、睡眠障碍等非特异症状。血压的大幅波动导致BPV增大,BPV与高血压导致的心脏损害和动脉硬化、微量白蛋白尿和肾功能损害、心血管事件发生率和死亡率均有密切关系[13]。为探讨高血压并焦虑抑郁病人24 h血压变异的特点,本研究采用动态血压仪监测病人白昼、夜间不同时段血压的变化,研究发现高血压合并焦虑抑郁组24 hSCV、24 hDCV、 nSCV、dDCV均高于原发性高血压组(P<0.01),尤其dDCV与nDCV与原发性高血压组比较差异有统计学意义(P<0.001),提示高血压合并焦虑抑郁病人血压波动性大于原发性高血压病人,尤其夜间血压波动更大,这可能是导致夜间心脑血管事件高发的重要因素。基于上述研究,在降压药物的选择上要优先选择长效制剂,保证24 h血压平稳,通过改善BPV,恢复血压变化的正常节律,最大限度减少心脑血管事件的发生。合并焦虑抑郁病人夜间血压BPV增大的原因考虑与焦虑抑郁等负性情绪导致睡眠障碍有关,入睡困难、易醒、多梦等症状在该类病人中普遍存在,加重了病人的血压波动性。
国外研究显示,RAAS参与了焦虑抑郁病人高血压的发病过程[4-5]。为了解高血压合并焦虑抑郁病人血浆RAAS的变化,本研究采用放射免疫法检测186例高血压合并焦虑抑郁病人与153例原发性高血压病人血浆PRA、ALD的水平,研究发现,合并焦虑抑郁病人卧位、立位PRA均明显高于原发性高血压病人,ALD水平卧位、立位也明显高于原发性高血压病人,提示RAAS激活参与了该类病人高血压的发生与发展。PRA增加使血管紧张素Ⅱ(AngⅡ)及Ald生成增加,AngⅡ使血管收缩,ALD促进了水钠潴留,二者协同加剧了高血压的恶性发展。该研究结果也为临床降压药物的优化选择提供了理论依据,针对病人体内RAAS激活的状况,临床选用AngⅡ转换酶抑制剂、血管紧张素受体拮抗剂或β受体阻滞剂作为降压药物的首选,理论上可能是最佳选择。
高血压合并焦虑抑郁病人的治疗除了常规的降压药物之外,非药物治疗及抗抑郁焦虑的治疗也是非常重要的环节,通过心理疏导,调整病人心态,正确对待疾病及生活中的各种矛盾,减轻精神压力。通过自我调节仍不能改善病情时可给予5-羟色胺(5-HT)再摄取抑制剂及苯二氮卓类药物进行干预。通过以上治疗措施,大部分病人可以改善临床症状,血压得到良好的控制。
