二甲醚水蒸气重整制氢反应机理研究进展
2020-05-23樊飞跃吴志豪
樊飞跃,赵 龙,吴志豪,侯 红
(中国环境科学研究院 环境基准与风险评估国家重点实验室,北京 100012)
能源是人类赖以生存的基础,也是国家经济发展的重要命脉,但是经过200多年的发展,煤、石油和天然气等化石能源已经被大量开采,造成这些不可再生能源面临枯竭。 随着人口数量的不断增加以及经济的快速发展,能源的需求量与日俱增,能源危机日益突出。 同时,化石燃料的过度开采和大量使用,也对环境造成了严重的污染。 为此,世界各国都在积极寻找和开发新型清洁能源。
氢能由于具有清洁高效、 可再生性等优势,被视为是21世纪最具发展潜力的清洁能源,受到了世界各国的广泛关注[1]。 然而,由于氢气的密度较低,难以被压缩和液化,而且易燃易爆,所以在输送和储存上都存在着极大的不便, 很难实现广泛的应用。 而利用含氢化合物(烃类、醇类、醚类等)进行原位在线重整制氢被认为是解决氢气制备、储存和运输问题的最现实方案, 目前主要有甲烷、 甲醇、乙醇、二甲醚等重整制氢技术。 但是甲烷和乙醇重整制氢反应需要的温度比较高,能耗高;甲醇有毒,一旦泄露会对环境和人体造成很大的危害,而且甲醇为液体,需要额外的气化装置,增加操作成本;而二甲醚(DME)无毒、无腐蚀性、对环境友好、易于储存和运输,并且重整制氢具有反应条件温和、产氢量高等优势,以此作为原料进行重整制氢比其他原料更具优势。
通常, 二甲醚水蒸气重整制氢反应(Dimethyl ether steam reforming,DME SR) 包括两步连续反应[2],第一步是DME在固体酸催化剂(氧化铝、分子筛等)上进行水解反应生成甲醇(CH3OCH3+H2O→2CH3OH),第二步是甲醇在金属催化剂(贵金属、Cu基、Zn基催化剂等)上进行水蒸气重整反应生成CO2和H2(CH3OH+H2O→CO2+3H2)。 由于两个反应需要不同的催化活性中心, 所以DME SR催化剂必须同时含有这两个活性中心, 是一种双功能催化剂,该技术研究的重点是高活性催化剂的开发。
目前关于DME SR的综述性文章主要集中于高效催化剂开发以及反应条件优化等方面,而关于反应机理的研究进展还鲜见报道。 基于此,本文对二甲醚水蒸气重整制氢反应机理以及动力学研究现状进行了总结, 为高效催化剂的开发提供理论依据。
1 二甲醚水蒸气重整制氢反应机理
1.1 二甲醚水解反应机理
二甲醚水解反应中比较常用的两种催化剂分别是γ-Al2O3和ZSM-5分子筛, 目前仅有数名研究者[3-6]进行了水解反应机理的研究,主要是基于实验研究与理论计算等方法。
Badmaev等[3]研究了二甲醚在H-ZSM-5分子筛上的水解反应行为, 发现水解反应是在B酸酸位上进行的,而且反应活性受到酸强度的影响。 根据实验结果,提出了二甲醚水解反应机理,如式(1)至式(4)所示。 由此可知,DME首先与分子筛(用“H+A-”表示)反应生成(CH3)2OH+A-离子(式(1)),该离子随后进行分解反应生成甲醇和CH3+A-(式(2)),所生成的CH3+A-进一步与水反应生成CH3OH2+A-(式(3)),最后,CH3OH2+A-通过分解反应生成甲醇和H+A-(式(4))。


图1 Stepwise机理(实线)和concerted机理(虚线)的势能面曲线(单位为kJ/mol)
Namuangruk等[4]使用Gaussian软件计算了H-ZSM-5分子筛上二甲醚水解反应机理,结果表明,H-ZSM-5上主要有两种水解反应机理,即stepwise和concerted机理(如图1所示),对于stepwise机理,DME首先通过脱甲基步骤生成甲氧基中间物种,甲氧基随后与水通过水解步骤生成甲醇,这两个步骤的活化能分别为168.6kJ/mol和81.8kJ/mol; 而对于concerted机理,由于脱甲基和水解步骤同时进行,所以只需一步即可生成甲醇,活化能为108.9kJ/mol。通过对比这两种反应机理的活化能, 发现DME水解反应更易以concerted机理进行,速率控制步骤为stepwise机理中的DME脱甲基步骤。此外,通过Gaussian软件计算得到的表观活化能为75.5kJ/mol,这与通过实验计算得到的表观活化能(76.5kJ/mol)相一致。
Meeprasert[5]利用Gaussian软件研究了掺杂胺的ZSM-5催化剂上DME水解反应机理,发现掺杂胺后,催化剂上除了正常的B酸位(Z[OH])以外,又产生了两种新的活性位,即质子化的Z[NH2]和非质子化的Z[NH]胺活性中心。通过对比不同活性位上stepwise和concerted两种路径的基元反应活化能,发现DME水解反应在Z[OH]和Z[NH]活性位上发生的路径为concerted,且Z[OH]上基元反应活化能最低,因而可以预测其具有最好的催化活性,而Z[NH2]并不能有效催化DME水解反应的进行,这是因为在该活性位上stepwise路径和concerted路径基元反应活化能都特别高。
Hirunsit等[6]借助VASP软件研究了γ-Al2O3上二甲醚水解反应机理,发现DME水解反应是在γ-Al2O3表面-OH基团上进行的,而羟基化(110)晶面比羟基化(100)晶面含有更多的-OH基团,从而具有更高的酸量,所以羟基化(110)晶面更加利于DME水解反应的进行。
1.2 甲醇水蒸气重整反应机理
1.2.1 甲醇水蒸气重整反应机理的实验研究
许多学者[7-8]已经对甲醇水蒸气重整反应(Methanol steam reforming,MSR)机理进行了研究,并提出了很多反应机理,但是到目前为止,对该反应机理仍然存在分歧,还没有统一的结论,这主要是由于甲醇水蒸气重整过程是在极短时间内完成的,使用原位红外(In situ FTIR)、脉冲场解析质谱(PFDMS)等常规分析手段很难检测到反应中间体的存在,而即使使用高分辨电子能量损失谱(HREELS)、二次离子质谱(SIMS)等高端分析手段也只能检测到少数中间体的存在。
通常,MSR反应机理的研究重点是围绕CO的产生途径,也就是说CO究竟是反应的一次产物还是二次产物。 归纳起来,主要有分解变换机理、一步重整机理、甲酸甲酯机理和甲醛机理四种观点。
(1)分解变换机理
也称为两步反应机理, 该机理是在20世纪70年代,捷克学者Pour等[9]在Cu/ZnO/Cr2O3/Al2O3催化剂上研究MSR反应时, 发现产物中存在一定量的CO,由此推测该反应可能经历甲醇分解反应和水汽变换反应两个步骤,如式(5)和式(6)所示。

由于CO是在第一步甲醇分解反应中产生的,是反应的一次产物,所以体系中CO浓度应该高于或等于水汽变换反应平衡时的浓度。 然而,Amphlett等[10]通过实验数据发现在Cu基催化剂上MSR反应产物中的CO浓度总是低于热力学平衡值,他们将这种现象归因于催化剂表面形成了积炭,但是积炭会造成催化剂失活,这与实验现象不符。 此外,天津大学李言浩等[11]使用原位红外光谱法对Cu系催化剂上MSR过程进行了分析, 证实了反应过程中CO2不是在CO之后产生的。
(2)一步重整机理
随后,数名研究者[12-14]提出了一步重整机理,如式(7)所示,即甲醇直接与水反应生成CO2和H2。

Geissler等[13]对商业Cu/ZnO/Al2O3催化剂上甲醇重整反应进行了研究,发现CO浓度低于水汽变换反应平衡计算值。 Agrell等[14]认为CO低于平衡值的原因是CO为反应的二次产物,是由逆水汽变换反应生成的,并通过实验发现体系中CO浓度随着停留时间的降低而降低,这进一步证明了CO是由逆水汽变换反应生成的。
这种反应机理已经被大部分研究者所接受,但是对于反应中间产物仍然存在一定的分歧。
(3)甲酸甲酯机理
随着研究者[15]对MSR反应中间物种的确定,提出了甲酸甲酯机理,如式(8)至式(10)所示,这种机理也被Jiang等[16-17]所证实。 他们认为甲醇首先通过脱氢反应生成甲酸甲酯(式(8)),随后甲酸甲酯进行水解反应生成甲酸(式(9)),最后甲酸通过分解反应生成CO2和H2(式(10)),其中,甲醇脱氢反应是MSR反应的速率控制步骤,而反应过程中CO是通过逆水汽变换反应生成的。
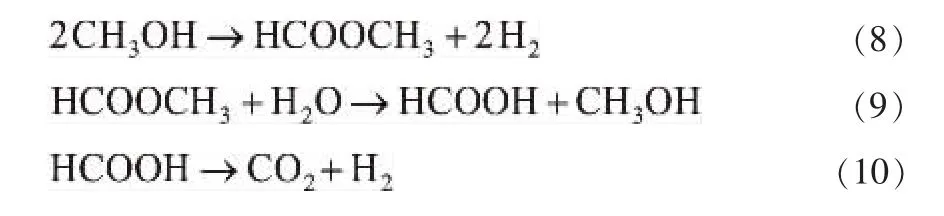
(4)甲醛机理
然而,Takezawa等[18]在研究Cu基催化剂上MSR反应时,发现中间产物是甲醛和甲酸,因而提出了另外一种反应机理,如式(11)至式(13)所示,该机理也被Breen等[19]以及Shishido等[20]所证实。他们认为甲醇首先通过脱氢反应生成甲醛(式(11)),然后甲醛进一步进行水解反应生成甲酸(式(12)),最后甲酸通过分解反应生成CO2和H2(式(13)),而CO则是通过逆水汽变换反应生成的。

最近,Frank等[21]基于Jiang等[17]、Peppley等[12]和Takezawa等[18]对MSR反应机理的研究,对Cu基催化剂上MSR反应机理进行了总结,并画出了循环过程图,如图2所示。 可以看出,该过程从CH3OH吸附在催化剂表面开始, 并假设A表面吸附中间物种,B表面吸附解离的氢,最终在A和B两个表面上完成整个循环反应。
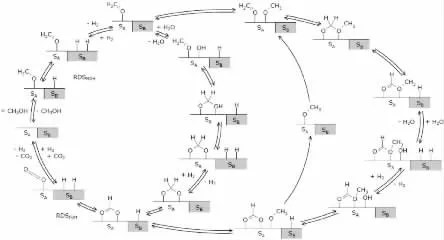
图2 Cu基催化剂上甲醇水蒸气重整(MSR)反应机理图
综上所述,甲醇水蒸气重整反应是一个复杂的过程,目前关于该反应机理还没有定论,但是随着人们对该反应认识的不断深入以及原位表征技术的发展,将有助于MSR反应机理的进一步研究。
1.2.2 甲醇水蒸气重整反应机理的理论研究
实验与理论相结合可以更深入、细致地揭示反应的机理,人们对此已经达成共识。 在实验上,由于受到检测分析技术的限制,只能检测到部分中间物种,因而反应机理仍处于争议之中。 近年来,计算机模拟作为一种强大、有效的研究方法,在许多非均相催化反应体系研究中卓有成效。
Lin等[22]基于密度泛函理论(Density functional theory,DFT) 计算研究了PdZn催化剂上甲醇水蒸气重整(MSR)反应机理,提出了如图3所示的反应路径。 由图可知,甲醇首先通过脱氢反应生成中间物种甲醛(CH2O*),随后CH2O*有两条反应路径,一条是CH2O*直接进行脱氢反应,最终产物为CO;另一条是CH2O*与水分解生成的OH*反应生成CH2OOH*,最终产物为CO2, 所以最终C1反应产物的种类取决于CH2O*的反应性。 通过对比不同催化剂上这两条路径的能垒和反应能,就可预测出最终产物,从而筛选出具有良好催化活性的催化剂。

图3 甲醇水蒸气重整反应机理图
目前许多研究者[22-25]已经利用DFT计算研究了不同金属表面(Cu(111)、Pd(111)、PdZn(111)和Co(111)等)上MSR反应机理,发现在PdZn(111)上MSR反应路径与Cu(111)上相似,CH2O*均倾向于与OH*进行反应生成CH2OOH*,导致最终产物为CO2和H2,这与实验结果相一致[26],而在Pd(111)和Co(111)表面,CH2O*优先进行直接脱氢反应, 导致CO和H2为主要产物,这与实验结果相一致[27]。
2 二甲醚水蒸气重整制氢动力学
由于DME SR反应比较复杂, 除了两个主反应外,还伴随着DME分解、甲烷化等副反应,所以关于该反应体系的动力学仅有数名研究者[28,29]进行了研究。
Feng等[28]以CuO/ZnO/Al2O3/ZrO2+ZSM-5作为催化剂,在固定床反应器中研究了进料比、空速和温度等条件对二甲醚水蒸气重整(DME SR)反应性能的影响,得到宏观动力学数据。 结合Park等[30]和Peppley等[12]分别提出的甲醇脱水制二甲醚和甲醇水蒸气重整反应动力学模型,获得了DME SR动力学模型。 最后,根据实验数据回归得到了动力学参数,并将其用于DME SR模拟计算中,取得了良好效果,进而可以指导工程和工艺设计。
Oar-Arteta等[29]对CuFe2O4/γ-Al2O3催化剂上二甲醚水蒸气重整反应(DME SR)动力学进行了研究,并结合DME水解、甲醇水蒸气重整和逆水汽变换这三个反应的动力学模型得到了DME SR反应动力学模型,通过非线性回归法拟合实验数据获得动力学参数,该模型能够很好地进行反应器模拟,如图4所示。

图4 二甲醚水蒸气重整制氢动力学模型
3 展望
二甲醚水蒸气重整(DME SR)反应以其反应条件温和、副产物少、产氢量高等优点,成为在线重整制氢的重要途径。 然而,由于该反应体系比较复杂,目前仍存在反应机理以及动力学尚不完全清楚等问题,限制了其大规模的应用。 因此,在今后的工作中, 需要进一步深入研究DME SR反应机理及动力学,以期为开发高活性、高稳定性催化剂提供理论基础。
